
- •54) Адиабатный процесс – термодинамический процесс, при котором система не получает теплоты извне и не отдает ее.
- •58) Идеальная тепловая машина Карно.
- •1) Теплопроводность (перенос энергии) ; 2) диффузия (перенос массы) ; 3) внутренние трение или вязкость (перенос импульса)
- •63) Вязкость - Явление вязкости связано с возникновением сил трения между слоями жидкости или газа, которые перемещаются параллельно друг другу, но с разными скоростями
- •30). Моменты импульса и силы относительно точки и неподвижной оси. Уравнение моментов для системы материальных точек.
- •43)Измерение температуры
- •56)Обратимые и необратимые тепловые процессы.
- •57)Энтропия.
- •57) Второй закон термодинамики.
- •37)Результирующее движение при этих условиях можно рассматривать как гармоническое колебание с пульсирующей амплитудой. Такое колебание называется биением.
- •Сложение гармонических колебаний одного направления и взаимно перпендикулярных колебаний.
- •- Одного направления
- •- Взаимно перпендикулярные
- •11)Внутренние и внешние силы.
- •33)Силы инерции при ускоренном поступательном движении системы отсчета. Свойства сил инерции.
- •2) На силы инерции не распространяется третий закон Ньютона.
- •3) Силы инерции приложены к центру масс тела.
- •4) Силы инерции являются внешними силами. В связи с этим внеинерциальных системах отсчета в общем случае не может быть замкнутых систем точек или тел.
- •59).Эффективное сечение рассеяния. Средняя длина свободного пробега молекул.
53)
Работа в термодинамике: находящийся в
сосуде газ оказывает на поршень площадью
S
давление p=F/S,
под действием которого поршень
перемещается на расстояние l,
изменяя объём газа на ∆V=Sl
и совершая работу A=Fl
или A=p∆V
-Изотермический
процесс (T=const).
Изотермический процесс описывается
законом Бойля - Мариотта: PV=const.
Диаграмма этого
процесса (изотерма) в координатах р, V
представляет собой гиперболу,
расположенную на диаграмме тем выше,
чем выше температура, при которой
происходил процесс.
Работа изотермического
расширения газа:
-Изобарный
процесс (p=const).
Диаграмма этого процесса (изобара) в
координатах р, V изображается прямой,
параллельной оси V. При изобарном
процессе работа газа при расширении
объема от V1
до V2
равна
- Изохорный процесс
(V=const).
Диаграмма этого процесса (изохора) в
координатах р, V изображается прямой,
параллельной оси ординат. При изохорном
процессе газ не совершает работы над
внешними телами, т.е
Уравнение Пуассона:
pVk=const
где p
– давление газа, V
- его объем, k
- показатель адиабаты, Cp
и Cv
- теплоёмкости газа соответственно при
постоянном давлении и постоянном
объёме.
55)
Политропный процесс — термодинамический
процесс, во время которого удельная
теплоёмкость c
газа остаётся неизменной. Предельными
частными явлениями политропного
процесса являются изотермический
процесс и адиабатный процесс. В случае
идеального газа изобарный процесс и
изохорный процесс также являются
политропическими.
Для идеального
газа уравнение политропы может быть
записано в виде:
pVn
= const
где величина
n=(C-Cp)/(C-Cv)
называется показателем политропы.
В зависимости от
процесса можно определить значение n:
1. Изотермический
процесс: n
= 1, так как PV1
= const,
значит PV
= const,
значит T
= const.
2. Изобарный процесс:
n
= 0, так как PV0
= P
= const.
3. Адиабатный
процесс: n
= γ,
это следует из уравнения Пуассона.
4. Изохорный процесс:
n=∞,
так как P1V1n=P2V2n=
const
, значит P1
/ P2
= (V2
/ V1)n,
значит V2
/ V1
= (P1
/ P2)(1
/ n),
значит, чтобы V2
/ V1
обратились в 1, n
должна быть бесконечность.
В ее основе лежит
круговой процесс который называется
циклом Карно
1-2: A1=Q1>0
– Изотерм. расширение
2-3: Q=0
– Адиабатическое расширение;
3-4: A2=Q2<0
– Изотермическое сжатие;
4-1: Q=0
Адиабатическое сжатие.
Для замкнутых
циклов работа совершаемая газом в цикле
Карно равна подводимому теплу. Тепловая
машина реализующая этот цикл имеет
максимальный КПД по сравнению с любым
другим циклом. =(T1-T2)/T1;
Для повышения КПД тепловых машин
Необходимо увеличивать температуру
нагревателя и уменьшать температуру
холодильника. КПД любой реальной
тепловой всегда меньше, чем у машины
Карно:
60)
Явление
переноса. В
термодинамической неравновесной
системе возникают особые неравновесные
процессы, называемые явлением переноса.,
в результате которых происходит перенос
в пространстве энергии, массы и импульса.
К явлениям переноса относятся:
61)
Теплопроводность.
Если в
некоторой области газа средняя
кинетическая энергия молекул больше,
чем в остальных областях, то за счет
хаотического движения молекул и
соударений между ними происходит
постоянное вырабатывание кинетической
энергии молекул по всему объему газа.
Энергия переносится из областей, где
температура газа выше в те области, где
она ниже.
Рассмотрим
одномерный случай: если T1
> T,
то dQ
= - æ (dT
/ dx)
S
dt
;
æ = 1/3 c
p
<v>
<ЛЯМДА> ; c
– теплоемкость, p
– плотность.
62)
Самодиффузия – частный случай диффузии
в чистом веществе или растворе постоянного
состава, при котором диффундируют
собственные частицы вещества. При С.
атомы, участвующие в диффузионном
движении, обладают одинаковыми
химическими свойствами, но могут
различаться по своим физическим
характеристикам
Вязкость или
внутреннее трение. В
потоке газа молекулы участвуют
одновременно в двух видах движений –
хаотическом тепловом и упорядоченном
направленном движении. Пусть <v>
- скорость хаотического теплового
движения, а <u>
- скорость упорядоченного движения
молекул ; u значительно меньше v
; В результате движения молекул, молекулы
из слоя газа, двигающегося с одной
поступательной скоростью u
будут перемешиваться с молекулами из
другого слоя. В результате столкновеня
молекул между собой молекулы из быстрого
слоя будут передавать часть своего
импульса молекулам из медленного слоя
и таким образом тормозиться. По этой
причине в газе возникает своеобразная
сила внутреннего трения, которая
замедляет движение быстрых слоев и
ускоряет движение медленных слоев.
10).Понятие
состояния в классической физике. Границы
применимости классического способа
описания движения частиц.Важным
свойством замкнутых термодинамических
систем является существование у них
равновесных состояний, в которых они
могут пребывать сколь угодно долго.
Для газа, заключенного в некотором
сосуде, равновесным является состояние,
в котором температура, давление и
плотность (или число молекул в единице
объема) в пределах объема газа одинаковы.
Если в каком-нибудь месте этого объема
вызвать местное нагревание или сжатие,
то в системе начнется процесс выравнивания
температур и давления. Этот процесс
будет происходить в течение того
времени, пока имеется внешнее воздействие.
Однако только после прекращения этого
воздействия процесс выравнивания
приведет систему к новому равновесному
состоянию.
В
термодинамике продолжало “работать”
и понятие неравновесного состояния.
Состояния изолированных термодинамических
систем, в которых они, несмотря на
отсутствие внешних воздействий, не
могут пребывать в течение конечных
промежутков времени, называются
неравновесными. Система, первоначально
находящаяся в неравновесном состоянии,
с течением времени переходит в равновесное
состояние.
Границы
применения: А) применима лишь к
сравнительно медленным движениям со
скоростями, заметно меньшими скорости
света в вакууме c≈ 300000 км/с Б)
заключается в ее неприменимости к
описанию явлений микромира, то есть к
движениям тел малой массы в малых
участках пространства.
Моментом
импульса (количества движения)
материальной точки А относительно
неподвижной точки О называется физическая
величина, определяемая векторным
произ¬ведением:
где
—радиус-вектор, проведенный из точки
О в точку А; —импульс материальной
точки; — псевдовектор, его направление
совпадает с направлением поступательного
движения правого
винта
при его вращении от к . Модуль вектора
момента импульса
Моментом
импульса относительно неподвижном оси
Z
называется скалярная величина Lz,
равная проекции на эту ось вектора
момента импульса, определенного
относительно произвольной точки О
данной оси. Момент импульса Lz,
не зависит от положения точки О на оси
Z.
При
вращении абсолютно твердого тела вокруг
неподвижной оси Z
каждая отдель¬ная точка тела движется
по окружности постоянного радиуса ri;
с некоторой скоро¬стью vi.
Скорость vi
и импульс mi
vi
перпендикулярны этому радиусу, т. с.
радиус является плечом вектора mi
vi.
Поэтому можем записать, что момент
импульса отдель¬ной частицы равен
и
направлен по оси в сторону, определяемую
правилом правого винта.
Температура
является важным параметром, определяющим
не только протекание технологического
процесса, но и свойства вещества. Для
измерения температуры в системе единиц
СИ принята температурная шкала с
единицей температуры Кельвин (К).
Начальной
точкой этой шкалы является абсолютный
нуль (0 К).
Для технологических
измерений часто применяют температурную
шкалу с единицей температуры градус
Цельсия (°С),
видов
термометров: цифровые, электронные,
инфракрасные, пирометры, биметаллические,
дистанционные, электроконтактные,
жидкостные, термоэлектрические, газовые,
термометры сопротивления и т.д. У каждого
термометра – свой принцип действия и
своя сфера применения
Шкала Фаренгейта
(Температура кипения чистой воды по
шкале Фаренгейта составила 212°)
Шкала Реомюра
Шкала Цельсия
Шкала Ранкина
(шкала широкого распространения не
получила) 1 град Р. ( °R) равен 5/9 К
Термодинамический
процесс называется обратимым, если он
может происходить как в прямом, так и
в обратном направлении, причем если
такой процесс происходит сначала в
прямом, а затем в обратном направлении
и система возвращается в исходное
состояние, то в окружающей среде и в
этой системе не происходит никаких
изменений.
Всякий процесс,
не удовлетворяющий этим условиям,
является необратимым.
Любой равновесный
процесс является обратимым. Обратимость
равновесного процесса, происходящего
в системе, следует из того, что ее любое
промежуточное состояние есть состояние
термодинамического равновесия;
независимо от того идет ли процесс в
прямом или в обратном направлении.
Реальные процессы сопровождаются
рассеянием энергии (из-за трения,
теплопроводности и т.д.), которая нами
не рассматривается. Обратимые процессы
— это идеализация реальных процессов.
Их рассмотрение важно по 2-м причинам:
1) многие процессы в природе и технике
практически обратимы; 2) обратимые
процессы являются наиболее экономичными;
имеют максимальный термический
коэффициент полезного действия, что
позволяет указать пути повышения КПД
реальных тепловых двигателей.
Пусть Q - теплота,
полученная термодинамической системой
в изотермическом процессе, а T -
температура, при которой произошла эта
передача теплоты. Величина Q/ T называется
приведенной теплотой. Приведенное
количество теплоты, сообщаемое
термодинамической системе на бесконечно
малом участке процесса будет равно dQ
/ T. В термодинамике доказывается, что
в любом обратимом процессе сумма
приведенных количеств теплоты,
передаваемая системе на бесконечно
малых участках процесса равна нулю.
Математически это означает, что dQ/T -
есть полный дифференциал некоторой
функции, которая определяется только
состоянием системы и не зависит от
того, каким путем перешла система в
такое состояние. Функция, полученный
дифференциал которой равен dS= dQ/ T -
называется энтропией. Энтропия
определяется только состоянием
термодинамической системы и не зависит
от способа перехода системы в это
состояние. S - энтропия. Для обратимых
процессов delta S = 0. Для необратимых delta
S > 0 - неравенство Клаудио. Неравенство
Клаудио справедливо только для замкнутой
системы. Только в замкнутой системе
процессы идут так, что энтропия
возрастает. Если система незамкнута и
может обмениваться теплотой с окружающей
средой, ее энтропия может вести себя
любым образом ; dQ = T dS ; При равновестном
переходе системы из одного состояния
в другое dQ = dU + dA ; delta S = (интеграл 1 - 2) dQ
/ T = (интеграл) (dU + dA) / T. Физический смысл
имеет не сама энтропия, а разность
энтропий при переходе системы из одного
состояния в другое.
Количество теплоты,
полученное от нагревателя, не может
быть целиком преобразовано в механическую
работу циклически действующей тепловой
машиной. Это и есть 2ой закон: в циклически
действующей тепловой машине невозможен
процесс, единственным результатом
которого было бы преобразование в
механическую работу всего количества
теплоты, полученного от источника
энергии - нагревателя). Второй закон
связан с необратимостью процессов в
природе. Возможна другая формулировка:
невозможен процесс, единственным
результатом которого была бы передача
энергии путем теплообмена от холодного
тела к горячему. Второй закон имеет
вероятный характер. В отличие от закона
сохранения энергии, второй закон
применим лишь к системам, состоящим из
очень большого числа частиц. Для таких
систем необратимость процессов
объясняется тем, что обратный переход
должен был бы привести систему в
состояние ничтожно малой вероятностью,
практически не отличимой от невозможности.
Самопроизвольные
процессы в изолированной системе всегда
проходят в направлении перехода от
маловероятного состояния в более
вероятное.
Пусть частота
одного колебания ω1=ω, а частота второго
колебания ω2=ω+Δω, причем, Δω<<ω.
Амплитуды обоих колебаний полагаем
одинаковыми и равными A. Для упрощения
расчетов полагаем начальные фазы
колебаний равными нулю. Тогда уравнения
складываемых колебаний будут иметь
следующий вид:
x1=A·cosωt
x2=A·cos(ω+Δω)t
Складывая эти
выражения и применяя тригонометрическую
формулу для суммы косинусов:
(cosα+cosβ=2cos((α-β)/2))cos((α+β)/2)),
получаем x=x1+x2=(2Acos(Δω/2)t)cosωt
Aбиений=|2Acos(Δω/2)t|
Система материальных
точек - такая совокупность материальных
точек, в которой движение каждой точки
зависит от положений или движений всех
остальных точек
В механике внешними
силами по отношению к данной системе
материальных точек называются те силы,
к-рые представляют собою действие на
эту систему других тел (других систем
материальных точек), не включенных нами
в состав данной системы. Внутренними
силами являются силы взаимодействия
между отдельными материальными точками
данной системы. Подразделение сил на
внешние и внутренние является совершенно
условным: при изменении заданного
состава системы некоторые силы, ранее
бывшие внешними, могут стать внутренними,
и обратно.
Скорость изменения
импульса системы равна главному вектору
всех внешних сил, действующих на эту
систему.
В итоге мы получаем
закон движения в неинерциальной системе
отсчета K'
ma' = –mW+F .
(6)
Отсюда мы видим,
что в смысле своего влияния на уравнения
движения частицы, ускоренное поступательное
движение системы отсчета эквивалентно
появлению однородного силового поля,
причем действующая в этом поле сила
равна произведению массы частицы на
ускорение W и
направлена в противоположную этому
ускорению сторону.
Свойства
сил инерции:
1) Силы инерции обусловлены
свойствами самих
неинерциальных
систем, а не взаимодействием тел. Они
существуюттолько в
неинерциальных
системах и не являются
меройвзаимодействия
тел.
5) Все
силы инерции, подобно силам
тяготения,пропорциональным массе тела.
Поэтому в однородном поле сил
инерции,
как и в однородном поле тяготения, все
тела движутся содним и тем же ускорением
независимо от их масс.
Эффективное
поперечное сечение s
равно отношению числа dN таких
переходов в единицу времени к
плотности nv потока
рассеиваемых частиц, падающих на мишень,
т. е. к числу частиц, проходящих в единицу
времени через единичную площадку,
перпендикулярную к их скорости v (n
- плотность
числа падающих частиц): s = dN/nv. Таким
образом, Эффективное
поперечное сечение имеет
размерность площади; обычно оно
измеряется в см2.
Молекулы газа,
находясь в состоянии хаотического
движения, непрерывно сталкиваются друг
с другом. Между двумя последовательными
столкновениями молекулы проходят
некоторый путь l,
который называется
длиной свободного пробега.
В общем случае длина пути между
последовательными столкновениями
различна, но так как
мы имеем дело
с огромным числом молекул и они находятся
в беспорядочном движении, то можно
говорить о
средней длине свободного пробега
молекул <l>.
Минимальное
расстояние, на которое сближаются при
столкновении центры двух молекул,
называется
эффективным диаметром молекулы
d
. Он зависит от скорости сталкивающихся
молекул. Так как за 1 с молекула проходит
в среднем путь, равный средней
арифметической скорости <v>,
и если <z>
≈ среднее число столкновений, испытываемых
одной молекулой газа за 1 с, то средняя
длина свободного пробега
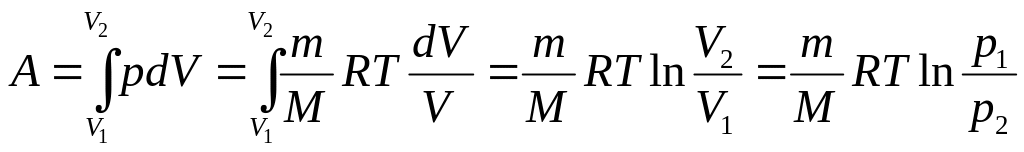 .
.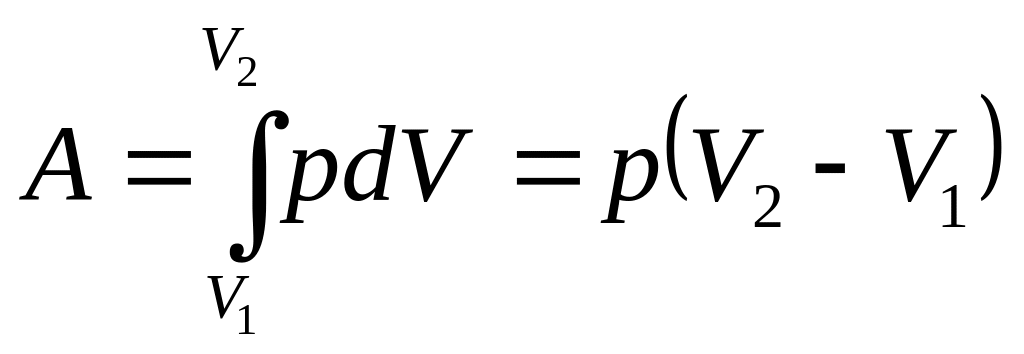 .
.![]() .
.54) Адиабатный процесс – термодинамический процесс, при котором система не получает теплоты извне и не отдает ее.
58) Идеальная тепловая машина Карно.
![]()
1) Теплопроводность (перенос энергии) ; 2) диффузия (перенос массы) ; 3) внутренние трение или вязкость (перенос импульса)
63) Вязкость - Явление вязкости связано с возникновением сил трения между слоями жидкости или газа, которые перемещаются параллельно друг другу, но с разными скоростями
![]()
30). Моменты импульса и силы относительно точки и неподвижной оси. Уравнение моментов для системы материальных точек.
43)Измерение температуры
56)Обратимые и необратимые тепловые процессы.
57)Энтропия.
57) Второй закон термодинамики.
37)Результирующее движение при этих условиях можно рассматривать как гармоническое колебание с пульсирующей амплитудой. Такое колебание называется биением.
Сложение гармонических колебаний одного направления и взаимно перпендикулярных колебаний.
- Одного направления
- Взаимно перпендикулярные
11)Внутренние и внешние силы.
33)Силы инерции при ускоренном поступательном движении системы отсчета. Свойства сил инерции.
2) На силы инерции не распространяется третий закон Ньютона.
3) Силы инерции приложены к центру масс тела.
4) Силы инерции являются внешними силами. В связи с этим внеинерциальных системах отсчета в общем случае не может быть замкнутых систем точек или тел.
59).Эффективное сечение рассеяния. Средняя длина свободного пробега молекул.
![]()
