
4. Холинергические механизмы
В последние годы широко и интенсивно изучается роль холинергических механизмов в формировании боли. Известно, что холинергические вещества возбуждают гиппокамп, введение морфина с холинергическими препаратами резко усиливает аналгезию. Обнаружено (А. К. Ярош, 1987), что у интактных крыс активация холинергической системы и накопление ацетилхо-лина способствуют аналгезии.
Активация холинергической медиации халантолином уменьшает двигательную реакцию на боль, но усиливает интенсивность эмоциональных проявлений. При блокаде Н- и в меньшей степени М-холинорецепторов в первые трое суток послеоперационного периода обнаружено ослабление ориентировочной реакции на боль Введение холиномиметика прозерина, а также М-холинергических веществ в зону центрального околоводопроводного вещества усили-
34
вает обезболивающий эффект, что является реп тыаюм ьовлече ния ацетилхолина ч реакцию обезболивания на уровне 1|К1Н1Ю мозга (А В Вальдман, 1980, Е В [оланои, 1979) Лмиааы.я холинергической сжгемы усиливаег, а б юката <-!- о^ 1аб ик ' \и)р финовую анестезию Высказывается предно ю/кьнпе ((1 \\ "1 и тап а1 а11 1984), чю связывание ацеттхо шна с онрек [сннымч центральными мускариновыми рецеторами ^ти\1\1ир\е1 высвобо/к дение ониоидных пепгидов, вовлеченных в пресс ана.ш.^ю
5. ГАМК-ергические механизмы
Гам\1ас1\1ино\1асл>1ная к1К!01с1 ^Г^М1\( регулирует болевую чхвствтсльнос гь, подавши дмиц^оьальгю по веденческие реакции на боль
Ноцицептивное воздейсгвие сопровождае',ся повышением уро^з ня ГАМК и угнетением ее фермешативнои ннактивации в стр\1\ турах переднего мозга (Ю Д Ишаюв, 1982, Ю Д Игнатов Б В. Андреева, 1982) Снижение в \или акти.коии фермеш 1 ГАМК трансферазы и уменьшение и ре^\льт^ге ^го'о ниактивс ции рассматривается как защитный механизм, напрев юиныи н.1 усиление процессов торможения (Г Э 1ал\стян, 19821 Ьоль а^ш вируя ГАМК и ГАМК ергическую передач\, обеснечиваег а-гаша цию к болевому стрессу
Введение ГАМК позитивных препаратов вызывает ана 1ге1и'о Например, введение агонисгов Г\ЧК рецепюров (бак юфен, ю-пакин) уменьшает хроническую боль \ животных и нормализ\е1 их поведение Учитывая это. считают целесообразным при хронической боли назначать ГАМК-позитивные среде гва (баклофюп депакин) с наркотическим аналгетиком типа промеюла (Ю Д И' натов, 1986)
6. Различные образования нервной системы
Контроль болевой ч\вивите'1Ьг10^п1 со ществляется множественными стр\кт\рами ЦНС ьаждая ш кот^ рых функционирует как самостоятельное обра-юв^т! 1^ ломт^^ се все они входят в состав сложной сисгемы аш ишпшщпни а)^! логично тому, как ощущение боли являегся пез\ иисиом ^ '1е1ра"111в ной функции ЦНС Возникновение боли. [\а'л \ л\^ 'гнор!! 'нь зав!' сит не только от интенсивности ноцицепгивчч-о поипе/иеппч но и от состояния различных звеньев ангинои^'^1]. ^вн^н ^исюмы
На уровне спинного мозга обнаружены I»,' механик, л 110131)-ления боли—эго сегменгарныи конт[юль и ^^>-1<_\!с1 н»1^ \о щщ^го контроля Сегметарный контроль осмце^и) г^оюя на \ ;чяи1С ^ад них рогов спинного мозга в желагино^нои ^бисШ ин С опасно воротной теории Р Мелыака и П Уолла (19ь')1 во^гр^ятие боли
35
зависит от баланса между притоком импульсов по толстым нервным волокнам, возникающих в результате действия неповреждающих факторов (например, поглаживание, растирание, электрораздраже ние, акупунктура), и по нервным проводникам малого диаметра (как следствие действия на ткани повреждающих факторов) Если доминирует приток импульсов по таким болевым нейронам, активируются спинно-таламические пути и появляется боль Если доминирует приток импульсов по толстым волокнам нейрона, возникает пресинаптическое торможение (входные ворота для болевой инфор мации закрываются — отсюда и название теории боли — «теория ворот»), следовательно, спинно-таламические пути не активируются и боль не возникает Жизненность этой концепции подтверждает эффективность обезболивания при поглаживании или растирании кожи, после удара, чрезкожной стимуляции, акупунктуре По совре менным данным, эти обезболивающие эффекты объясняются не только сегментарным контролем, но и включением надсегментар ных механизмов контроля, в том числе и гуморальных, особенно опиоидных
Обнаружена гипоталамо спинальная система торможения боли Аксоны нейронов паравентрикулярного, медиального преоптиче-ского ядра, дорзальных отделов гипоталамуса спускаются в спинной мозг и, заканчиваясь в желатинозной субстанции, осуществляют супраспинальный контроль болевой чувствительности на уровне спинного мозга Эта система активируется аналгетиком циклозо цином (В Н Шток, 1988)
Важное значение в обезболивании на уровне спинного мозга принадлежит энкефалинергическим образованиям, норадреналину и серотонину в желатинозной субстанции задних рогов, опиатным рецепторам Местом приложения действия морфия и морфомимети-ков является и желатинозная субстанция спинного мозга Этот обезболивающий эффект блокируется налаксоном. Значение серото нина в обезболивании на спинальном уровне подчеркивается наблюдением, когда его уменьшение в спинном мозге уменьшает интенсивность морфиновой анестезии Однако А А Панин с соавт (1984) считают это следствием влияния нисходящих волокон, а не существованием спинальных серотонинергических нейронов В настоящее время многие исследования подтверждают, что эндогенные опиаты, как и препараты опия, блокируют выделение субстанции Р задних рогов спинного мозга Уменьшение или отсутствие медиатора боли — субстанции Р является, вероятно, тем механизмом, который вызывает обезболивание на уровне задних рогов спинного мозга, т е. осуществляет «воротный» контроль боли
Система супраспинального контроля обусловлена влиянием на спинной мозг различных структур головного мозга Это связано с такими структурами, как перивентрикулярные зоны, периакведук
36
тальные субстанции, ядра шва ствола мозга (Е. О. Брагин, 1985)
По данным В Н Шток (1988), антиноцицепция зрительного бугра связана с ретикулярным таламическим ядром, при стимуляции которого тормозные импульсы идут к другим ядрам зрительного бугра
Установлено, что контроль болевой чувствительности системой ЦСОВ — ядра шва не зависит от влияния опиатной системы В клинике при сильных болях у неоперабельных больных используется стимуляция через вживленные электроды ядер гипоталамуса и ЦСОВ, составляющих важное звено в противоболевой системе (В П Лебедев с соавт , 1986) При этом воздействие постоянного тока и прямоугольных импульсов с частотой 77 Гц через 10—15 минут после включения тока вызывает адаптацию к боли, которая продолжается 8—12 часов после его выключения Эксперименты на животных и клинические наблюдения показывают, что раздражение центрального серого околоводопроводного вещества, ядер шва, черной субстанции, синего пятна, ростральной части хвостатого ядра и перегородки вызывают состояние аналгезии. Установлено, что эти эффекты связаны с такими гуморальными факторами, как эндор-фины и энкефалины, серотонин, норадреналин, а также активацией ГАМК и глицина Есть основания полагать, что нисходящие пути антиноцицептивной системы являются норадрен-серотонин-дофаминергическими Некоторые нисходящие тормозные влияния представлены на рис 14
Центральные структуры головного мозга оказывают не только нисходящее влияние на спинальном уровне, но и модифицируют болевые сигналы в местах их переключения различных центральных структур мозга Имеются многочисленные наблюдения, когда раздражение ряда структур мозга дает уменьшение боли или эффект обезболивания и, наоборот, их разрушение усиливает боль Последнее свидетельствует о том, что выключение отдельных компонентов антиноцицептивной системы усиливает боль и косвенно подтверждает постоянное тормозное влияние АНЦ-системы на болевые проводящие пути и формирование боли
Аналгетическая система мозга включает ядра гипоталамуса (паравентрикулярные и медиальные преоптические ядра дорзаль-ного отдела), центральное серое околоводопроводное вещество мозга, ядра шва, гигантоклеточное ядро Как уже говорилось, ги-поталамо-спинальная аналгетическая система заканчивается в желатинозной субстанции и активируется аналгетиком циклозицином.
При активации медиальных ядер гипоталамуса, центрального серого околоводопроводного вещества, ядер шва и ретикулярной формации развивается мощная аналгезия. При разрушении же центрального пучка покрышки дорзомедиальных ядер гипоталамуса, таламуса введение столбнячного токсина в задние рога спин-
37
Рис 14 Нисходящие пу ти к дорсальному рогу
Прямые проекции к дор зальному рогу начинаются от клеток ядра Эдингера — Вестфатя ретикулярной фор мации моста голубого локу са и ядра большого шва Про екнии от околоводопроводнои серой области к большому 1нв\ рассматриваются важ ными для стимуляционно вы званной аналгезии, хотя все нисходящие системы являют ся важными модуляторами соматосенсорной передачи (К Мс)с|е\мс7 В 5апс1ге\у 1485)
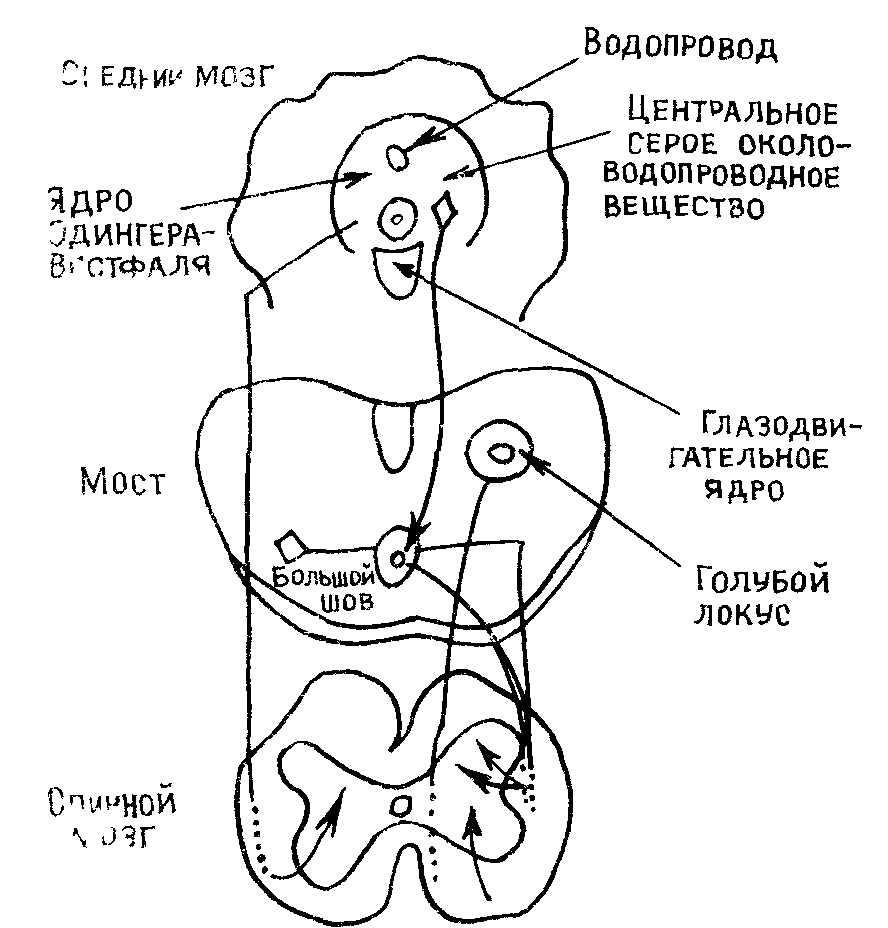
11ого мены, •фигочьныи ихгор, ядра тройничного нерва резко уси 1ИВДСТ бо и рые 01Ч\ ни ння ити вызывает спонтанные боли (Р Мель-',лк с со^в I \Ч~^, Г Н Крыжановскии, 1973, 1974, 1980) Таким обрчо»!, выктюченне отютьныу звеньев антиноцицептивнои систе мы пон^жасг 1]ор01 бо ювои ч\ вствительности и, облегчая проведение ноцниепгивнык и\и1\ 1ьсов. усиливает боль
С('У1и юи.|41орная обькгь кор1>1 яв тяетс.я важным звеном анти-ноцичепгчи 1»- > <1р\ шение выбывает неукротимую боль и гиперпа-тию, которые по мнению Р А Д\риняна (1980), могут возникать даже в огвет на тактильное раздражение Роль коры в антино цн цеп ции ^ак 1ючается в подав юнии защитных и сомачовегетатив ных реф юксов на боль, что связано с угнетением нейронов IV— \ II пла<т11н заднего рога (В Н Шток, 1988)
Говоря о значении различных образовании ЦНС в антиноцицеп-ции, следует, подчеркнуть ее большую роль, ибо хорошо известно, что при определенном насгрое, ожидании боли человек усилием воли может активировать антиноцицептивную систему, в результате чего спокойнее переносит болевые воздействия очень большой интенсивности В коре мозга нисходящие тормозные влияния идут от соматосенсорнои обтасти коры и ее моторной зоны Причем, 01 коры торможение синаптическои передачи осуществляется как на уровне Гс-мамуса, так и контрлатерально, на уровне заднего ро1 а спинною мои а Что касается тормозных влияний от ЦСОВ-ядра шва, ю они двусторонние и проецируются также на уровне
,{8
задних рогов спинного мозга Тормозное влияние коры осуществляется как прямопостсинаптическое (через вставочные нейроны), так и пресинаптическое (М Циммерман, 1985).
Примерная схема нисходящих тормозных влияний при боли представлена на рис 15.
В последнее время сделана попытка выделить 4 основные аналь-гетические системы нейрональную опиатную — энкефалинергиче-скую, нейрональную неопиатную — норадреналин —, серотонин—, дофаминергическую, гормональную опиатную (эндорфиновую) и гормональную неопиатную (пептиды и другие регуляторы).
Анализируя боль различных звеньев антиноцицептивной системы, можно заключить, что опиоидный и серотонинергический механизмы регулируют болевой порог синергентно, хотя есть сомнения, что серотонинергический механизм ограничивает болевую афферен-тацию Адренергический механизм способен увеличивать или уменьшать болевую чувствительность Каждая анальгетическая система — опиатная, моноаминергическая, холинергическая, ГАМК-ер-гическая, гормональная и нервная—функционирует не изолированно, а в тесной связи и зависимости друг с другом и другими системами, что позволяет как подавлять боль, так и избегать ее.
Патогенез острой боли
Происхождение боли в настоящее время объясняется несколькими теориями. В конце XIX века практически одновременно
появились две взаимоисключающие друг друга теории механизма боли Это «теория специфичности» Фрея и «теория интенсивности» Гольдшейдера
Согласно «теории специфичности», боль возникает в результате возбуждения специальных болевых рецепторов (ноцицепторов) раздражением, сила которого превышает порог болевой чувствительности Эта теория предполагает наличие проводящих болевых путей и центральных их образований, благодаря чему боль и расценивается как специфическое чувство.
По «теории интенсивности» формирование боли связано с раздражением рецепторов и особенно нервных проводников, ответственных за формирование основных чувств (зрения, вкуса, слуха, обоняния, осязания), любым раздражителем, сила которого превышает определенный порог. Поэтому появление боли в результате избытка стимуляции стало основой «теории интенсивности».
Обе теории имеют свои достоинства и недостатки. Известно, что боль возникает преимущественно при раздражении свободных нервных окончаний, болевые импульсы проводятся по А-дельта
39
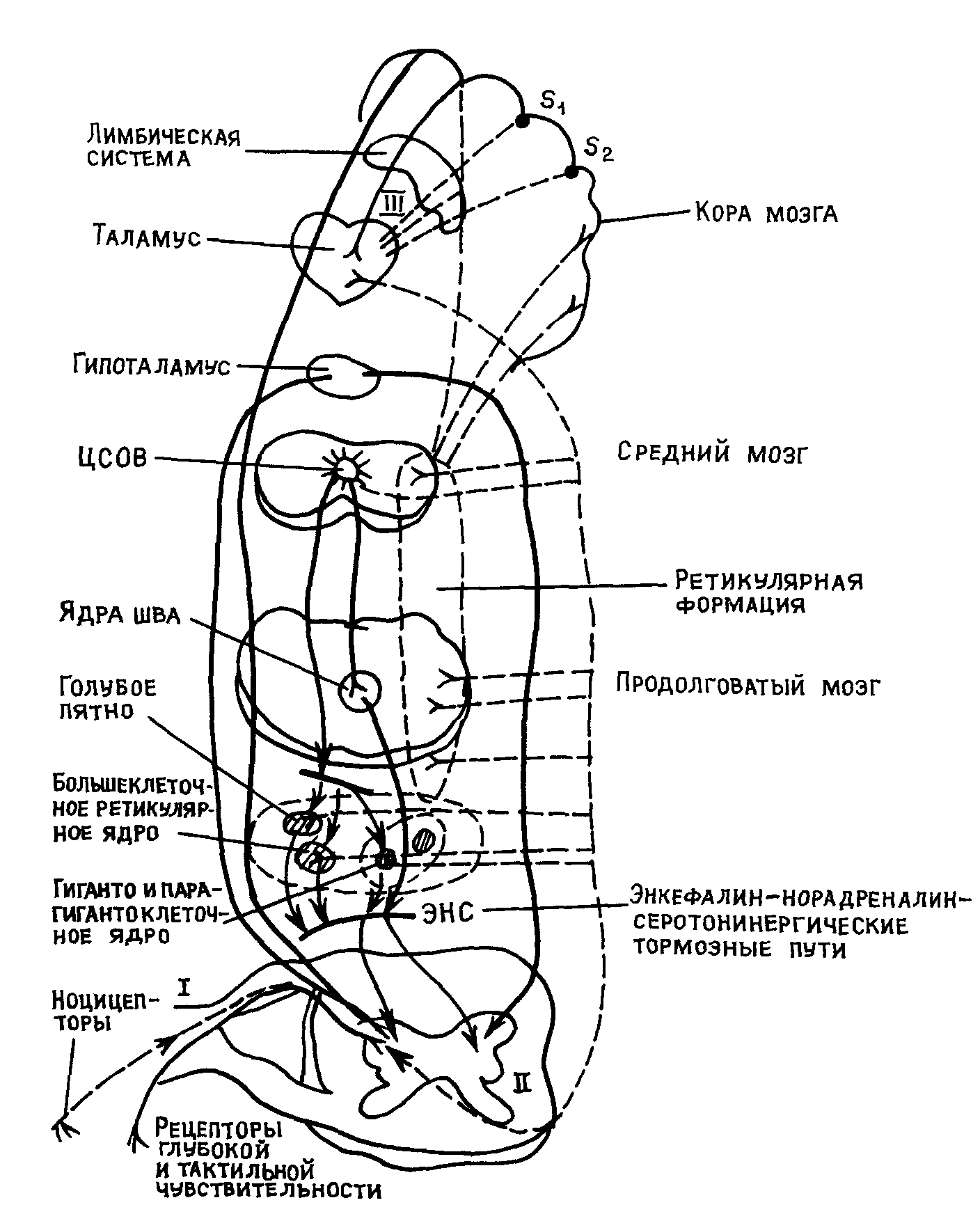
Рис 15 Примерная схема нисходящих и других антиноцицептивных тормозных влиянии
—————— нисходящие и другие тормозные пути
— — — болевые пути (1, II, 111 — нейроны болевых путей)
и С-волокнам, имеются определенные болевые центры — заднего рога спинного мозга, ретикулярная формация, таламус, соматосен сорная область коры мозга Однако эта теория не объясняет, почему боль развивается при действии любых сверхсильных раздражителей, в том числе и других рецепторов
По мнению Ю П Лиманского (1985), теория специфичности важна для понимания качества, интенсивности, продолжительности боли, ее локализации, но она не может объяснить гипералгезию, отраженные боли, неудачи хирургического лечения хронической боли путем перерезок периферических или центральных болевых путей
В то же время теория интенсивности, хотя и не учитывает специализации рецепторов, но подчеркивает важную роль сумма ции сенсорного взаимодействия между быстро и медленно проводящими путями в происхождении боли
Наибольшее распространение в мире получила теория Р Мель-зака и П Уолла, получившая название теории воротного контроля (воротной теории) Она заключается в том, что желатинозная субстанция заднего рога (II и III пластины) обеспечивает контроль поступающих в спинной мозг афферентных импульсов и выступает в роли ворот, поэтому теория и получила свое название Причем, важное значение принадлежит Т-клеткам желатинозной субстанции Под влиянием импульсов, поступающих по толстым миелино-вым А-волокнам, происходит кратковременное возбуждение Т-кле ток и клеток желатинозной субстанции, где происходит пресинап-тическое торможение терминалей, в этих условиях болевые импульсы не проходят дальше в центральные мозговые структуры и боль не возникает По современным представлениям закрытие «ворот» связано с образованием энкефалинов, которые тормозят реализацию важнейшего медиатора боли — субстанции Р Если увеличивается приток афферентации по А-дельта и С-волокнам, активируются Т-клетки и ингибируются клетки желатинозной субстанции, что снимает ингибиторный эффект нейронов желатинозной субстанции на терминали афферентов с Т-клетками Поэтому активность Т клеток превышает порог возбуждения и возникает боль вследствие облегчения передачи болевых импульсов в мозг «Входные ворота» для болевой информации в этом случае открываются, и импульсы по волокнам, прежде всего неоспинно-таламического тракта, попадают в вентробазальный таламус и соматосенсорную область коры, а по палеоспинно-таламическому тракту в ретикулярную формацию, медиальный интраламинарный таламус, лимбические образования и двигательную зону коры Таким образом, клетки желатинозной субстанции подавляются афферентацией по тонким и возбуждают ся афферентацией по толстым нервным волокнам
По современным представлениям «открытие ворот» связано с
41
образованием субстанции Р и облегчением проведения болевых импульсов в мозг для формирования ощущения боли По мнению авторов этой теории, соотношение афферентации, поступающей в спинной мозг по толстым миелиновым А-волокнам, и болевой им-пульсации по А дельта и С-волокнам играет решающую роль как в формировании боли, так и в нормальном восприятии окружающего мира. Важным положением этой теории является учет центральных влияний на «воротный контроль» в спинном мозге, ибо такие процессы, как жизненный опыт, внимание оказывают влияние на формирование боли Следует отметить, что ЦНС осуществляет контроль сенсорного входа за счет ретикулярных, кортико-спинальных и пирамидных влияний на воротную систему Например, Р Мельзак (1981) приводит такой пример: женщина неожиданно обнаруживает у себя уплотнения в груди и, беспокоясь, что это рак, может вдруг почувствовать боль в груди Если ее беспокойство будет продолжаться, боль может усиливаться и даже распространиться на плечо и руку Если врачу, к которому она обратится, удастся убедить ее, что это уплотнение не представляет опасности, может наступить моментальное прекращение боли
Жизненность этой теории подтверждается клинической практикой, где широкое применение тактильного раздражения, электростимуляции кожи и акупунктуры облегчает или исключает болевые эффекты, т. к в этом случае превалирует поступление аффе рентации по толстым миелиновым А-волокнам, роль которой в формировании нормального ощущения подтверждает теория Мельзака и Уолла
К недостаткам теории необходимо отнести утверждение, что торможение проведения импульсов осуществляется в пресинаптиче ской мембране и только на уровне спинного мозга (Р А Дури-нян, 1981).
Большой интерес представляет теория происхождения хронических болей, которая была сформулирована в 1973, 1974, 1979 гг. Г Н. Крыжановским и заключается в том, что хроническая боль возникает в результате подавления тормозных механизмов, особенно на уровне задних рогов спинного мозга и таламуса При этом в мозге формируется генератор возбуждения (своего рода «станция отправления»). Под влиянием экзогенных и эндогенных факторов в определенных структурах ЦНС вследствие недостаточности тормозных механизмов возникают генераторы патологически усиленного возбуждения, активирующие положительные связи, вызы вая эпилептизацию нейронов одной группы и повышение возбудимости других нейронов
Как уже говорилось ранее, в формировании острой боли выделяют первичное быстрое, локализованное болевое ощущение, и такая боль получила название эпикритической Эта быстрая лока
42
лизованная первичная или эпикритическая боль эволюционно является более молодой и ее формирование связывают с передачей ноцицептивной информации по миелиновым волокнам группы А с участием неоспинно-таламического тракта В последующем на смену острой боли приходит тупое вторичное нелокализованное диффузное чувство боли, получившее название протопатической боли Ее формирование происходит на более поздних этапах развития и связано с образованием медиаторов боли и медленной передачей болевой информации по безмиелиновым волокнам группы С, преимущественно по палеоспинно-таламическому тракту В классическом виде эпикритическая и протопатическая боль наблюдается при уколе, ожоге, разрезе При анализе болей различной локализации отмечено, что внутренние органы очень скудно снабжены ноцицепторами. Они реагируют только на растяжение или сокращение соответствующих органов или их сосудов и не дают болевого эффекта при уколах, разрезах, ожогах (сердце, печень, почки, селезенка, яичники, плевра, перикард, брыжейка, мочевой пузырь) Висцеральные боли характеризуются как протопатические Они более диффузны, носят аффективный характер и легко провоцируются дополнительными воздействиями Характер висцеральных болей, по мнению С. И Франкштейна, Л Н Сергеева (1985), определяется недостаточностью тормозных механизмов, в норме уменьшающих формирование боли
Как показали исследования Г Н Крыжановского (1980), соматические боли при блокаде тормозных синапсов также носят прото патический характер
Следует отметить, что современное медицинское образование дает концепцию исключительно острой боли, хотя хроническая боль, ее этиология, патогенез и особенно лечение имеют большое значение Дело в том, что хроническая боль еще недостаточно изучена, и только в последние годы появились фундаментальные иссле дования в этом плане (Г Н Крыжановский, 1980, обзор ВОЗ, 1986, Р ^ \Уа11, 1984, Р Мельзак, 1981, Ю. П Лиманский, 1986; К Мас1е\У1сг, В 5ап(1ге\у, 1986)
Следует отметить различие не только патогенеза, но и так тики лечения острой и хронической боли Так, при острой боли лечение направлено на этиологию —"устранение причины боли, при хронической, наряду с этиотропным методом, широко используется облегчение боли
Анализируя течение боли, Р ^ \Уа11 (1979) выделил три фазы — ближайшую, острую и хроническую Он считает, что во время ближайшей фазы боль не успевает сформироваться, начинается лишь активная борьба с источником повреждения, попытка защи ты, уход в безопасное место, призыв к помощи И только в острой фазе, когда организм сделал попытку обезопасить себя или уже
43
обезопасил, возникает боль, которая информирует организм о необходимости создать условия для выздоровления и устранения возможных последствии повреждения В хронической фазе боль резко ограничивает или полностью прекращает движение, формируется состояние депрессии В связи с этим Р О \Уа11 считает, что боль является для организма сигналом к переходу его в состояние отдыха и восстановления
На рис 16 представлен патогенез острой боли Ее возникновение связано с активацией ноцицепторов и передачей болевой информации по специфическим чувствительным нервным волокнам, с существенной интеграцией болевой информации на уровне спинного мозга, ретикулярной формации среднего мозга, таламуса, а также соматосенсорной области коры и лимбических образований переднего мозга При действии на ноцицепторы болевых раздражителей возникает их деполяризация, и импульсы в первую очередь поступают по быстропроводящим волокнам группы А дельта с после дующей активацией и безмиелиновых С-волокон Передача импульсов осуществляется с помощью медиатора боли субстанции Р, которая, высвобождаясь из пузырьков в области ноцицепторов, вызывает дополнительное возбуждение, с резким увеличением потока болевой информации в мозг, что неразрывно связано с другими биохимическими изменениями (гистамин, ацетилхолин, серо тонин, кинины, простагландины, изменение рН) и приводит к смене острой локализованной боли на разлитую или протопатическую
Вещество Р выделяется не только в области рецепторов, но и в задних рогах спинного мозга, в местах переключения болевой информации (в верхней части мозгового ствола, среднего мозга, особенно в области сильвиевого водопровода), здесь имеются также вещества, оказывающие противоположное влияние на проведение боли, а следовательно, и ее формирование Так, субстанция Р, глютамат возбуждают ноцицептивные нейроны, а глицин, серото-нин, норадреналин, дофамин, энкефалины, соматостатин, холи-цистокинин, нейротензин тормозят их активность (Ш О ШЛНз, 1985) Ноцицептивная информация поступает в задние рога спинного мозга и в головной мозг (преимущественно в желатинозную субстанцию) по восходящим ноцицептивным путям (спинно-тала-мический тракт, спинно ретикулярный и спинно-мезэнцефаличе-ский), которые проходят в антеролатеральном (передне боковом) квадранте спинного мозга Перерезкой его (хордотомия) можно добиться обезболивания, хотя у человека затем болевое чувство может восстановиться, что говорит об участии в передаче боли и других путей
Исследованиями XV ^ ШЛНа (1985) доказано, что клетки спинно таламического тракта возбуждаются аппликацией глютамата, субстанции Р и тормозятся мет и лей-энкефалином, серотонином,
44
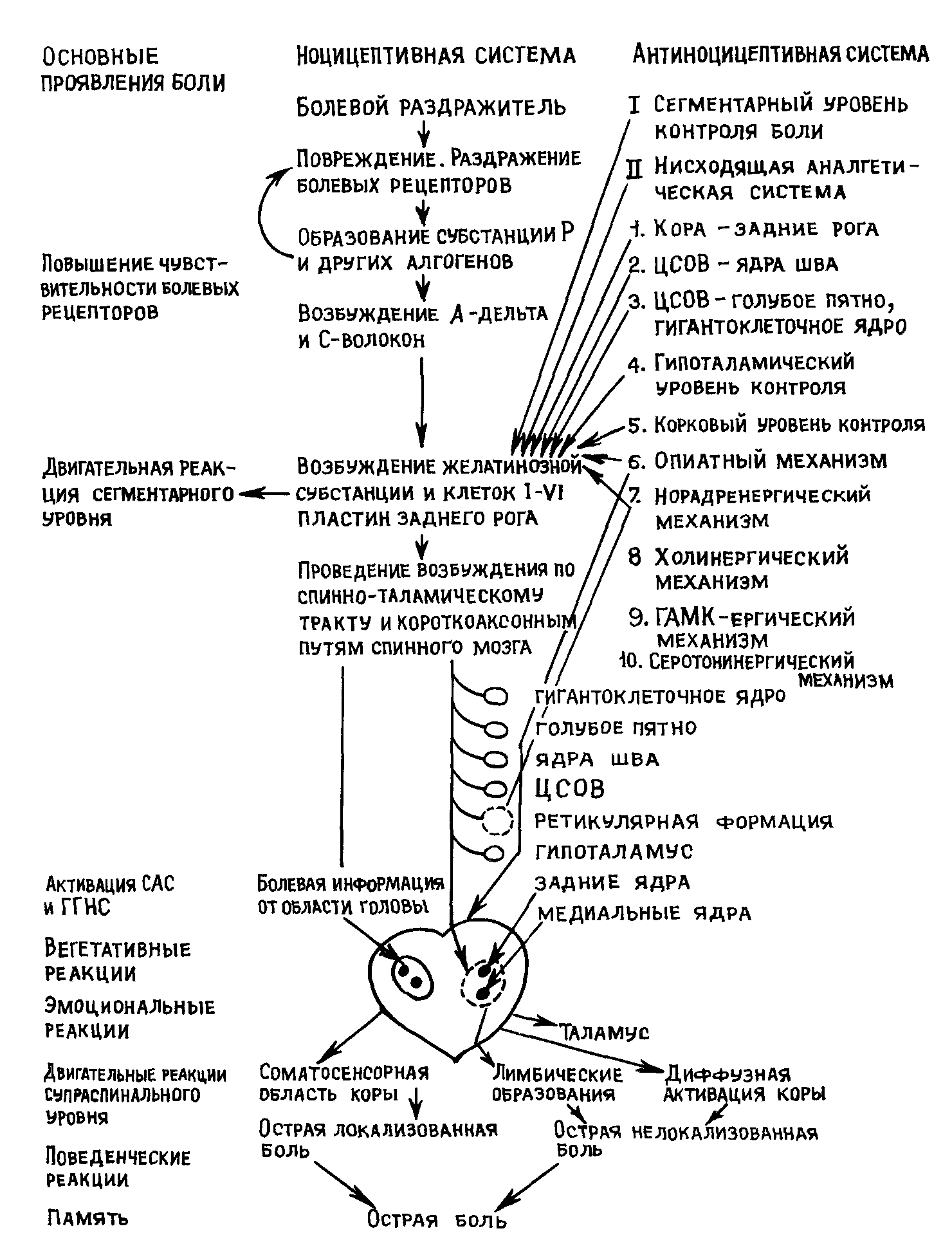
Рис 16 Патогенез острой боли 45
норадреналином, дофамином, глицином, гамма-аминомасляной кислотой, ацетилхолином Переключение болевой информации на спин-но-ретикулярный тракт происходит во II и VII пластинах заднего рога спинного мозга Одна часть информации проходит по перекресту (особенно в пояснично крестцовом отделе) на противоположную сторону, другая же, не прекращаясь, поднимается по это му тракту в латеральные ретикулярные ядра, ядра нижней оливы и другие Установлено, что ретикулярная формация принимает учас тие в мотивационно-аффективном компоненте болевого ответа
Ноцицептивная информация по спинно-мезэнцефалическому тракту поступает латерально в околоводопроводное серое вещество, клиновидное ядро, ядра Даркшевича, Эдингера — Вестфаля По мнению '\У ^ \У1И15 (1985), болевая информация, поступающая в мозг, не только передается, но и модулируется (изменяется) Например, нейрохирургические перерезки медиальной части среднего мозга ослабляют боль, повреждение центрального серого околоводопроводного вещества вызывает гипералгезию, а если возбуждение появляется около серого вещества — развивается аналгезия Болевая информация проходит и по спинно цервикаль-ному тракту, который начинается от III, IV и V пластинок заднего рога спинного мозга и поступает в шейные ядра, а уже оттуда по аксонам этих перекрещивающихся ядер к медиальным лемнис-
кам
Таким образом, вся болевая информация попадает в верхнюю часть мозгового ствола, среднего мозга, особенно сильвие-вого водопровода, где обнаружено большое количество субстан ции Р и эндорфинов Благодаря этому именно в этих образованиях осуществляется регуляция (фильтр) болевой информации
Ноцицептивная информация проходит и через гипоталамус, включая его в патогенетическое звено боли Мы уже знаем, что гипоталамусу принадлежит большая роль в синтезе и секреции энкефалинов и эндорфинов, а также в усилении образования гипо физом тропных гормонов и бета липотропина, из которого и образуются эндогенные опиаты гормонального происхождения, кроме того, активируется и симпатоадреналовая система Важную роль в формировании боли играет зрительный бугор (его вентропосте ролатеральное и вентропостеромедиальное ядро, медиальный тала-мус, задняя группа ядер таламуса), который связан с соматосен-сорной областью, лимбическими образованиями, двигательной и другими областями коры Именно с участием этих структур и происходит формирование ощущения острой боли Учитывая, что фор мирование боли обязательно сопровождается активацией антино-цицептивной системы, хотя бы вкратце рассмотрим, что же влияет на уменьшение или исчезновение боли Это прежде всего информация, которая поступает по толстым волокнам и на уровне зад
46
них рогов спинного мозга,усиливает образование энкефалинов, за счет которых на сегментарном уровне уменьшается образование субстанции Р и передача болевых импульсов по спинно-таламиче-скому тракту На уровне ствола мозга включается нисходящая аналгетическая система гигантоклеточное ядро ядра шва, которая посредством серотонин , норадреналин-, энкефалинергиче-ских механизмов оказывает нисходящие влияния на задние рога и таким образом на болевую информацию За счет возбуждения симпато-адреналовой системы и включения гемодинамических механизмов также тормозится передача болевой информации, и это является важным фактором усиления образования эндогенных опиа-тов Наконец, за счет возбуждения гипоталамуса и гипофиза акти вируется образование энкефалинов и эндорфинов, а также усиливается прямое влияние нейронов гипоталамуса на задние рога мозга На всех релейных участках мозга (задние рога, ЦСОВ, тала-мус) имеется обилие опиатных рецепторов, с которыми соединяются эндогенные опиаты (энкефалины и эндорфины) Кроме этого, у человека установлены и корковые влияния на все участки переключения болевой информации и двигательную активность
Патогенез хронической боли
Различные нарушения тканей и нервной системы могут вести к формированию хро нической (патологической) боли При длительном повреждении тканей (воспаление, переломы, аутоим-мунные процессы, опухоли) формирование боли происходит так же, как и при острой, только постоянная болевая информация, вызывая резкую активацию гипоталамуса и гипофиза, симпато ад-реналовой системы, лимбических образований мозга,сопровождается более сложными и продолжительными изменениями со стороны психики, поведения, эмоциональных проявлений, отношения к окружающему миру, отличительной особенностью которого является «уход больного в боль» Если при острой боли мы наблюдаем не редко самопроизвольное ее купирование за счет активации анти-ноцицептивной системы, то при хронической за счет преобладания активности болевой системы над противоболевой обезболивания не наступает В формировании хронической боли (например, при воспалении), вероятно, в связи с повышением чувствительности ре цепторов, снижением болевого порога возникает боль в ответ на неболевые воздействия (например, касание, легкое давление, дви жение)
Однако при повреждении различных отделов нервной системы механизмы хронической боли различны Так, нарушения в области латерального таламуса, включающего вентропостеролатеральное ядро, вызывают синдром жгучей, нелокализованной боли на проти-
47
воположной стороне с выраженными эмоциональными компонен тами Это объясняется тем, что приток афферентной информации не ограничивается и воспринимается как боль Повреждение ни сходящих аналгетических путей или спинного мозга на уровне зад них рогов также является важным фактором формирования хрони ческой боли
Даже морфиновая анестезия зависит от целостности нисходя щих аналгетических путей, ибо при их повреждении морфин умень шает свой аналгетический эффект Однако хроническую боль в спин ном мозге можно уменьшить активацией таламических проводящих путей, ответственных за контроль боли
Фантомные боли (боли в ампутированных конечностях) объяс няются в основном дефицитом афферентной информации и соглас но теории Мельзака и Уолла (1965) в результате этого тормозное влияние Т клеток на уровне рогов спинного мозга снимается, а лю бая афферентация из области заднего рога воспринимается как болевая В некоторых случаях хроническая боль может возникать без каких либо внешних раздражении за счет того, что перифери ческие афференты продолжают возбуждаться как, например, при повреждении или регенерации нерва, когда возможны переход воз буждения с одного аксона на другой или возникновение спонтан ного потенциала действия распространяющегося в любом направ лении Причем, при повреждении нерва (перерезка, травма) сни жается пре и постсинаптическое торможение в заднем роге спин ного мозга, а при ризотомии (перерезке заднего корешка между спинальным ганглием и задним корешком) резко повышается чув ствительность клеток заднего рога к субстанции Р, соматостати ну, холецистокинину Электрофизиологически после деафферента ции в первые месяцы обнаружены участки (преимущественно в об ласти V пластинки, получающей суммарную соматосенсорную и но цицептивную информацию) со спонтанной, нерегулярной гиперак тивностью Именно это и расценивают как важный механизм хро нической деафферентационной боли Однако через несколько меся цев после денервации спонтанная электрическая активность пони жается в клетках заднего рога и повышается на других централь ных уровнях (на уровне таламуса — в вентробазальном комплексе и медиальной таламической области) Кстати, если на начальных этапах денервации субстанция Р в заднем роге уменьшается, то в последующем она снова увеличивается
До сих пор не установлено является ли дорзальный рог час тично ответственным за деафферентационную боль или участвует в подавлении нарушенной активности заднего рога Вследствие поте ри или уменьшения афферентного притока возникает деафферента ционная боль, и происходит перестройка центральных болевых пу тей В результате экспериментальных исследований хронической
48
боли установлено, что животные отгрызают деафферентированную конечность
Патогенез хронической боли представлен на рис 17
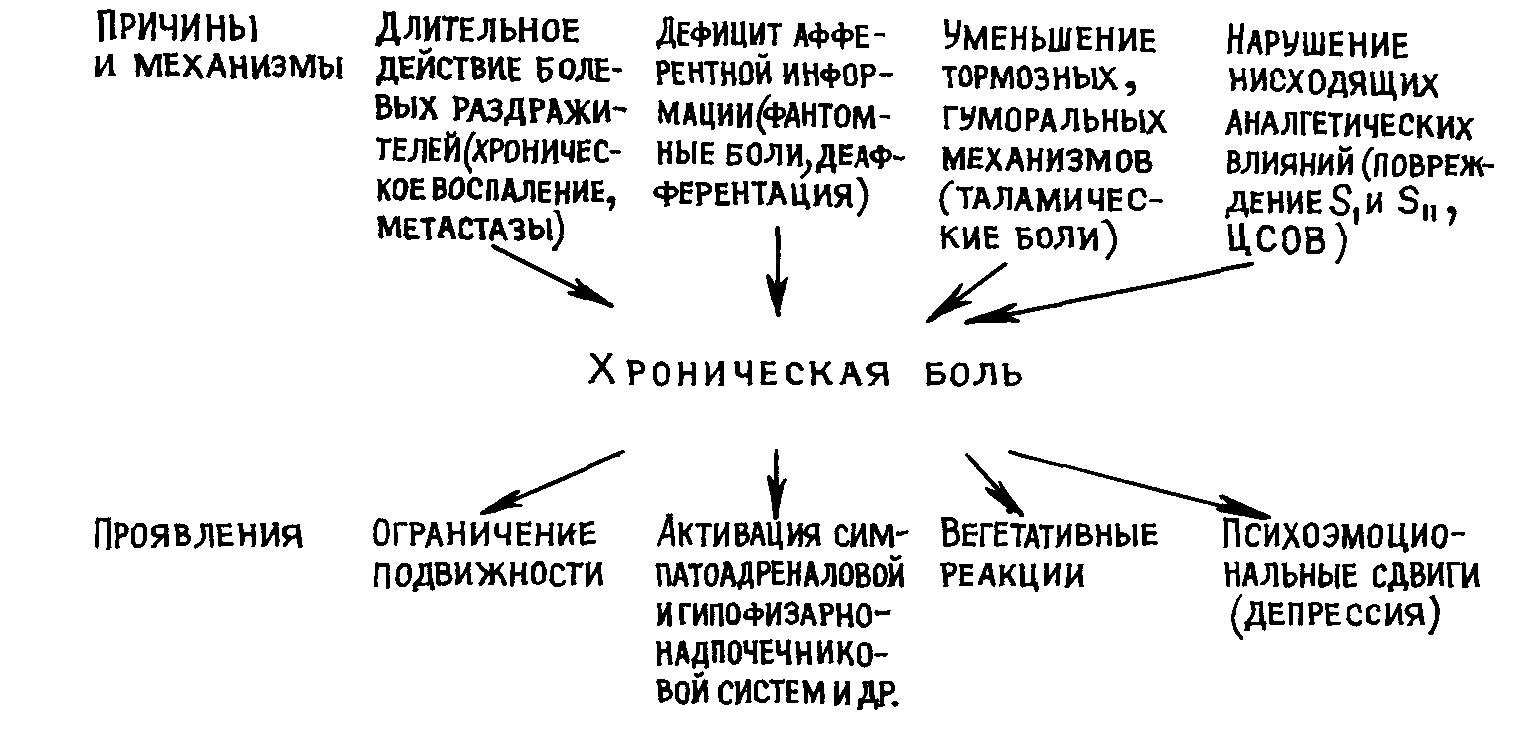
Рис 17 Патогенез хронической боли
Рассматривая механизмы боли очень важно остановиться на особенностях формирования отраженной и проекционной боли
Известно что нередко поражение внутренних органов сопро вождается болью в определенном участке кожи Такая боль полу чила название отраженной Ее возникновение связано с тем, что афференты внутренних органов и кожи связаны с одними и теми же нейронами заднего рога спинного мозга, которые дают начало спинно таламическому тракту Поэтому афферентация идущая от внутренних органов (при их поражении), повышает возбудимость и соответствующего дерматома, что воспринимается как боль в этом участке кожи Кроме того это облегчает передачу афферен тации из соответствующего участка кожи (дерматома) и обеспечи вает его повышенную чувствительность (гиперестезию) (рис 18)
Проекционная боль возникает при сдавлении, повреждении нерва (например, при травме лучевого нерва сдавлении задних спинно мозговых корешков) Это происходит в области иннерва ции чувствительного нерва и связано с распространением возбуж дения как в ЦНС, так и на периферию в зону иннервации (рис 19)
49
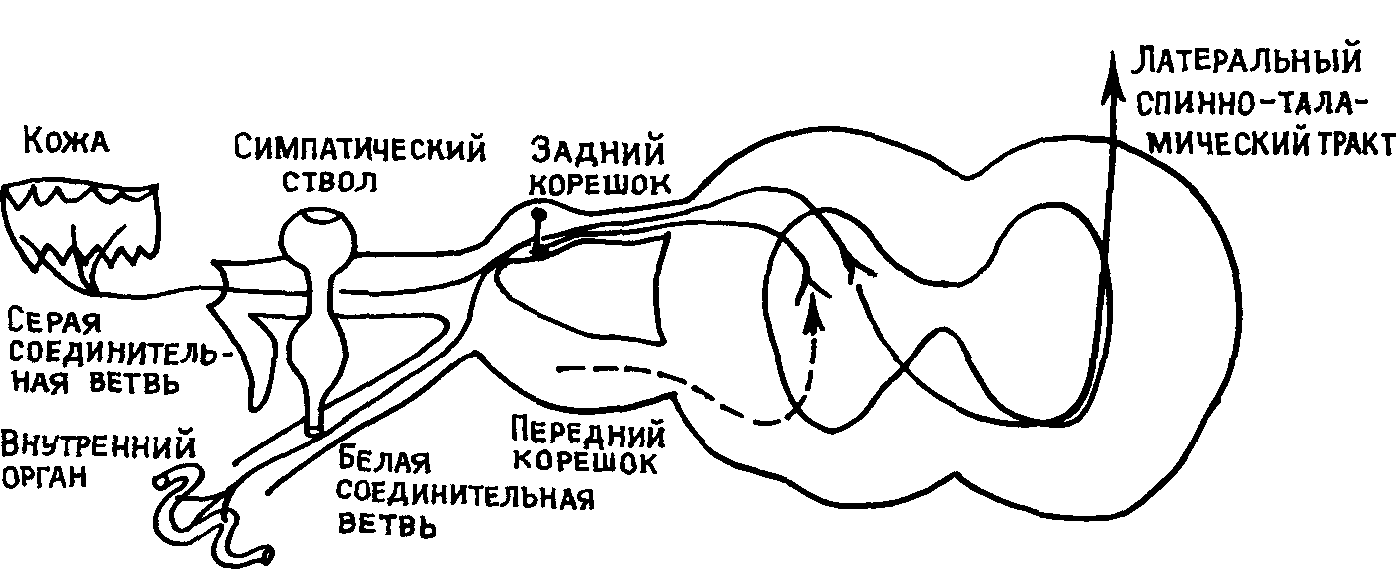
Рис 18 Схема отраженной боли (Р Шмидт 1985)
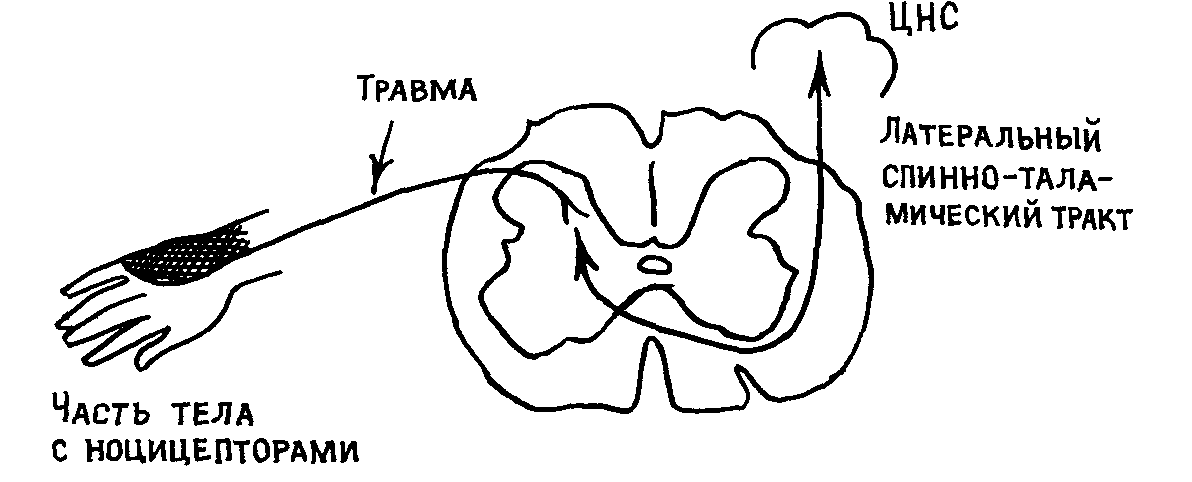
Рис 19 Схема возникновения проецируемой боли (Р Шмидт
1985)
Факторы, определяющие формирование боли
Боль является субъективным ощущением и ее восприятие зависит от многих фак торов — силы, продолжительности ноци
цептивного раздражителя, обширности, индивидуальной чувстви тельности, конкретной обстановки, времени, прошедшего с момен та действия болевого раздражителя (например, первичная остро
50
локализованная боль и вторичная жгучая протопатическая нелока лизованная боль), состояния нейротрансмиттерного и медиатор ного обмена, традиций, культуры, оценки ситуации, внимания
Следует подчеркнуть, что интенсивность боли зависит от силы и локализации повреждения ткани в органах человека Хорошо известно, что при повреждении ядер зрительного бугра возникает мучительная, плохо локализуемая боль Такие же мучительные боли могут наблюдаться при повреждении нервных стволов (каузалгии), тройничного нерва, ампутации конечностей (фантомные боли), дви жении камней по желчным и мочевыводящим путям
Состояние организма и отдельных его систем существенно влия ет на болевые ощущения, причем их интенсивность может как по нижаться, так и резко повышаться Знание этих процессов имеет исключительно важное значение для научно обоснованной профи лактики и лечения Эмоциональное состояние организма также крайне важно для формирования ощущения боли, понижения болевого порога и повышения болевой чувствительности, что особенно ярко проявляется при страхе и ожидании боли
Установлено, что как только полностью восстанавливается реге нерирующий нерв в коже, выявляется ее болезненность (гиперпа тия), когда даже при касании, легком уколе, охлаждении, согре вании повышается болевая чувствительность (сенситизация) Такое же явление отмечено после механического болевого воздействия, воспаления, когда легкое давление, тепло, прилив крови или изме нение положения поврежденного участка вызывают боль Именно поэтому у больных повышается болевая чувствительность в после операционном периоде Такая же закономерность обнаружена и у экспериментальных животных Например, у крыс после лапарото мии повышение болевой чувствительности наблюдается в течение 9 дней послеоперационного периода (А К Ярош, 1987)
Болевые синдромы провоцируются и усиливаются погодными, в том числе холодовыми и тепловыми воздействиями, усилению боли способствуют такие функциональные изменения в организме, как агрессия или истерия, менструация Причем, нередко боли имеют множественный характер (в костях, суставах, внутренних органах), нередко трудно локализуются (больные обычно говорят, что болит все тело) Вне всякого сомнения для появления боли и повышения к ней чувствительности важен тип высшей нервной деятельности, особенно такие ее свойства, как впечатлитель ность и внушаемость
Болевая чувствительность находится в зависимости от нейро трансмиттерного и медиаторного обмена (А В Калюжный, Е В Го ланов, 1980) Известно, что серотонинергический антиноцицептив ный механизм оказывает тормозное влияние на болевую чувстви тельность Блокада серотонина ведет к гипералгезии, и это свя
51
зано с понижением болевого порога Также обнаружено, что при депрессии в плазме крови уменьшается содержание серотонина
Как уже говорилось ранее, при депрессии повышается чувствительность, а назначением антидепрессантов удается уменьшить имеющуюся боль Установлено, что при введении извне норадре-налина резко увеличивается боль, блокада тормозных медиаторов также вызывает сильную боль Так, в опытах Г Н Крыжановского (1973, 1974, 1979) введением столбнячного токсина в спинной мозг блокировали тормозные медиаторы ГАМК, и глицин, и поэтому у экспериментальных животных возникла сильная патологическая боль, которая могла также провоцироваться слабым раздражением, и только введение тормозного медиатора глицина уменьшало болевой эффект
Учитывая важное значение порога боли в болевом ощущении, обнаружили его зависимость от времени суток, причем болевая чувствительность повышается к вечеру Обнаружено понижение болевого порога, а следовательно, повышение болевой чувствительности в зависимости от возраста так, у детей и пожилых людей болевая чувствительность повышена Определенное влияние на боле вые ощущения оказывает гормональный баланс, особенно женских половых гормонов Избыток их уменьшает аналгетический эффект таких веществ, как морфин, промедол
В ходе эксперимента выявлено, что предварительное введение крысам эстрадиола на фоне овариэктомии снижает аналгезию анальгина и промедола (С Ф Сливко, Н П Милованова, 1987)
Для врача крайне важно знание тех условий и воздействий, при которых ощущение боли уменьшается или полностью исчезает Доказано, что резкое возбуждение, например при стрессе, понижает болевую чувствительность Примером этого является отсутствие боли у раненых солдат, получивших ранения во время атаки Эти наблюдения находят подтверждение и в экспериментах Так, если вызвать резкое возбуждение кошки, а затем нанести болевое раздражение током, то она может его даже не заметить Показано, что при стрессе, вызванном болевым воздействием, в мозге увели чивается количество эндогенных опиатов, а в крови бета-эндорфина гипофиза, кортикотропина, который и активирует антиноцицептив-ную систему Однако такие изменения возникают позже, а в начале стресса, по мнению Е О Брагина (1985), антиноцицепция обеспечивается неопиоидными системами Вероятно, это связано с активацией адренергических механизмов Наследственно обусловленное отсутствие болевой чувствительности, механизмы которого неясны до настоящего времени, встречается крайне редко Боль, связанная с регенерацией нерва, значительно подавляется при введении а-ад-реноблокатора фентоламина Повышение болевого порога и, следовательно, уменьшение или снятие боли наблюдается при внушении,
52
приятных эмоциях Вот почему исключительно важным для умень шения боли является психоэмоциональное влияние врача на больного (беседы с целью снятия напряжения больного, введение пла-цебо и т д )
Наконец, в монографии Р Мельзака «Загадка боли» (1981) приводятся многочисленные примеры, когда воспитание, культура народа являются важными факторами снижения болевой чувствительности Говоря о методах уменьшения хронической боли, Р Мель-зак (1981) относит сюда гипнотическое внушение, использование приемов для подавления боли, отвлечения внимания, обучения больных методам биоуправления и физическим упражнениям, применение методов социальной адаптации, психологических или фармакологических методов устранения депрессии В последнее время широко применяется акупунктурное снятие боли
По данным Л В Калюжного (1984), порог боли определяется взаимодействием ноцицептивной и антиноцицептивной систем Так, понижение болевого порога может быть вызвано не только повышением активности ноцицептивной системы, но и подавлением или разрушением антиноцицептивной (снижение влияния опиоидного, серотонинергического механизмов)
Нарушение функций организма. Вегетативные и поведенческие реакции при боли
Боль является сложным актом и включает двигательные, вегетативные, эмоциональные и другие компоненты По мнению
А В Вальдмана (1972), в реакции на боль можно выделить 3 уровня это перцепция боли (ее восприятие), переносимость боли и системные изменения
Первый уровень, по его мнению, осуществляется спинальными механизмами, а последние реализуются при участии гипоталами-ческих, лимбических и неокортикальных структур Дальнейшие исследования А В Вальдмана (1979—1980) показали, что целост ная ответная реакция при болевом воздействии определяется ноцицептивной системой сегментарного уровня и антиноцицептивной надсегментарной системой Он полагает, что ноцицептивная система сегментарного уровня обеспечивает активацию системы действия (защитные реакции избегания), а антиноцицептивная система над-сегментарного уровня обеспечивает контроль афферентного входа, модуляцию сегментарной интеграции высоко- и низкопороговой афферентации, что и определяет адаптацию к повреждающим факторам Некоторые авторы (Ю В Буров, Е А Кияткин, 1987)
53
выделяют так называемые активные формы деятельности, направленные на устранение боли. К ним относятся сгибание и одерги-вание конечности, отпрыгивание, подпрыгивание, что в конечном итоге избавляет организм от дальнейшего повреждения. Если отдельные поведенческие акты не дали избавления от боли, то активируются прежде всего механизмы эндогенной аналгезии, что, по мнению авторов, связано с активацией опиатных, норадренергических, дофамин-, серотонин- и холинергических нейромедиаторных систем с увеличением оборота медиаторов в ряде структур мозга.
Клиническая картина определяется интенсивностью и длительностью боли, она может сопровождаться за счет формирования сегментарных и супраспинальных реакций вздрагиванием, одерги-ванием (например, конечности), убеганием, изменениями мимики лица и движения, стонами, криками и даже плачем.
Очень точную характеристику реакции человека на боль дали Р. Мельзак и П. Уолл (1965). По их мнению, болевая реакция при внезапном повреждении кожи сопровождается вздрагиванием, сги-бательным рефлексом, изменением положения тела, вокализацией, ориентировкой головы и глаз с целью рассмотреть поврежденный участок, воскрешением в памяти предыдущего опыта в подобных ситуациях, предвидением последствий и многими другими формами поведения, направленными на уменьшение сенсорных и эмоциональных компонентов боли, такими как потирание поврежденного участка, реакции избегания.
Расстройства функции нервной системы при интенсивной боли проявляются нарушением сна, сосредоточенности, полового влечения, повышенной раздражительностью и другими симптомами возбуждения или угнетения. При хронической интенсивной боли резко уменьшается двигательная и социальная активность человека. Больной находится в состоянии депрессии, он печален, развивается состояние тоски и безнадежности, наблюдается, как правило, повышение болевой чувствительности в результате снижения болевого порога.
Как показали физиологические исследования (К. В. Судаков, 1980), электроэнцефалографические изменения на острое повреждение проявляются генерализованной реакцией суммарной активности любой структуры мозга, включая кору полушарий, где возникает десинхронизация ЭЭГ, либо в различных структурах мозга упорядоченным регулярным ритмом с частотой 4—7 Гц. И тем не менее при боли отмечено избирательное возбуждение, преимущественно ядер перегородки, дорзомедиального ядра гипоталамуса, структур перивентрикулярной, перефорникулярной области среднего мозга, что, по мнению автора, позволяет расценивать боль как интегративную реакцию структур различных уровней мозга.
Считают, что небольшая боль учащает, а очень сильная замед-
54
ляет дыхание вплоть до его остановки. Может увеличиться частота пульса, системное артериальное давление, развиться спазм периферических сосудов. Кожные покровы бледнеют, а если боль непродолжительна, спазм сосудов сменяется их расширением (гиперемией), что проявляется покраснением кожи. Боль оказывает сильное влияние на секреторную и двигательную функцию желудочно-кишечного тракта, увеличивается слюноотделение, за счет возбуждения симпато-адреналовой системы сначала выделяется густая слюна, а затем за счет активации парасимпатического отдела нервной системы жидкая. В последующем уменьшается аппетит, секреция слюны, желудочного, панкреатического, кишечного сока, желчи, нарушается система выделения, замедляется моторика желудка и кишечника, возможна рефлекторная олигоанурия. При очень резкой боли появляется угроза развития шока, особенно травматического, ожогового, кардиогенного.
Резкая активация при интенсивной боли нервной, симпато-адреналовой, гипоталамо-гипофизарно-надпочечниковой и других систем ведет к биохимическим изменениям в виде увеличения потребления кислорода, распада гликогена, гипергликемии, гиперлипиде-мии (вследствие усиления распада жира в жировых депо), нарушениям ферментативных процессов, водно-солевого обмена, формированию лейкоцитоза.
Хронические боли, по данным В. А. Куршева (1984), сопровождаются сильными вегетативными реакциями. Так, например, кар-диалгии и головные боли сочетались с подъемом АД, температуры тела, тахикардией, диспепсией, полиурией, усилением потоотделения, тремором, жаждой, голодом, головокружением. Тяжелые болевые воздействия вызывают нарушение метаболизма мозга в виде перехода аэробного на гликолитический путь окисления, повышения концентрации аммиака, снижение аспартата и усиление катаболизма АТФ. При хронической боли отмечены явления миокардио-дистрофии, недостаточность кровообращения, увеличение экскреции 17-кетостероидов, свободных и суммарных 17-оксикортикостерои-дов (А. П. Ромаданов, В. С. Михайловский, 1980).
Многочисленными исследованиями (С. А. Еремина с соавт., 1969, 1979, 1987, Г. Н. Кассиль, 1969) при остром болевом стрессе показаны фазные изменения со стороны симпато-адреналовой, гипота-ламо-гипофизарно-надпочечниковой систем, системы гипоталамус — гипофиз—щитовидная железа, поджелудочной железы. В крови увеличивается содержание адреналина, норадреналина, кортикостерои-дов, уровень сахара, кальция. Повышается свертываемость крови. При некоторых заболеваниях боль, нередко непереносимая и мучительная, является самым главным признаком процесса, например, при гастрите, язвенной болезни желудка и 12-перстной кишки, геморрое, трещине прямой кишки, переломах костей, при образовании
55
камней в почках, желчном пузыре и их движении по желчным и мочевыводящим путям, повреждении таламуса и нервных проводников.
Оценка боли
Чаще всего методы определения интенсивности боли касаются поверхностной и глубокой, но не висцеральной (например,сердечной, желудочной, кишечной, почечной).
По мнению Д. Г. Беляева (1986), для оценки висцеральной боли чаще всего используется балонный метод. Помещая балон в полый орган (кишечник, пузырь) и раздувая, можно моделировать боль и давать ей оценку.
Вследствие различия порога болевой чувствительности, а также отсутствия методов объективного исследования, клиническая оценка боли, несмотря на ее исключительную важность, весьма затруднительна. Обычно при оценке боли используют субъективные, объективные и поведенческие показатели. Боль может быть охарактеризована самим больным. Субъективные показатели представляют собой оценку, которую дает сам больной, характеризуя интенсивность боли, ее продолжительность, время появления, зависимость от климатических и других условий. Объективные показатели регистрирует врач или исследователь. Он наблюдает поблед-нение, расширение зрачка, изменение артериального давления, частоты пульса и дыхания, секреции гормонов (кетахоламинов, глюко-кортикоидов), уровня серотонина, изменение электрокардиограммы и энцефалограммы и др.
К поведенческим показателям боли относятся одергивание, крик, стон, убегание, изменение осанки тела, походки.
Все вышеназванные показатели боли будут зависеть от интенсивности ее. При болях средней интенсивности вегетативные и поведенческие реакции могут и не обнаруживаться (В. А. Куршев, 1984).
А. К. Сангайло (1964) предложил метод сенсометрии, с помощью которого определяется порог тактильных ощущений, порог боли, порог переносимости боли, что позволяет давать характеристику соматосенсорного и психоэмоционального статуса больного, причем оценка последнего производится по диапазону, а не по порогу болевой чувствительности. И. А. Шугайлов (1985) предлагает проводить количественную оценку болевой реакции путем подачи на исследуемые ткани импульсного напряжения с плавно увеличивающейся амплитудой и одновременной регистрацией силы тока, вегетативных реакций и ощущений у испытываемого. Причем определяется порог болевого ощущения, болевой толерантности реагирования,
56
диапазон болевой чувствительности. В. А. Куршев с соавт. (1984) считают целесообразным проводить комплексную оценку боли по четырехмерной шкале тестов-баллов: объективные тесты, субъективно-объективные, объективные данные и социально-бытовой статус. В клинике используется простой метод оценки боли по 3 степеням— легкая (1 балл), средняя (2 балла), сильная (3 балла). Современная оценка боли в клинике дана К. Ь. 5уг]'а\'а, §. К. Спартап (1984).
У экспериментальных животных оценку боли осуществляют по порогам вокализации (крика) в ответ на электростимуляцию корня хвоста крысы (Г. Н. Кассиль, 1969; Б. А. Андреев, 1984) и по латентному периоду одергивания хвоста при термическом воздействии. В зарубежной литературе эти тесты оценки боли называются «1аП-Шск» — одергивание, легкий удар хвостом и «по1е-р1а1е» — горячая пластинка.
В клинической практике необходимо знать степень уменьшения боли после приема лекарств, поэтому очень важны критерии болеутоления. В. М. Жоров (1984) предлагает использовать субъективные и объективные данные:
а) субъективные ощущения больных в баллах (по Гологор-скому):
1 балл — наличие боли в состоянии покоя;
2 балла — боль в состоянии покоя отсутствует, но сохраняется при углубленном дыхании и кашле;
3 балла — больной может глубоко дышать и кашлять.
При 2—3 баллах больной находится в дремотном состоянии;
б) объективные — учитываются изменения АД, частота пульса, КЩР-крови, электроэнцефалограмма и концентрация аналгетиков в крови.
Биологическое значение боли
Биологическое значение боли неоднозначно. Если рассматривать ее с эволюционных позиций, то боль выполняет роль сигнала об угрозе или о возникшем повреждении тканей, хотя, как известно, ряд заболеваний вначале может протекать бессимптом-но (опухоли, кариес, парадонтоз, поражение печени, почек, сердца, мозга и др.). Боль, являясь сигналом опасности, заставляет больного обратиться к врачу и нередко является важным признаком постановки диагноза.
Защитное значение боли определяли еще древние греки, называя ее «сторожевым псом здоровья». Ярким доказательством этого является отсутствие боли при ряде злокачественных опухолей, в результате чего больной нередко обращается к врачу с обширным
57
процессом, когда радикальное лечение практически невозможно
Боль обычно характеризуется эмоциональным компонентом, с помощью которого формируется аффективная (эмоциональная) реакция организма в виде нападения или бегства, крика и др В то же самое время возникновение боли является важным моментом исключения повреждения в организме за счет организации защитных процессов организма, ухода от повреждающего фактора, изменения нервной, гипоталамо гипофизарно надпочечниковой, антино-цицептивной систем, метаболизма, иммунитета, фагоцитоза и т д (Р А Дуринян, 1981, Ф Г Углов, В А Копылов, 1985)
Таким образом, боль сигнализирует, с одной стороны, о наличии повреждения, а с другой стороны — о включении защитных и репаративных процессов, являющихся основой для ее нивелирования и исчезновения По мнению Ф Г Углова и В А Копылова (1985), пока патогенное воздействие или патологический процесс ограничены, нервная, эндокринная, антиноцицептивная системы обеспечивают адаптацию и болевое ощущение не возникает, но как только воздействие на организм превышает определенный предел (а этим пределом является, вероятно, повреждение тканей), возникает боль, что является сигналом для мобилизации нервных, сердечно-сосудистых, метаболических, антиноцицептивных механизмов По мнению Ю Д Игнатова (1982), сердечно-сосудистые реакции при боли направлены на увеличение нутритивных потребностей скелетной мускулатуры
Учитывая вышеизложенное, Ф Г Углов и В А Копылов (1985) предлагают использовать боль в качестве лечебного фактора, ко торый «мобилизует функциональные способности органов и их защитные механизмы» Тем более что в последнее время доказана первостепенная роль в защитных реакциях организма опиоидных пептидов, которые, по данным А А Зозули с соавт (1988), оказывают выраженный стимулирующий эффект на такие показатели гуморального и клеточного иммунитета, как антителообразование, миграционная способность лейкоцитов
Ю П Лиманский (1986) рассматривает боль как трехпрограмм ную реакцию организма, сформированную в ходе эволюционного развития
Первая программа, по его мнению, включается при кратковре менном возбуждении ноцицепторов и быстропроводящей А-дельта-афферентной системы, в результате чего формируются сравнительно простые защитные рефлексы Именно в связи с этим боль рас сматривается как предупреждающий фактор Действительно, Р Мельзак в книге «Загадка боли» приводит яркие примеры, когда врожденная нечувствительность к боли делает организм нежизне способным из за отсутствия формирования рефлекторных защитных реакций
58
Вторая программа включается при непродолжительном возбуждении А-дельта и С-волокон, что сопровождается активацией вегетативных функций (сердце, дыхание, кровообращение) и аффек-тивно-мотивационными компонентами общей защитной реакции с изменением поведения, соматическими висцеральными, соматовисце ральными и висцеро-висцеральными реакциями, возбуждением локальных и общих аналгетических систем
Третья программа реакции на боль включается при длительном раздражении ноцицепторов с активацией аналгетических систем, обеспечивающих уменьшение подвижности и активацию механизмов заживления поврежденного участка Если острая боль явля ется для организма сигналом опасности, то патологическая боль, в том числе хроническая, выступая в качестве сильного стрессор-ного фактора, оказывает пагубное воздействие на больного, его семью, окружающих (Б В Петровский, 1980)
Когда организм получил сигнал опасности и произошло уже разрушение ткани, а ноцицептивный раздражитель продолжает действовать, то вслед за эпикрической быстролокализованной болью в связи с продолжающимся поступлением импульсов и образованием медиаторов боли, возникает протопатическая боль Хроническая боль характеризуется дезорганизацией нормальной функции регуляторных механизмов. Боль, сигнализируя о неблагополучии в организме, становится ненужной и опасной, так как при любом сильном стрессе нарушается нервная, эндокринная, сердечно-сосудистая системы, подавляется иммунитет, развивается шок, расстраи вается психика (Р А Дуринян, 1986)
При хронической боли гемодинамические сдвиги уже не могут реализовываться в виде двигательных актов Они утрачивают адап тивный характер (как это имеет место при острой боли) и «приобретают значение самостоятельных патогенетических причин для развития патологического состояния» (Ю Д Игнатов, 1982)
При хронической боли больной все внимание, все свои помыслы сосредоточивает на боли, уходит в себя, резко ограничивает свои интересы, изменяет поведение Таким образом, хроническая боль снижает сопротивляемость организма, истощает его силы, дезорганизует центральные механизмы жизненных функций Человек перестает получать удовольствие от жизни, становится психически неполноценным, гомеостаз его резко нарушается
Поэтому самая главная задача врача заключается в том, что бы уменьшить или полностью снять болевое ощущение у человека, облегчить таким образом его страдания Различия проявлений острой и хронической боли можно было бы свести к следующим основным положениям-
1 При хронической боли автономные рефлекторные реакции постепенно уменьшаются и в конечном счете исчезают, а прева
59
лируют вегетативные расстройства.
2 При хронической боли, как правило, не бывает самопроизвольного купирования боли, для ее нивелирования требуется вмешательство врача
3 Если острая боль выполняет важнейшую защитную функцию, то хроническая вызывает более сложные и длительные расстройства в организме и приводит, по мнению Л ^ Вогпса (1985), «к прогрессивному изнашиванию, вызванному нарушением сна и аппетита, снижением физической активности, часто избыточным лечением, что способствует общему утомлению и слабости».
4. Кроме страха, характерного для острой и хронической боли, для последней свойственны также депрессия, гипохондрия, безнадежность, отчаяние, устранение больных от социально-полезной деятельности, а в тяжелых случаях появляются у них суицидальные идеи и даже попытки их реализации
5 Проблема хронической боли является для общества одной из самых дорогостоящих (3 ^ Вотса, 1985)
Моделирование боли
Как уже говорилось, болевая реакция у больного определяется на основании опроса, визуального наблюдения за внешним
обликом и поведением, а также специальными исследованиями типа пальпации, постукивания, укола иглой, пассивного или активного движения конечностей, туловища
Описаны механические, электрические, тепловые, химические, звуковые, ультразвуковые методы вызывания боли
В клинике чаще используются механические способы раздражения в виде уколов, давления (Д Г. Беляев, 1986)
Острая боль у экспериментальных животных моделируется электрическим или тепловым воздействием У крыс острая боль вызывается (А А Зайцев, 1984) электрическим раздражением хвоста через игольчатые электроды, с постепенно нарастающей интенсивностью или путем механического раздражения хвоста градуированным зажимом
Е О. Брагин (1985) моделировал боль введением крысам подкожно 1 мл 1 н раствора уксусной кислоты, 1,25% формалина, 4,5% КС1 или помещением животных на горячую пластинку (1== =60°С) на 3 мин.
В К Решетняк, М Л Кукушкин моделировали острую боль у кошек в свободном поведении Биполярные электроды предварительно вживляли в тыльную часть предплечья обеих передних лап. Ноцицептивные электрические раздражения наносились через эти электроды в виде пачек импульсов (частота импульсов в пачке —
60
5 имп/сек , длительность импульса — 1 мсек , продолжительность пачки — 1 сек ) Интенсивность раздражения увеличивается градуально от 100 мв до 30 в
Для учета и характеристики болевых реакций у кошек, собак, крыс при нарастании интенсивности раздражителя предложены следующие критерии (А В Вальдман, Ю. Д Игнатов, 1976, Ю Н Васильев с соавт , 1979) (табл 3).
Таблица 3
Критерии интенсивности боли
Уровень реакции |
Характеристика реакции |
1 2 3 4 5 |
Порог отвечнои реакции вздрагивание век, сгибание стимули руемой конечности Сгибание стимулируемой конечности, вздрагивание головы, за-жмуривание, прижимание ушей Вздрагивание всем телом облизывание, изменение позы, оди ночные передвижения, вокализация Интенсивный многократный крик, постоянное передвижение, бес покойство Генерализованные движения, побег с криком, агрессивность |
Ю Д Игнатов, А. В Дмитриев (1986), А В Дмитриев (1982) для воспроизведения боли вживляли электроды в пульпу зуба кролика и в свободном поведении вызывали ее раздражение Интенсивность раздражения дозировали в порогах кратно начальным про явлениям реагирования животных на стигмы Один порог соответствует открыванию пасти и облизыванию Большой интерес представляет моделирование хронической боли в виде центральных болевых синдромов (Г Н. Крыжановский, 1973, 1974, 1979, 1981) Введением столбнячного токсина в задние рога спинного мозга, ядра таламуса, каудальное ядро тройничного нерва удалось воспроизвести боль спинального, таламического происхождения и невралгию тройничного нерва
Хроническая боль моделируется и другими методами Так, В В Кравцов (1961), Е П Макарова, Б В Андреев (1984) моделировали хроническую боль наложением на седалищный нерв полихлорвиниловой трубки на 1 мм меньше диаметра нерва Шелковой лигатурой нерв ущемлялся на протяжении 5 мм и подшивался к мышцам бедра
Хроническая боль также воспроизводится (Е П Макарова,
61
Б. В. Андреев, 1984) раздражением париетальной брюшины. Для этого в нее вживляют электроды диаметром 1 мм, концы которых выводят в тыльной области шеи и раздражают электричеством с 1-го по 10-й день в течение 30 мин. (30 сек. раздражения каждые 3 мин.: 20 Гц, 1 мсек., интенсивность подбирается по появлению вокализации), с 10-го по 15-й день — по 60 мин. ежедневно (30 сек. раздражения каждую минуту). Другие методы моделирования и регистрации боли приведены в монографии Г. Н. Кассиль «Наука о боли» (1970).
Общие принципы и механизмы обезболивания
При установлении причины боли задача врача заключается в облегчении страданий больного путем ее уменьшения или
устранения, особенно хронической боли, которая нарушает функциональные системы организма, изменяет психику и поведение человека, делая его нетрудоспособным. Наряду с этиологическим лечебные воздействия должны носить патогенетический характер и осуществляться на основании знания физиологических, психофизиологических, биохимических механизмов боли и антиноцицепции.
Лечение боли различного генеза нашло отражение в ряде последних фундаментальных исследований отечественных и зарубежных авторов (А. В. Вальдман, 1972; Л. В. Авдей, И. К. Данусе-вич, 1976; Л. В. Калюжный, 1984; В. Н. Шток, 1988; Р. Мельзак, 1981; Ргаст1са1 тапа^етеп^ о{ Рат, 1986; Рекомендации ВОЗ, 1986; ОПаепЬеге, Ое Уап1, 1985).
В современной медицинской практике для облегчения или снятия боли используются следующие методы:
1) психологические;
2) физические;
3) хирургические;
4) фармакологические;
5) нейрохирургические.
1. Психологические методы направлены на снятие напряжения, чувства страха, обеспокоенности больного, которые, как известно, понижают болевой порог. Врач добивается этого проведением беседы с больным, введением плацебо, путем аутотренинга, расслабляя больного. Для обезболивания используется гипнотическое внушение. Интересно, что у людей, находящихся в состоянии гипнотического сна (К. М. Каграманов, 1980), внушение боли, как и реальное болевое раздражение (укол кожи иглой), вызывает на ЭЭГ реакцию десинхронизации.
62
Указанные выше сравнительно простые процедуры, вероятно, усиливают выброс энкефалинов в спинно-мозговую жидкость и образование эндорфинов, которые, блокируя проведение болевых импульсов, уменьшают или полностью прекращают болевое ощущение.
В последние годы, особенно для лечения головных и шейных болей, обусловленных повышенным напряжением мышц, используют метод биологической обратной связи, который заключается в том, что после прохождения специального курса больные могут произвольно вызывать расслабление мышц, добиваясь, таким образом, снятия стресса и уменьшения боли. Более подробно психотерапевтические аспекты боли даны в монографии И. Харди (1988).
