
- •1. Массообменные процессы.
- •1.1. Массообмен в технологии строительных материалов.
- •1.4. Движущая сила массообменных процессов.
- •1.5. Основные законы массопередачи.
- •1.6. Массопередача в системах с твердой фазой.
- •Содержание:
- •Массообменные процессы………………………………………………………………………………………………………
- •Массообмен в технологии строительных материалов……………………………………………………
- •Список литературы:
1. Массообменные процессы.
1.1. Массообмен в технологии строительных материалов.
Технологические процессы, скорость которых определяется скоростью переноса вещества из одной фазы в другую, называется массообменные процессами, а аппаратура для проведения этих процессов – массообменной аппаратурой. Основные массообменные процессы – абсорбция, адсорбция, экстракция, ректификация, сушка, кристаллизация, растворение, плавление.
В технологии строительных материалов наиболее важное значение имеют сушка, растворение, плавление и кристаллизация. Остальные из перечисленных процессов имеют отношение к технологии строительных материалов, поскольку они применяются при получении полимеров и производстве на их основе строительных материалов из пластмасс.
Рассмотрим только основные массообменные процессы в технологии строительных материалов.
СУШКА - даление влаги из твёрдых влажных материалов путём её испарения. Сушка имеет большое значение в технологии почти всех строительных материалов, особенно в производстве керамики всех типов. Процесс сушки заключается в переходе воды из твёрдого материала в паровую или газовую фазу.
КРИСТАЛЛИЗАЦИЯ – выделение твёрдой фазы в виде кристаллов из растворов и расплавов. Кристаллизация из растворов происходит при твердении вяжущих веществ; кристаллизация из расплавов – при обжиге керамических изделий и при производстве портландцементного клинкера. Кристаллизация характеризуется переходом вещества из жидкой фазы в твёрдую.
Из приведённых примеров видно, что в описываемых процессах общим является переход вещества из одной фазы в другую – МАССОПЕРЕДАЧА. Этот переход связан с явлениями конвективного переноса и молекулярной диффузии, поэтому такие процессы и называют массообменными, или диффузионными.
Массопередачей называют переход вещества из одной фазы в другую в направлении достижения равновесия. Все массообменные процессы обратимы. В массообмене участвуют как минимум три вещества: отдающее вещество – первая фаза, воспринимающее вещество – вторая фаза и распределяемое вещество, переходящее из одной фазы в другую.
Обозначим первую фазу G, вторую L, а распределяемое вещество М.
Поскольку процессы обратимы, вещество М может переходить из фазы G в фазу L и наоборот, в зависимости от концентрации вещества в этих фазах.
Допустим, что распределяемое вещество в какой-то момент находится только в фазе G и имеет концентрацию Y. В фазе L в этот же момент вещества М нет, т.е. его концентрация Х =0. Если фазы G и L привести в соприкосновение, начнётся переход вещества М из фазы G в фазу L, и в последней концентрация вещества окажется X >0. Как только вещество М появится в фазе L, начнётся и обратный его переход в фазу G, но до некоторого момента число частиц М, переходящих в единицу времени через поверхность контакта фаз, будет больше в направлении G >L и меньше в направлении L >G. Конечным итогом будет переход М из фазу L. Через какое-то время число частиц, переходящих за это время из L в G. Наступает равновесное состояние. Концентрации М в обеих фазах в этот момент станут равновесными. Для каждого конкретного случая существуют строго определённые равновесные концентрации, т.е. любой концентрации Х соответствует равновесная концентрация Yp и наоборот, любой концентрации Y соответствует равновесная концентрация Xp. Это значит, что
 (1.1)
(1.1)
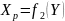 .
(1.2)
.
(1.2)
Условия равновесия могут быть выражены не только через концентрации, но и через другие параметры вещества — через энтальпию, химический потенциал и др.
Знание равновесных концентраций позволяет выяснить направление процесса. Если Y >Yp значит Х <Хp и вещество будет переходить из G в L. Если X >Xp (т.е. Y < Yp), будет переходить перенос М из L в G.
Скоростью перехода распределяемого вещества из одной фазы в другую пропорциональна разности между фактической концентрацией вещества в данной фазе и равновесной его концентрацией в этой фазе.
Основные вопросы, изучаемые в массопередаче, законы фазового равновесия; движущая сила массообменных процессов; коэффициенты скорости массообменных процессов. Последние два вопроса определяют кинетику таких процессов.
1.2. Основные уравнения массопередачи Основной закон массопередачи можно сформулировать следующим образом: скорость процесса равна движущей силе, деленной на сопротивление, т.е.

где dM - количество вещества, перешедшего из одной фазы в другую; dF — поверхность массообмена; dτ — время; Δ – движущая сила процесса (Δ X или Δ Y); R — сопротивление. Если вместо R взять обратную величину 1/R = К — коэффициент скорости, в данном случае коэффициент массопередачи, то

Если определять dM в единицу времени, то уравнение (4) имеет вид:

(4) и (5) — основные уравнения массопередачи.
В реальных аппаратах равновесные концентрации никогда не достигаются. Рабочие концентрации всегда отличаются от равновесных. Разность между рабочей и равновесной концентрацией, характеризующая степень отклонения от равновесия, и является движущей силой массообменных процессов.
1.3. Материальный баланс массообменных процессов. В общем виде материальный баланс массообменных процессов может быть составлен
следующим образом. Обозначим массовые скорости распределяющих фаз вдоль поверхности их раздела (в кг/ч) через G и L, а концентрацию распределяемого вещества соответственно через Y (кг/кг) и X (кг/кг). Если Y > Yp, а потери отсутствуют, то Y уменьшается, а Х увеличивается. Для элемента поверхности имеем:

Интегрируя в пределах от начальных до конечных концентраций Yн – Yк и Xн – Xк, получим:

Из уравнения (7) рассчитываем массовые расходы распределяющих фаз:

Если уравнение (6) проинтегрировать от начальных до текущих концентраций, то получим G(Yн-Y )= L(X-Xн).
Откуда:

Здесь L/G – удельный расход одной из распределяющих фаз. Это уравнение в общем виде:

Из уравнения (10) видно, что концентрация вещества в распределяющих фазах связана линейной зависимостью. Уравнение прямой, выражающее зависимость между рабочими концентрациями, называется рабочей линией процесса.

