
- •Экзаменационный билет № 1
- •1. Собственная масса m0. Соответствующую массу будем определять как константу, входящую в релятивистское соотношение
- •5.Время жизни частицы - средняя продолжительность существования нестабильных элементарных частиц. Согласно теории относительности
- •Проблема построения единой теории сильного, слабого и электромагнитного взаимодействий (модели Великого объединения)
- •Экзаменационный билет № 2
- •Существуют 4 типа взаимодействия:
- •Экзаменационный билет № 3
- •38. Ядерные взаимодействия и ядерные реакции. Общие закономерности и различные механизмы ядерных реакций. Особенности протекания ядерных реакций под действием различных частиц.
- •Экзаменационный билет № 4
- •37.Радиоактивность и закономерности радиоактивного распада; процессы сопровождающие радиоактивный распад и их физическая интерпретация.
- •Экзаменационный билет № 5
- •Экзаменационный билет № 6
- •6. Механика жидкости и газа. Основные уравнения равновесия и движения жидкостей. Гидростатика несжимаемой жидкости. Барометрическая формула.
- •35.Элементы зонной теории твердых тел. Обобществление электронов в кристалле, энергетический спектр электронов в кристалле, металлы, диэлектрики и полупроводники с точки зрения зонной модели.
- •Экзаменационный билет № 7
- •Экзаменационный билет № 8
- •2 Волновая функция и ее свойства. Уравнения Шредингера для стационарных состояний. Принцип причинности в квантовой механике
- •Экзаменационный билет № 9
- •Экзаменационный билет № 10
- •Экзаменационный билет № 11
- •Экзаменационный билет № 12
- •Экзаменационный билет № 13
- •Экзаменационный билет № 14
- •Общие условия равновесия и устойчивости
- •Равновесие гомогенной системы
- •Экзаменационный билет № 15
- •Экзаменационный билет № 16
Экзаменационный билет № 11
1. Распределение скоростей молекул газа. Закон распределения скоростей Максвелла. Принцип детального равновесия. Закон распределения Больцмана. Энтропия и вероятность. Метод наиболее вероятного распределения в статистике Больцмана. Статистика Ферми-Дирака, Бозе-Эйнштейна. Теорема Нернста. Квантовая теория теплоемкости Эйнштейна.
2. Статистическая термодинамика квантовых идеальных одноатомных газов. Распределение Бозе-Эйнштейна и Ферми-Дирака. Сопоставление распределений М.-Б., Б.-Э. и Ф.-Д. Вырождение квантовых газов. Теплоёмкость твёрдых тел.
1. Распределение скоростей молекул газа. Закон распределения скоростей Максвелла. Принцип детального равновесия. Закон распределения Больцмана. Энтропия и вероятность. Метод наиболее вероятного распределения в статистике Больцмана. Статистика Ферми-Дирака, Бозе-Эйнштейна. Теорема Нернста. Квантовая теория теплоемкости Эйнштейна.
Распределение
по скоростям молекул идеального газа.
Максвелл.
В одномерном
случае распределение молекул идеального
газа по одной из компонент скорости,
например,
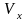 описывается нормальным распределением
описывается нормальным распределением
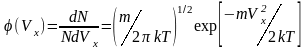 ,
(1)
,
(1)
где
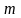 - масса молекулы,
- масса молекулы,
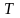 - абсолютная температура,
- абсолютная температура,
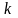 постоянная Больцмана.
постоянная Больцмана.
При этом средняя
скорость молекул равна нулю, а стандартное
отклонение
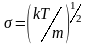 .
.
Г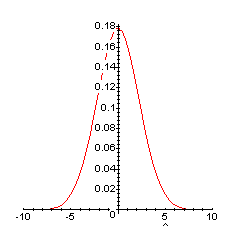 рафик
функции (1) имеет вид:
рафик
функции (1) имеет вид:
Для двумерного
случая распределение молекул идеального
газа, компоненты скорости которых
заключены в интервалы от
до
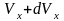 и от
и от
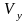 до
до
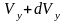 имеет вид:
имеет вид:
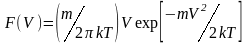 ,
(2) где
,
(2) где
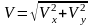 ;
;
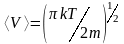 - средняя скорость движения молекул;
- средняя скорость движения молекул;
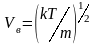 - вероятная скорость движения молекул.
- вероятная скорость движения молекул.
В трехмерном случае распределение частиц по величине скорости описывается распределением Максвелла:
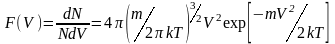 ,
(3) где
,
(3) где
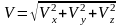 ;
;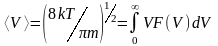 - средняя скорость движения молекул;
- средняя скорость движения молекул;
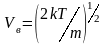 - вероятная скорость движения молекул
(максимум F(V)).
- вероятная скорость движения молекул
(максимум F(V)).
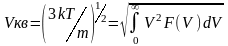 - Среднеквадратичная скорость молекул
- Среднеквадратичная скорость молекул
График функции (3) изображен на рис. 2.
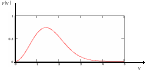 Рис. 2
Рис. 2
Значение функции распределения имеет смысл доли молекул, скорости которых лежат в пределах V…V+dV.
Интеграл от нормального распределения F(V), взятый в пределах от некоторой скорости V1 до некоторой скорости V2 дает относительное количество (долю) молекул, скорости которых лежат в диапазоне от V1 до V2. Интеграл от нормального распределения F(V) по всем скоростям от 0 до бесконечности дает 1 - все молекулы находятся в данном скоростном диапазоне. Площадь под графиком, ограниченная двумя вертикальными линиями, соответствующими скоростям V1 и V2, равна относительному количеству молекул в данном скоростном диапазоне (от V1 до V2).В любой части системы, содержащей достаточно большое количество молекул в состоянии термодинамического равновесия, справедливо распределение Максвелла для скоростей молекул.
Детального равновесия принцип, общее положение статистической физики, согласно которому любой микроскопический процесс в равновесной системе протекает с той же скоростью, что и обратный ему. Когда система, состоящая из большого числа частиц, находится в равновесии, постоянными во времени остаются лишь физические величины, относящиеся к системе в целом (они называются термодинамическими величинами). В то же время составляющие систему отдельные микрочастицы меняют своё состояние: в равновесной системе происходят столкновения частиц (атомов, молекул и др.), могут протекать химические реакции и т.п. Конечно, чтобы равновесие сохранялось, наряду с любым таким микропроцессом должен осуществляться и обратный ему (т. к., действуя лишь в одном направлении, микропроцесс может привести к изменению состояния системы в целом). Детального равновесия принцип утверждает, что скорость любого микропроцесса (число происходящих за 1 сек событий этого микропроцесса) совпадает в состоянии равновесия со скоростью обратного ему процесса. Скорость при этом трактуется статистически — как среднее по большому числу одинаковых микропроцессов.
В квантовой теории Детального равновесия принцип состоит в равенстве вероятностей прямого и обратного процессов. Этими процессами могут быть квантовые переходы, реакции между элементарными частицами и т.д.
Распределение Больцмана.
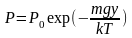
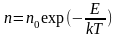 Энтропия
и вероятность. Им. Т.С., в кот определены
суммарная энтропия, стат вес. Проделано
отверстие, мол-лы вылетают. – процесс
необратимый. Энтроп. и стат вес увеличив.,
Энтропия
и вероятность. Им. Т.С., в кот определены
суммарная энтропия, стат вес. Проделано
отверстие, мол-лы вылетают. – процесс
необратимый. Энтроп. и стат вес увеличив.,
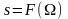
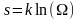
Статистика Ф.-Д., Б.-Э. Волновая функция системы бозонов симметрична, а фермионов – антисимметрична относительно перестановки любой пары частиц. Волновая функция квантового идеального газа представляется произведением волновых функций отдельных частиц и полностью определяется заданием чисел заполнения nk каждого к-го одночастичного состояния. Требование антисимметрии волновой функции системы фермионов приводит к тому, что они удовлетворяют принципу Паули: в заданном квантовом состоянии может находиться не более одной частицы, т.е. nk=0; 1. В каждом одночастичном состоянии бозе-газа может находиться любое число частиц: nk=0;1;2,…N, где N – общее число частиц в системе.
Распределение частиц по одночастичным квантовым состояниям зависит от того, являются ли частицы бозонами или фермионами. В соответствии с этим существуют две квантовые статистики: статистика Бозе-Эйнштейна (для бозонов) и статистика Ферми-Дирака (для фермионов). Функция распределения по квантовым состояниям обоих классов частиц имеет вид:
 =
=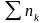
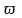 (nk)
=
(nk)
=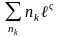
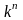 k
/
k
/
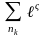 k
1. Распределение
бозе-частиц по состояниям называется
распределением Бозе-Эйнштейна:
=
k
1. Распределение
бозе-частиц по состояниям называется
распределением Бозе-Эйнштейна:
=
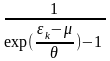 оно было установлено в 1924 г. Распределение
частиц по энергиям найдем, умножив
на число gk
микросостояний
с энергией
оно было установлено в 1924 г. Распределение
частиц по энергиям найдем, умножив
на число gk
микросостояний
с энергией
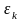 :
(
)
=
:
(
)
=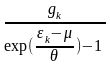 2. Распределение
Ферми-Дирака Среднее
число ферми-частиц в к-ом состоянии
равно:
=
2. Распределение
Ферми-Дирака Среднее
число ферми-частиц в к-ом состоянии
равно:
=
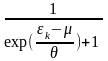 Распределение электронов по эгеогиям
(s=
Распределение электронов по эгеогиям
(s=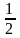 )
будет
(
)
=
)
будет
(
)
=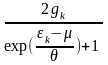 сопоставление
распределений М-Б, Б-Э и Ф-Д: все
эти три функции распределения идеальных
газов можно записать в едином виде:
=
сопоставление
распределений М-Б, Б-Э и Ф-Д: все
эти три функции распределения идеальных
газов можно записать в едином виде:
=
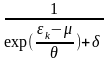 , (1) где
, (1) где
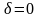 для распределения М-Б,
для распределения М-Б,
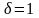 для распределения Ф-Д,
для распределения Ф-Д,
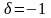 для распределения Б-Э. На рис приведены
графики этих функций распределения. Из
(1 ) видно, что распределения Б-Э и Ф-Д
переходят в распределение М-Б, т.е. газ
становится классическим, если
для распределения Б-Э. На рис приведены
графики этих функций распределения. Из
(1 ) видно, что распределения Б-Э и Ф-Д
переходят в распределение М-Б, т.е. газ
становится классическим, если
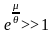 .
(2) Если
.
(2) Если
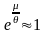 ,
то функция распределения газа отличается
от максвелл-больщмановской и говорят,
что газ вырожден. Величина
,
то функция распределения газа отличается
от максвелл-больщмановской и говорят,
что газ вырожден. Величина
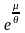 называется фактором вырождения, выражение
(2) – критерием невырожденности, а
противоположные неравенства – критерием
сильного вырождения.
называется фактором вырождения, выражение
(2) – критерием невырожденности, а
противоположные неравенства – критерием
сильного вырождения.
Теплоемкость
твердых тел
рассчитывается по формуле Дюлонга и
Пти:
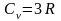 Твердое
тело рассматривается как совокупность
N
независимых атомов, колеблющихся с
одной и той же частотой ν. Однако средняя
энергия, приходящаяся на одну степень
свободы, полагается равной не КТ, а
вычисляется по формуле Планка для
средней энергии линейного осциллятора:
Твердое
тело рассматривается как совокупность
N
независимых атомов, колеблющихся с
одной и той же частотой ν. Однако средняя
энергия, приходящаяся на одну степень
свободы, полагается равной не КТ, а
вычисляется по формуле Планка для
средней энергии линейного осциллятора:
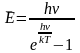 (1)энергия грамм-атома, имеющего 3N
степеней свободы, равна:
(1)энергия грамм-атома, имеющего 3N
степеней свободы, равна:
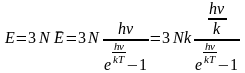 (2), величину
(2), величину
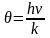 ,
имеющего размерность температуры,
Эйнштейн назвал характеристической
температурой тела. Следовательно
,
имеющего размерность температуры,
Эйнштейн назвал характеристической
температурой тела. Следовательно
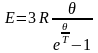 ,
дифференцируя по температуре, получим
,
дифференцируя по температуре, получим
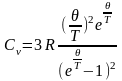
При низких
температурах (Т<<θ),
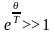 ,
вследствие чего единицей в знаменателе
можно пренебречь и записать:
,
вследствие чего единицей в знаменателе
можно пренебречь и записать:
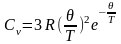 При Т
При Т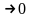
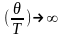 ,
а
,
а

Теорема Нернста: когда система приходит к температуре абсолютного нуля, то энтропия приходит к 0.следовательно достигнуть абс. 0 нельзя.
2. Статистическая термодинамика квантовых идеальных одноатомных газов. Распределение Бозе-Эйнштейна и Ферми-Дирака. Сопоставление распределений М.-Б., Б.-Э. и Ф.-Д. Вырождение квантовых газов. Теплоёмкость твёрдых тел.
При
температурах Т<Т0
(
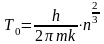 )
система частиц становится квантовой.
Квантовые частицы помимо волновых
свойств обладают собственным (спиновым)
механическим моментом. Его величина
равна
)
система частиц становится квантовой.
Квантовые частицы помимо волновых
свойств обладают собственным (спиновым)
механическим моментом. Его величина
равна
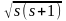 h
,где спин s
– целое (включая нуль) или полуцелое
положительное число, определяемое
природой частиц. Таким образом, состояние
квантовой частицы данного типа
определяется волновой функцией
Ψ(x,y,z)
и спиновым числом ms
(характеризующим одно из возможных
значений проекций спинового момента
на фиксированную ось). Возможны 2s+1
состояний с заданной волновой функцией,
отличающейся ориентацией спина.
h
,где спин s
– целое (включая нуль) или полуцелое
положительное число, определяемое
природой частиц. Таким образом, состояние
квантовой частицы данного типа
определяется волновой функцией
Ψ(x,y,z)
и спиновым числом ms
(характеризующим одно из возможных
значений проекций спинового момента
на фиксированную ось). Возможны 2s+1
состояний с заданной волновой функцией,
отличающейся ориентацией спина.
Так как в отсутствие магнитного поля энергия частицы не зависит от ориентации спина, то наличие спина увеличивает число квантовых состояний с заданной энергией в 2s+1 раз. В зависимости от того, является ли спин целым или полуцелым, частицы делятся на два класса: бозе-частицы, или бозоны (с целым спином), и ферми-частицы, или фермионы (с полуцелым спином). Бозонами являются фотон (s=1), π- и К-мезоны (s=0). Большинство элементарных частиц (электроны, протоны, нейтроны и др.) имеют спин s = и являются фермионами.
Спин сложной частицы определяется числом входящих в нее фермионов. Если это число четное (Н, Н2, Не4), то сложная частица является бозоном, если нечетное (D, HD) – фермионом.
Волновая функция системы бозонов симметрична, а фермионов – антисимметрична относительно перестановки любой пары частиц. Волновая функция квантового идеального газа представляется произведением волновых функций отдельных частиц и полностью определяется заданием чисел заполнения nk каждого к-го одночастичного состояния. Требование антисимметрии волновой функции системы фермионов приводит к тому, что они удовлетворяют принципу Паули: в заданном квантовом состоянии может находиться не более одной частицы, т.е. nk=0; 1. В каждом одночастичном состоянии бозе-газа может находиться любое число частиц: nk=0;1;2,…N, где N – общее число частиц в системе.
Распределение частиц по одночастичным квантовым состояниям зависит от того, являются ли частицы бозонами или фермионами. В соответствии с этим существуют две квантовые статистики: статистика Бозе-Эйнштейна (для бозонов) и статистика Ферми-Дирака (для фермионов). Функция распределения по квантовым состояниям обоих классов частиц имеет вид:
= (nk) = k / k 1. Распределение бозе-частиц по состояниям называется распределением Бозе-Эйнштейна: = оно было установлено в 1924 г. Распределение частиц по энергиям найдем, умножив на число gk микросостояний с энергией : ( ) = 2. Распределение Ферми-Дирака Среднее число ферми-частиц в к-ом состоянии равно: = Распределение электронов по эгеогиям (s= ) будет ( ) = сопоставление распределений М-Б, Б-Э и Ф-Д: все эти три функции распределения идеальных газов можно записать в едином виде: = , (1) где для распределения М-Б, для распределения Ф-Д, для распределения Б-Э. На рис приведены графики этих функций распределения. Из (1 ) видно, что распределения Б-Э и Ф-Д переходят в распределение М-Б, т.е. газ становится классическим, если . (2) Если , то функция распределения газа отличается от максвелл-больщмановской и говорят, что газ вырожден. Величина называется фактором вырождения, выражение (2) – критерием невырожденности, а противоположные неравенства – критерием сильного вырождения.
Теплоемкость твердых тел рассчитывается по формуле Дюлонга и Пти: Твердое тело рассматривается как совокупность N независимых атомов, колеблющихся с одной и той же частотой ν. Однако средняя энергия, приходящаяся на одну степень свободы, полагается равной не КТ, а вычисляется по формуле Планка для средней энергии линейного осциллятора: (1)энергия грамм-атома, имеющего 3N степеней свободы, равна: (2), величину , имеющего размерность температуры, Эйнштейн назвал характеристической температурой тела. Следовательно , дифференцируя по температуре, получим
При низких температурах (Т<<θ), , вследствие чего единицей в знаменателе можно пренебречь и записать: При Т , а
