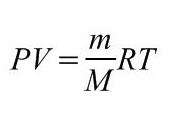- •2. Плавление и отвердевание кристаллических тел и объяснение этих процессов на основе представлений о дискретном строении вещества. Удельная теплота плавления.
- •Уравнение Теплового Баланса. Первый Закон Термодинамики
- •Первый закон термодинамики
- •Применение первого закона термодинамики к процессам в одноатомных идеальных газах
- •Первый закон Ньютона
- •[Править] Современная формулировка
- •Второй закон Ньютона
- •[Править] Современная формулировка
- •Третий закон Ньютона
- •[Править] Современная формулировка
- •2. Проводники в электростатическом поле. Диэлектрики в электрическом поле. Поляризация диэлектриков. Проводники в электрическом поле.
- •И деальный газ оказывает на стенки сосуда давление 1,01•105 Па. Тепловая скорость движения молекул 500 м/с. Найдите плотность газа.
- •1. Сила упругости. Закон Гука. Силы трения. Силы упругости
- •Закон Гука
- •2. Потенциальность электростатического поля. Потенциал и разность потенциалов.
- •Найти максимальную высоту, на которую поднимется камень, брошенный вертикально вверх со скоростью 20 м/с?
- •1. Импульс. Закон сохранения импульса. Реактивное движение.
- •2. Электроемкость. Конденсаторы. Энергия электрического поля конденсатора.
- •3. Шар массой 1 кг, летящий со скоростью 4 м/с, при ударе сжимает пружину. Найти максимальную энергию сжатия пружины.
- •1. Работа силы. Кинетическая энергия. Потенциальная энергия. Закон сохранения механической энергии. Работа силы (сил) над одной точкой
- •Работа силы (сил) над системой или неточечным телом
- •2. Сила тока. Закон Ома для участка цепи.
- •1. Статика. Момент силы. Условия равновесия твердого тела.
- •2. Сопротивление. Электрические цепи.
- •1. Возникновение атомистической гипотезы строения вещества и ее экспериментальные доказательства. Размеры и масса молекул. Количество вещества. Моль. Постоянная Авогадро.
- •Возрождение и раннее Новое время
- •2. Последовательное и параллельное соединения проводников.
- •[Править] Катушка индуктивности
- •[Править] Электрический конденсатор
- •[Править] Мемристоры
- •3. Через какой промежуток времени с момента старта мотоциклист, двигаясь с постоянным ускорением 5 м/с2 , разовьет скорость 90 км/ч?
- •1. Броуновское движение. Силы взаимодействия молекул. Строение газообразных, жидких и твердых тел. Тепловое движение молекул.
- •Построение классической теории
- •2. Основное уравнение мкт. Давление идеального газа. Связь давления и температуры.
- •3. Резистор сопротивлением r подключен к параллельно соединенным батареям с эдс 1и 2 и внутренними сопротивлениями соответственно r1 и r2. Определить ток, текущий через нагрузку.
- •1. Модель идеального газа. Границы применимости модели. Основное уравнение молекулярно-кинетической теории газа.
- •2. Работа и мощность тока. Электродвижущая сила. Закон Ома для полной цепи.
- •Эдс индукции
- •2. Электрический ток в металлах.
- •3. Напряженность поля в точке а направлена на восток и равна 2 • 105 н/Кл. Какая сила и в каком направлении будет действовать на заряд -3 мкКл?
- •1. Внутренняя энергия. Работа в термодинамике. Количество теплоты. Теплоемкость.
- •Работа в термодинамике
- •2. Зависимость сопротивления от температуры.
- •3. Сила взаимодействия двух одинаковых точечных зарядов, находящихся на расстоянии 0,5 м, равна 3,6 н. Найдите значения этих зарядов.
- •1. Первый закон термодинамики. Изопроцессы. Изотермы Ван-дер-Ваальса. Адиабатный процесс.
- •2. Сверхпроводимость.
- •1. Второй закон термодинамики: статистическое истолкование необратимости процессов в природе. Порядок и хаос.
- •2. . Собственная и примесная проводимости полупроводников, p— n переход. Полупроводниковый диод.
- •1. Тепловые двигатели: двигатель внутреннего сгорания, дизель. Холодильник: устройство и принцип действия. Кпд двигателей. Проблемы энергетики и охраны окружающей среды.
- •2. Транзистор.
- •3. Два шара массами 1 и 2 кг, скользят по гладкой поверхности на запад и север со скоростями 10 и 5 м/с соответственно. Определить направление и модуль импульса системы шаров.
- •2. Электрический ток в жидкостях.
- •1. Влажность воздуха. Кристаллические и аморфные тела. Модели строения твердых тел.
- •2. Электрический ток в вакууме. Электрический ток в газах. Плазма.
2. Основное уравнение мкт. Давление идеального газа. Связь давления и температуры.
Молекулярно-кинетическая теория (сокращённо МКТ) — теория XIX века, рассматривавшая строение вещества, в основном газов, с точки зрения трёх основных приближенно верных положений:
все тела состоят из частиц: атомов, молекул и ионов;
частицы находятся в непрерывном хаотическом движении (тепловом);
частицы взаимодействуют друг с другом путём абсолютно упругих столкновений.
Основными доказательствами этих положений считались:
Диффузия
Броуновское движение
Изменение агрегатных состояний вещества
В современной (теоретической) физике
термин молекулярно-кинетическая теория
уже не используется, хотя он встречается
в учебниках по курсу общей физики. В
современной физике МКТ заменила
кинетическая теория, в русскоязычной
литературе — физическая
кинетика, и статистическая
механика. В этих разделах физики
изучаются не только молекулярные
(атомные или ионные) системы, находящиеся
не только в «тепловом» движении, и
взаимодействующие не только через
абсолютно упругие столкновения.
![]() .
(24.1)
.
(24.1)
Уравнение (24.1) называют
основным уравнением
молекулярно-кинетической теории.
Обозначив
среднее значение кинетической энергии
поступательного движения молекул
идеального газа
![]() :
:
![]() ,
,
получим
![]() .
(24.2)
.
(24.2)
Давление идеального газа равно двум третям средней кинетической энергии поступательного движения молекул, содержащихся в единице объема
Давление идеального газа.
Связь между давлением, температурой, объемом и количеством молей газа ("массой" газа). Универсальная (молярная) газовая постоянная R. Уравнение Клайперона-Менделеева = уравнение состояния идеального газа.
|
Ограничения практической применимости:
Внутри диапазона точность уравнения превосходит точность обычных современных инженерных средств измерения. Для инженера важно понимать, что для всех газов возможна существенная диссоциация или разложение при повышении температуры. |
3. Резистор сопротивлением r подключен к параллельно соединенным батареям с эдс 1и 2 и внутренними сопротивлениями соответственно r1 и r2. Определить ток, текущий через нагрузку.
Билет №13
1. Модель идеального газа. Границы применимости модели. Основное уравнение молекулярно-кинетической теории газа.
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
Модель широко применяется для решения задач термодинамики газов и задач аэрогазодинамики. Например, воздух при атмосферном давлении и комнатной температуре с большой точностью описывается данной моделью. В случае экстремальных температур или давлений требуется применение более точной модели, например модели газа Ван-дер-Ваальса, в котором учитывается притяжение между молекулами.
Различают классический идеальный газ (его свойства выводятся из законов классической механики и описываются статистикой Больцмана) и квантовый идеальный газ (свойства определяются законами квантовой механики, описываются статистиками Ферми — Дирака или Бозе — Эйнштейна). Границы применимости модели идеального газа зависят от рассматриваемой задачи. Если необходимо установить связь между давлением, объемом и температурой, то газ с хорошей точностью можно считать идеальным до давлений в несколько десятков атмосфер. Если изучается фазовый переход типа испарения или конденсации или рассматривается процесс установления равновесия в газе, то модель идеального газа нельзя применять даже при давлениях в несколько миллиметров ртутного столба.
Давление газа на стенку сосуда является следствием хаотических ударов молекул о стенку, вследствие их большой частоты действие этих ударов воспринимается нашими органами чувств или приборами как непрерывная сила, действующая на стенку сосуда и создающая давление.