
- •Расчет параметров физико-химические свойства стекол
- •2.1. Вязкость стекол и расплавов
- •Расчет вязкости по методу м. В. Охотина
- •2.2. Поверхностное натяжение
- •2.3. Плотность стекла
- •2.5. Электрические свойства стекол
- •Расчет электрических свойств стекла
- •2.6. Теплофизические свойства стекол
- •2.7. Химическая устойчивость стекол
- •2.8. Оптические свойства стекол
- •Расчет оптических свойств стекла
2.7. Химическая устойчивость стекол
По характеру действия на стекло реагенты можно разделить на две группы. К первой группе относятся вода, влажная атмосфера, растворы кислот (кроме фосфорной и плавиковой), нейтральные или кислые растворы солей, т. е. реагенты с рН, равным семи и ниже. Ко второй группе относятся реагенты с рН среды выше семи, т. е. растворы щелочей, карбонатов и т. п. компонентов. По механизму воздействия к этой группе относятся также фосфорная и плавиковая кислоты.
Повышение температуры способствует ускорению разрушения стекла любым реагентом. С повышением температуры на каждые 10 ºС в области до 100 ºС скорость растворения растет в 1,5-2 раза. В автоклавах в условиях повышенных температур и давлений удается полностью растворить большинство силикатных стекол.
Перемешивание реагентов, движение жидкости также способствует более сильному разрушению стекла.
Большое влияние на скорость химического разрушения стекол оказывает качество их отжига. Закаленные стекла в общем случае разрушаются в 1,2-2 раза быстрее, чем стекла хорошо отожженные.
Устойчивость стекол к реагентам первой группы. Механизм действия этих реагентов на стекло заключается в том, что они вызывают удаление из поверхностного слоя щелочных компонентов путем гидролиза силикатов и последующего растворения гидроксидов. Схему гидролиза щелочных силикатов поверхностного слоя можно представить в виде
![]()
Растворимые гидроксиды щелочных металлов легко покидают места своего образования, диффундируя в раствор. Трудно растворимые гидроксиды остаются на поверхности стекла вместе с кремнеземистым остовом, состав которого соответствует составу конденсированных кремниевых кислот. Образовавшийся поверхностный слой отличается от исходного повышенной концентрацией оксида кремния, пронизан ультратонкими порами, заполненными продуктами гидролиза. Толщина и плотность кремнеземистого слоя влияет на скорость диффузии молекул воды к неразрушенному слою стекла. Образование поверхностного кремнеземистого слоя толщиной более 50 нм резко замедляет процесс дальнейшего разрушения стекла. При действии на поверхность стекла растворов кислот (соляной, азотной, муравьиной) в основном протекают те же процессы. При разбавлении кислот гидролиз усиливается, возрастает количество вещества, переходящего в раствор. В результате образуется более крупнопористый, толстый слой.
Образование на поверхности стекла кремнеземистого слоя снижает химическую активность поверхности, ее электропроводность, коэффициент отражения, в то время как прозрачность стекла остается высокой. Химическое связывание щелочных компонентов поверхностного слоя достигается также при контакте поверхности стекла со средой, содержащей кислые газы. Образующиеся сернокислые или углекислые соединения щелочных металлов легко смываются с поверхности.
Если поверхность стекла не омывается водой или раствором, т. е. если не происходит удаления растворимых продуктов реакции – гидрооксидов щелочных и некоторых щелочноземельных металлов, то они могу вызывать глубокие местные разрушения поверхности. Такие условия могут создаваться, например, при упаковке плоских листов стекла в ящик. Тонкие зазоры между листами обладают способностью капилляров втягивать и задерживать влагу. Устойчивость стекол к воде проверяют кипячением порошков в воде или растворах кислот, оценивают по количеству щелочей и других растворимых компонентов, перешедших в раствор. По химической устойчивости стекла делят на пять гидролитических классов (см. табл. 2.15).
Состав стекла оказывает большое влияние на химическую устойчивость. В серии силикатных стекол высокой химической устойчивостью к действию реагентов первой группы обладают кварцевое стекло, бopocиликатные, алюмосиликатные стекла. Существенно возрастает химическая устойчивость стекол при введении в состав оксидов титана, циркония, ниобия, тантала.
Таблица 2.15/ Гидролитическая классификация стекол
Гидролитический класс |
Ускоренный метод |
Методы Международной комиссии |
|
|||
количество выщелоченной Na2О, мг |
количество 0,01 N HСl, израсходованной на титрование выщелоченных компонентов, см3 |
DIN 12111 устойчивость к воде, количество выщелоченной Na2О, мг |
DIN 12116 устойчивость к 20 % НСl, потери массы, мг, на 100 см2 поверхности стекла |
|||
I – не изменяемые водой |
0-0,11 |
0-0,32 |
0-0,06 |
0-0,7 |
||
II – устойчивые стекла |
0,11-0,20 |
0,32-0,65 |
0,06-0,12 |
0,7-1,5 |
||
III – твердые аппаратные |
0,20-0,87 |
0,65-2,80 |
0,12-0,53 |
1,5 |
||
IV – мягкие аппаратные |
0,87-2 |
2,80-6,50 |
0,53-1,24 |
– |
||
V – нестойкие стекла |
2 и выше |
6,50 и выше |
1,24 и выше |
– |
||
Влияние оксидов щелочных и щелочноземельных металлов на химическую устойчивость стекол определяется растворимостью гидроксидов металлов в реагентах первой группы. Химическая устойчивость стекла тем выше, чем ниже растворимость соответствующих гидроксидов.
В ряду щелочных силикатов устойчивость понижается в направлении от литиевых к калиевым. При наличии в стекле оксидов двух щелочных металлов (суммарное содержание не ниже 10 мол. %) химическая устойчивость у стекол оказывается на 30-45 % выше, чем устойчивость стекол, содержащих эквивалентное количество одного из оксидов щелочных металлов.
Силикаты щелочноземельных металлов являются более химически устойчивыми, чем силикаты щелочных металлов. Химическая устойчивость понижается в ряду Be–Mg–Са–Sr–Ва. Цинксодержащие стекла отличаются высокой, а свинецсодержащие стекла – низкой химической устойчивостью. Введение оксидов алюминия, бора, а также других многозарядных ионов способствует эффективному повышению химической устойчивости стекол к реагентам первой группы.
Большинство распространенных промышленных стекол, основывающихся на натриево-кальциево-силикатной системе, относятся к III и IV гидролитическим классам. Более высокие показатели химической устойчивости характерны для медицинских и химико-лабораторных стекол.
Химическая устойчивость изделий из стекла к реагентам первой группы может быть значительно повышена путем специальной обработки или защиты поверхности. В качестве защитных покрытий могут применяться прозрачные пленки кремнийорганических соединений, фториды магния, оксиды алюминия и цинка. Обработку поверхности изделия можно проводить растворами кислот или выдержкой в атмосфере кислых газов.
Устойчивость стекол к реагентам второй группы. Реагенты второй группы разрушают непосредственно кремнекислородный каркас стекла. В результате полностью удаляются поверхностные слои, причем скорость стравливания остается постоянной, а глубина травления оказывается пропорциональной времени действия раствора. Разрушение поверхностного слоя можно представить в виде реакции
![]()
В результате воздействия растворов щелочей на силикатное стекло образуются стабильные анионы типа SiО , SiО , Si2O и соответствующие легкорастворимые силикаты щелочных металлов.
По силе воздействия гидроксиды щелочных металлов при одинаковой нормальности растворов располагаются в ряд NaOH–КОН–LiОH, в котором наиболее сильным действием обладает NaOH. Растворы карбонатов натрия и калия оказывают более сильное разрушающее действие на стекло, чем растворы едких щелочей равной нормальности. Гидроксиды щелочноземельных металлов действуют подобно гидроксидам щелочных металлов. Сила воздействия реагентов убывает в ряду Ba(OH)2–Sr(OH)2–Ca(ОН)2. Устойчивость стекол к действию щелочей характеризуют по потере массы на 100 см2 поверхности образца в результате кипячения в двунормальном растворе NaOH или в смеси 0,5 нормального раствора NaOH и 0,5 нормального раствора Na2CO3.
Классификация стекол по щелочеустойчивости допускает следующие уровни потерь для первых трех классов по методике Международной комиссии DIN 12122 (в мг массы на 100 см2 поверхности образца): 1-й класс – от 0 до 75; 2-й класс – от 75 до 150; 3-й класс – от 150 и более.
Щелочеустойчивость стекол мало зависит от состава. При кипячении кварцевого стекла в растворах щелочей его поверхность значительно разрушается. Однако в серии силикатных стекол кварцевое стекло оказывается более устойчивым по сравнению с многокомпонентными стеклами. Исключение составляют многоциркониевые стекла, а также стекла с высоким содержанием диоксида олова и оксида лантана. Разрушение стекол растворами фосфатов сопровождается образованием растворимых гидросиликофосфатов. По интенсивности разрушения силикатных стекол растворы фосфатов значительно превосходят растворы щелочей.
При действии плавиковой кислоты стравливание поверхностного слоя сопровождается образованием фтористых соединений кремния. Процесс отравления плавиковой кислотой можно представить в виде
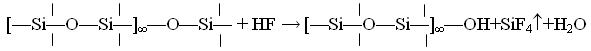
Химическая устойчивость силикатных стекол к реагентам второй группы по порядку величины примерно в 100 раз ниже, чем к реагентам первой группы. Максимальная потеря массы по гидролитической классификации в растворах реагентов первой группы составляет около 1,5 мг на 100 см2 поверхности стекла, в то время как в случае реагентов второй группы – до 150 мг на 100 см2. После действия реагентов второй группы поверхность стекла становится матовой, ухудшается прозрачность.
