- •Тверской государственный технический университет
- •Е.А. Панкратов, н.Ю. Старовойтова
- •Химия и физика полимеров
- •Часть 1
- •Химия и физика полимеров
- •Часть I
- •Учебное пособие
- •170026, Г. Тверь, наб. А. Никитина, 22
- •Список условных сокращений
- •Введение в специальность
- •Основные понятия и определения
- •1.2. Молекулярная масса и молекулярно-массовое распределение
- •1.3. Важнейшие свойства полимерных веществ
- •1.4. Классификация полимеров
- •1.5. Номенклатура полимеров
- •Основные принципы номенклатуры регулярных линейных однотяжных органических полимеров
- •Основные принципы номенклатуры сополимеров
- •2. Синтез полимеров: поликонденсация
- •Основы теории поликонденсации
- •Характеристика процесса
- •Функциональность мономера
- •Классификация поликонденсационных процессов
- •Гомо- и гетерополиконденсация
- •Типы химических реакций, используемых при поликонденсации
- •И типы полимеров, образующихся при поликонденсации
- •Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
- •Равновесная поликонденсация
- •Особенности равновесной поликонденсации
- •Начало роста цепи
- •Процесс роста цепи
- •Остановка роста цепи
- •1. Наличие в системе выделяющегося низкомолекулярного продукта реакции и установление равновесия между прямой и обратной реакциями.
- •Механизмы реакций равновесной поликонденсации
- •Кинетика равновесной поликонденсации
- •Неравновесная поликонденсация
- •Особенности неравновесной поликонденсации
- •Кинетика неравновесной поликонденсации
- •Способы проведения поликонденсации
- •Поликонденсация в твердой фазе, расплаве, растворе
- •Поликонденсация в эмульсии
- •Межфазная поликонденсация
- •Трехмерная поликонденсация
- •Совместная поликонденсация
- •3. Синтез полимеров: полимеризация
- •3.1. Основы теории полимеризации
- •Характеристика процесса
- •Цепные и ступенчатые реакции полимеризации
- •Термодинамика полимеризации
- •Миграционная полимеризация
- •3.3. Радикальная полимеризация
- •3.3.1. Характеристика радикальных процессов
- •Мономеры
- •Инициирование
- •Рост цепи
- •Обрыв цепи
- •Кинетический анализ радикальной полимеризации Вывод общего кинетического уравнения радикальной полимеризации
- •Типичная кинетическая кривая радикальной полимеризации
- •Ингибиторы и замедлители радикальной полимеризации
- •Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация
- •Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Характеристика ионных процессов
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
- •Ионно-координационная полимеризация
- •Алфиновые катализаторы
- •Катализаторы Циглера-Натта
- •Оксидные катализаторы
- •Ионная сополимеризация
- •4. Химические превращения
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Реакции, приводящие к увеличению молекулярной массы
- •Реакции, приводящие к уменьшению молекулярной массы
- •Старение полимеров
- •Библиографический список
И типы полимеров, образующихся при поликонденсации
Функциональные группы |
НМ продукт реакции |
Образующаяся межзвенная связь |
Тип образующегося полимера |
|
Первая |
Вторая |
|||
-ОН |
НООС- |
Н2О |
|
Сложный полиэфир |
-ОН |
RООС- |
ROH |
|
Сложный полиэфир |
-OH |
HO- |
Н2О |
-O- |
Простой полиэфир |
-ОН |
Cl- |
HCl |
-O- |
Простой полиэфир |
-NH2 |
Cl- |
HCl |
-NH- |
Полиамин |
-NH2 |
HOOC- |
Н2О |
|
Полиамид |
-NH2 |
|
HCl |
|
Полиамид |
-NH2 |
|
HCl |
|
Полиуретан |
-NH2 |
О=С=N- |
----- |
|
Полимочевина |
-ОН |
О=С=N- |
----- |
|
Полиуретан |
|
|
Cl (в виде NaCl) |
|
Полиуглеводород |
|
|
HCl |
|
Полиуглеводород |
|
|
Н2О |
|
Полиуглеводород |
Полиалкилирование
а) синтез фенолоальдегидных смол:
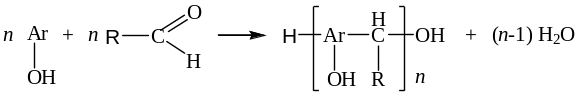
b) синтез полиалкиленфениленов:
nCl-RАrR-Cl → [-RАrR-]n +nCl2
c) cинтез полифениленов:
n Ar → [-Ar-]n + nH2
В табл. 4 показаны варианты получения различных поликонденсационных полимеров в зависимости от сочетания функциональных групп.
Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
При поликонденсации, если молекула мономера содержит две или более функциональных группы, возможно протекание двух конкурирующих типов реакций:
бимолекулярные (межмолекулярные) реакции, протекающие с образованием продуктов поликонденсации;
n a-(M)-b → -(M)n- + n ab,
где М – СПЗ, а, b –части функциональных групп, отщепляющиеся в ходе реакции;
мономолекулярные (внутримолекулярные) реакции, приводящие к образованию циклов – реакции циклизации.
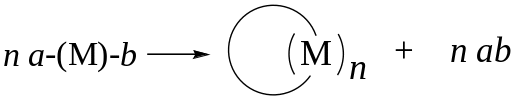
В некоторых случаях реакции циклизации могут происходить через стадии образования димера и тримера.
Вероятность циклизации определяется строением исходных мономеров и условиями реакции.
Для определения соотношения между циклизацией и поликонденсацией необходимо учитывать 2 фактора: термодинамический и кинетический.
Термодинамическим фактором является термодинамическая устойчивость циклов. Она зависит от числа атомов в цикле, поэтому для бифункциональных мономеров большое значение имеет количество СН2-групп (или других групп атомов) между функциональными группами: термодинамическая устойчивость циклов уменьшается с увеличением напряженности цикла. На рис. 2 показана зависимость способности к циклизации от числа СН2-групп в цикле. Данная зависимость характерна для циклов, состоящих из метиленовых групп. Для углеродных атомов с другими заместителями и для гетероциклов эта зависимость имеет тот же вид, однако может смещаться вправо или влево (в сторону циклов с большим или меньшим размером).
Наиболее напряженными являются 3- и 4-членные циклы; при переходе к 5-6-7-членным циклам напряжение резко уменьшается, снова увеличивается для 8-14-членных циклов и далее при переходе к циклам больших размеров уменьшается.Таким образом, ряд термодинамической устойчивости циклов следующий: 3;4;9-13; 8; 14 и выше; 5;7;6.
Ц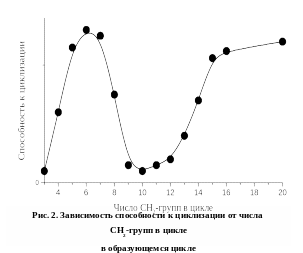 иклы,
состоящие из 4 и менее атомов углерода,
сильно напряжены из-за высокого углового
напряжения (вследствие больших отклонений
валентных углов от нормального
тетраэдрического угла 10928').
В циклах с числом атомов углерода >4
эти напряжения отсутствуют. Тем не
менее, 8-14-членные циклы являются
неустойчивыми. Это связано с тем, что
атомы заместителей в этих циклах
находятся внутри кольца на таких
расстояниях, что отталкивают друг
друга, и возникает транс-аннулярное
напряжение. В циклах с числом членов
более 14 подобное отталкивание уже не
имеет места.
иклы,
состоящие из 4 и менее атомов углерода,
сильно напряжены из-за высокого углового
напряжения (вследствие больших отклонений
валентных углов от нормального
тетраэдрического угла 10928').
В циклах с числом атомов углерода >4
эти напряжения отсутствуют. Тем не
менее, 8-14-членные циклы являются
неустойчивыми. Это связано с тем, что
атомы заместителей в этих циклах
находятся внутри кольца на таких
расстояниях, что отталкивают друг
друга, и возникает транс-аннулярное
напряжение. В циклах с числом членов
более 14 подобное отталкивание уже не
имеет места.
Кинетическим фактором является кинетическая разрешимость. Она зависит от возможности сближения двух функциональных групп, находящихся на разных концах молекулы. Чем меньше вероятность их встречи во времени, тем ниже кинетическая разрешимость циклизации.
На кинетическую разрешимость влияют 2 фактора – концентрация и температура. С повышением концентрации мономеров в системе начинают преобладать межмолекулярные контакты и уменьшается вероятность циклизации. С повышением температуры увеличивается доля процессов циклизации, т.к. энергия активации реакции циклизации, как правило, выше, чем энергия активации поликонденсации.
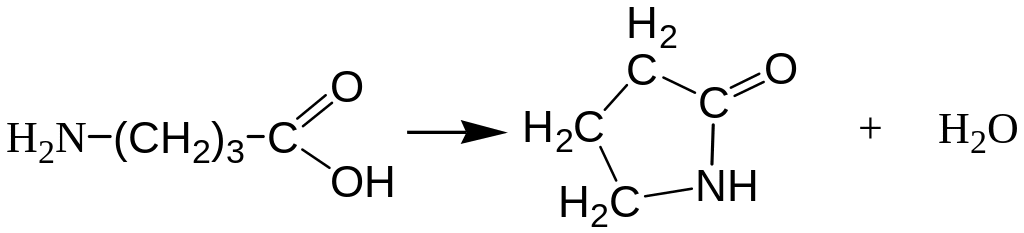
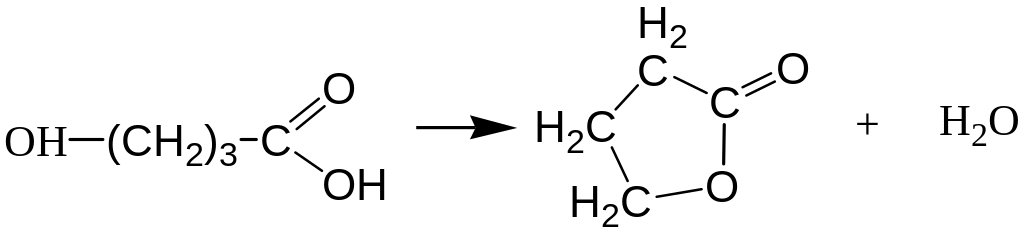
Возможность образования циклов определяется совокупностью термодинамических и кинетических факторов. Если строение исходных мономеров таково, что существует возможность образования 5-членных циклов, то наблюдается только циклизация, т.к. это выгодно и термодинамически, и кинетически (расстояние между концами короткой молекулы маленькое и вероятность встречи их велика). Например, γ-аминомасляная или γ-оксимасляная кислоты при конденсации образуют только пирролидон или бутиролактон соответственно:
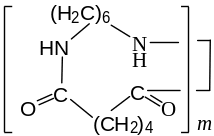
При возможности образования 6-7-членных циклов поликонденсация и циклизация протекают параллельно, т.к. возрастает длина молекулы и, следовательно, уменьшается кинетическая разрешимость циклизации. При наличии между функциональными группами 8 и более атомов в основной цепи реакция поликонденсации преобладает над циклизацией. Однако в процессе поликонденсации могут образовываться циклы даже с числом атомов в цикле 20 и более. Например, при поликонденсации гексаметилендиамина и адипиновой кислоты наряду с линейным полимером образуется некоторое количество макроциклов с числом СПЗ в цикле m=20-30:
nH2N(CH2)6NH2 + nHOOC(CH2)4COOH (2n-1)H2O +
+
 +
H-[-HN(CH2)6NHOC(CH2)4CO-]n-m-OH
+
H-[-HN(CH2)6NHOC(CH2)4CO-]n-m-OH