
1.2. Постановка задачи о расчёте вариантов получения кормового МКФ или камерного двойного суперфосфата, удовлетворяющих ГОСТу
В промышленности получают кормовой МКФ, как и двойной суперфосфат, путём обработки фосфатов фосфорной кислотой по камерному методу, который осуществляется в несколько стадий, отличающихся друг от друга аппаратурным оформлением.
Стадия основного разложения осуществляется в смесителе и суперфосфатной камере, затем дозревание (вызревание, доразложение на складе). Процесс сушки кормового МКФ производится после дозревания на складе. При получении же двойного суперфосфата следующей стадией является нейтрализация свободной кислоты, гранулирование, а затем сушка.
Технологический режим получения кормового МКФ и двойного суперфосфата во многом схож: используется фосфорная кислота концентрации 48-52% P2O5 (69-75% H3PO4), температура на стадии разложения составляет 353-373К (80-100С), дозревание происходит в одинаковых условиях. Однако при получении кормового МКФ расходуют несколько больше фосфорной кислоты (норма фосфорной кислоты для МКФ составляет 1,1 –1,25 от стехиометрического количества, для двойного суперфосфата – 1,05-1,1). Сушка кормового МКФ осуществляется при более высоких температурах (температура продукта 403-423К (130-150С)) для обеспечения высокой степени обесфторивания продукта, для двойного суперфосфата -373-383К (100-110С). На схеме приведены принципиальные потоки производства двойного суперфосфата из апатита камерным способом .
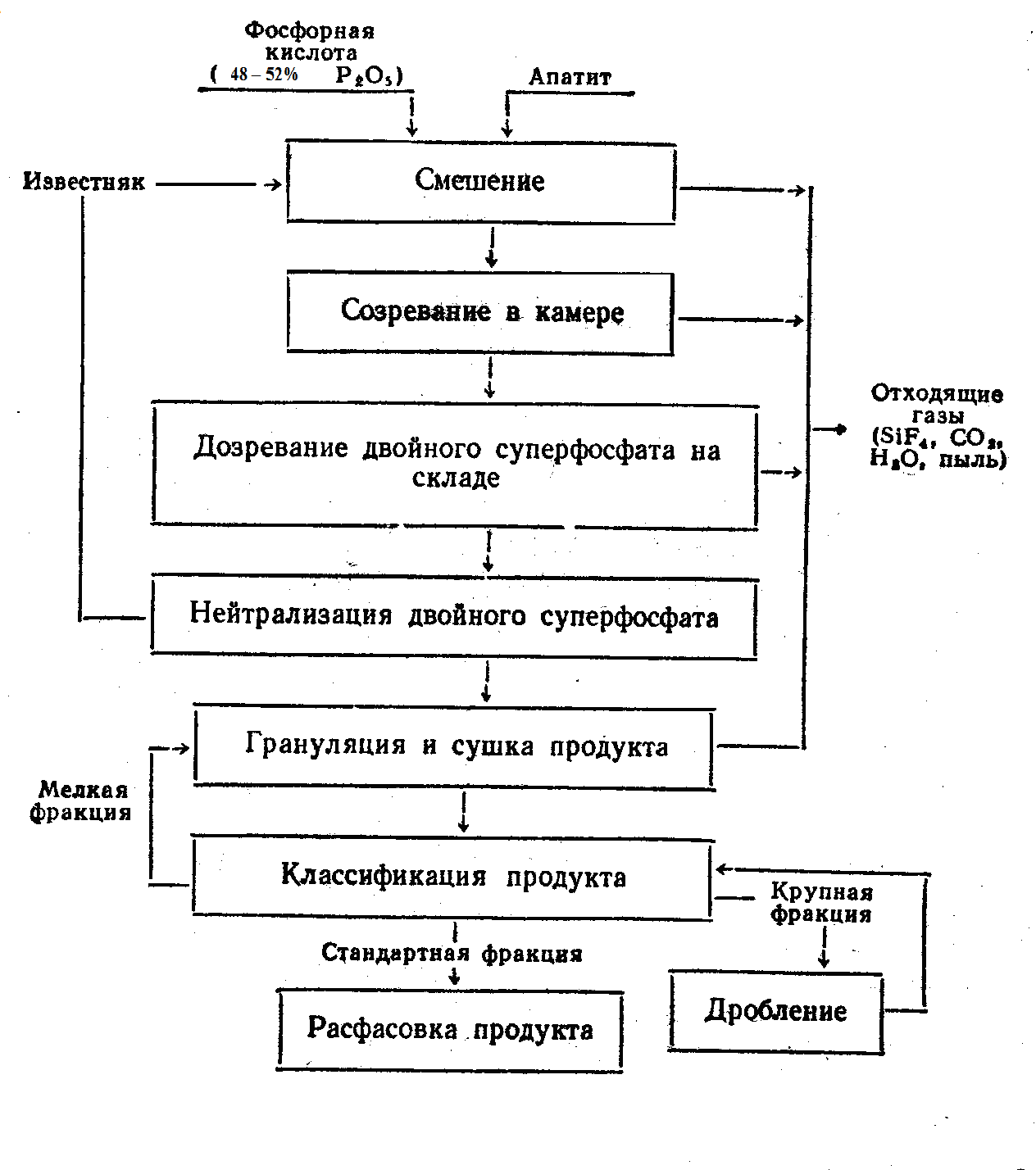
Рис.1.1. Получение двойного суперфосфата камерным способом
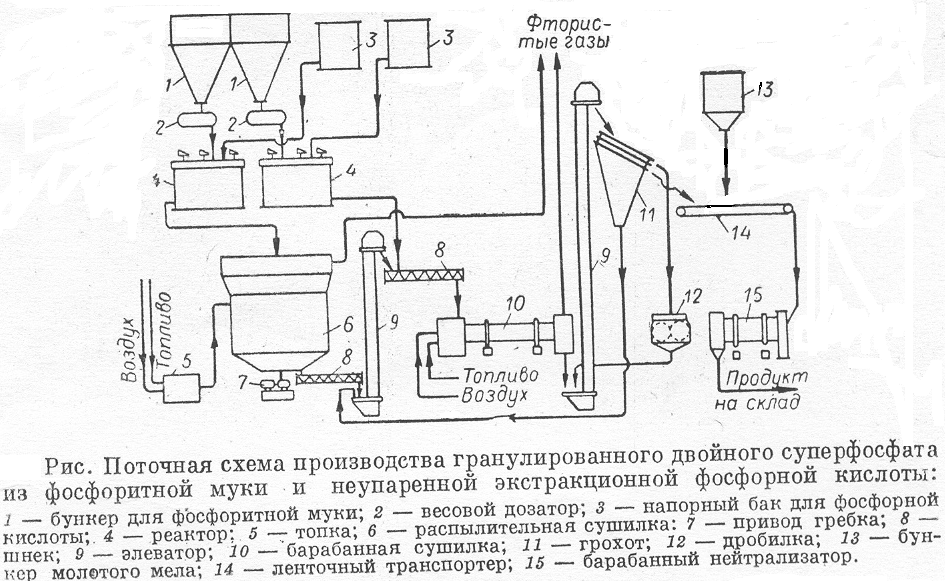
Недостатком камерного способа производства двойного суперфосфата является необходимость использования концентрированной термической фосфорной кислоты или упаренной экстракционной фосфорной кислоты (дополнительные расходы энергии на выпарку) для разложения фосфатов; перемешивания и длительного складского вылеживания продукта (затраты энергии и капитальные затраты на сооружение склада). Кроме того, при складском дозревании продукта выделяются сильно разбавленные фтористые газы, улавливание которых затруднительно. От этих недостатков свободен метод получения двойного суперфосфата по поточной схеме. В случае использования неупаренной экстракционной фосфорной кислоты (ЭФК) фосфаты разлагают в смесителях – реакторах, а избыточную влагу удаляют сушкой продукта в распылительных и вращающихся сушилках (см. рис. ниже).
При использовании полученной из апатитового концентрата кислоты с концентрацией 28-32% P2O5 (41-46% Н3РО4), при перемешивании пульпы в течение одного часа при 343-363K (70-900С) в непрерывно действующих реакторах фосфорит разлагается на 50-55%. Вытекающая из реакторов пульпа разделяется на два потока. Часть её (около половины) высушивается в распылительной сушилке топочными газами. Температура выходящих из сушилки газов- 398-403K (125-1300С). Температура высушенного материала не превышает 368K (950С). Продукт смешивают в шнековом смесителе-грануляторе со второй частью пульпы; сюда же поступает небольшое количество ретура (фракция размером меньше 1 мм). Затем гранулы, содержащие 20-22% влаги, высушивают в прямоточной барабанной сушилке до влажности 3-4%. В процессе сушки разложение фосфорита продолжается, и общая степень разложения сырья увеличивается до 80-85% ( и более при применении Н3РО4 повышенной концентрации- 37-40% P2O5). Продукт, выходящий из барабанной сушилки с температурой 368K (950С), направляется на грохочение. Гранулы с размерами от одного до 4-х мм нейтрализуют мелом в горизонтальном вращающемся барабане-нейтрализаторе для уменьшения свободной кислотности до 5% и ниже; это- готовый продукт, он содержит 42-44% P2O5усв. Частицы крупнее 4 мм измельчают в дробилке, смешивают с ретуром и возвращают в смеситель- гранулятор.
Таблица 1.2.
Характеристика продуктов
Продукты |
Содержание компонентов в продуктах, % |
||||
P2O5* с.к.р. |
P2O5 усв. |
P2O5св. не более |
F не более |
H2O не более |
|
Двойной суперфосфат ГОСТ 16306-75
Монокальцийфосфат ГОСТ 23999-80 |
- |
491 |
2,5 |
- |
4 |
- |
431 |
5,0 |
- |
5 |
|
55 |
- |
- |
0,2 |
4 |
|
50 |
- |
- |
0,2 |
4 |
|
![]() Примечание:
P2O5
с.к.р.-растворимое в 0,4%НСl.
Примечание:
P2O5
с.к.р.-растворимое в 0,4%НСl.
МКФ кормовой и двойной суперфосфат должны удовлетворять следующим основным показателям, указанным в табл.1.2.
Цель работы: Освоение методики расчёта по уравнениям реакций материальных балансов процесса производства кормового фосфата или двойного суперфосфата камерным способом на основе фосфорной кислоты (экстракционной и термической) из различного сырья (фосфорита, апатита).
Задание:
Используя полученные исходные данные (табл.1.3), по программе RP2.BAS рассчитать варианты материального баланса производства кормового МКФ или двойного суперфосфата по камерному способу.
Используя расчётные и литературные данные, сопоставить качественные показатели продукта и обосновать возможность получения продукта с более высокими ТЭП при изменении исходных данных: качественных показателей сырья (апатит, фосфорит), нормы и выбора вида кислоты (термическая или экстракционная).
По номеру студента в списке группы выбрать из таблицы свой вариант задач и их решения представить в отчёте вместе с условиями задач.
Порядок выполнения работы:
Набор исходных данных (табл.1.3) после получения задания для самостоятельного решения производится с дисплея компьютера после уточнения у преподавателя варианта и объёма необходимых расчётов. Изучите технологический режим получения МКФ камерным и поточным методом. После изучения подберите один или несколько вариантов показателей технологического режима, и сведите их в таблицу исходных данных и проанализируйте результаты расчётов, выполненных по использованной рабочей программе.
В отчёте приведите характеристику сырья (фосфорита, апатита), продуктов -кормового МКФ и двойного суперфосфата по камерному способу, параметры технологического режима, принципиальную схему производства продуктов, исходные данные для расчётов, таблицы результатов расчётов материального баланса и качественных показателей продуктов, список использованной литературы.
Если по качественным показателям полученный продукт (кормовой МКФ или двойной суперфосфат) не соответствует требованиям ГОСТа, то необходимо пересмотреть параметры технологического режима, выбрать по литературным и практическим данным улучшенный вариант, позволяющий получить продукт, удовлетворяющий стандарту.
Предполагаем, что на всех стадиях производства МКФ происходит постепенное разложение минералов, входящих в состав фосфатного сырья, с одинаковой скоростью и по следующим основным уравнениям (1.2.1-1.2.10):
Расчёт относительного количества фосфорной кислоты (a), которое необходимо для разложения исходных компонентов сырья в реакциях (1.2.1; 1.2.9; 1.2.10; 1.2.5; 1.2.6), воды (b), которая выделяется в результате разложения исходных компонентов сырья в реакциях (1.2.1; 1.2.10; 1.2.5; 1.2.6), а также основных и побочных продуктов (с), которые образуются в каждой из реакций (1.2.1; 1.2.9; 1.2.10; 1.2.5; 1.2.6; 1.2.7; 1.2.8) с соответствующими стехиометрическими коэффициентами.
Ca3(PO4)2 + 4 H3PO4 + 3H2O = 3Ca(H2PO4 ) 2∙ H2O (1.2.1)
![]() ;
;
![]() ;
;
![]()
(98; 18; 310; 252- Mr- H3PO4; H2O; Ca3(PO4)2 ; Ca(H2PO4 ) 2 ∙ H2O)
CaF2 + 2 H3PO4 + H2O = Ca(H2PO4)2∙ H2O + 2HF (1.2.2)
CaCO3+ 2 H3PO4 = Ca(H2PO4)2∙ H2O + CO2 (1.2.3)
MgCO3 + 2 H3PO4 = Mg(H2PO4)2 + CO2 + H2O (1.2.4)
Fe2O3 + 2 H3PO4 = 2FePO4 + 3 H2O (1.2.5)
![]()
![]()
![]()
(98; 18; 160; 151 - Mr - H3PO4; H2O; Fe2O3; FePO4)
Al2O3 + 2 H3PO4 = 2AlPO4 + 3 H2O (1.2.6)
![]()
![]()
![]()
(98; 18; 102; 122 - Mr - H3PO4; H2O; Al2O3; AlPO4)
4HF + SiO2 = SiF4 + 2H2O (1.2.7)
2HF + SiF4 = H2SiF6 (1.2.8)
![]() ;
;
![]() ;
;
![]()
(18; 19; 144; 60 - Mr - H2O; F; H2SiF6)
CaO + 2H3PO4 = Ca(H2PO4)2∙H2O (1.2.9)
![]() ;
;
![]()
(98; 56; 252 - Mr - H3PO4; CaO; Ca(H2PO4 ) 2 ∙ H2O)
MgO + 2H3PO4 = Mg(H2PO4)2 + H2O (1.2.10)
![]() ;
;
![]() ;
;
![]()
(98; 18; 40,3; 218,3 - - Mr - H3PO4; H2O; MgO; Mg(H2PO4)2)
Фтористый водород, выделяющийся при разложении сырья по реакции (1.2.2), соединяясь с кремнеземом, образует четырёхфтористый кремний (1.2.7), который может выделяться в газовую фазу, или образовывать кремнефтористоводородную кислоту, находящуюся в составе продукта (1.2.8). Допускаем, что фтор после разложения находится во всех фазах в виде H2SiF6.
Фосфор находится в сырье в виде трикальцийфосфата Ca3(PO4)2, с которым связана часть CaO, оставшаяся в виде CaF2, CaCO3 и др. Вместо расчёта по уравнениям реакций (1.2.3-1.2.4), расчёт ведётся по упрощённым уравнениям (1.2.9-1.2.10).
Степень разложения сырья составляет после камеры 75-80%, после дозревания на складе 80-90%, на стадии сушки монокальцийфосфата происходит дополнительное разложение минералов, входящих в состав сырья.
Программа расчётов материального баланса состоит из следующих разделов:
1.2.1. Расчёт состава фосфатного сырья.
1.2.2. Расчёт расхода фосфорной кислоты.
1.2.3. Расчёт состава продукта после разложения сырья в камере.
1.2.4. Расчёт состава продукта после стадии дозревания на складе.
1.2.5. Расчёт состава продукта после стадии сушки.
1.2.6. Расчёт качественных показателей продукта.
Исходные данные для расчёта приводятся в таблице 1.3.
Таблица 1.3
Исходные данные к программе RP2.BAS в системе QBASIC
Показатель |
Единица измерения |
Идентификатор вели-чины |
Варианты исходных данных
|
Контрольный пример[1]
|
||
фосфатного сырья |
кг |
Q |
1000
|
1000 |
||
2. Состав фосфатного сырья: CaO P2O5 MgO Fe2O3 Al2O3 F CO2 |
Доли единицы |
САО Р2О5 GMO FE2O3 AL2O3 F CO2 |
0,3 0,25 0,02 0,01 0,009 0,02 0,06 |
0,39 0,27 0,03 0,02 0,01 0,02 0,07 |
0,4 0,28 0,02 0,01 0,01 0,02 0,06
|
0,42 0,28 0,02 0,01 0,009 0,02 0,06
|
3. Концентрация фосфорной кислоты |
То же |
С |
0,7 |
0,75 |
0,72 |
0,7 |
4. Норма фосфорной кислоты |
>> |
Н |
1,1 |
1,0 |
1,2 |
1,05 |
5. Степень разложения по стадиям: разложение сырья в камере; дозревание продукта на складе; сушка продукта. |
>> |
X1
X2
X3 |
0,8
0,9
0,93 |
0,7
0,9
0,93 |
0,8
0,9
0,93
|
0,8
0,9
0,93 |
6. Степень выделения фтора в газовую фазу по стадиям: разложение; дозревание; сушки. |
>> |
F1 F2 F3 |
0,1 0,6 0,8 |
0,1 0,6 0,8 |
0,1 0,6 0,8 |
0,1 0,6 0,8 |
7. Испарение воды по стадия разложение; дозревание. |
>> |
W1 W2 |
0,1 0,15 |
0,1 0,15 |
0,1 0,15 |
0,1 0,15 |
8. Содержание воды в готовом продукте.
|
>> |
W3 |
0,03 |
0,03 |
0,03 |
0,03 |
9. Степень дегидратации Ca(H2PO4)2∙H2O. |
>> |
Y |
0,4 |
0,4 |
0,4 |
0,4 |
Описание алгоритма решения задачи.
Отметим, что в каждом разделе все употребляемые вещества обозначаются с помощью идентификаторов языка QBASIC [7].
1.2.1. Расчёт состава фосфатного сырья (таблица 1,3-1 вариант)
Масса компонентов исходного сырья (кг)
Расчётная часть:
Масса СаО, связанного в виде Ca3(PO4)2 в пересчете на Р2О5:
CAOT : P2O5∙ 3∙56/142 = 1,183 ∙P2O5∙ Q;
CAOT=1,183∙ 0,25∙ 1000 = 295,75
Масса Ca3(PO4)2 в пересчете на Р2О5
TK : 310 ∙P2O / 142 = 2,183 ∙P2O5 ∙Q;
TK = 2,18 ∙0,25∙1000 = 545,75
Масса СаО, связанного в виде других соединений:
GCAO : CAO ∙Q – CAOT; GCAO = 0,3∙1000 – 295,75 = 4,25.
Масса MgO : GMGO = GMO ∙Q. Масса MgO = 0,02∙1000 = 20.
Масса Fe2O3 : GFEO=FE2O3 ∙Q. Масса Fe2O3 = 0,01∙1000 = 10.
Масса Al2O3: GALO= AL2O3 ∙Q. Масса Al2O3 = 0,009∙1000 = 9.
Масса F: GF=F∙Q Масса F = 0,02∙1000 = 20.
Масса CO2:GCO=CO2∙Q Масса CO2 = 0.06∙1000 = 60.
Массу «прочих» определяют по разности между общей массой фосфатного сырья (например, 1000 кг ) и суммарной массой известных компонентов
PR = Q – (TK +GCAO +GFEO +GALO +GMGO +GF +GCO).
Масса прочих PR = 1000 - 545.75 - 4.25 – 20 – 10 – 9 – 20 - 60 = 331.
1.2.2.Расчёт количества фосфорной кислоты
Исходные данные:
Концентрация фосфорной кислоты (H3PO4) – C (доли единицы).
Норма расхода фосфорной кислоты, доли от стехиометрического количества – Н.
Различные виды расчёта количества фосфорной кислоты кг.
Количество фосфорной кислоты рассчитывают по уравнениям 1.2.1, 1.2.5, 1.2.6, 1.2.9, 1.2.10.
Стехиометрическое количество H3PO4 :
GK = TK ∙4 ∙98 /310 + GCAO ∙2∙98/56 + GFEO∙2∙98/160 + GMGO∙2∙98/40,3 +G ALO ∙ 2 ∙98 / 102.
GK = 545,75 ∙4 ∙98 / 310 + 4,25 ∙2∙ 98 / 56 + 10 ∙2∙ 98/ 160 + 20 ∙2 ∙ 98 / 40,3 + 9 ∙2 ∙98/ 102 = 831,7.
Практическая норма H3PO4 :
GKH = GK∙H.
GKH = 831.7∙1.1 = 914.9
Практическая норма фосфорной кислоты заданной концентрации:
GKP = GKH/C
GKP = 914,9 / 0,7 = 1307.
1.2.3. Расчёт состава продукта после разложения сырья в камере.
Исходные данные:
Степень разложения сырья – X1= 0,8 (в долях единицы).
Степень выделения фтора в газовую фазу – F1= 0,1 (в долях единицы).
Доля испарившейся H2O, вносимой с кислотой – W1=0,1 (в долях единицы).
Масса компонентов пульпы кг.
1) Состав пульпы, образующейся по уравнениям 1.2.1, 1.2.9, 1.2.5, 1.2.6, 1.2.10:
Ca(H2PO4) ∙Н2 О : CAP = (TK ∙X1∙3 ∙252) / 310 + (GCAO ∙X1 ∙ 252) / 56
CAP = (545,75 ∙0,8 ∙3 ∙252) / 310 + (4,25 ∙0,8 ∙252) / 56 = 1080,4. 1080,14.
FePO4 : FEP = GFEO ∙X1 ∙2∙151 / 160 = 1,89 ∙GFEO ∙ X1.
FEP = 1,89 ∙10 ∙0,8 = 15,12.
AlPO4 : ALP = GALO ∙X1 ∙2 ∙122 / 102.
ALP = 2,39 ∙9 ∙0,8 = 17,21.
Mg(H2PO4) : GMP = GMGO ∙X1 ∙218,3 /40,3 = 5,42 ∙GMGO ∙X1
GMP = 5,42 ∙20 ∙0,8 = 86,72.
H2SiF6 : GFK = (GF ∙X1 ∙144 / 6∙19) ∙ ( 1- F1) = 1,26 ∙GF ∙X1∙ (1 - F1).
GFK = 1,26 ∙20 ∙0,8 ∙0,9 = 18,14.
H3PO4 своб : GKS = GKH – GK ∙X1 = GK∙ (H - X1).
GKS = 831,7 ∙ 0,3 = 249,5. 249,51.
H2O : H2O(1) = (GKP - GKH) + (GFEO ∙3∙18 / 160 + GALO ∙3∙18 / 102 + GMGO 18 / 40,3 + GF ∙ 2 ∙ 18 / 6 ∙19 – TK ∙ 3 ∙18 / 310) ∙X1 – W1∙ (GKP – GKH) = (GKP – GKH) ∙ (1-W1) + (0,34 ∙ GFEO + 0,53 ∙ GALO + 0,45 ∙ GMGO + 0,316 ∙ GF – 0, 17 ∙ TK) ∙X1.
H2O(1) = (1307– 914,9) ∙ 0,9 + (0,34 ∙ 10 + 0,53 ∙ 9 + 0,45 ∙ 20 + 0,314 ∙ 20 – 0,17 ∙ 545,75) ∙ 0,8 = 295,48.
Неразложенное сырьё
HS = TKO + CAOO + FEOO + ALOO + GMOO + FO + COO
В том числе:
Ca3(PO4)2 : TKO = TK ∙ (1-X1); TKO = 545,75 ∙ 0,2 = 109,15.
CaO : CAOO = GCAO ∙ (1-X1); CAOO = 4,25 ∙ 0,2 = 0,85.
Fe2O 3: FEOO = GFEO ∙ (1-X1) FEOO = 10 ∙ 0,2 = 2.
Al2O 3: ALOO = GALO ∙ (1-X1) ALOO = 9 ∙ 0,2 = 1,8.
MgO : GMOO = GMGO ∙ (1-X1) GMOO = 20 ∙ 0,2 = 4.
F : FO = GF ∙ (1-X1) FO = 20 ∙ 0,2 = 4.
CO2: COO = GCO ∙ (1-X1) COO = 60 ∙ 0,2 = 12.
HS = 109,15 + 0.85 + 2 + 1.8 + 4 + 4 + 12 = 133,8.
Прочие смеси:
PRO(1) = PR – GF ∙ X1 ∙60 / 6 ∙ 19 = PR – 0,53 ∙ GF ∙ X1.
PRO(1) = 331 – 0,53 ∙ 20 ∙ 0,8 = 322,52.
2) Состав газовой фазы:
CO2 : CO2G = GCO ∙ X1, CO2G = 60 ∙0,8 = 48.
H2SiF6 : FKG = GF ∙X1 ∙F 1∙144 / 6 ∙ 19 FKG = 1,26 ∙20 ∙ 0,8 0,1 = 2,02.
= 1,26 ∙ GF ∙ X1 ∙ F1.
H2O: H2OG = (GKP – GKH) ∙ W1 H2OG = (1307 – 914,9) ∙ 0,1 = 39,21.
Полученные данные заносят в таблицу 1.4.
Таблица 1.4.
Разложение фосфатов в камере
Приход |
Масса, кг |
Расход |
Масса, кг |
||
1. Фосфатное сырьё в том числе: Ca3(PO4)2 (в пересчёте на P2O5) CaO (в пересчёте на P2O5) Fe2O3 Al2O3 MgO F CO2 прочие |
Q = 1000
TK = 545,75 GCAO=4,25
GFEO=10 GALO=9 GMGO=20 GF=20 GCO=60 PR=331 |
1. Пульпа (подкамерный продукт): в том числе Ca(H2PO4)2∙ ∙H2O FePO4 AlPO4 Mg(H2PO4)2 H2SiF6 H3PO4 H2O неразложенное сырьё прочие |
CAP = 1080,14 FEP = 15,12 ALP = 17,21 GMP = 86,72 GFK = 18,14 GKS = 249,51 H2O(1) =295,48 HS = 133,8 PRO(1)=322,52 |
||
|
|
2. Газовая фаза, в том числе: H2SiF6 CO2 H2O |
FKG = 2,02 CO2G = 48 H2OG = 39,21 |
||
Итого: |
2307 |
Итого: |
2308,11 |
||
Неувязка баланса Х, % = 0,05 |
|
||||
1.2.4. Расчёт состава продукта после стадии дозревания на складе
Исходные данные:
Состав пульпы подкамерного продукта из таблицы 1.4.
Степень разложения сырья – Х2 =0,9 (в долях единицы).
Степень выделения фтора в газовую фазу – F2 = 0,6 (в долях единицы).
Доля испаряемой воды, вносимой с пульпой – W2=0,15 (в долях единицы).
Масса компонентов продукта на стадии дозревания кг.
На стадии дозревания происходит дальнейшее разложение компонентов сырья фосфорной кислотой
1). Состав вызревшего продукта:
Ca(H2PO4)2 ∙H2O : CAP = CAP = (2,44 ∙ 545,75+4,5 ∙ 4,25) ∙ 0,9=1215,68
=(2,44 ∙TK+4,50 ∙ GCAO) ∙ X2, .
FePO4 : FEP = 1.89 ∙ GFEO ∙Х2, FEP = 1, 89 ∙10 ∙ 0,9 = 17,01.
AlPO4 : ALP = 2,39 ∙ GALO ∙ X2, ALP = 2,39 ∙ 9 ∙ 0,9 = 19,36.
Mg(H2PO4)2 : GMP = 5,42 ∙ GMGO ∙ X2, GMP = 5,42 ∙ 20 ∙ 0.9 = 97,59.
H2SiF6 : GFK = 1,26 ∙ GF ∙ X2∙ (1 – F2), GFK = 1,26 ∙20 0,9 ∙ 0,4 = 9,07.
H3PO4 : GKS = GKH – GK ∙X2 = GKS = 831,7∙ 0,2 = 166,34.
= GK∙ (H – X2),
H2O: H2O(2) = H2O(1) ∙ (1 – W2) + (X2 – X1) ∙ (0,34 ∙ GFEO + 0,53 ∙GALO + 0,45 ∙ GMGO + 0,316 ∙ GF – 0,17 ∙ TK),
H20(2) = 295,72 ∙ 0,85 + 0,1∙ (0,34 ∙10 + 0,53 ∙ 9 + 0,45 ∙ 20 + 0,316 ∙ 20 – 0,17 ∙ 545,75) = 243,89.
Неразложенное сырьё: HS =
=(TK + GCAO + GMGO + GFEO + GALO + GCO + GF) ∙ (1 – X2)
HS = (545,75 + 4,25 + 20 + 10 + 9 + 60 + 20) ∙ 0,1 = 66,9.
Прочие примеси:
PRO(2) = PRO(1) – 0,53 ∙ GF ∙ X2, PRO(2) = 322,52 – 0,53 ∙ 20 ∙ 0,9 = 312,98.
2) Состав газовой фазы:
CO2: CO2G = GCO ∙ (X2 – X1), CO2G = 60 ∙ 0,1 = 6.
H2SiF : FKG=
= 1,26 ∙G F∙ (X2 ∙ F2 – X 1 ∙ F1), FKG = 1,26 ∙20(0,9 ∙ 0,6 – 0,8 ∙ 0,1) = 11,59.
H2O : H2OG = H2O(1) ∙ W2 H2OG = 295,72∙ 0,15 = 44,35.
Полученные данные заносят в таблицу 1.5
Таблица 1.5
МКФ на стадии дозревания на складе готового продукта
Компоненты |
Приход, кг |
Расход, кг |
Ca(H2PO4)2 ∙ H2O FePO4 AlPO4 Mg(H2PO4)2 H2SiF6 H3PO4 H2O неразложенное сырьё прочие |
CAP = 1080,14 FEP = 15,12 ALP = 17,21 GMP = 86,72 GFK = 18,14 GKS = 249,51 H2O(1) = 295,72 HS = 133,8 PRO(1) = 322,52 |
CAP = 1215,68 FEP = 17,01 ALP = 19,36 GMP = 97,59 GFK = 9,08 GKS = 166,34 H2O(2) = 243,89 HS = 66,9 PR(2) = 312,98 |
CO2 H2SiF6 H2O |
CO2G = 48 FKG = 2,02 H2OG = 39,21 |
CO2G = 6 FKG = 11,59 H2OG = 44,35 |
Итого: |
2308,11 |
2210,76 |
Неувязка баланса X % = 4,2 |
|
|
1.2.5. Расчёт состава продукта после стадии сушки
Исходные данные:
Состав вызревшего продукта из таблицы 1.5.
Степень разложения сырья – Х3= 0,93 (в долях единицы).
Степень выделения фтора в газовую фазу – F3=0,8 (в долях единицы).
Содержание влаги в готовом продукте – W3= 0,08 (в долях единицы).
5. Степень дегидратации продукта –Y=0,4.
Масса компонентов высушенного продукта кг.
Состав высушенного продукта:
Ca(H2PO4)2 ∙H2O : CAP = ( 2,44 ∙ 545,75 + 4,5 ∙ 4,25) ∙ 0.93 = 1256,20.
CAP= (2,44 ∙ TK + 4,50 ∙ GCAO) ∙ X3,
FePO 4: FEP = 1,89 ∙ GFEO ∙ X3, FEP = 1,89 ∙10 ∙ 0,93 = 17,58.
AlPO4 : ALP = 2,39 ∙ GALO ∙ X3, ALP = 2,39 ∙ 9 ∙ 0,93 = 20.
Mg(H2PO4)2 : GMP = 5.42∙GMGO∙ X3, GMP = 5,42 ∙2 ∙ 0,93 = 100,8.
H2SiF 6: GFK = 1,26∙GF∙X3∙ (1 – F3), GFK = 1,26 ∙2 0 0,93∙ 0,2 = 4,69.
H3PO 4: GKS = GKH – GK ∙X3 = GKS = 831,7 ∙ 0,17 = 141,39.
= GK∙ (H – X3)
Неразложенное сырьё:
HS = (TK + GCAO + GMGO +
+ GFEO + GALO + GCO + GF) ∙ (1 – X3)
HS = (545,75 + 4,25 + 20 + 10 + 9 + 60 + 20) ∙ 0,07 = 46,83
Прочие:
PRO(3) = PRO(2) – 0,53 ∙ GF ∙ X3,
PRO(3) = 312,98 – 0,53 ∙ 20 ∙ 0,93 = 303,12
GMKF = CAP + FEP + ALP + GMP + GFK + GKS + HS + PRO,
где GMKF – масса продукта.
GMKF = 1256,20+ 17,58 + 20 + 100,08 + 4,69 + 303,12+ 141,39+46,83=1890,61
H2OMFK=GMFK∙W3/(1-W3), H2OMFK = 1890,61∙ 0,03 / 0,97 = 58,47
.
2) Состав газовой фазы:
CO2 : CO2G = GCO ∙ (X3 – X2 )
CO2G = 60 ∙ 0,03 = 1,8.
H2SiF6 : FKG =1,26 ∙ GF∙ (X3 ∙ F3 – X2 ∙ F2), .
FKG = 1,26 ∙20∙ (0,93 ∙ 0,8 – 0,9 ∙ 0,6) =5,0 4.
H2O: H2OG = H2O(2) + (X3 – X2) ∙ (0,34 ∙ GFEO + 0,53 ∙ GALO + 0,45 ∙GMGO + 0,316 ∙GF – 0,17 ∙TK) – H2OMFK,
H2OG = 243,89 + 0,03∙ (0,34 ∙10 + 0,53∙ 9 + 0,45 ∙ 20+ 0,316 ∙20 – 0,174 ∙545,75) –58,47 =183,28.
Полученные данные заносят в таблицу 1,6
Таблица 1.6
МКФ на стадии сушки
Компоненты |
Приход, кг |
Расход, кг |
Ca(H2PO4)2 H2O FePO4 AlPO4 Mg(H2PO4)2 H2SiF6 H3PO4 H2O неразложенное сырьё прочие |
CAP = 1215,68 FEP = 17,01 ALP = 19,36 GMP = 97,59 GFK = 9,07 GKS = 166,34 H2O(2) = 243,89 HS = 66,9 PRO(2) = 312,98 |
CAP = 1256,2 FEP = 17,58 ALP = 20 GMP = 100,8 GFK = 4,69 GKS =141,39 H2OМКF = 58,47 HS =46,83 PRO(3) = 303,12 |
CO2 H2SiF6 H2O |
CO2G = 6 FKG = 11,59 H2OG = 44,35 |
CO2G = 1,8 FKG = 5,14 H2OG = 183,28 |
Итого: |
2210,76 |
2139,3 |
Неувязка баланса X, % =3,2 |
|
|
1.2.6. Расчёт качественных показателей продукта
Содержание P2O5 (в долях единицы):
P2O5MKF = (Q ∙ P2O5 + 0,724 ∙ GKH) / (GMKF + H2OMKF),
P2O5MKF = (1000 ∙ 0,25 + 0,724 ∙ 914,9) / (1890,61+58,47) = 0,468.
Содержание P2O5 усв (в долях единицы):
P2O5USV = (0,563 ∙ CAP + 0,47 ∙FEP + 0,58 ∙ALP + 0,564 ∙GMP + 0,724 ∙GKS) / (GMKF + H2OMKF),
P2O5USV = (0,563 ∙1256,2+ 0,47 ∙17,577 + 0,582 ∙ 20 + 0,564 ∙100,8 + 0,724∙ 141,39) / ((1890,61+58,47) = О,44.
Содержание P2O5 св (в долях единицы):
P2O5SV = 0.724 ∙ GKS / (GMKF+H2OMKF), P2O5SV=0,724 ∙141,39/ (1890,61+58,47) = 0,053.
Содержание фтора (в долях единицы):
F = (GF∙ (1 – X3) + 0.792∙FK) / GMKF + H2OMKF),
F = (20∙ 0,07 + 0,792 ∙ 4,68) / (1890,61+58,47) = 0,0026.
H2O= H2OMKF/ (GMKF + H2OMKF) (в долях единицы),
H2O = 57,92/1949,08=0,03.
Данные заносят в таблицу 1.7.
Таблица 1.7
Качественные показатели монокальцийфосфата
Содержание показателей продукта, в долях единицы |
||||
P2O5 |
P2O5USV |
P2O5SV |
F |
H2O |
0,468 |
0,44 |
0,053 |
0,0026 |
0,03 |
1.3. Краткие сведения для самостоятельного решения задач [2,3]
В производстве фосфорной кислоты степень разложения фосфата серной кислотой характеризуется коэффициентом разложения:
Kразл=(0,7∙100%)/(CCaO/![]() )
(1.3.1)
)
(1.3.1)
где 0,7— отношение молекулярных масс СаО/SО3 в сульфате кальция Ссао и — концентрации СаO и SОз в фосфогипсе.
Фосфогипсом или фосфорополугидратом называют осадок сульфата кальция СаSО4∙2Н2О или СаSО4∙0,5Н2О, содержащий неразложившиеся фосфаты.
Для облегчения расчетов по уравнениям используют следующие понятия. Нормой серной кислоты называют число массовых долей моногидрата Н2SО4, приходящихся на 100 масс, долей фосфата. Стехиометрическую норму Н2SО4 определяют, исходя из общего содержания СаО в фосфате:
98 •Ссаo/56= 1,75 Ссао масс. долей на 100 масс. долей фосфата, (1.3.2)
где 98 и 56 — молекулярные массы Н2SО4 и СаО; Ссао — содержание СаО в 100 масс. долях фосфата.
Если концентрация серной кислоты с, а коэффициент избытка ее (то есть, отношение фактического количества к стехиометрическому) составляет а, то расход кислоты равен:
mK=1,75∙CCaO∙a/c (1.3.3)
Масса образовавшегося в результате реакции сухого фосфогипса (СаSО4∙2Н2О) или фосфополугидрата (СаSО4∙0,5Н2О) в расчете на единицу массы фосфата
оценивается гипсовым числом: gr=mг/mф,
где mг и mф — массы фосфогипса (фосфорополугидрата) и фосфорита (апатита). В производстве суперфосфата стехиометрической нормой серной кислоты называют число массовых долей серной кислоты (моногидрата), приходящихся на 1 масс, долю Р2О5, рассчитанное по уравнению реакции:
Ca5F(PO4)3+3,5H2SO4=3,5CaSO4+1,5Ca(H2PO4)2+HF (1.3.4)
исходя из предположения, что реакция идет до конца:
3,5M (H2SO4 )/1,5M (P2O5)=343/213= 1,61. (1.3.5)
Выход суперфосфата на 1 т сырья определяют по формуле:
MC=CФ ∙1000/CC, (1.3.6)
где Сф и CC — содержание Р2О5 соответственно в исходном фосфате и в полученном суперфосфате.
Процентное отношение усвояемого Р2О5 к общему содержанию в продукте называют коэффициентом разложения сырья.
K=CусвP2O5∙100/CобщP2O5 (1.3.7)
Пример 1. Определите коэффициент избытка а серной кислоты при получении простого суперфосфата, если норма серной кислоты (моногидрата) 68 масс. долей на 100 масс. долей апатитового концентрата с содержанием Р2О5 39,4 %. .
Решение. Стехиометрическую норму серной кислоты определяем, используя коэффициент 1,61 (формула 1.3.5). На одну масс. долю Р2О5 необходимо 1,61 масс. долей серной кислоты, следовательно, на 39,4 масс. долей Р2О5, содержащихся в 100 кг апатитового концентрата, нужно:
1,61∙39,4 = 63,4 (кг).
Отсюда коэффициент избытка равен:
а=68/63,4 = 1,07.
Стехиометрическую норму фосфорной кислоты x (в кг/100кг фосфата) рассчитывают по реакциям разложения компонентов сырья в соответствии с его минералогическим составом или по формуле
![]() ,
(1.3.8)
,
(1.3.8)
где a,b,c,d и e- содержание СаО, Ме2О3, MgO, P2O5- в разлагаемом фосфате и концентрация первого иона Н+ в фосфорной кислоте, %; 145- условная средневзвешенная молекулярная масса полуторных окислов.
Пример 2. Определить расход фосфорной кислоты, необходимой для разложения 100 кг фосфата, содержащего 26% P2O5, 41,8% СаО, 5,08% Ме2О3. Концентрация в кислоте первого иона водорода,определённая титрованием с диметилгельбом, равна 0,712%.
Решение. По формуле (1.3.8)
находим:
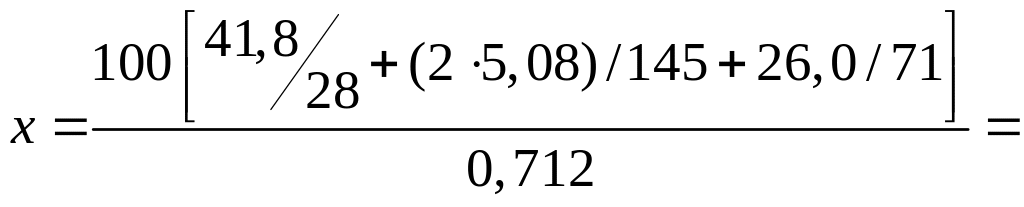
![]()
Пример 3. На 1000 кг двойного суперфосфата расходуется 366,7 кг фосфорной кислоты (в расчёте на P2O5) и 349,1 кг апатитового концентрата. Определить избыток кислоты на 100 кг апатитового концентрата по сравнению со стехиометрическим её количеством.
Решение. Согласно уравнению реакции
Са5F(PO4)3+7H3PO4+5H2O=5Ca(H2PO4)2∙H2O+HF (1.3.9)
теоретический расход фосфорной кислоты на 100 кг апатита составляет
![]() ,
,
где 142 504 –молекулярные массы P2O5 и Са5F(PO4)3.
Фактический расход кислоты на 100 кг апатитового концентрата равен
(100∙366,7)/349,1=105,04 кг P2O5
Следовательно, применяемый избыток кислоты составляет
![]()
Пример 4. На разложение 1000 кг апатитового концентрата, содержащего 39,8% Р2О5, расходуется 1950 кг 54%-ной фосфорной кислоты (в пересчете на Р2О5). Определите, сколько извести добавляют для полной нейтрализации избытка фосфорной кислоты и какова концентрация Р2О5 общ и Р2О5 усв в готовом продукте. Степень разложения апатитового концентрата 80%. Содержание СаСОз в известняке 95%. Степень использования его 90%. Фосфор в апатите находится в виде соли Са5F(РО4)з.
Решение. Процентное содержание Ca5F(PO4)3 в апатите составляет:
2∙504∙39,8 /3∙142-=94,2 (%).
Масса Са5F(РО4)з, вступившего во взаимодействие с фосфорной кислотой, с учетом степени разложения:
1000∙0,942∙0,80 = 753,6 (кг)
Масса Р2О5 в фосфорной кислоте:
1950∙0,54=1053 (кг).
Рассчитаем, сколько фосфорной кислоты пошло на разложение 753,6 кг фторапатита в соответствии с уравнением реакции (1.3.9):
753,6∙7∙142/2∙504=743,13 (кг).
При этом получается суперфосфата:
753,6∙5∙252/504= 1134 (кг),
где 252 — молекулярная масса Са(Н2РО4)2∙Н2О. Избыток фосфорной кислоты (в пересчете на Р2О5):
1053—743,13=309,9 (кг).
Масса известняка, необходимая для его нейтрализации, согласно уравнению реакции:
309,9∙100/142=218,2 (кг),
где 100 — молекулярная масса СаСО3.
При этой реакции образовалось Са(Н2РО4)2∙Н2О:
309,9∙252/142 =549,96 (кг).
Всего суперфосфата вместе с неразложившейся частью апатита:
1134 + 549,96+(1000—753,6) =1930,36 (кг) Определяем массу Р2О5усв в 1683,96 кг суперфосфата: 1683,96 ∙142 /252 = 948,9 (кг)
и процентное содержание его в готовом продукте:
948,9∙100% / 1683,96 =49,2 (%).
Определяем массу Р2О5 в неразложившемся апатите:
(1000—753,6)∙0,398 = 98,07 (кг)
и массу Р2О5общ: 948,9 + 98,07 = 1046,97 (кг).
Процентное содержание Р2О5Общ в готовом продукте составит:
1046,97∙100%/1930,36=54,2%.
1.3.1. Задачи и ответы для самостоятельного решения
1. Определите процентное содержание Р5О5 во флотационном фосфорите, перерабатываемом в простой суперфосфат. Процесс протекает в стандартной суперфосфатной камере диаметром 7,1 м, высотой 2,5 м и интенсивностью 600 кг/м3 в 1 ч суперфосфата, содержащего 15% Р2О5. В сутки перерабатывается 7130 т фосфорита. Ответ: 30% Р2О5 .
2. Определите теоретический расход серной кислоты в расчете на моногидрат для разложения 5000 кг апатитового концентрата, содержащего 50,5% СаО. Ответ: 4419 кг
3. Определите расход башенной (75%-ной) серной кислоты для обработки 1 т апатитового концентрата, содержащего 52,3% СаО, если норма серной кислоты составляет 98,9% от стехиометрической массы. Ответ: 1206,9 кг
4. При разложении фосфорита, содержащего 25% Р2О5, образовалось 3850 кг фосфогипса. Считая, что разложение фосфорита произошло полностью, определите, сколько 35%-ной Н3РО4 получено при этом. Гипсовое число gг= 1,6. Ответ: 372 кг
5. 12 000 кг фосфорита обрабатывают серной кислотой. Анализ показал, что в полученном фосфогипсе содержание СаО 43,5%, SОз 56,5%. Определите массу неразложившегося фосфата Са3(РO4)2. Ответ: 1092 кг
6. Рассчитайте, сколько теоретически необходимо серной кислоты (73%-ной) и воды для обработки 100 кг апатитового концентрата, содержащего 72% . Са3(РO4)2, с целью получения: а) экстракционной фосфорной кислоты полугидратным методом, т. е. с образованием
СаSО4∙0,5 Н2О; б) простого суперфосфата. Ответ: а) 91 кг; 6,27 кг; б) 60,70 кг; 4,18 кг
7. Из апатитового концентрата, содержащего 37% Р2О5, получают экстракционную фосфорную кислоту дигидратным способом. Полученная 30%-ная Н3РО4 в пересчете на Р2О5 после выпаривания содержит 43,5% Р2О5. Сколько упаренной кислоты можно получить из 1000 кг апатитового концентрата? Сколько воды удаляется при выпаривании? Ответ: 849,4 кг; 382,2 кг
8. Обрабатывают 1500 кг апатитового концентрата (СаО 52%, Р2О5 39,4%) башенной 75%-ной серной кислотой. Сколько воды нужно добавить для получения 35%-ной но содержанию Р2О5 фосфорной кислоты (процесс полугидратный)? Норма серной кислоты 105% от стехиометрической. Ответ: 746,25 кг.
9. 1000 кг апатитового концентрата (39,4% Р2О5) обрабатывают серной кислотой. Коэффициент извлечения Р2О5 при экстракции 98%, потери Р2О5 при фильтрации 20%. Гипсовое число 1,6. В результате разбавления при экстракции и отмывке отношение жидкой фазы к твердой 3:1. Концентрация образующейся при этом фосфорной кислоты 32%.Каков массовый выход пульпы и продукционной кислоты? Ответ:6400; 1196кг.
10. Составьте материальный баланс производства 500 кг экстракционной фосфорной кислоты 35%-ной концентрации (Р2О5) по следующим данным: апатитовый концентрат содержит СаО 51,3%, Р2О5 39,1%. Концентрация серной кислоты 78%. Норма серной кислоты 98,8% от стехиометрической по СаО. Отношение жидкой фазы к твердой в пульпе 2,5 : 1. Потери Р2О5 при экстракции и отмывке 4 %. Выделение газообразной фазы за счет фтора в виде SiF4 8,21 кг. Ответ. Приход: 466,22 кг апатитового концентрата, 511,10 кг серной кислоты, 1551,2 кг воды. Расход: 500 кг фосфорной кислоты, 746,6 кг фосфогипса; 8,21 кг потери.
11. Сколько фосфорита 92%-ной концентрации Ca3(PO4)2 нужно разложить в электрической печи для получения 1000 кг 73%-ной Н3РО4? Сколько энергии для этого необходимо?
Ca3(PO4)2+5C+2SiO2=P2+5CO+Ca3Si2O7; ΔН=1460 кДж/моль.
Ответ: 1154,59 кг; 5438·103 кДж
12. Определите теоретический расход воздуха, необходимый для сжигания 500 кг жидкого фосфора (Р), содержащего 0,98 % примесей. Коэффициент избытка воздуха а=1,2. Содержание влаги 10 %. Ответ: 2580,6 м3
13. Сколько воды расходуется в 1 ч для образования и разбавления фосфорной кислоты в башне сжигания, если масса сжигаемого фосфора 2350 кг/ч, в башне улавливается 53,2% от общей массы образующегося Р2О5, а концентрация полученной кислоты 73% Н3РО4. Ответ: 2406,33 кг
14. Рассчитайте расходные коэффициенты сырья — апатитового концентрата, содержащего 86 % Са3(РО4)2, серной кислоты (моногидрата) и воды для получения 1 т простого суперфосфата. Ответ: 7836,2 кг; 426 кг; 39,1 кг
15. Рассчитайте норму серной кислоты (моногидрата и 68%-ной кислоты) на разложение 100 масс, долей апатитового концентрата, содержащего 39,6% Р2О5 Коэффициент избытка a= 1,3. Ответ: 82,88 кг; 121,88 кг
16. Рассчитайте расход серной кислоты и воды на разложение 350 кг апатитового концентрата. Нормы серной кислоты (моногидрата) 68 масс, долей на 100 масс, долей апатита. Концентрация кислоты 75%-ная. Разложение ведут 69%-ной кислотой. Ответ: 317,3 кг; 32,7 кг
17. При обработке 100 кг апатитового концентрата, содержащего 39,6% Р2О5, серной кислотой получен камерный суперфосфат, содержащий 20,5% Р2О5. После его вызревания на складе содержание Р2О5 составило 20,63%. Определите, сколько суперфосфата получено. Сколько воды выделилось при его вызревании? Ответ: 191,09 кг; 2,8 кг
18. Составьте материальный баланс производства простого суперфосфата из 1000 кг апатитового концентрата по следующим данным: содержание Р2О5 в апатитовом концентрате 41,2%, концентрация серной кислоты 78%-ная. Норма моногидрата 79 масс, долей, на 100 масс, долей апатита. Разложение ведут 68%-ной кислотой. Камерный суперфосфат содержит 20,4% Р2О5, суперфосфат (вызревший на складе) —20,65% Р2О5. Ответ. Приход: 1000 кг апатитового концентрата, 1012,8 кг воды. Расход: 1995,16 кг суперфосфата, 14,6 кг воды.
19.
Определите коэффициент разложения
сырья и выход
камерного суперфосфата по следующим
данным: в
сырье содержится 39,4% Р2О5;
в суперфосфате — 20,15% Р2О5общ
и 17,6 Р205усв.![]() Ответ:
87,3%; 1955,33 кг
Ответ:
87,3%; 1955,33 кг
20. Определите теоретические расходные коэффициенты обогащенного фосфорита, содержащего 30% Р2О5 и 70%-ной в пересчете на Р2О5 фосфорной кислоты, на производство 1 т двойного суперфосфата. Ответ: 563,5 кг; 563,5 кг.
21. Определите расход фосфорной кислоты для разложения фосфата, содержащего 26 % Р2О5. Фосфор в сырье содержится в виде Са5F(РО4)3. Ответ: 837 кг
22. Для получения 1000 кг двойного суперфосфата расходуется 370,7 кг фосфорной кислоты (в расчете на Р2О5) и 350 кг апатитового концентрата. Определите избыток кислоты на 1000 кг апатитового концентрата по сравнению со стехиометрической массой. Ответ: 7,4%.
23. Определите, сколько известняка необходимо для нейтрализации Р2О5своб в 100 кг суперфосфата, если концентрация оксида Р2О5 26,15%. В результате нейтрализации содержание Р2О5своб понижается до 2,92%. Содержание СаСОз в известняке 95%, степень использования его 75%- Сколько углекислого газа выделится при этом? Ответ: 24,65 кг; 7,20 кг
24. 192 кг апатитового концентрата, содержащего 61% гидроксилапатита ЗСа3(РО4)2•Са(ОН)2, обрабатывают стехиометрической нормой фосфорной кислоты. Определите концентрацию (в %) Р2О5общ и Р2О5уcв в полученном суперфосфате. Степень разложения сырья 85%. Ответ: 54%; 51,2%
25. 250 кг апатитового концентрата, содержащего фосфор в виде Са5F(РО4)з (концентрация Р2О5 39,2%), обрабатывают стехиометрической нормой фосфорной кислоты. При этом получается суперфосфат следующего состава: Р2О5общ=50%, Р2О5уcв=46,2%, а Р2О5своб практически нет. Определите степень разложения апатитового концентрата. Ответ: 85,71%
26. 350 кг апатитового концентрата, содержащего 85% Са5F(РО4)3, разлагают фосфорной кислотой, норма которой составляет 120% от стехиометрической. Степень разложения 100%. Определите содержание Р2О5 (свободного в %). Ответ: 3,6%.
1.3.2. Список рекомендуемой литературы.
Л.Г.Корс, Ю.Ф.Болтнев, Н.В. Корс Применение методов математического моделирования в химии и химической технологии: Учебно-практическое пособие. – К-д: Изд-во РГУ им.И.Канта,2006.-135с.
Сборник задач по химич. технологии: Учеб. пособ. для студентов хим. и хим-биол. спец.пед.ин-тов/И.И.Беляева и др.-М: Просвещение, 1982.-143 с.
Расчёты по технологии неорганических веществ. /Под ред.проф. М.Е. Позина.- Л.: Химия.-1977.-496 с.
4. Основы химической технологии./ Под ред. И.П.Мухлёнова.-М.: ВШ.-1991.-463 с.
5. Р.С.Соколов. Химическая технология.-М.: Гуманит. Изд. Центр ВЛАДОС, 2003.- Т.1.-368 с.
6. ХЭ в пяти томах. /Под ред. И.Л.Кнунянца.- Изд-во «Советская энциклопедия». М.: 1990. т.2.-С.937-938, 869-870.
7. В.Ф.Очков. Языки программирования - GW BASIK и QBASIK- сравнительное описание. М.: Энергоатомиздат.-1992.- 76 с.
8. Позин М.Е. Технология минеральных удобрений.-Л.:Химия.-1989.
