
- •II.Процессы защиты гидросферы (очистка сточных вод)
- •Глава 6. Использование воды в оборотных системах водоснабжения
- •6.2. Оборотное водоснабжение
- •6.3. Технологическая вода и сточные воды
- •6.4. Замкнутые системы водного хозяйства промышленных предприятий
- •Глава 7. Удаление взвешенных частиц из сточных вод
- •7.1. Процеживание и отстаивание
- •7.2. Удаление всплывающих примесей
- •7.3. Фильтрование
- •7.4. Удаление взвешенных частиц под действием центробежных сил и отжиманием
Глава 6. Использование воды в оборотных системах водоснабжения
6.1. Свойства и классификация вод
Вода играет решающую роль во многих процессах, протекающих в природе, и в обеспечении жизни человека. В промышленности воду используют как сырье и источник энергии, как хладоагент, растворитель, экстрагент, для транспортирования сырья и материалов и др.
Ресурсы воды. Это запасы пресных поверхностных (речных, озерных, болотных, ледниковых) и подземных вод какой-либо территории. Общее количество природной воды на Земле составляет 1386 млн. км3. В основном (свыше 97,5%) это соленые воды. Количество пресной воды — 35 млн. км3. Однако подавляющая часть пресной воды является труднодоступной для людей, так как она в основном находится в полярных ледниках и водоносных слоях под землей. В СНГ запас пресных поверхностных вод составляет 40,5 тыс. км3. Из них: в озерах — 26 тыс. км3 (в том числе в Байкале — 23 тыс.км3); в ледниках — 11тыс. км3; в болотах около 3 тыс. км3; в руслах рек всего 235 км3. Объем потребления пресной воды в мире достигает приблизительно 3900 млрд. м3/год. Около половины этого количества потребляется безвозвратно, а другая половина превращается в сточные воды.
Природная вода—это вода, которая качественно и количественно формируется под влиянием естественных процессов при отсутствии антропогенного воздействия. Ее качественные показатели находятся на естественном среднемноголетнем уровне. В зависимости от степени минерализованности (в г/л) воды делятся: на пресные (с содержанием солей <1), солоноватые (1-10), соленые (10-50) и рассолы (>50). В свою очередь, пресные воды подразделяются на воды малой минерализованности (до 200мг/л), средней минерализованности (200-500 мг/л) и повышенной минерализованности (500-1000 мг/л). По преобладающем}- анион}- все воды делятся на гидрокарбонатные, сульфатные и хлоридные.
Жесткость природных вод обусловливается присутствием в них солей кальция и магния и выражается концентрацией ионов Са2+ и Mg2+ в ммоль экв/л. Различают общую, карбонатную и некарбонатную жесткость. Общая жесткость представляет собой сумму двух последних, карбонатная связана с присутствием в воде бикарбонатов кальция и магния, а некарбонатная — сульфатов, хлоридов, нитратов кальция и магния.
Физические свойства воды. Плотность чистой воды при 35°С и атмосферном давлений — 999 кг/м3. С увеличением концентрации примесей плотность воды возрастает. Морская вода с концентрацией солей 35 кг/м3 имеет среднюю плотность 1028 кг/м3 при 0°С. Изменение солесодержания на 1 кг/м3 изменяет плотность на 0,8 кг/м3.
Вязкость μ воды с повышением температуры t уменьшается следующим образом:
t,°C |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
μ*10-3, Па-с |
1,797 |
1,523 |
1,301 |
1,138 |
1,007 |
0,895 |
0,800 |
0,723 |
С увеличением солесодержания вязкость воды повышается. Поверхностное натяжение σ воды при 18°С составляет 73, при 100°С — 52,5 мН/м. Теплоемкость воды при 0°С составляет 4180 Дж/(кг* °С), а при 35°С достигает минимума. Теплота плавления при переходе льда в жидкое состояние составляет 330 кДж/кг, теплота парообразования равна 225 0 кДж/кг при атмосферном давлении и температуре 100°С.
Электрические свойства воды. Вода — слабый проводник электрического тока: удельная электрическая проводимость при 18°С равна 4,9*10-8 См/м (4,41-10-8 1/0м-см); диэлектрическая постоянная равна 80. Наличие растворенных солей в воде увеличивает ее электрическую проводимость, которая изменяется в зависимости от температуры.
Оптические свойства воды. Прозрачность и мутность воды зависят от содержания в ней механических примесей, находящихся во взвешенном состоянии. Чем больше примесей в воде, тем больше ее мутность и меньше прозрачность. Прозрачность определяется длиной пути луча, проникающего вглубь воды, и зависит от длины волны луча. Ультрафиолетовые лучи проходят через воду легко, а инфракрасные — плохо. Показатель прозрачности используют для оценки качества воды и содержания в ней примесей.
Загрязнение воды. Вследствие антропогенного воздействия природная вода загрязняется различными веществами, что приводит к ухудшению ее качества. Под качеством воды понимают совокупность физических, химических, биологических и бактериологических показателей. Загрязнения, поступающие в водную среду; изменяют эти показатели.
Можно выделить следующие тенденции в изменении качества природных вод под влиянием хозяйственной деятельности людей:
снижение рН пресных вод в результате их загрязнения серной и азотной кислотами из атмосферы, увеличение содержания в них сульфатов и нитратов; повышение содержания ионов кальция, магния, кремния в подземных и речных водах вследствие вымывания и растворения подкисленными дождевыми водами карбонатных и других горных пород;
повышение содержания в природных водах ионов тяжелых металлов, прежде всего, свинца, кадмия, ртути, мышьяка и цинка, а также фосфатов (>0,1 мг/л), нитратов, нитритов и др.;
повышение содержания солей в поверхностных и подземных водах в результате их поступления со сточными входами, из атмосферы и за счет смыва твердых отходов (например, солесодержание многих рек ежегодно повышается на 30-50 мг/л и более; из 1000 т городских отходов в грунтовые воды попадает до 8 т растворимых солей);
повышение содержания в водах органических соединений, прежде всего, биологически стойких (ПАВ, пестицидов, продуктов их распада и других токсичных, канцерогенных и мутагенных веществ);
снижение содержания кислорода в природных водах, прежде всего, в результате повышения его расхода на окислительные процессы, связанные с эвтрофикацией водоемов, с минерализацией органических соединений, а также вследствие загрязнения поверхности водоемов гидрофобными веществами и сокращения доступа кислорода из атмосферы (в отсутствие кислорода в воде развиваются восстановительные процессы, в частности, сульфаты восстанавливаются до сероводорода);
снижение прозрачности воды в водоемах (в загрязненных водах размножаются вирусы и бактерии, возбудители инфекционных заболеваний);
потенциальная опасность загрязнения природных вод радиоактивными изотопами химических элементов.
Природная вода, подвергаемая антропогенному загрязнению, называется денатурированной или природно-антропогенной. В случае необходимости перед использованием воды в промышленности ее очищают в соответствии со специфическими требованиями данного производства.
К лассификация
вод
по
целевому назначению. Воду,
используемую в промышленности,
подразделяют на охлаждающую,
технологическую и энергетическую
(рис. II-1).
лассификация
вод
по
целевому назначению. Воду,
используемую в промышленности,
подразделяют на охлаждающую,
технологическую и энергетическую
(рис. II-1).
Рис. II-1. Классификация вод по целевому назначению
Вода часто служит для охлаждения жидких и газообразных продуктов в теплообменных аппаратах. В этом случае она не соприкасается с материальными подтоками и не загрязняется, а лишь нагревается. В промышленности 65-80% расхода воды потребляется для охлаждения. На крупных химических предприятиях потребление охлаждающей воды достигает 440 млн. м3/год. Суммарное количество воды, заключенной в системах охлаждения на предприятиях химической промышленности, составляет 20 млрд. м3/год.
Технологическую воду подразделяют на средообразующую, промывающую и реакционную. Средообразующую воду используют для растворения и образования пульп, при обогащении и переработке руд, гидротранспорте продуктов и отходов производства; промывающую — для промывки газообразных (абсорбция), жидких (экстракция) и твердых продуктов и изделий; реакционтто — в составе реагентов, а также при азеотропной отгонке и аналогичных процессах. Технологическая вода непосредственно контактирует с продуктами и изделиями.
Э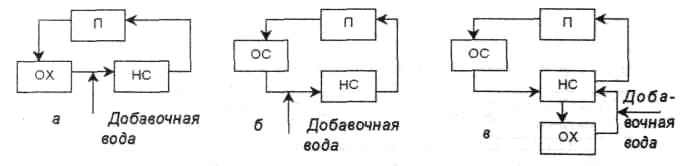 нергетическая
вода потребляется для получения пара
и нагревания оборудования, помещений,
продуктов.
нергетическая
вода потребляется для получения пара
и нагревания оборудования, помещений,
продуктов.
Рис. 11-2. Схемы оборотного водоснабжения: а — с охлаждением воды; 6 — с очисткой воды; в — с очисткой и охлаждением воды; П — производство; НС — насосная станция; ОХ — охлаждение воды; ОС — очистка сточной воды
