
Тема: качественные реакции на белки
1. ЦЕЛЬ
Изучить качественные реакции, используемые для обнаружения белков и определения их аминокислотного состава.
2. ЗАДАЧИ
2.1. Провести биуретовую реакцию.
2.2. Провести нингидриновую реакцию.
2.3. Провести ксантопротеиновую реакцию.
2.4. Провести реакцию на аргинин.
2.5. Провести реакцию на тирозин.
2.6. Провести реакции на серосодержащие аминокислоты.
2.7. Сделать выводы и оформить отчет.
3. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Белки – это высокомолекулярные органические соединения, состоящие из остатков аминокислот, которые связаны друг с другом при помощи пептидных связей. В состав белков входят 18–20 различных аминокислот. Одни из них организм может синтезировать самостоятельно – это заменимые аминокислоты. Другие, незаменимые, в организме синтезироваться не могут и должны поступать с пищей. Все аминокислоты, входящие в состав белков, являются α-аминокислотами, так как только аминогруппа, стоящая в α-положении, способна образовывать пептидную связь. Все α-аминокислоты, за исключением глицина, имеют ассиметричный углеродный атом и поэтому являются оптически активными соединениями. Они способны вращать плоскость поляризованного луча или вправо, или влево. Первые называются правовращающими и обозначаются знаком (+), вторые – левовращающими (–). Кроме этого, аминокислоты образуют два ряда стериоизомеров – L и D. В состав живых организмов входят L (–) - аминокислоты.
Для обнаружения белка применяют цветные реакции. Они делятся на два типа: общие, или универсальные, и специфические. К универсальным реакциям относятся биуретовая (на пептидную связь) и нингидриновая (на α-аминокислоты). При их помощи можно открыть любой белок. К специфическим относятся реакции на отдельные аминокислоты. Это реакции на функциональные группы радикалов аминокислот, входящих в состав белков. При их помощи можно открыть только тот белок, в состав которого они входят.
Значение цветных реакций состоит в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах и установить аминокислотный состав различных природных белков. Эти реакции применяются как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот.
Биуретовая реакция (Пиотровского) открывает пептидную связь(−CО−NH−) в белке. В щелочной среде раствор белка, взаимодействуя с ионами меди, приобретает сине-фиолетовый цвет. Продукты неполного гидролиза белка – пептоны дают розовое окрашивание.
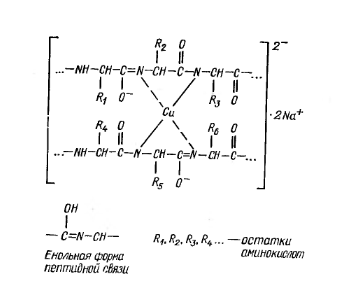
Биуретовую реакцию способны давать вещества, которые содержат не менее двух пептидных связей. Пептидные связи могут существовать в двух формах: кетоформе и енольной. В щелочной среде они переходят в енольную форму. При прибавлении ионов меди образуется биуретовый комплекс в результате соединения меди с пептидной группировкой белка. Окраска биуретового комплекса зависит от количества пептидных связей, концентрации белка и количества ионов меди в растворе. Она изменяется от синей до красной с преобладанием фиолетовой.
Нингидриновая реакция характерна для аминогрупп, находящихся в α-положении и входящих в состав белков, а также полипептидов и свободных аминокислот. В результате взаимодействия α-аминокислоты с нингидрином образуется шиффово основание, которое перегруппировывается, декарбоксилируется и расщепляется на альдегид и аминодикетогидринден. Образовавшийся иминодикето-гидринден конденсируется еще с одной молекулой нингидрина.
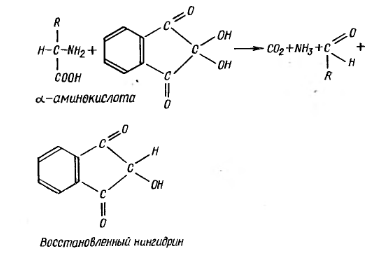
Образовавшееся соединение превращается в окрашенную енольную форму, получившую название «сине-фиолетовый комплекс Руэмана».
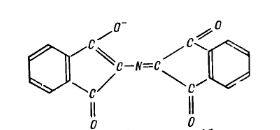
Сине-фиолетовый комплекс Руэмана.
В присутствии органических растворителей (спирта или ацетона) образовавшееся шиффово основание не распадается, поскольку в соединении нет воды. Конденсируясь с нингидрином, оно содержит в своем составе радикал исходной аминокислоты, который обусловливает различную окраску: голубую, красную, синюю, фиолетовую, а в присутствии иминокислоты пролина – желтую.
К специфическим реакциям относятся реакции Мульдера, Миллона, Сакагучи, Фоля.
Ксантопротеиновая реакция (Мульдера) происходит только при наличии в белке ароматических аминокислот (тирозин, фенилаланин, триптофан). Реакция обусловлена образованием нитропроизводных циклических аминокислот. При добавлении к таким белкам концентрированной азотной кислоты протекает реакция нитрования с образованием окрашенных в желтый цвет нитросоединений. При добавлении щелочи желтая окраска переходит в оранжевую, так как в щелочной среде нитропроизводные аминокислот образуют соли хиноидной структуры, имеющие оранжевый цвет:
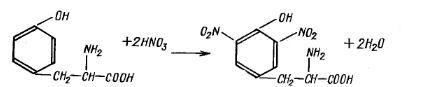
тирозин динитротирозин (желтого цвета)
С белками, содержащими тирозин, идет также реакция Миллона. Реактив Миллона представляет собой смесь нитратов (HgNO3) и нитритов (HgNO2) ртути (I), растворенных в концентрированной азотной кислоте. При добавлении к раствору белка реактива Миллона его компоненты взаимодействуют с фенольным ядром тирозина. При этом образуется осадок ртутной соли динитротирозина, окрашенный в кроваво-красный цвет. Химизм реакции можно представить в следующем виде:

К раствору белка не следует добавлять избыток реактива Миллона, так как он содержит азотную кислоту, которая при взаимодействии с белком может дать желтое окрашивание (ксантопротеиновая реакция), маскирующее реакцию Миллона. Для ускорения появления окраски раствор можно подогреть.
Р еакция
Сакагучи
идет с белками, которые содержат аргинин.
В присутствии щелочи образуется
розово-красное окрашивание с α-нафтолом.
Аргинин имеет гуанидиновую группировку
(NH2−C−(NH)2),
которая в присутствии α-нафтола
окисляется гипобромидом в щелочной
среде, в результате чего образуется
продукт конденсации розово-красного
цвета.
еакция
Сакагучи
идет с белками, которые содержат аргинин.
В присутствии щелочи образуется
розово-красное окрашивание с α-нафтолом.
Аргинин имеет гуанидиновую группировку
(NH2−C−(NH)2),
которая в присутствии α-нафтола
окисляется гипобромидом в щелочной
среде, в результате чего образуется
продукт конденсации розово-красного
цвета.
Химизм реакции следующий:
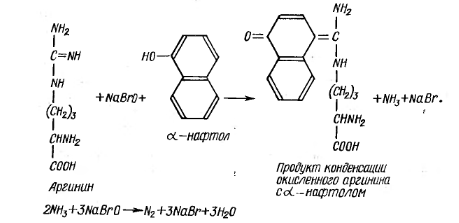
Белки, содержащие сульфгидрильные группы (–SH) можно обнаружить при помощи реакции Фоля. Предварительно проводят щелочной гидролиз белка, при котором отщепляется сульфидная группа, которую обнаруживают при помощи тех или иных реактивов. При проведении реакции Фоля действуют плюмбитом натрия (Na2PbO2), который образуется в результате взаимодействия ацетата свинца Pb(СН3СОО)2 и гидроксида натрия NaOH, в результате чего образуется черный нерастворимый осадок сульфида свинца. Химизм реакции следующий:
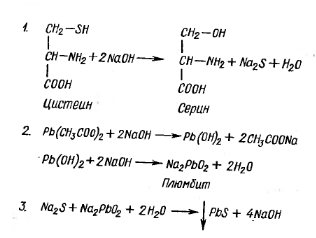
Метионин хотя и содержит серу, этой реакции не дает, так как сера в нем прочно связана с метильной группой, а не с водородом.
4. ПРАКТИЧЕСКАЯ ЧАСТЬ
4.1. Биуретовая реакция (Пиотровского)
