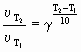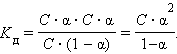Мате́рия (от лат. materia — вещество) — философская категория для обозначения объективной реальности, которая отображается нашими ощущениями, существуя независимо от них (объективно).
Вещество (в химии) — физическая субстанция со специфическим химическим составом
Когда с веществом происходит физическое изменение, состав его молекул остается прежним, т.е. вещество сохраняет свою химическую индивидуальность. Существует три типа основных физических превращений – плавление, испарение и замерзание. Лед – твердое вещество – при плавлении превращается в воду – жидкость, которая при замерзании снова становится льдом. Молекулы льда и воды состоят из одних и тех же элементов (H и O), находящихся в одинаковых пропорциях. Когда лед тает, никаких химических реакций не происходит. Другой тип физических превращений – изменение формы вещества, например при его резании, шлифовании, измельчении, растворении, эмульгировании и т.д. Еще один тип физического превращения – сублимация (возгонка), переход твердого вещества непосредственно в газообразное. Именно это превращение имеет место, когда мокрое белье сохнет на морозе.
Химические превращения
происходят постоянно и повсюду; при этом изменяется химическая индивидуальность веществ, одни вещества превращаются в другие с иными свойствами. Так, при ржавлении железа образуется новое вещество – ржавчина (оксид железа). Химические превращения могут сопровождаться физическими изменениями. При горении древесины (твердое вещество) образуются диоксид углерода (газ), вода (жидкость) и углерод (твердое вещество). Химические превращения чрезвычайно многообразны, их изучением и классификацией занимается наука химия. Вот некоторые типы превращений, принятые в химии.
Предмет химии — химические элементы и их соединения, а также закономерности, которым подчиняются различные химические реакции.
Атом состоит из атомного ядра и электронов. Ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов. В стандартной модели элементарных частиц как протоны, так и нейтроны состоят из элементарных частиц, называемых кварками. Наряду с лептонами, кварки являются одной из основных составляющих материи. И первые и вторые являются фермионами.
Правило Клечковского (также Правило n+l; также используется название правило Маделунга) — эмпирическое правило, описывающее энергетическое распределение орбиталей в многоэлектронных атомах.
-
Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитального квантовых чисел
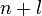 .
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением
.
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением
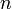 .
.
Распределение электронов в атоме происходит по принципу Паули, который может быть сформулирован для атома в простейшем виде: в одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел: n, l, , :
Z (n, l, , ) = 0 или 1,
где Z (n, l, , ) - число электронов, находящихся в квантовом состоянии, описываемых набором четырех квантовых чисел: n, l, , . Таким образом, принцип Паули утверждает, что два электрона, связанные в одном и том же атоме различаются значениями, по крайней мере, одного квантового числа.
Периоди́ческая систе́ма хими́ческих элеме́нтов (табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы).
Периодический закон был сформулирован Д. И. Менделеевым в следующем виде (1871): «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».[1]
В настоящее время Периодический закон Д. И. Менделеева имеет следующую формулировку: «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
Неметаллы, Неметаллы. Неметаллы — Категория неметаллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. Расположение их в главных подгруппах соответствующих периодов следующее. Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов.
Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал.
В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром.
Металл - это элемент, который имеет небольшое количество внешних электронов и с готовностью отдает их. Все металлы (кроме ртути) тверды при нормальных условиях. Однако твёрдость их различна.
Неметаллы имеют большее (по сравнению с металлами) количество внешних электронов. Они обладают способностью присоединять дополнительные электроны. В свободном виде при комнатной температуре ряд из них газы, другие - твердые и один - жидкий.
Окисление - процесс отдачи электронов, с увеличением степени окисления.
При окисле́нии вещества в результате отдачи электронов увеличивается его степень окисления. Атомы окисляемого вещества называются донорами электронов, а атомы окислителя — акцепторами электронов.
Восстановле́нием называется процесс присоединения электронов атомом вещества, при этом его степень окисления понижается.
При восстановлении атомы или ионы присоединяют электроны. При этом происходит понижение степени окисления элемента. Примеры: восстановление оксидов металлов до свободных металлов при помощи водорода, углерода, других веществ; восстановление органических кислот в альдегиды и спирты; гидрогенизация жиров и др. К ним относятся элементы, расположенные в главных подгруппах первой и второй групп Периодической системы (калий, натрий, барий, кальций и др.). Восстановителями являются также водород, сероводород, аммиак, йодистоводородная кислота и ее соли, ион хлора, соли двухвалентного олова и другие вещества, содержащие в своем составе атомы, находящиеся в низшей степени окисления и, следовательно, способные только повышать свою степень окисления за счет отдачи электронов.
К окислителям относятся также азотная кислота и ее соли, концентрированная серная кислота, хлорная и бромная вода, кислородные кислоты хлора и брома и их соли, бихромат и хромат калия и другие вещества, содержащие в своем составе атомы, находящиеся в высшей степени окисления и поэтому способные только понижать свою степень окисления за счет принятия электронов.
> 2 — неметаллические свойства. » 2 — амфотерные свойства. Групповая аналогия: аналогия по числу валентных электронов. Сходство в группе ограничено валентностью и формой некоторых соединений: Cl+7 и Mn+7; Cl2O7 и Mn2O7, …. Электронная аналогия: сходное строение внешних электронных слоёв или подуровней: H, Li, Na; Be, Mg; Zn, Cd, Hg; B, Al, Ta; Se, Y, La, Ac; Ce — Lu, инертные газы (ns2nP6) Полная электронная аналогия: сходное электронное строение во всех степенях окисления (Ti, Zn, Hf — +4).
На каждом энергетическом уровне возобновляется конфигурация электронов внешнего слоя. Первая энергия ионизации — энергия, необходимая для удаления из атома 1 электрона. В пределах групп с увеличением заряда ядра эта энергия убывает. Сродство к электрону — изменение энергии, сопровождающееся присоединением электрона к изолированному атому с образованием отрицательного иона. В периодах возр, в группах уб. Электроотрицательность — интегральная характеристика, предложенная Полингом для оценки реакционной способности атома.
Относительная электроотрицательность
Лантаноиды имеют значения относительных электроотрицательностей в области 1,08 – 1,14;
Актиноиды имеют значения относительных электроотрицательностей в области 1,11 – 1,20;
Элементы VIII группы периодической системы (благородные газы) имеют нулевую электроотрицательность;
Условной границей между металлами и неметаллами считается значение относительной электроотрицательности равное 2.
Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой. Образование связи
Простая ковалентная связь образуется из двух неспаренных валентных электронов, на один
от каждого атома:
A· + ·В → А : В
В результате обобществления электроны образуют заполненный энергетический уровень. Связь образуется, если их суммарная энергия на этом уровне будет меньше, чем в первоначальном состоянии (а разница в энергии будет не чем иным, как энергией связи).
Заполнение электронами атомных (по краям) и молекулярных (в центре) орбиталей в молекуле H2. Вертикальная ось соответствует энергетическому уровню, электроны обозначены стрелками, отражающими их спины.
Согласно теории молекулярных орбиталей, перекрывание двух атомных орбиталей приводит в простейшем случае к образованию двух молекулярных орбиталей (МО): связывающей МО и антисвязывающей (разрыхляющей) МО. Обобществленные электроны располагаются на более низкой по энергии связывающей МО.
Простой ковалентной связью соединены атомы в молекулах простых газов (Н2, Cl2 и др.) и соединений (Н2О, NH3, CH4, СО2, HCl и др.). Соединения с донорно-акцепторной связью — катион аммония NH4+, тетрафторборат анион BF4− и др. Соединения с семиполярной связью — закись азота N2O, O−-PCl3+.
При получении энергии извне, один либо несколько электронов могут повышать свою энергию, поднимаясь на более высокие энергетические состояния. Такие состояния атома называются возбужденными.
Направленность связи обусловлена молекулярным строением вещества и геометрической формы их молекулы. Углы между двумя связями называют валентными.
Насыщаемость — способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей.
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d) орбиталей центрального атома многоатомной молекулы с возникновением того же числа орбиталей, эквивалентных по своим характеристикам.
Ионная связь — прочная химическая связь, образующаяся между атомами с большой разностью (>1,7 по шкале Полинга) электроотрицательностей, при которой общая электронная пара полностью переходит к атому с большей электроотрицательностью.Это притяжение ионов как разноименно заряженных тел. Примером может служить соединение CsF, в котором «степень ионности» составляет 97 %.
Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов и интерметаллических соединений.
Ван-дер-ваальсовы силы — силы межмолекулярного взаимодействия с энергией 0,8 — 8,16 кДж/моль. Этим термином первоначально обозначались все такие силы, в современной науке он обычно применяется к силам, возникающим при поляризации молекул и образовании диполей. Открыты Я. Д. ван дер Ваальсом в 1869 году.
К ван-дер-ваальсовым силам относятся взаимодействия между диполями (постоянными и индуцированными). Название связано с тем фактом, что эти силы являются причиной поправки на внутреннее давление в уравнении состояния реального газа Ван-дер-Ваальса. Эти взаимодействия в основном определяют силы, ответственные за формирование пространственной структуры биологических макромолекул.
Ван-дер-ваальсовы силы также возникают между частицей (макроскопической частицей или наночастицей) и молекулой и между двумя частицами.[1][2][3]
Водородная связь, вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А).
Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
Окси́д (о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом.
Химические свойства Основные оксиды
1. Основный оксид + кислота → соль + вода
CuO + H2SO4 → CuSO4 + H2O
Примечание: кислота ортофосфорная или сильная.
2. Сильноосновный оксид + вода → щелочь
CaO + H2O → Ca(OH)2
3. Сильноосновный оксид + кислотный оксид → соль
CaO + Mn2O7 → Ca(MnO4)2
Na2O + CO2 → Na2CO3
4. Основный оксид + водород → металл + вода
CuO + H2 → Cu + H2O
Примечание: металл менее активный, чем алюминий.
[Править] Кислотные оксиды
1. Кислотный оксид + вода → кислота
SO3 + H2O → H2SO4
Некоторые оксиды, например SiO2, с водой не реагируют, поэтому их кислоты получают косвенным путём.
2. Кислотный оксид + основный оксид → соль
CO2 + CaO → CaCO3
3. Кислотный оксид + основание → соль + вода
SO2 + 2NaOH → Na2SO3 + H2O
Если кислотный оксид является ангидридом многоосновной кислоты, возможно образование кислых или средних солей:
Ca(OH)2 + CO2 → CaCO3↓ + H2O
CaCO3 + CO2 + H2O → Ca(HCO3)2
4. Нелетучий оксид + соль1 → соль2 + летучий оксид
SiO2 + Na2CO3 → Na2SiO3 + CO2↑
5. Ангидрид кислоты 1 + безводная кислородосодержащая кислота 2 → Ангидрид кислоты 2 + безводная кислородосодержащая кислота 1
P2O5 + 2HClO4 (безводн) → Cl2O7 + 2HPO3
[Править] Амфотерные оксиды
При взаимодействии с сильной кислотой или кислотным оксидом проявляют основные свойства:
ZnO + 2HCl → ZnCl2 + H2O
При взаимодействии с сильным основанием или основным оксидом проявляют кислотные свойства:
ZnO + 2KOH + H2O → K2[Zn(OH)4] (в водном растворе)
ZnO + CaO → CaZnO2 (при сплавлении)
Номенклатура
В соответствии с номенклатурой ИЮПАК, оксиды называют словом «оксид», после которого следует наименование химического элемента в родительном падеже, например: Na2O — оксид натрия, Al2O3 — оксид алюминия. Если элемент имеет переменную степень окисления, то в названии оксида указывается его степень окисления римской цифрой в скобках сразу после названия (без пробела). Например, Cu2О — оксид меди(I), CuO — оксид меди(II), FeO — оксид железа(II), Fe2О3 — оксид железа(III), Cl2O7 — оксид хлора(VII).
Часто используют и другие наименования оксидов по числу атомов кислорода: если оксид содержит только один атом кислорода, то его называют монооксидом, моноокисью или закисью, если два — диоксидом или двуокисью, если три — то триоксидом или триокисью и т. д. Например: монооксид углерода CO, диоксид углерода СО2, триоксид серы SO3.
Также распространены исторически сложившиеся (тривиальные) названия оксидов, например угарный газ CO, серный ангидрид SO3 и т. д.
В начале XIX века и ранее тугоплавкие, практически не растворимые в воде оксиды химики называли «землями»
Гидрокси́ды (гидроо́киси) — соединения оксидов химических элементов с водой.
Со́ли —
класс химических соединений, к которому
относятся вещества,
состоящие из катионов
металла
(или катионов аммония
![]() ;
известны соли фосфония
;
известны соли фосфония
![]() или
гидроксония
или
гидроксония
![]() )
и анионов
кислотного остатка.
)
и анионов
кислотного остатка.
Свойства
1. Диссоциируют в растворах или расплавах:
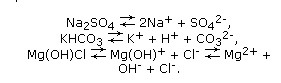
2. Способны подвергаться гидролизу (кроме солей, образованных одновременно сильными одноосновными кислотами и щелочными металлами):
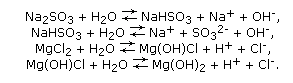
3. Могут взаимодействовать с основными и амфотерными гидроксидами, кислотами и солями, вступая в реакции обмена (смотри выше: пункт 7).
4. Способны вступать в многочисленные окислительно-восстановительные реакции, реакции диспропорционирования:
3KClO = KClO3 + 2KCl,
2FeCl3 + H2S = S + 2FeCl2 + 2HCl.
Энергетический эффект химического процесса возникает за счет изменения в системе внутренней энергии U или энтальпии H. Внутренней энергией системы называют энергию всех видов движения и взаимодействия тел или частиц, составляющих систему (кинетическая энергия межмолекулярного взаимодействия, вращательная энергия, колебательное движение атомов и групп в молекуле, энергия взаимодействия электронов между собой и с ядрами).
Энтальпи́я, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Проще говоря, энтальпия - это та энергия, которая доступна для преобразования в теплоту при определенных температуре и давлении.
Закон Гесса — основной закон термохимии, который формулируется следующим образом:
Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данное химическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы).
Химическое сродство, термин, применяющийся для характеристики способности данных веществ к химическому взаимодействию между собой или для характеристики степени устойчивости получающегося при этом соединения к разложению на исходные вещества.
Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на принципиальную возможность химической реакции; это термодинамический потенциал следующего вида:
![]()
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Химические реакции протекают и в прямом, и в обратном направлениях:
Реагенты |
|
Энтропи́я (от греч. ἐντροπία — поворот, превращение) в естественных науках — мера беспорядка системы, состоящей из многих элементов.
В химических процессах одновременно действуют два противоположных фактора — энтропийный (TΔS) и энтальпийный (ΔH). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (G):
![]()
Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Важным понятием химической кинетики является скорость химической реакции. Эта величина определяет, как изменяется концентрация компонентов реакции с течением времени.
Закон действующих масс в кинетической форме (основное уравнение кинетики) гласит, что скорость элементарной химической реакции пропорциональна произведению концентраций реагентов в степенях, равных стехиометрическим коэффициентам в уравнении реакции[1]. Это положение сформулировано в 1867 году норвежскими учёными К. Гульдбергом и П. Вааге. Для элементарной химической реакции:
![]()
закон действующих масс может быть записан в виде кинетического уравнения вида:
![]()
где
![]() —
скорость
химической реакции,
—
скорость
химической реакции,
![]() —
константа
скорости реакции.
—
константа
скорости реакции.
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль/л.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, но не зависит от их концентрации.
Изменение температуры оказывает резкое влияние на константу скорости, а следовательно, и на скорость химической реакции. В подавляющем большинстве случаев скорость химической реакции с нагреванием возрастает.
В 1879 г. голландский исследователь Г. Вант-Гофф обнаружил, что при повышении температуры на каждые 10 градусов скорость химической реакции возрастает, в среднем, в 2-4 раза (правило Вант-Гоффа):
|
(5.9) |
где
![]() -
скорость реакции при температуре T1
(начальная температура системы);
-
скорость реакции при температуре T1
(начальная температура системы);
![]() -
скорость реакции при температуре T2
(конечная температура системы);
-
скорость реакции при температуре T2
(конечная температура системы);
g - температурный коэффициент реакции. Это число, показывающее, во сколько раз возрастает скорость данной реакции при повышении температуры на 10 градусов, т.е.
![]() ,
,
где kT - константа скорости реакции при температуре Т;
kT+10 - константа скорости реакции при температуре (Т+10);
Если концентрации реагентов равны 1 моль/л, то
![]()
Влияние температуры на скорость реакции тем значительнее, чем больше значение g . Так, если g равен трем, то при увеличении температуры на 100 ° скорость реакции возрастет в 310 раз, т.е. приблизительно в 59 тыс. раз. Следует иметь в виду, что правило Вант-Гоффа позволяет лишь примерно оценить влияние температуры на скорость реакции. Оно применимо для реакций, энергия активации которых находится в пределах: 80 < Ea < 170 кДж. Чем больше Еa, тем большую величину имеет g . Графическая зависимость скорости реакции от температуры показана на рис. 5.4.
Энергия активации в химии и биологии — минимальное количество энергии, которое требуется сообщить системе (в химии выражается в джоулях на моль), чтобы произошла реакция. Термин введён Сванте Августом Аррениусом в 1889. Типичное обозначение энергии реакции Ea.
Источником активации молекул может служить не только кинетическая энергия молекул, но и световая энергия, поглощаемая электронами, находящимися на периферии и слабо связанными с ядром атома.
Катализа́тор — химическое вещество, ускоряющее или замедляющая реакцию, но не входящее в состав продуктов реакции
Механизм действия Катализаторов обычно объясняют образованием промежуточных соединений с одним из реагирующих веществ. Так, если медленно протекающую реакцию А + В = АВ вести в присутствии Катализатора К, то катализатор вступает в химическое взаимодействие с одним из исходных веществ, образуя непрочное промежуточное соединение:
А + К = АК
Реакция протекает быстро, так как энергия активации этого процесса мала. Затем промежуточное соединение АК взаимодействует с другим исходным веществом, при этом катализатор высвобождается:
АК + В = АВ + К
Энергия активации этого процесса также мала, а потому реакция протекает с достаточной скоростью. Если теперь оба процесса, протекающие одновременно, суммировать, то получим окончательное уравнение быстро протекающей реакции:
А + В = АВ
Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре прямая-обратная реакция равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем.[1]
А2 + В2 ⇄ 2AB
В состоянии равновесия скорости прямой и обратной реакции становятся равными.
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями (либо, в зависимости от условий протекания реакции, парциальными давлениями, концентрациями или фугитивностями) исходных веществ и продуктов в состоянии химического равновесия (в соответствии с законом действующих масс). Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.
принципа Ле Шателье упрощают: равновесная система, на которую оказывают воздействие, смещает равновесие так, чтобы уменьшить влияние этого воздействия.
принципа Ле Шателье упрощают: равновесная система, на которую оказывают воздействие, смещает равновесие так, чтобы уменьшить влияние этого воздействия.
РАСТВОРЫ, однофазные системы, состоящие из двух или более компонентов. По своему агрегатному состоянию растворы могут быть твердыми, жидкими или газообразными.
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры.
Наиболее часто применяемые способы выражения концентрации: массовая доля, молярная концентрация, молярная концентрация эквивалента, молярная доля, объемная доля, титр.
Массовую долю W(X) выражают в долях единицы, процентах (%), промилле (тысячной части процента) и в миллионных долях (млн—1). Массовую долю рас–считывают по формулам:
W(X) = m(X)/m (р-р),
W(X) = m(X)/m (р-р) × 100%,
где m(X) – масса данного компонента X (растворен–ного вещества), кг (г);
m (р-р) – масса раствора, кг (г).
Молярную концентрацию выражают в моль/м3 , моль/дм3 , моль/см3 , моль/л, моль/мл. В медицине предпочтительнее применение единиц моль/л. Моляр–ную концентрацию рассчитывают по формуле:
C(X) = n(Х)/V(p-p) = m(X)/M(X) × V(р-р),
где n(Х) – количество растворенного вещества системы, моль;
M(X) – молярная масса раство–ренного вещества, кг/моль или г/моль;
m(X) – масса растворенного вещества соответ–ственно, кг или г;
V(р-р) – объем раствора, л. Молярную концентрацию
b(X) выражают в единицах моль/кг.
Форма записи, например: Ь(НСl) = 0,1 моль/кг. Рас–считывают молярную концентрацию по формуле:
b(X) = n(Х)/m(р-ль) = m(X)/M(X) × m(р-ль)
где m(р-ль) – масса растворителя, кг.
В химии широко используют понятие эквивалента и фактора эквивалентности.
Согласно второму началу термодинамики при р, Т = = const вещества самопроизвольно могут растворяться в каком-либо растворителе, если в результате этого процесса энергия Гиббса системы уменьшается, т. е.
ΔG = (ΔН – TΔS) < 0.
Величину ΔН называют энтальпийным фактором, а величину TΔS – энтропийным фактором растворения.
При растворении жидких и твердых веществ энтропия системы обычно возрастает (ΔS > 0), так как растворяе–мые вещества из более упорядоченного состояния пе–реходят в менее упорядоченное. Вклад энтропийного фактора, способствующий увеличению растворимости, особенно заметен при повышенных температурах, по–тому что в этом случае множитель Т велик и абсолютное значение произведения TΔS также велико, соответст–венно возрастает убыль энергии Гиббса.
При растворении газов в жидкости энтропия системы обычно уменьшается (ΔS < 0), так как растворяемое вещество из менее упорядоченного состояния (боль–шого объема) переходит в более упорядоченное (ма–лый объем). Снижение температуры благоприятствует растворению газов, потому что в этом случае множи–тель Т мал и абсолютное значение произведения TΔS будет тем меньше, а убыль энергии Гиббса тем больше, чем ниже значение Т.
В процессе образования раствора энтальпия систе–мы также может как увеличиваться (NaCI), так и умень–шаться (КОН). Изменение энтальпии процесса раство–рения нужно рассматривать в соответствии с законом Гесса как алгебраическую сумму эндо– и экзотермиче–ских вкладов всех процессов, сопровождающих про–цесс растворения. Это эндотермические эффекты раз–рушения кристаллической решетки веществ, разрыва связи молекул, разрушения исходной структуры рас–творителя и экзотермические эффекты образова–ния различных продуктов взаимодействия, в том числе сольватов.
Для простоты изложения приращение энтальпии раст–ворения ΔНраств можно представить как разность энер–гии Екр, затрачиваемой на разрушение кристаллической решетки растворяемого вещества, и энергии Есол, выде–ляющейся при сольватации частиц растворенного веще–ства молекулами растворителя. Иначе говоря, измене–ние энтальпии представляет собой алгебраическую сумму изменения энтальпии ΔНкр в результате разруше–ния кристаллической решетки и изменения энтальпии ΔНсол за счет сольватации частицами растворителя:
ΔНраств = ΔНкр + ΔНсол,
где ΔНраств – изменение энтальпии при растворении.
Однако растворение благородных газов в органичес–ких растворителях нередко сопровождается поглоще–нием теплоты, например гелия и неона в ацетоне, бен–золе, этаноле, циклогексане.
При растворении твердых веществ с молекулярной кристаллической структурой и жидкостей молекуляр–ные связи не очень прочные, и поэтому обычно ΔНсол > ΔНкр Это приводит к тому, что растворение, например, спиртов и сахаров представляет собой экзотермиче–ский процесс (ΔНраств < 0).
При растворении твердых веществ с ионной решет–кой соотношение энергий Екр и Есол могут быть различ–ным. Однако в большинстве случаев энергия, выделяе–мая при сольватации ионов, не компенсирует энергию, затрачиваемую на разрушение кристаллической решет–ки, следовательно, и процесс растворения является эн–дотермическим.
Таким образом, термодинамические данные позво–ляют прогнозировать самопроизвольное растворение различных веществ на основе первого и второго начал термодинамики.
РАСТВОРЫ НЕЭЛЕКТРОЛИТОВ, бинарные или многокомпонентные мол. системы, состав которых может изменяться непрерывным образом (по крайней мере, в некоторых пределах). В отличие от растворов электролитов. в растворы неэлектролитов (мол. растворах) заряженные частицы в сколько-нибудь заметных концентрациях отсутствуют. растворы неэлектролитов могут быть твердыми, жидкими и газообразными.
Пар, находящийся в равновесии с жидкостью, называется насыщенным. При данной температуре давление насыщенного пара над каждой жидкостью - величина постоянная. Опыт показывает, что при растворении в жидкости какого-либо вещества давление насыщенного пара этой жидкости понижается. Таким образом, давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем при той же температуре. Разность между этими величинами принято называть понижением давления пара над раствором (или понижением давления пара раствора). Отношение величины этого понижения к давлению насыщенного пара над чистым растворителем называется относительным понижением давления пара над раствором.
Второй закон Рауля – понижение температуры кипения и повышение температуры замерзания раствора прямо пропорционально моляльной концентрации раствора:
|
|
первый закон Рауля – парциальное давление над раствором прямо пропорционально мольной доле растворенного вещества.
Криоскопия (от греч. κρύο — холод и греч. σκοπέω смотрю) — метод исследования растворов, в основе которого лежит измерение понижения температуры замерзания раствора по сравнению с температурой замерзания чистого растворителя.
Эбулиоскопия (от лат. ebulio — вскипаю) — метод исследования растворов, основанный на измерении повышения их температуры кипения по сравнению с чистым растворителем. Используется для определения молекулярной массы растворенного вещества, активности растворителя, степени диссоциации (или изотонического коэффициента).
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества (меньшей концентрации растворителя).
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
Вант-Гоффа закон осмотического давления, определяет давление молекул растворённого вещества на полупроницаемую перепонку, отделяющую раствор от чистого растворителя и непроницаемую для растворённого вещества.
Растворы электролитов, содержат в заметных концентрациях ионы-катионы и анионы. образующиеся в результате электролитической диссоциации молекул растворенного вещества.
Степенью
диссоциации
()
электролита называется отношение числа
его молекул, распавшихся на ионы, к
общему числу молекул электролита в
растворе,
т. е. ![]()
Важной характеристикой электролитов служит степень диссоциации α:
|
|
Аналогичная поправка вносится в законы Рауля, и изотонический коэффициент определяется следующим образом:
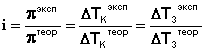 (III.19)
(III.19)
Изотонический коэффициент для растворов электролитов всегда больше единицы, причем с разбавлением раствора i возрастает до некоторого целочисленного значения.
Изотонический коэффициент (также фактор Вант-Гоффа; обозначается i) — безразмерный параметр, характеризующий поведение вещества в растворе.
Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как: HCl, HBr, HI, HNO3).
Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты), основания p-, d-, и f- элементов.
![]()
|
|
Это соотношение называют законом разбавления Оствальда.
Принципиальное отличие сильных электролитов от слабых состоит в том, что равновесие диссоциации сильных электролитов полностью смещено вправо:
|
|
|
а потому константа равновесия (диссоциации) оказывается величиной неопределенной. Снижение электропроводности при увеличении концентрации сильного электролита обусловлено электростатическим взаимодействием ионов.
Дебай и Хюккель, предложив модель, которая легла в основу теории сильных электролитов, постулировали:
Электролит полностью диссоциирует, но в сравнительно разбавленных растворах (C = 0,01 моль·л–1).
Каждый ион окружен оболочкой из ионов противоположного знака. В свою очередь, каждый из этих ионов сольватирован. Это окружение называется ионной атмосферой.
Активность, будучи подставлена в выражения законов для разбавленных растворов неэлектролитов, делает эти формулы применимыми для растворов электролитов. Аналитическая концентрация связана с активностью простым соотношением:
а = γс, (7.24)
где а – активность; с – аналитическая концентрация; γ – коэффициент активности.
Коэффициенты активности показывают меру отличия свойств реальных растворов от идеальных.
Кажущаяся степень диссоциации, также как и степень диссоциации в концентрированных растворах меньше единицы и увеличивается с уменьшением концентрации, стремясь к единице. Но в растворах сильных электролитов это связано с образованием из сольватированных ионов ассоциатов, которые ведут себя как недиссоциированные молекулы, т.е. не участвуют в переносе электричества и движутся как единое целое. Основное отличие ионных ассоциатов от недиссоциированных молекул в том, что в ассоциатах расстояние между сольватированными ионами значительно больше, чем в молекулах, т.к. между ионами находится растворитель. При уменьшении концентрации доля ассоциатов уменьшается, число частиц растворенного вещества увеличивается, и кажущаяся степень диссоциации растет.