
- •Введение
- •Раздел 1. Строение металлов
- •1.1. Атомно-кристаллическое строение
- •1.2. Дефекты строения кристаллических тел
- •1.3. Кристаллизация металлов
- •1.4. Формирование структуры деформированных металлов
- •Раздел 2. Строение сплавов
- •2.1. Фазы и структура металлических сплавов
- •2.2. Диаграммы состояния (фазового равновесия сплавов)
- •2.3. Диаграмма состояния системы железо – углерод
- •Раздел 3. Строение полимеров
- •3.1. Молекулярная структура полимеров
- •Раздел 4. Методические указания к решению задач
- •4.1. Общий алгоритм решения задач
- •Варианты контрольной работы Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Библиографический список
- •Содержание
- •Раздел 1. Строение металлов……………………………………...4
- •1.1. Атомно-кристаллическое строение…………..............4
- •Раздел 2. Строение сплавов………………………………………27
- •Раздел 3. Строение полимеров…………………………………...44
- •Раздел 4. Методические указания к решению задач……………46
Раздел 3. Строение полимеров
3.1. Молекулярная структура полимеров
Полимерами называют вещества, макромолекулы которых состоят из многочисленных повторяющихся элементарных звеньев, представляющих собой одинаковую группу атомов. Молекулярная масса таких молекул составляет от 500 до 1 000 000.
В молекулах полимеров различают главную цепь, построенную из большого числа атомов. Боковые цепи имеют значительно меньшую протяженность.
По форме макромолекулы полимеров делят на линейные, разветвленные, плоские, ленточные, пространственные или сет-чатые (рис. 3.1). Длина линейной макромолекулы в нес-колько тысяч раз больше ее поперечного сечения. Макро-молекулам поэтому присуща гибкость. Такие макромолекулы, обладая достаточно высокой прочностью вдоль главной цепи, слабо связаны между собой и обеспечивают высокую элас-тичность материала. Нагрев вызывает размягчение, а после-дующее охлаждение - затвердевание полимера (полиамид, полиэтилен).
Разветвленная макромолекула содержит боковые ответ-вления (рис. 3.1, б), что затрудняет сближение макромолекул и понижает межмолекулярное взаимодействие. Полимеры с по-добной формой макромолекул отличаются пониженной проч-ностью, повышенной плавкостью и рыхлостью. С гибкостью макромолекул полимеров связаны многие свойства полимеров: обратимая высокоэластичная деформация, достигающая десятков сотен процентов, ползучесть. Наиболее четко высокоэластичность проявляется в резинах и каучуках.
Увеличение химической связи между макромолекулами очень сильно сказывается на их гибкости. Так натуральный кау-чук, вулканизированный 3% серы, имеет относительное удли-нение при разрыве 800 – 900%, прочность на разрыв 29 – 32 МПа. Эбонит, тот же каучук, но отвержденный до 30% серы, имеет относительное удлинение при разрыве менее 20% и прочность на разрыв 52 – 54 МПА. Увеличивая количество вулканизатора – серы, мы тем самым повышаем энергию межатомной связи.

Рис. 3.1. Формы макромолекул полимеров: а - линейная; б - разветвленная; в - сетчатая
Раздел 4. Методические указания к решению задач
4.1. Общий алгоритм решения задач
Прочитайте и сформулируйте условие задачи, представьте физико-химические и химические явления и процессы, описанные в ней, определите, что необходимо найти;
выделите ключевые слова в задании;
изучите теоретическую литературу по выделенным ключевым словам и понятиям;
продумайте, какие новые данные необходимо найти, чтобы ответить на вопрос задачи; сформулируйте подзадачи (отдельные вопросы), которые необходимо решить для получения ответа на поставленный в ней вопрос;
найдите взаимосвязь между изученными понятиями и тем, что необходимо найти;
определите, каким методом будет решаться задача (аналитическим, графическим, арифметическим);
определите в какой последовательности рациональнее решать промежуточные задачи; запишите эту последовательность;
произведите все необходимые в данной задаче действия согласно плану;
проверьте и проанализируйте полученный результат; сравните его с целью, поставленной в задаче;
запишите полученный ответ.
Решение задач по диаграммам состояния включает выполнение следующих заданий:
Начертить заданную диаграмму состояния.
В каждой области диаграммы указать структуры, образующиеся в сплавах данной системы в состоянии равновесия. На диаграммах указать соответствующий равновесию фазовый состав. При решении задач следует выделить вертикальными пунктирными линиями области, имеющие разный структурный состав, и в каждой области указать соответствующие структурные составляющие.
Указать на диаграмме состояния составы заданных в задаче сплавов и провести соответствующие им вертикальные линии.
Построить схематически в координатах температура — время кривые охлаждения сплавов. Диаграммы состояний характеризуют превращения, протекающие при медленном охлаждении (нагреве). Они в зависимости от состава сплава могут протекать различно, а следовательно, сплавы могут иметь разные по характеру температурные кривые охлаждения (нагревания). Первичная кристаллизация, т. е. кристаллизация из жидкого состояния, протекает для чистых металлов при постоянной температуре с определенным тепловым эффектом, вследствие чего на кривых охлаждения при температуре затвердевания (и на кривых нагревания при температуре плавления) обнаруживается остановка (горизонтальный участок).
В системах из двух компонентов первичная кристаллизация протекает указанным образом, т. е. при постоянной температуре, только в сплавах эвтектического состава, в сплавах - химических соединениях и в тех твердых растворах, состав которых отвечает на диаграмме положению минимума или максимума.
Кристаллизация остальных сплавов происходит в интервале температур. Так как образование кристаллов из жидкости идет с выделением тепла, то этому процессу соответствует замедление охлаждения сплава, что изменяет наклон кривой охлаждения. Поэтому начало процесса кристаллизации этих сплавов характеризуется перегибом на кривой охлаждения. Окончание процесса кристаллизации может в зависимости от числа фаз характеризоваться на кривой охлаждения перегибом или горизонтальным участком.
Если сплав по окончании затвердевания однофазный (твердый раствор), то в течение всего процесса кристаллизации в равновесии находятся две фазы: жидкость и кристаллы твердого раствора. Окончание затвердевания характеризуется перегибом (изменяется наклон кривой) на кривой охлаждения. На диаграмме состояния этому случаю соответствует наклонный ход линии солидуса и изменение температуры кристаллизации при изменении концентрации сплава (рис. 2.2).
В сплавах - механических смесях (гетерогенные системы), образующих эвтектику, в момент окончания затвердевания на линии солидуса находятся в равновесии три фазы: кристаллы обоих компонентов (или их растворов и соединений) и жидкость. Поэтому окончание первичной кристаллизации происходит при постоянной температуре и характеризуется остановкой (горизонтальным участком) на кривой охлаждения (рис. 2.3). На диаграмме состояния этому случаю соответствует горизонтальный ход линии солидуса (прямая линия).
Кривая охлаждения, которую строят при выполнении задачи, должна показывать не только характер превращения, но кроме того, и относительное количество сплава, превращающегося при постоянной температуре. Это следует из того, что температурная остановка зависит от теплового эффекта превращения и при одинаковой массе и скорости охлаждения сплава пропорциональна количеству образующейся эвтектики.
Чтобы указать протяженность горизонтального участка на кривой охлаждения, следует выбрать масштаб для изображения кристаллизации сплава, содержащего 100 % эвтектики. При построении требуемых в задаче кривых охлаждения удобно, например, принять горизонтальный участок кривой для эвтектического сплава длиной 10 мм, а затем по правилу отрезков определить относительное количество эвтектики, образующейся при кристаллизации данного сплава, и показать кристаллизацию эвтектики на кривой охлаждения в виде горизонтального участка, соответствующего по длине ее относительному количеству. Например, при наличии в сплаве 50 % эвтектики крис-таллизацию следует представить (в принятом масштабе) горизонтальным участком длиной 5 мм.
Часто в сплавах одной системы в зависимости от концентрации и числа образующихся фаз происходят оба вида превращения. Например, в сплавах системы, приведенной на рис. 2.4, кристаллизация α -фазы (а также β-фазы) протекает при переменной температуре, а затвердевание эвтектики - при постоянной.
В сплавах с перитектическим превращением (рис. 2.5.) кривая охлаждения 1 обнаруживает: перегиб, указывающий начало кристаллизации (в равновесии находятся две фазы: жидкость и выделяющиеся первичные кристаллы фазы, богатой более тугоплавким компонентом); горизонтальный участок (остановка), отвечающий перитектической реакции, при которой в условиях равновесия находятся три фазы: первичные, кристаллы фазы, богатой тугоплавким компонентом, жидкость и образующиеся кристаллы фазы, богатой более легкоплавким компонентом.
Построить схему кристаллизации заданных сплавов, показать графически структуры, образующиеся в процессе кристаллизации, а также превращения, протекающие в этих сплавах при охлаждении. Схема кристаллизации должна быть построена в том же масштабе (для температур), какой был принят ранее. Для изображения каждой отдельной структуры необходимо предварительно установить условные обозначения, указав, что представляет собой данная структурная составляющая (твердый раствор, механическая смесь, химическое соединение).
Необходимо стремиться к тому, чтобы приводимые изображения максимально близко воспроизводили реальные структуры, которые наблюдаются в заданном или аналогичном сплаве при металлографическом анализе. Чистые металлы и твердые растворы в состоянии равновесия (после отжига) имеют в микроскопе зернистое (полиэдрическое) строение, подобное, например, полиэдрической структуре α-железа (феррита) или полиэдрам твердого раствора цинка в меди после обработки давлением и отжига. Если в сплавах данной системы образуются твердые растворы нескольких типов, то каждому из них следует давать другое условное изображение, как это показано, нап-ример, на диаграмме, приведенной на рис. 2.4.
Химические соединения могут быть в виде кристаллов различной формы: при распаде твердых растворов они часто отлагаются в виде сетки по границам зерен или образуют включения пластинчатой или игольчатой формы. Эвтектики и эвтектоиды, кристаллизуются в виде участков гетерогенной структуры различной измельченности: точечного, плас-тинчатого или зернистого вида.
При построении схемы кристаллизации следует учитывать примерное количество каждой составляющей. Так, при выделении из твердого раствора небольшого количества вторичных кристаллов другой фазы вследствие уменьшения растворимости с понижением температуры следует изображать эту фазу в виде мелких кристалликов (например, на границах зерен) на фоне полиэдрической структуры основного твердого раствора.
Дать характеристику состояния заданных сплавов при температурах, указанных в задаче.
Если сплав при температуре, указанной в задаче, окажется гетерогенным, то надо определить фазы или структуры, присутствующие в сплаве, указать состав каждой составляющей и количество отдельных составляющих в процентах. Для этого необходимо провести через точку, определяющую данный сплав при заданной температуре, горизонталь до пересечения с линиями диаграммы, т. е. коноду - линию, показывающую составы фаз, находящиеся в равновесии; затем, опустив перпендикуляры из концов коноды на абсциссу, определить концентрацию каждой фазы.
Далее по правилу отрезков надо определить относи-тельное количество отдельных фаз или структур, присут-ствующих в сплаве в состоянии равновесия. Количество присутствующих в сплаве эвтектики или эвтектоида следует рассчитывать для температур их образования. Результаты расчета необходимо привести в виде таблицы ниже диаг-раммы, как это показано, например, в решении задачи.
ЗАДАЧА № 1. По диаграмме состояния Cu-Ni опре-делить фазовый состав и количественное соотношение фаз спла-ва с 50% меди и 50% никеля при температуре 1250°С. Оп-ределить температуры фазовых превращений этого сплава и постройте кривую охлаждения. Объяснить ход полученных кри-вых и указать, какие процессы, происходящие в этом сплаве, характеризуют отдельные участки кривых. Определить темпе-ратуру плавления этого сплава.
РЕШЕНИЕ.
1. Прочитав содержание задачи, выделяем исходные данные. Исходными данными будут: диаграмма состояния Cu-Ni, сплав с содержанием 50% Cu и 50% Ni, температура - 1250°С.
2. Определяем, что необходимо найти. Необходимо найти: фазовый состав сплава при 1250°С; количественное соотношение фаз сплава при 1250°С; температуру плавления; температуры фазовых превращений (критические точки).
3. Выделяем ключевые слова: сплав, диаграмма состо-яния, фаза, фазовый состав, количественное соотношение фаз, температура фазовых превращений, кривая охлаждения, температура плавления.
4. Дадим определения выделенным словам. Сплавы - сложные вещества, получаемые сплавлением двух и более простых веществ. Диаграмма состояния представляет собой график в координатах состав сплава - температура, на котором отражены продукты, образующиеся в результате взаи-модействия компонентов сплава друг с другом в условиях термодинамического равновесия при различных температурах. Этими продуктами являются вещества, имеющие в зависимости от температуры и состава определенное агрегатное состояние, специфический характер строения и вполне определенные свойства. Их принято называть фазами. Причем фазой считается определенная часть системы, образованной компонентами сплава, которая во всех своих точках имеет одинаковые состав, строение и свойства.
Жидкая фаза представляет собой раствор расплавленных компонентов.
Твердые фазы являются зернами, имеющими опре-деленную форму, размер, состав, специфику строения и свойства. Твердые фазы можно наблюдать в микроскоп. Это могут быть твердые растворы, химические соединения, а также зерна чистых компонентов, не образующих с другими компонентами ни твердых растворов, ни химических соеди-нений.
Диаграмма состояния разделена линиями на области. Отдельные области могут состоять только из одной фазы, а некоторые - из двух, имеющих разные составы, строение и свойства. Анализируя диаграмму состояния, можно составить представление о специфике свойств сплавов данной системы компонентов и характере их изменения в зависимости от состава, а также о возможности термической обработки сплавов и температуре нагрева для ее проведения.
В диаграммах состояния содержится информация, необходимая для создания и обработки сплавов различного назначения.
Температуры фазовых превращений – это критические температуры при которых сплав переходит из твердого состояния в жидкое. Эта температура находится на линии ликвидус.
Кривая охлаждения строится по найденным критическим точкам в координатах температура – время.
5. Выделим новые данные, т.е. данные, необходимые для решения задачи.
Для определения фазового состава и количественного соотношения фаз, необходимо знать правило отрезков и правило фаз.
6. Вычертим диаграмму состояния (как указано на рис. 4.1). Заданная диаграмма представляет собой диаграмму состо-яния с неограниченной растворимостью компонентов друг в друге, имеющих одинаковые типы решеток и исходное строение наружных электронных оболочек.
7. В каждой области укажем структуры. Выше линии ликвидуса АСВ находиться область жидкой фазы Ж. Под ней до линии солидуса ADB расположена дфухфазная область α + Ж. Фаза α представляет собой твердый раствор компонентов Cu и Ni. Область, расположенная под линией солидуса, является однофазной (фаза α).
8. Укажем на диаграмме состояния состав заданной в задаче сплава и проведем соответствующую вертикальную линию (см. рис. 4.1, а).
9. Построим схематично в координатах температура – время кривую охлаждения сплава (см. рис. 4.1, б). Кристалл-лизация сплава происходит в интервале температур. Точка С соответствует началу процесса кристаллизации, при которой из жидкости начинается выделение зерен твердого раствора α (Ж→α). Эта температура соответствует 1350°С. Процесс кристаллизации продолжается до точки D. При температуре, соответствующей точке D, кристаллизация завершается. Ниже точки D идет охлаждение сплава со структурой твердого раствора α.
Приведем схематичное изображение структур (см. рис. 4.1, в).
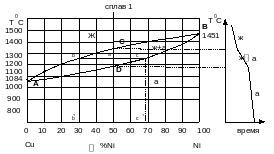
а б

в
Рис. 4.1. Диаграмма состояния Cu - Ni: а - диаграмма; б - кривая охлаждения; в - схема кристаллизации
10. При заданной температуре 1250°С сплав состоит из двух фаз - жидкой и твердой α - фазы. Укажем состав этих фаз при 1250°С. Для этого необходимо провести через точку, определяющую заданный состав при заданной температуре (точка а), горизонталь до пересечения с линиями диаграммы, т.е. коноду - линию, показывающую составы фаз (точки b и с). Опускаем перпендикуляры из концов коноды на абциссу и определяем концентрацию каждой фазы. Проекция точки пересечения коноды с линией ликвидус (b) на концен-трационную ось (b') определяет состав жидкой фазы, а проекция точки пересечения с линией солидус (с') – определяет состав твердой фазы α. Согласно этому получаем: состав жидкой фазы – 60% Ni и 40% Cu.
11. Далее по правилу отрезков определяем относительное количество фаз.
Количество жидкой фазы: Qж = ac/bc∙100% = 10/25∙100% = 40%. Количество твердой фазы: Qα = ba/bc∙100% = 15/25∙100% = 60%.
12. Температура плавления соответствует точке С(13500С).
ЗАДАЧА 2. Вычертите диаграмму состояния железо – це-ментит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 0.83% углерода. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
РЕШЕНИЕ.
1. Выделяем исходные данные. Ими будут: диаграмма состояния железо – цементит, сплав с 0.9% углерода.
2. Необходимо найти: критические точки фазовых прев-ращений, структуру при комнатной температуре, название сплава.
3. Ключевые слова: диаграмма состояния железо – цементит.
4. Дадим определения ключевым словам. Диаграмма состояния железо – цементит дает представление о строении железографитовых сплавов – сталей и чугунов. Содержание углерода в диаграмме ограничивается 6.67%, так как при этой концентрации образуется химическое соединение – карбид железа (Fe3C) или цементит, который и является вторым компонентом данной диаграммы. В системе (Fe – Fe3C) сплавы с содержанием углерода до 2.14% называют сталями. Если в стали углерода более 0.8%, то ее называют заэвтектоидной.
5. Вычертим диаграмму состояния и укажем на ней заданный сплав. Проведем соответствующую вертикальную линию 1 (см. рис. 4.2.).
6. Построим схематично в координатах температура – время кривую охлаждения заданного состава сплава.Опишем превращения, которые испытывает сплав при критических точках. Образование кристаллов аустенита (А) происходит в интервале температур 1- 2 (Ж→А). Состав аустенита изменяется по линии солидус AE, состав жидкой фазы по линии ликвидус AС. В точке 2 кристаллизация аустенита закан-чивается, и от точки 2 до точки 3 структурных изменений в нем не происходит, аустенит просто охлаждается. При охлаждении в диапазоне температур между точками 3 - 4 из кристаллической решетки аустенита выделяется избыточный углерод с образованием вторичного цементита Ц11 (А→Ц11). При этом содержание углерода в аустените изменяется по линии ES. На линии PSK при температуре 727°С происходит эвтектоидное превращение, при котором аустенит превращается в перлит (А→П). Поэтому при комнатной температуре структура сплава состоит из перлита и вторичного цементита (П+Ц11).
7. Так как заданный сплав содержит углерода более 0.8%, значит он относится к завтектоидной стали.
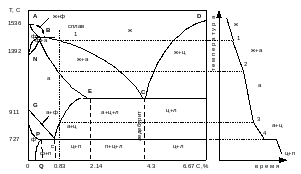
а б
Рис. 4.2. Диаграмма состояния Fe - C: а - диаграмма состояния; б - кривая охлаждения для стали с 0.8% углерода
8. Запишем полученный ответ: структура заданного спла-ва при комнатной температуре – перлит и вторичный цементит. Заданный сплав относится к заэвтектоидной стали.
