
- •1. Введение. Предмет и прикладное значение дисциплины. Основные понятия, терминология, модели жидкости.
- •3. Ротор вектора скорости и его физический смысл в вихревом сечении, теорема Стокса. Правила действий с оператором Гамильтона.
- •4. Термодинамические характеристики рабочего тела, параметры состояния в идеальных и реальных газах, молекулярно-кинетическое обоснование. Первый и второй законы термодинамики. Изменение энтропии.
- •5. Плотность и сплошность среды, основные определения, виды жидкостей, виды течений. Понятие о полных параметрах состояния.
- •7. Кризис течения в капельных жидкостях, запирание каналов по расходу. Меры борьбы с кавитацией.
- •8. Кризис течения в сжимаемых жидкостях. Запирание по расходу.
- •10. Напряжения, действующие в жидкостях. Силы, вызванные вязкостью.
- •11. Работа, тепло и ускорение, вызванные силами вязкости. Примеры проявления составляющих вязкости, вихревой эффект.
- •13. Методы исследования течений сплошных сред (подходы Эйлера и Лагранжа, физическое и численное моделирование).
- •16. Измерение статического давления в потоках. Управление чувствительностью к углу скоса потока.
- •19. Измерение скорости и направления потока.
- •22. Основные гидродинамические понятия, свойства элементарной струйки тока, виды расхода, плотность тока. Причины различия расхода через поперечное и живое сечения канала.
- •25. Консервативность законов сохранения. Уравнение неразрывности в общем виде (консервативное и неконсервативное). Частные случаи уравнения неразрывности.
- •28. Анализ формулы расхода. Запирание каналов по расходу. Воздействия, способные вызвать запирание каналов по расходу.
- •29. Силы, действующие в жидкости. Уравнения движения в форме Эйлера и Навье-Стокса.
- •31. Частные случаи уравнения Эйлера: уравнение Эйлера в гидростатике – абсолютное и относительное равновесие, уравнение равновесия и уравнение поверхности уровня, международная стандартная атмосфера.
- •37. Уравнение количеств движения (первое уравнение Эйлера) в общем виде. Тензор импульса и его компоненты. Неконсервативная форма для расчета силового взаимодействия потока и обтекаемых тел.
- •40. Нестационарное и стационарное одномерное уравнение количеств движения. Уравнение количества движения для элементарной струйки.
- •42. Понятие о принципе работы турбомашин. Энергетическая форма уравнения моментов количества движения, коэффициенты нагрузки (закрутки, напора), нагруженность ступени.
- •44. Уравнение энергии для идеального и реального энергоизолированного течения, политропический интеграл, t-s-диаграммы процессов ускорения/торможения.
- •46. Изоэнтропный и адиабатный потоки. Работа и кпд турбомашин, t-s диаграммы.
- •48. Потери энергии в канале постоянного сечения (трубе) для капельных и сжимаемых жидкостей. Основные виды местных сопротивлений – конфузор и внезапное сжатие, диффузор и внезапное расширение.
- •52. Уравнение Гюгонио и анализ геометрического воздействия. Связь сжимаемости со скоростью потока, вывод и анализ. Другие уравнения и формулы, подтверждающие или повторяющие анализ уравнения Гюгонио.
- •56. Кинематика движения жидкой частицы. Виды движения. Вихревое и потенциальное движение, условия незавихренности, потенциал скорости. Основные понятия. Уравнения, описывающие вихревое течение.
- •58. Распространение слабых возмущений в упругой среде. Виды и свойства характеристик. Простые двумерные волны и их источники. Механизм пересечения стационарных характеристик.
- •62. Законы сохранения в теории скачков уплотнения и ударных волн. Природа потерь в нормальных разрывах поля скоростей.
- •64. Динамическое соотношение на поверхностях нормального разрыва. Ударная адиабата Гюгонио. Системы скачков уплотнения, их реализация в сверхзвуковых входных устройствах.
- •68. Отражение волн сжатия и скачков уплотнения от твердой стенки. Правильное и Маховское отражение от плоской твердой стенки.
- •70. Режимы истечения из сопла Лаваля. Диаграмма режимов истечения. Использование обращенного сопла Лаваля на режиме глубокого перерасширения для сверхзвуковых входных устройств.
4. Термодинамические характеристики рабочего тела, параметры состояния в идеальных и реальных газах, молекулярно-кинетическое обоснование. Первый и второй законы термодинамики. Изменение энтропии.
Совершенный газ – упрощенная модель реального газа, с принятыми допущениями:
Полностью отсутствуют межмолекулярные силы;
Молекулы в виде материальных точек, обладающих массой;
Теплоемкость, газовая постоянная, показатель адиабаты и молярная масса неизменны и не зависят от температуры;
Агрегатное состояние неизменно при любых условиях.
Газ можно рассматривать как совершенный до температуры 2500 К, при более высоких температурах начинаются процессы диссоциации, ионизации и рекомбинации.
Идеальный газ – совершенный газ, лишенный свойств вязкости.
Параметры состояния рабочего тела:
Давление. Согласно МКТ, давление – результат ударов хаотически и непрерывно движущихся молекул о стенки сосуда. Основное уравнение кинетической теории для модели идеального газа:
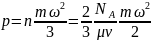
 число молекул вещества в
число молекул вещества в
 ;
;
 масса молекулы, кг;
масса молекулы, кг;
 средняя квадратичная скорость молекул,
м/с;
средняя квадратичная скорость молекул,
м/с;
 число Авогадро (число молекул в 1
кмоле);
число Авогадро (число молекул в 1
кмоле);
 молярная масса вещества, кг/кмоль;
молярная масса вещества, кг/кмоль;
 молярный объем вещества,
молярный объем вещества,
 .
Моль – количество вещества, в котором
содержится столько молекул, сколько
содержится атомов в изотопе углерода
массой 0,012 кг.
.
Моль – количество вещества, в котором
содержится столько молекул, сколько
содержится атомов в изотопе углерода
массой 0,012 кг.

При постоянной температуре давление
определяется только числом молекул в
единице объема, и не зависит от рода
молекул. При
 свойства газа определяются только
числом молекул.
свойства газа определяются только
числом молекул.
Температура. Согласно МКТ, абсолютная термодинамическая температура – величина, пропорциональная средней кинетической энергии поступательного движения молекул газа. По уравнению Больцмана, для модели идеального газа:

 константа Больцмана.
константа Больцмана.
Абсолютный ноль температуры – ноль по
шкале Кельвина ( ),
при котором прекращается движение
молекул.
),
при котором прекращается движение
молекул.
Плотность и удельный объем. Это количество вещества, заключенное в единице объема:

Эти три параметра состояния связаны между собой уравнением Клапейрона-Менделеева, для одного килограмма идеального газа:

 удельная газовая постоянная, Дж/кг∙К.
При умножении
удельная газовая постоянная, Дж/кг∙К.
При умножении
 на молярную массу, получается универсальная
газовая постоянная, одинаковая для
всех газов (на основании закона Авогадро
о том, что при одинаковых давлении и
температуре все газы имеют одинаковый
молярный объем, при н.у. равный 22,4
м3/кмоль).
на молярную массу, получается универсальная
газовая постоянная, одинаковая для
всех газов (на основании закона Авогадро
о том, что при одинаковых давлении и
температуре все газы имеют одинаковый
молярный объем, при н.у. равный 22,4
м3/кмоль).
Значение универсальной газовой постоянной при н.у. (101325 Па и 273,15 К) равно:

Вид термодинамического процесса
определяется показателем политропы
 ,
из уравнения политропного процесса,
для идеальных газов:
,
из уравнения политропного процесса,
для идеальных газов:


При
 процесс будет изобарным,
процесс будет изобарным,
 изотермическим,
изотермическим,
 изохорным,
изохорным,
 адиабатным. Чем выше показатель политропы,
тем меньше сжимаемость и больше упругость
газов.
адиабатным. Чем выше показатель политропы,
тем меньше сжимаемость и больше упругость
газов.
Теплоемкость тела – количество тепла, необходимое для нагрева единицы вещества на один градус Кельвина. Истинная теплоемкость соответствует бесконечно малому изменению температуры:

В газодинамике используют массовые теплоемкости – изобарную и изохорную:




 показатель адиабаты.
показатель адиабаты.
Энтальпия – сумма потенциальной
внутренней энергии
 и потенциальной энергии давления
и потенциальной энергии давления
 для единицы вещества:
для единицы вещества:


Уравнение состояния через полную
энтальпию и внутреннюю энергию
 :
:

Модуль упругости – количественная оценка сжимаемости газа, отношение изменения давления к вызванному им относительному изменению плотности:

Упругость газов, в зависимости от давления и вида термодинамического процесса, на 3-4 порядка меньше упругости капельных жидкостей. На малых скоростях газовых потоков их свойство сжимаемости проявляется незначительно, поэтому их рассматривают как поток капельной жидкости.
Первый закон термодинамики: подводимые
к газу удельное тепло трения
 и внешнее тепло
и внешнее тепло
 расходуются на изменение внутренней
энергии
расходуются на изменение внутренней
энергии
 и на работу деформации
и на работу деформации
 ,
иначе говоря, на изменение энтальпии и
работу проталкивания:
,
иначе говоря, на изменение энтальпии и
работу проталкивания:

Второй закон термодинамики: рост количества подводимого тепла увеличивает приращение энтропии, в то время как рост температуры, при которой к системе подводится тепло, снижает приращение энтропии.

Свойства реальных рабочих тел описываются уравнением Ван-дер-Ваальса:

экспериментальная константа,
характеризующая силы межмолекулярного
взаимодействия,
суммарный объем, занимаемый молекулами
при
 .
Влияние переменных уравнения на
давление:
.
Влияние переменных уравнения на
давление:
К увеличению давления приводит:
 увеличение скорости хаотического
движения молекул;
увеличение скорости хаотического
движения молекул;
 увеличение концентрации молекул
увеличивает межмолекулярные силы;
увеличение концентрации молекул
увеличивает межмолекулярные силы;
 уменьшается оттягивающее действие на
молекулы, приближающиеся к стенке;
уменьшается оттягивающее действие на
молекулы, приближающиеся к стенке;
 уменьшение свободного пробега молекул
и увеличение количества ударов о стенку;
уменьшение свободного пробега молекул
и увеличение количества ударов о стенку;
Также уравнение состояния может иметь
вид
 ,
где
,
где
 коэффициент сжимаемости природного
газа, определяется по номограммам.
коэффициент сжимаемости природного
газа, определяется по номограммам.
