
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные понятия химии
- •Где м(х) – мольная масса вещества х, fэкв.(х) – фактор эквивалентности вещества х.
- •1.2 Основные законы химии
- •2 Основные классы неорганических соединений
- •2.1 Простые вещества
- •2.2 Сложные вещества
- •Тема 2 «растворы» лекция №3 «общие свойства растворов»
- •1 Классификация систем, состоящих из двух и более веществ
- •2 Способы выражения состава растворов
- •1) Массовая доля (ω) – отношение массы растворенного вещества к массе раствора
- •3) Равномерное распределение сольватов (гидратов) в растворителе. Является следствием диффузии и требует затраты энергии.
- •4 Растворимость
- •4.1 Растворимость газов в жидкостях. Закон Генри
- •4.2 Растворимость твердых веществ в воде
- •Лекция № 4 «растворы неэлектролитов»
- •1 Свойства растворов неэлектролитов
- •1.1 Закон Рауля
- •2) Растворенное вещество – нелетучее и не диссоциирующее на ионы.
- •1.2 Криоскопический и эбуллиоскопический законы Рауля
- •- Криоскопический закон, - эбуллиоскопический закон,
- •2 Осмос
- •3 Применение законов Рауля и уравнения Вант-Гоффа к растворам электролитов
- •Лекция № 5 «растворы электролитов»
- •1.2 Диссоциация слабых электролитов
- •2 Закон разбавления Оствальда
- •3 PH водных растворов
- •3.1 Ионное произведение воды
- •Ионно-обменные и окислительно-восстановительные реакции
- •Лекция № 6
- •«Ионно-обменные реакции»
- •3) Образование осадков
- •4) Образование комплексных соединений
- •3 Гетерогенные равновесия в растворах электролитов.
- •Лекция № 7 «Гидролиз солей»
- •1 Общие представления о гидролизе
- •2 Различные случаи гидролиза
- •1) Гидролиз соли образованной слабым основанием и сильной кислотой
- •4) Гидролиз солей, образованных многозарядными катионами и анионами
- •5) Совместный гидролиз двух солей, образованных слабой кислотой и слабым основанием
- •5 Смещение равновесия при гидролизе
- •5.1 Влияние добавок различных веществ на гидролиз
- •5.2 Влияние температуры на смещение гидролиза
- •5.3 Влияние концентрации гидролизующейся соли
- •Лекция № 8 «окислительно-восстановительные реакции»
- •1 Основные понятия
- •5 Взаимодействие металлов с водой, кислотами и щелочами
- •Электрохимические процессы
- •Лекция №9
- •«Гальванические элементы»
- •1 Электродный потенциал на границе металл – раствор
- •2 Принцип работы гальванического элемента
- •3 Водородный электрод сравнения. Электрохимический ряд
- •4 Уравнение Нернста
- •96500 Кл/моль),
- •5 Элементы
- •Лекция № 10 «электролиз»
- •3 Количественные расчёты в электролизе
- •4 Аккумуляторы
- •1) Свинцовый аккумулятор
- •2) Кадмиево-никелевый аккумулятор (кн)
- •3) Железо-никелевый аккумулятор (жн)
- •Лекция № 11 «коррозия и защита металлов от коррозии»
- •2.2 Гальванокоррозия
- •1) Гальванокоррозия чугуна в нейтральной среде:
- •2) Гальванокоррозия чугуна в кислой среде:
- •3) Контактная коррозия железа и меди в нейтральной среде.
- •2.3 Электрокоррозия
- •3 Способы защиты металлов от коррозии
- •3.1 Изолирование металлов от внешней среды
- •1) Гальванокоррозия оцинкованного железа в нейтральной среде
- •2) Гальванокоррозия луженого железа в кислой среде
- •3.2 Изменение состава коррозионной среды
- •3.3 Рациональное конструирование
- •3.4 Электрохимические способы защиты от коррозии
- •1) Протекторная защита.
- •2) Катодная защита.
- •Тема 5 основные закономерности протекания химических процессв лекция № 12
- •1 Энергетика химических процессов.
- •2 Закон Гесса
- •Разберем данный вопрос на примере образования из простых веществ углекислого газа. Данное превращение можно провести по реакции
- •Или через промежуточный продукт (со) в две реакции:
- •1) Реакция горения этана выражается термохимическим уравнением
- •2) Рассчитать количество тепла, необходимое для испарения 1 м3 воды.
- •9.3 Энтропия
- •9.4 Энергия Гиббса
- •Лекция № 13
- •Химическая кинетика – учение о скоростях и механизмах протекания химических реакций.
- •1 Скорость реакции
- •1. История развития учения о строении атома
- •1.1. Модель атома по резерфорду
- •1.2. Модель атома по бору
- •1) Электрон в атоме может вращаться вокруг ядра не по любым, а только по строго определённым орбитам, которые называются стационарными.
- •2) Двигаясь по стационарным орбитам, электрон не излучает энергию.
- •1) Была неприменима для описания спектров атомов более сложных, чем водород;
- •2) Не могла объяснить различной интенсивности спектральных линий в спектре даже атома водорода.
- •1.3. Современные представления об атоме
- •2. Квантово–механическая модель атома
- •2.1. Квантовые числа
- •2.4. Соответствие электронных формул элементов и положением их в периодической таблице
- •3. Периодический закон и периодическая таблица д.И.Менделеева
- •3.1. Периодический закон
- •3.2.Периодическая таблица д.И.Менделеева
- •3.3 Периодичность изменения свойств элементов в периодической таблице
- •3.3.1 Радиусы атомов в периодах радиусы атомов по мере увеличения заряда ядра уменьшаются вследствие увеличения электростатического взаимодействия электронов с ядром.
- •3.3. 6 Прогнозирование свойств элементов по положению в периодической таблице
- •Лекция № 15 «Химическая связь, строение молекул и строение вещества»
- •2. Метод валентных связей
- •1) Обменный – два атома предоставляют по одному электрону на образование общей электронной пары.
- •2) Донорно-акцепторный – один атом (донор) предоставляет электронную пару, а второй (акцептор) – свободную орбиталь.
- •3. Основные характеристики химической связи
- •4. Типы химических связей
- •4.1.Ковалентная связь – это связь между двумя атомами за счет образования общей электронной пары.
- •4.3. Металлическая связь
- •4.4. Водородная связь
- •5. Строение гидридов элементов II-периода
- •«Химическая связь, строение молекул и строение вещества»
- •2. Метод валентных связей
- •1) Обменный – два атома предоставляют по одному электрону на образование общей электронной пары.
- •2) Донорно-акцепторный –
- •3. Основные характеристики химической связи
- •4. Типы химических связей
- •4.1. Ковалентная связь – это связь между двумя атомами посредством общей электронной пары.
- •4.2. Ионная связь – это связь между противоположно заряженными ионами.
- •4.3. Металлическая связь
- •4.4. Водородная связь
- •Химия элементов
- •Лекция № 16
- •«Свойства s-элементов»
- •1. Щелочные металлы
- •2. Бериллий, магний и щелочноземельные металлы
- •3. Химические свойства s-элементов
- •4. Физико–химические свойства водорода и гелия
- •5. Физико–химические свойства воды
- •5.2. Физические свойства воды
- •5.3. Химические свойства воды
- •Лекция № 17 «жесткость воды»
- •1. Общие понятия
- •3. Единица измерения жесткости
- •4. Водоподготовка
- •5. Водоумягчение
- •1.3. Алюминий
- •1.4. Индий. Галлий. Таллий
- •2.1. Электронное строение и общая характеристика
- •2.2. Углерод и его соединения
- •2.3. Кремний
- •2.4. Германий. Олово. Свинец
- •Лекция № 19 «свойства р-элементов
- •V и VI групп»
- •1.1. Электронное строение и общая характеристика
- •1.2. Азот
- •1.3. Фосфор
- •1.4. Мышьяк, сурьма, висмут
- •2.1. Введение
- •2.2. Кислород
- •2.3. Сера
- •2.4. Сравнение свойств водородных соединений р-элементов VI группы
- •2.5. Селен. Теллур
- •Лекция № 20
- •1.1. Электронное строение и общая характеристика VII группы (галогены)
- •Галогены проявляют нечетные валентности
- •1.2 Физические свойства галогенов
- •1.3 Химические свойства галогенов
- •1.4 Водородные соединения галогенов
- •1 .5 Кислородсодержащие соединения галогенов
- •1.6 Применение галогенов
- •1.7 Положение в периодической таблице и общая характеристика р-элементов VIII группы
- •Лекция № 21
- •1. Определение комплексных соединений
- •1) Диссоциация сульфатов калия и алюминия
- •2) Дисоциация двойной соли – алюмокалиевых квасцов
- •3)Диссоциация комплексного соединения
- •2. Состав комплексных соединений
- •1) Комплексный ион – [Fe(сn)6]-3,
- •Примеры состава комплексных соединений
- •3. Номенклатура комплексных соединений
- •[Pt(nh3)4Cl2]Cl2 –хлорид дихлоротетраамминплатины (IV)
- •4. Диссоциация комплексных соединений
- •5. Реакции с участием комплексных соединений
- •5.1. Образование комплексных соединений
- •5.2. Преход от одного комплексного соединения к другому
- •5.3 Разрушение комплексного соединения
- •Лекция № 22
- •Введение
- •1.1. Физические свойства
- •1.2. Химические свойства
- •Вопрос № 3 Составьте уравнения реакций, протекающих при осуществлении следующих превращений Cu→Cu(no3)2→Cu(oh)2 →CuSo4.
- •Лекция № 23
- •Лекция № 24
- •2.1 Элементы триады железа
- •2.2 Платиновые металлы
- •Лекция 25 «органические соединения» введение
- •1) Замещения атомов водорода по связям с с–н,
- •2) Разрыва связей с–с.
- •1.2. Непредельные (ненасыщенные) углеводороды
- •Ацетилен с2н2, или сн±сн
- •2. Карбоциклические
- •2.1. Предельные циклические углеводороды
- •2.2. Ароматические углеводороды
- •3. Клыссы органических соединений
- •3.1. Галогенпроизводные
- •3.2. Спирты и фенолы
- •3.3. Простые эфиры
- •3.4. Альдегиды и кетоны
- •3.5. Карбоновые кислоты
- •3.6. Сложные эфиры карбоновых кислот. Жиры
- •3.7. Амины
- •3.8. Аминокислоты и белки
- •Лекция № 26 «полимеры» Введение
- •3.Поликонденсеционные полимеры
- •4. Структура и состояния полимеров
- •Лекция № 27 «рабочие вещества низкотемпературной техники» Введение
- •1 Моль co2 – 6·1023 молекул co2 – 44г – 22,4л(н.У.).
- •1. Хладагенты неорганического происхождения
- •1.1. Номенклатура неорганических хладагентов
- •1.2. Физические и химические свойства неорганических хладагентов
- •2. Хладагенты органического происхождения (углеводороды)
- •2.1. Строение и номенклатура
- •2.2. Физические и химические свойства
- •3. Хладагенты органического происхождения (галогенпроизводные)
- •3.2.Цепные реакции(пределы взрываемости, разрушение озонового слоя)
2.4. Сравнение свойств водородных соединений р-элементов VI группы
В ряду Н2O – Н2S − Н2Sе − Н2Те с увеличением молекулярных масс должно наблюдаться повышение температур кипения. Как видно из рисунка 3 данная зависимость соблюдается, за исключением Н2О. Установлено, что аномальное повышение температуры кипения Н2О является следствием образования водородных связей между отдельными молекулами воды.
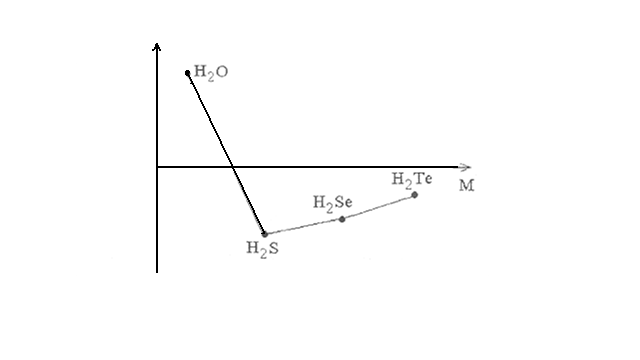
Рисунок 3 – зависимость температуры кипения водородных соединений р-элементов VI группы от молекулярной массы
2.5. Селен. Теллур
Селен по свойствам близок к сере. Селеновая кислота (Н2SеO4) также является сильной кислотой. Теллуровая кислота (Н2ТеO4) же кислота является очень слабой кислотой. Все соединения селена и теллура ядовиты.
Селен и теллур – полупроводники. Теллур служит легирующей добавкой к свинцу, улучшая его механические свойства.
Лекция № 20
« Р-ЭЛЕМЕНТЫ VII и VIII ГРУПП. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ »
1. Р-ЭЛЕМЕНТЫ VII и VIII ГРУПП
1.1. Электронное строение и общая характеристика VII группы (галогены)
В главную подгруппу VII группы входят элементы:
фтор (F), хлор (l), бром (Вr), йод (I) и астат (Аt). У атомов галогенов во внешнем электронном слое находится по семь электронов – ns2np5.
На рисунке 1 приведены энергетические диаграммы валентных зон галогенов в основном и возбужденных состояниях из которых видно, что фтор одновалентен, а остальные
Галогены проявляют нечетные валентности
1, 3, 5, 7.
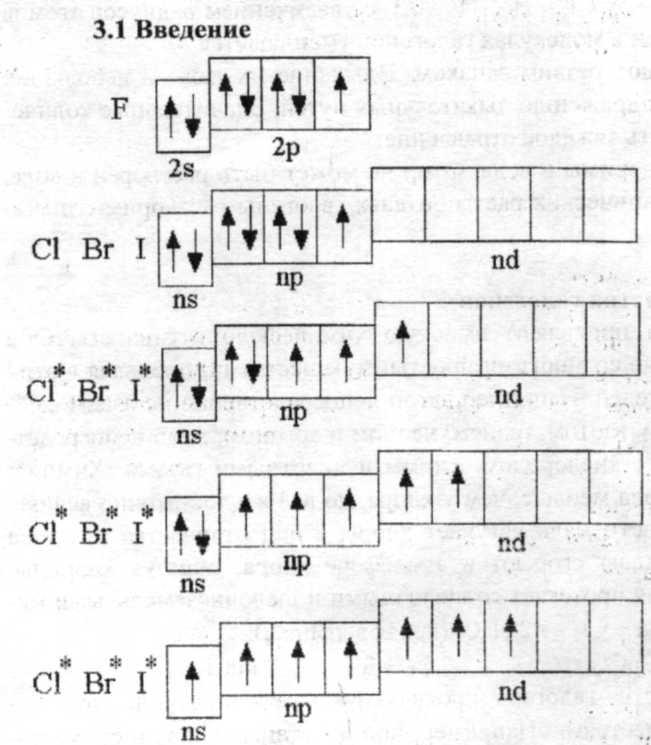
Рис. 1 Энергетические диаграммы валентных зон галогенов
Каждый галоген в своей подгруппе является наиболее сильным окислителем. С повышением порядкового номера элементов в ряду F, С1, Br, I и At уменьшается окислительная способность элементов.
Фтор – проявляет только степень окисления -1.
С1,Br,I–проявляет степени окисления:-1, 0, +1, +3, +5, +7.
1.2 Физические свойства галогенов
Фтор – газ бледно-жёлтого цвета;
Хлор – газ жёлто-зелёного цвета;
Бром – красно-бурая жидкость;
Йод – кристаллическое вещество темно-фиолетового цвета. При нагревании йод сублимируется (возгоняется), превращаясь в пар фиолетового цвета; при охлаждении пары йода кристаллизуются, минуя жидкое состояние.
Молекулы простых веществ двухатомны:
F2, С12, Br2, I2.
Галогены слабо растворимы в воде, но значительно лучше в органических растворителях. Фтор нельзя растворить в воде, так как он окисляет её
F2+ 2Н2O = 4НF + О2.
При растворении хлора в воде происходит его частичное (примерно на 1∕3) самоокисление-самовосстановление по реакции
С12 + Н2O ↔ НС1+ НС1О.
Полученный раствор называется хлорной водой. Он обладает сильными кислотными и окислительными свойствами и применяется для обеззараживания питьевой воды.
1.3 Химические свойства галогенов
Галогены проявляют высокую химическую активность. Они вступают во взаимодействие с многими простыми веществами, проявляя свойства окислителей. Самый активный неметалл фтор непосредственно не взаимодействует только с кислородом, азотом, гелием, неоном и аргоном; хлор непосредственно не взаимодействует с кислородом, азотом и инертными газами. Бром и йод химически менее активны. Многие металлы сгорают в атмосфере хлора, образуя хлориды:
2Na + С12 → 2NaCl (яркая вспышка);
Сu + С12 → СuС12;
2Fe + 3Сl2 → 2FeCl3.
Фтор со многими неметаллами реагирует с взрывом:
Н2 + F2 → 2HF; Si + 2F2 → SiF4; S + 3 F2 → SF6.
В его атмосфере фтора горят такие устойчивые вещества, как стекло и вода:
SiО2 + 2F2 → SiF4 + О2, 2Н2О+ 2F2 → 4HF +О2.
Окислительная активность галогенов уменьшается от фтора к астату, а восстановительная активность галогенид-ионов в этом направлении увеличивается. Из этого, что более активный галоген вытесняет менее активный из растворов его солей.
С12+ 2NaI → I2+ 2NaCl,
Вг2+ 2NaI → I2+ 2NaBr,
Cl2+ 2NaBr → Br2 + 2NaCl.
