
тест
.docxВопрос: К моменту установления равновесия в газофазной реакции H2 + I2 <=> 2HI концентрация HI оказалась равной 2.4 моль/л. Какими были (моль/л) первоначально равные концентрации йода и водорода, если константа равновесия K = 5.76? 1. 3 2. 4.4 3. 1 4. 2.2 5. 8.6 Ответ: 4 Правильно!
Вопрос: Во сколько раз увеличится скорость реакции при увеличении температуры на 20℃, если температурный коэффициент скорости равен 3,3? 1. 66 2. 10.89 3. 23.3 4. 8 5. 6.6 Ответ: 2 Правильно!
тест "Вопросы к зачету МП -I"
Вопрос: При действии щелочи на гидроксид цинка образуются ионы 1. ZnOН+ 2. ZnO22- 3. H+ 4. Zn2+ 5. OH- Ответ: 5 Неправильно!
Вопрос:
Константе
равновесия реакции N2 +
3H2 ⇔
2NH3 соответствует
выражение
1. ![]() 2.
2. ![]() 3.
3. ![]() 4.
4. ![]() 5.
5. ![]() Ответ: 5
Правильно!
Ответ: 5
Правильно!
Вопрос: При сгорании 2,4 г. магния выделяется 60,25 кДж тепла. Стандартная энтальпия образования MgO равна 1. -60,25 кДж/моль 2. +60,25 кДж/моль 3. -602,5 кДж/моль 4. +602,5 кДж/моль 5. –1205 кДж/моль Ответ: 4 Неправильно!
Вопрос: Смешали 100 г 10 %-ного раствора HNO3 и 300 г 30%-ного раствора HNO3. Массовая доля полученного раствора равна 1. 40 2. 25 3. 20 4. 30 5. 2,25 Ответ: 2 Правильно!
Вопрос: Согласно второму закону Рауля: 1. ΔT(кип.) = EСm 2. ΔP/Po = χ(р-ренного вещества) 3. P(осм.) = СМRT 4. PV = nRT Ответ: 1 Правильно!
Вопрос: Добавление _________ к раствору ZnCl2 приводит к ослаблению гидролиза 1. Na2CO3 2. Na2SO4 3. FeCl3 4. CH3COONa 5. NaCN Ответ: 3 Правильно!
Вопрос: Электроны распределяются в квантовых ячейках на подуровнях 1. по соотношению главного и побочного квантовых чисел 2. по принципу Паули 3. по уравнению Де-Бройля 4. по правилам Клечковского 5. по правилу Хунда Ответ: 2 Неправильно!
Вопрос: Элементы N, F, B, O, K, Li расположены в порядке возрастания их радиусов 1. N, O, F, B, Li, K 2. F, B, N, O, Li, K 3. F, O, N, B, Li, K 4. K, Li, B, N, O, F Ответ: 3 Правильно!
Вопрос: Элемент, электронная формула которого имеет окончание ....4р3, находится в 1. Ш периоде IVА группе 2. IV периоде VА группе 3. V периоде IVА группе 4. III периоде IVВ группе 5. IV периоде VВ группе Ответ: 2 Правильно!
Вопрос: Электронная формула____ соответствует атому в стационарном состоянии 1. …2s22p63s13p1 2. …3s23p33d3 3. …3p64s23d3 4. …3p64s13d34p1 5. …6s25d14f145d96p36d1 Ответ: 5 Неправильно!
Вопрос: Образование связей описывается sp3-гибридизацией в молекуле 1. C2H4 2. CH4 3. PH3 4. H2S 5. CO2 Ответ: 2 Правильно!
Вопрос: Сумма коэффициентов в уравнении Mo + KClO3 + KOH → MoO42- + Cl- равна 1. 4 2. 6 3. 5 4. 7 5. 12 Ответ: 5 Неправильно!
Вопрос: В гальваническом элементе Cu/CuSO4(0,1M)//CuSO4(1M)/Cu при замене 0,1М-го раствора CuSO4 на 0,01М ЭДС 1. увеличится в 2 раза 2. увеличится в 10 раз 3. уменьшится в 2 раза 4. уменьшится в 10 раз 5. не изменится Ответ: 4 Неправильно!
Вопрос: При электролизе водного раствора ________ на катоде выделяется металл: 1. BaCl2 2. Mg(NO3)2 3. NaCl 4. KNO3 5. СuCl2 Ответ: 4 Неправильно!
Вопрос: Координационная формула дицианоаргентата (I) калия 1. K3[Ag(CN)4] 2. K[Ag(CN)2] 3. K[Au(CN)2] 4. K[Al(CNS)4] 5. K[Ag(CNS)2] Ответ: 2 Правильно!
Вопрос: Электроосмос используется для 1. предотвращения коагуляции 2. определения заряда частиц 3. для очистки коллоидных растворов от ионов 4. препятствия коалесценции Ответ: 3 Неправильно!
Вопрос: Мицеллы сульфата бария {m[BaSO4]nSO42-2(n-x)K+}2x-2хK+ образуются при сливании равных объемов растворов BaCl2 и K2SO4 при условии, что концентрация раствора хлорида бария ________ концентрации сульфата калия 1. больше 2. равна 3. меньше 4. значительно ниже Ответ: 1 Неправильно!
тест "Вопросы к зачету МП -I"
Вопрос: Характер оксида кремния (IV) 1. кислотный 2. основный 3. амфотерный 4. амфотерный с преобладанием кислотного 5. безразличный Ответ: 1 Правильно!
Вопрос: В ходе реакции A + 2B ⇒ C при уменьшении концентрация вещества A на 0,05 моль/л концентрация вещества B 1. снизилась на 0,05 моль/л 2. снизилась на 0,15 моль/л 3. повысилась на 0,25 моль/л 4. снизилась на 0,10 моль/л Ответ: 3 Неправильно!
Вопрос: При образовании 2 молей газообразного HCl выделилось 184,6 кДж тепла. Стандартная энтальпия образования HCl равна 1. -184,6 кДж/моль 2. +184,6 кДж/моль 3. –92,3 кДж/моль 4. +92,3 кДж/моль 5. -46,15 кДж/моль Ответ: 3 Правильно!
Вопрос: Для приготовления 1 л 6 %-ного раствора (пл. 1,048 г/мл) требуется_________мл 50 % - ного раствора KOH(пл. 1,538 г/мл) 1. 8,2 2. 15,0 3. 81,77 4. 125,76 5. 12,6 Ответ: 3 Правильно!
Вопрос: Согласно первому закону Рауля : 1. ΔT(кип.) = EСm 2. ΔT(зам.) = KСm 3. ΔP/Po = χ(р-ренного вещества) 4. P(осм.) = СМRT 5. PV = nRT Ответ: 4 Неправильно!
Вопрос: Из приведенных ниже солей не гидролизуется 1. NaClO 2. NH4ClO4 3. CH3COONa 4. NaClO4 5. NaCN Ответ: 4 Правильно!
Вопрос: Количество электронов на уровнях рассчитывается по 1. уравнению Шредингера 2. уравнению Де-Бройля 3. принципу Гейзенберга 4. принципу Паули 5. правилам Клечковского Ответ: 4 Правильно!
Вопрос: Элементы N, F, B, O, K, Li расположены в порядке возрастания их радиусов 1. N, O, F, B, Li, K 2. F, B, N, O, Li, K 3. F, O, N, B, Li, K 4. K, Li, B, N, O, F Ответ: 3 Правильно!
Вопрос: Элемент, у которого на третьем р-подуровне 2 неспаренных электрона, находится в 1. Ш периоде IVА группе 2. IV периоде IVB группе 3. V периоде IVА группе 4. III периоде IVВ группе 5. V периоде IVВ группе Ответ: 1 Правильно!
Вопрос: Электронная формула____соответствует атому в стационарном состоянии 1. …2p63s23p33d1 2. …2p63s13p33d2 3. …2p63s13p33d3 4. …2p63s13p4 5. …2p63s23p4 Ответ: 5 Правильно!
Вопрос: Образование связей описывается sp2-гибридизацией в молекуле 1. C2H4 2. CH4 3. PH3 4. H2S 5. CO2 Ответ: 4 Неправильно!
Вопрос: Сумма коэффициентов правой части уравнения MnSO4 + KClO3 + KOH → MnO42- + Cl- равна 1. 17 2. 14 3. 31 4. 12 5. 24 Ответ: 4 Неправильно!
Вопрос: В качестве катода при никелевом аноде следует взять_______, чтобы ЭДС гальванического элемента была наибольшей 1. олово 2. медь 3. свинец 4. серебро 5. цинк Ответ: 5 Неправильно!
Вопрос: При электролизе водного раствора ________в прианодном пространстве рН < 7 1. Na2S 2. K3PO4 3. NaCl 4. KBr 5. NaI Ответ: 2 Правильно!
Вопрос: Координационная формула хлорида дихлоротетрааквахрома (III): 1. [Cr(H2O)4]Cl3 2. Cr(H2O)2Cl2]Cl 3. [Cr(H2O)4Cl2]Cl 4. [Cr(H2O)3Cl3] 5. [Cr(H2O)6]Cl3 Ответ: 3 Правильно!
Вопрос: Эффект рассеяния света характеризует 1. грубодисперсные гетерогенные системы 2. высокодисперсные гетерогенные системы 3. гомогенные системы 4. окрашенные истинные растворы Ответ: 2 Правильно!
Вопрос: Мицеллы иодида серебра {m[AgI]nI-(n-x)K+}x-хK+ образуются при сливании равных объемов растворов AgNO3 и KI при условии, что концентрация раствора нитрата серебра ________ концентрации иодида калия 1. больше 2. равна 3. меньше 4. значительно ниже Ответ: 1 Неправильно!
тест "Классификация неорганических соединений для МП,ЭКТ, ЭТМО"
Вопрос: Укажите формулы амфотерных оксидов 1. ZnO 2. Na2O 3. Al2O3 4. CO2 5. N2O Ответ: 1,3 Правильно!
Вопрос: Укажите формулу кислотного гидроксида 1. HCl 2. HBr 3. H2ZnO2 4. HNO3 5. Mg(OH)2 Ответ: 4 Правильно!
Вопрос: Укажите оксид, реагирующий с CaO 1. Na2O 2. MgO 3. BaO 4. SiO2 5. SiO Ответ: 4 Правильно!
Вопрос: Укажите формулу сероводородной кислоты. 1. H2SO3 2. H2S2O7 3. H2S 4. H2SO4 5. H2S2O3 Ответ: 3 Правильно!
Вопрос: Укажите название солей азотной кислоты. 1. нитриты 2. нитриды 3. нитраты 4. азиды 5. амиды Ответ: 3 Правильно!
Вопрос: Укажите схему суммарной диссоциации серной кислоты. 1. H2SO4 ⇄ 2H+ + SO42- 2. H2SO3 ⇄ 2H+ + SO32- 3. H2S ⇄ 2H+ + S2- 4. H2SO4 ⇄ H+ + HSO4- 5. H2SO3 ⇄ H+ + SO3- Ответ: 1 Правильно!
Вопрос: Укажите вещество, при добавлении которого уменьшается диссоциация селенистой кислоты. 1. H2SO4 2. NaOH 3. Na2SO4 4. H2O 5. NaCl Ответ: 5 Неправильно!
Вопрос: Укажите группу формул, соответствующих следующим солям: сульфит бария; сульфид натрия; сульфат кальция. 1. BaSO4; Na2SO3; CaS 2. BaSO3; Na2S; CaSO4 3. BaSO3; Na2SO3; CaSO4 4. BaS; Na2SO4; CaSO3 5. BaS; Na2SO4; CaSO3 Ответ: 2 Правильно!
Вопрос:
Укажите
формулу тиосерной
кислоты
1.  2.
2. 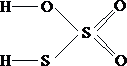 3.
3. 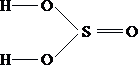 4.
4. 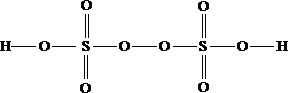 5.
5. 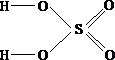 Ответ: 2
Правильно!
Ответ: 2
Правильно!
Вопрос: Укажите формулу средней (нормальной) соли 1. K2Cr2O7 2. KАl(SO4)2 3. CrOHSO4 4. Cr(HSO4)3 5. CaClBr Ответ: 1 Правильно!
Вопрос: Укажите формулу кислой соли 1. K2Cr2O7 2. KАl(SO4)2 3. CrOHSO4 4. Cr(HSO4)3 5. CaClBr Ответ: 4 Правильно!
Вопрос: Укажите формулу основной соли 1. [Ag(NH3)2]Cl 2. [Al(OH)2]2SO4 3. Na2CrO4 4. Mg(HSe)2 5. KAl(SO4)2 Ответ: 2 Правильно!
Вопрос:
Укажите
реакцию, в результате которой можно
получить основную
соль
1. ![]() 2.
2. ![]() 3.
3. ![]() 4.
4. ![]() 5.
H2SO4 +
NaOH →
Ответ: 2
Неправильно!
5.
H2SO4 +
NaOH →
Ответ: 2
Неправильно!
Вопрос:
Укажите
реакции, в результате которых можно
получить кислые соли
1. ![]() 2.
2. ![]() 3.
Al(OH)3 +
KOH →
4.
3.
Al(OH)3 +
KOH →
4. ![]() Ответ: 1
Неправильно!
Ответ: 1
Неправильно!
Вопрос: Укажите формулу дигидрофосфата калия 1. K2HPO4 2. K2HPO3 3. KH2PO4 4. KPO3 5. KH2PO3 Ответ: 3 Правильно!
Вопрос: Для последовательного осуществления превращений по схеме SO2 → H2SO3 → BaSO3 → Ba(OH)2 → Ba(H2PO4)2 необходимы вещества ____ 1. H2SO4; H2O; SO3; H3PO4 2. H2;KOH; ВaCl2;H3PO4(недостаток.) 3. H2О; ВаO; NaOH;H3PO4(избыток.) 4. SO3;О2; КОН; H3PO4(избыток.) Ответ: 3 Правильно!
Вопрос: С помощью какого реагента можно отличить в растворах KNO3 и NH4NO3 1. HNO3 2. K2SO4 3. AgNO3 4. NaOH 5. H2SO4 Ответ: 1 Неправильно!
тест "Способы выражения концентрации растворов"
Вопрос: Сколько граммов серной кислоты нужно взять для приготовления 2 л 0,2 н.раствора? 1. 39,2 г 2. 1,96 г 3. 3,92 г 4. 19,6 г 5. 9,8 г Ответ: 4 Правильно!
Вопрос: Сколько граммов хлорида алюминия содержится в 2 л 0,5 н. раствора? 1. 133,5 г 2. 44,5 г 3. 22,5 г 4. 66,75 г 5. 11,25 г Ответ: 4 Неправильно!
Вопрос: Определить процентную концентрацию раствора азотной кислоты, полученного путем прибавления 1 л воды к 100 мл 94% раствора плотностью 1,5 г/мл. 1. 12,26% 2. 1,22% 3. 0,854% 4. 8,54% 5. 12,81% Ответ: 1 Правильно!
Вопрос: Сколько граммов 2 н. раствора хлорида натрия (ρ = 1,4 г/мл) необходимо для приготовления 200 г 5,85% раствора? 1. 280 г 2. 70 г 3. 100 г 4. 50 г 5. 140 г Ответ: 4 Неправильно!
Вопрос: Определить объем 4 н. раствора гидроксида натрия, необходимый для нейтрализации 20 мл 2М раствора серной кислоты. 1. 20 мл 2. 10 мл 3. 40 мл 4. 60 мл 5. 25 мл Ответ: 1 Правильно!
тест "Гидролиз"
Вопрос: Сульфат натрия при растворении в воде 1. гидролизуется по катиону 2. гидролизуется по аниону 3. гидролизуется по катиону и аниону 4. не гидролизуется Ответ: 4 Правильно!
Вопрос: Сульфит натрия при растворении в воде 1. гидролизуется по одной ступени 2. гидролизуется по первой ступени 3. гидролизуется необратимо 4. не гидролизуется Ответ: 3 Неправильно!
Вопрос: Сульфат натрия при растворении в воде образует 1. основание и кислоту 2. кислую соль и основание 3. основную соль и кислоту 4. не гидролизуется Ответ: 4 Правильно!
Вопрос: рН среды в растворе сульфида хрома (III) 1. =7 2. > 7 3. <7 4. ≥ 7 Ответ: 1 Правильно!
Вопрос: При гидролизе __________ образуется основная соль 1. K2S 2. FeCl2 3. Al2S3 4. NH4CN Ответ: 4 Неправильно!
Вопрос: pH наименьшее в растворе соли _____ при равной концентрации всех солей (KHF = 1·10-4; KHClO = 3·10-8; KHCN = 5·10-10; KCH3COOH = 2·10-5). 1. NH4F 2. NH4ClO 3. CH3COONH4 4. NH4CN Ответ: 3 Неправильно!
Вопрос: Степень гидролиза нитрита калия в 0,1М растворе равна __, если KHNO2 = 5·10-4. 1. 4,6·10-7 2. 3,7·10-1 3. 2,3·10-3 4. 1,4·10-5 Ответ: 4 Правильно!
Вопрос: Уравнение: Al3+ + HOH ⇔ AlOH2+ + H+ относится к гидролизу соли_____ 1. AlCl3 2. AlOHCl2 3. Al2(CO3)3 4. Al2S3 Ответ: 1 Правильно!
Вопрос: В растворе соли _____ рН < 7 1. Na2CO3 2. Na2SO4 3. FeCl3 4. CH3COONa Ответ: 1 Неправильно!
Вопрос: Добавление _________ к раствору CuSO4 приводит к ослаблению гидролиза 1. Na2CO3 2. Na2SO4 3. NaCN 4. CrCl3 Ответ: 2 Неправильно!
тест "Строение атома"
Вопрос: Укажите количество энергетических состояний на f-подуровне четвертого уровня: 1. 3 2. 5 3. 6 4. 7 5. 14 Ответ: 5 Неправильно!
Вопрос: Укажите емкость р- и d- подуровней пятого энергетического уровня: 1. 2 и 6 2. 6 и 10 3. 2 и 14 4. 1 и 7 5. 6 и 14 Ответ: 2 Правильно!
Вопрос: Укажите последовательность заполнения следующих подуровней 3p 3d 4s 4p 4d 5s: 1. 3p 4d 4s 3d 4p 5s 2. 4s 3p 3d 4p 4d 5s 3. 3p 3d 4s 4p 4d 5s 4. 3p 4s 3d 4p 5s 4d 5. 3p 4s 4p 3d 5s 4d Ответ: 3 Неправильно!
Вопрос: Укажите электронную формулу, соответствующую атому в возбужденном состоянии: 1. 1s22s22p2 2. …3s23p33d1 3. …4s23d104p3 4. …4s23d5 5. …6s25d14f7 Ответ: 4 Неправильно!
Вопрос: Укажите положение ( № группы, подгруппу и № периода) в таблице Д.И.Менделеева элемента , у которого на 5р-подуровне есть 2 неспаренных электрона: 1. Ш период VА группа 2. IV период IVB группа 3. V период IVА группа 4. III период IVВ группа 5. V период IVB группа Ответ: 5 Неправильно!
тест "Строение атома"
Вопрос: Укажите количество орбиталей d-подуровня четвертого энергетического уровня: 1. 6 2. 10 3. 5 4. 32 5. 4 Ответ: 3 Правильно!
Вопрос: Укажите емкость третьего уровня: 1. 10 2. 8 3. 18 4. 32 5. 14 Ответ: 1 Неправильно!
Вопрос: Укажите последовательность заполнения следующих подуровней 4d 5s 5p 5d 5f 6s 6p: 1. 4d 5s 5p 5d 5f 6s 6p 2. 5s 4d 5p 5d 6s 5f 6p 3. 5s 4d 5p 5d 6s 6p 5f 4. 5s 4d 5p 6s 5d 6p 5f 5. 4d 5s 5p 5d 6s 5f 6p Ответ: 4 Правильно!
Вопрос: Укажите электронную формулу, соответствующую атому в стационарном состоянии: 1. …3s23p43d2 2. …3s23p64s1 3. …2s12p1 4. …4s23d104p34d1 5. …4s13d104p2 Ответ: 1 Неправильно!
Вопрос: Укажите положение ( № группы, подгруппу и № периода) в таблице Д.И.Менделеева элемента электронный паспорт которого заканчивается на ....4s2 1. Ш период IVА группа 2. IV период IVB группа 3. IV период IIА группа 4. III период IVВ группа 5. V период IVВ группа Ответ: 3 Правильно!
тест "Классификация неорганических соединений для МП,ЭКТ, ЭТМО"
Вопрос: Укажите формулы амфотерных оксидов 1. ZnO 2. Na2O 3. Al2O3 4. CO2 5. N2O Ответ: 2,3,1 Неправильно!
Вопрос: Укажите формулу кислотного гидроксида 1. HCrO2 2. H3FeO3 3. H2SO4 4. H2ZnO2 5. HF Ответ: 3 Правильно!
Вопрос: Укажите оксид, реагирующий с Al2O3. 1. N2O 2. Na2O 3. SiO 4. NO 5. CO Ответ: 3 Неправильно!
Вопрос: Укажите формулу азотной кислоты. 1. NH3 2. HNO2 3. HNO3 4. N2Н4 5. HN3 Ответ: 3 Правильно!
Вопрос: Укажите название солей сероводородной кислоты. 1. сульфаты 2. пиросульфаты 3. сульфиты 4. сульфиды 5. тиосульфаты Ответ: 4 Правильно!
Вопрос: Укажите схему суммарной диссоциации гидроксида фосфора (V). 1. H3PO4 ⇄ 3H+ + PO43- 2. H3PO4 ⇄ H+ + H2PO4- 3. H4P2O7 ⇄ 4H+ + P2O74- 4. H3PO3 ⇄ 3H+ + PO33- 5. HPO3 ⇄ H+ + PO3- Ответ: 1 Правильно!
