
Масс-спектрометрия анализа объектов окружающей среды 2013
.pdf
Введение 27
для замеров на «кухне», например для проверки качества пищевых продуктов, простых экологических тестов или контроля здоровья.
С главы 10 начинается блок, посвященный наиболее значимым типам загрязнений окружающей среды. Метод индуктивно связанной плазмы с масс-спектрометрическим детектированием (ИСП МС) является наиболее быстрым и информативным для качественного и количественного определения химических элементов в пробах. Менее минуты достаточно для того, чтобы получить надежную информацию о наличии и уровнях большинства химических элементов таблицы Д. И. Менделеева. Поскольку диапазон линейности метода достигает 12 порядков, за один ввод пробы можно получить информацию и о макроэлементах, и об элементах, присутствующих в ультраследовых количествах. Этому замечательному методу посвящена глава 10.
Достаточно большая группа химических соединений в объектах окружающей среды объединяется термином «летучие». Это связано исключительно с низкой величиной давления их паров. В эту группу входят самые разнообразные органические вещества. Опасность соединений этой группы для человека и экосистемы в целом лежит в широком диапазоне, а их присутствие должно контролироваться в атмосфере, воде, других образцах и продуктах. Масс-спектрометрическому анализу таких соединений, которые можно разделить на антропогенные и биогенные, посвящена глава 11.
Побочные продукты дезинфекции, возникающие при подготовке питьевой воды, а также при эксплуатации плавательных бассейнов и утилизации отходов, представляют собой серьезную экологическую проблему, нанося существенный вред здоровью человека. Не существует лучшего метода качественного и количественного определения этих соединений, чем масс-спектрометрия. Об этом повествуется в главе 12.
Глава 13 посвящена опасным современным экотоксикантам: фармацевтическим препаратам, наночастицам, металлоорганическим соединениям. Набор этих ксенобиотиков неуклонно возрастает год от года с появлением новых продуктов, часто не самых экологичных. И вновь следует сказать, что для их детектирования не существует более эффективного метода, чем масс-спектрометрия.
Пестициды всегда считались приоритетными загрязняющими веществами. Различные варианты ГХ/МС или ЖХ/МС показали свою эффективность в определении этих экотоксикантов в объектах окружающей среды. Тем не менее в связи с широчайшим разнообразием структур и наличием очень жестких требований по чувствительности и надежности определение пестицидов продвинутыми хроматомасс-спектроме- трическими методами представлено в главе 14.
Масс-спектрометрия является единственным аналитическим методом, способным надежно определять суперэкотоксиканты: полихлорированные дибензодиоксины и дибензофураны. Благодаря своей высочайшей токсичности и стабильности эти ксенобиотики должны контролироваться на постоянной основе. Более 30 лет им уделяется особое внимание. Ежегодный представительный научный форум посвящен исключительно этим соединениям. Детали масс-спектрометрического определения этих веществ представлены в главе 15.
Загрязнение атмосферы является важным аспектом химии окружающей среды. Глава 16 названа «Масс-спектрометрия атмосферных аэрозолей». Уникальные результаты, включая анализ единичных частиц, наглядно демонстрируют преимущество масс-спектрометрии перед другими аналитическими методами в подобных анализах.

28 Введение
Что происходит, когда загрязняющее вещество попадает в организм человека? Возможность масс-спектрометрического изучения взаимодействия экотоксикантов с ДНК является предметом главы 17. Чрезвычайная сложность задачи требует высочайшей чувствительности метода и возможности работать как с целевыми, так и нецелевыми аддуктами ксенобиотиков с биомолекулами.
В четырех последних главах рассматриваются масс-спектрометрические подходы, которые привели к созданию новых направлений научных исследований. В частности, появилась возможность прямого анализа состава самых сложных смесей природных соединений. Сверхвысокая разрешающая способность масс-спектрометрии с преобразованием Фурье позволяет идентифицировать и оценить уровни тысяч индивидуальных родственных природных соединений без какого-либо предварительного разделения. Главы 18 и 19 знакомят читателя с новейшими дисциплинами: петролеомикой и гуминомикой.
Масс-спектрометрия изображений (имиджинг) — еще одно уникальное научное направление, возникшее в самом конце XX века. Этот удивительный метод позволяет детектировать и картировать распределение тысяч самых разнообразных соединений в органах и тканях животных и растений, в минералах, овощах и фруктах, произведениях искусства. Стало возможным устанавливать распределение экотоксиканта, лекарственного препарата или его метаболитов в целом организме лабораторного животного или определять, какие белки и где конкретно генерируются организмом в качестве отклика на проникновение чужеродного вещества в организм. Эти аспекты рассматриваются в главе 20.
Глава 21 посвящена изотопной масс-спектрометрии — красивому методу, базирующемуся на существовании природных изотопов химических элементов. Соотношение этих изотопов зависит от происхождения образца. Измерив отношения D/H или 13C/12C, можно делать выводы о подлинности произведений искусства, определять, на каком заводе синтезировано данное вещество, устанавливать, природным или синтетическим является полезный ингредиент (аскорбиновая или лимонная кислота) в соках и напитках. Этот мощный метод полезен в криминалистике (анализ наркотиков) и в допингконтроле (различие между эндогенными и синтетическими стероидами).
Таким образом, я надеюсь, что читатель не только обнаружит в этой книге много полезной для своей будущей работы информации, но и просто получит удовольствие, знакомясь с фантастическими возможностями современной экологической масс-спектрометрии.
Литература
[1].Cooks R. G., Ifa D. R., Sharma G., Tadjimukhamedov F. Kh., Ouyang Zh. (2010). «Persrectives and retrospectives in mass spectrometry: one view». European Journal of Mass Spectrometry, 16, 3: 283—300.
[2].Kluge H.-Jurgen (2010). «High accuracy mass spectrometry for fundamental studies». European Journal of Mass Spectrometry, 16, 3: 269—282
ГЛАВА 1
ОСНОВНЫЕ ПРИНЦИПЫ МАСС-СПЕКТРОМЕТРИИ
Альберт Лебедев
1.1. Базовые аспекты
Для того чтобы получить масс-спектр, необходимо ввести образец в ионный источник масс-спектрометра, ионизировать молекулы (получить положительные или отрицательные ионы), разделить эти ионы по величинам m/z (отношение их массы к заряду) и установить число ионов с каждым m/z. Компьютер управляет всеми процессами и проводит обработку данных. Принципиальная схема масс-спектрометра представлена на рис. 1.1. Дополнительные узлы могут добавляться для решения более сложных задач.
Таким образом, масс-спектрометрия является аналитическим методом, оперирующим заряженными атомами и молекулами химических соединений. Принципиальным моментом является ионизация молекул образца или перевод ионов, уже имеющихся в растворе или в твердой матрице, в газовую фазу. Отношение массы к заряду (m/z) ионов может быть точно измерено, что позволяет установить молекулярные массы ингредиентов образца. Можно также инициировать фрагментацию исходных молекулярных ионов с получением набора фрагментных ионов. Эти ионы представляют собой наиболее стабильные фрагменты исходной молекулы и позволяют делать выводы о ее структуре. Интенсивности и величины m/z молекулярного и фрагментных ионов на графике по осям y и x соответственно называются масс-спектром. Обычно график нормализуется на 100 % по наиболее интенсивному пику в спектре. Масс-спектр — уникальная характеристика химического вещества. Для работы с масс-спектром необходимы только атомные массы химических элементов, точнее природных изотопов этих элементов. Поскольку атомные и молекулярные массы — простые и широко используемые характеристики, масс-спектры значительно проще для интерпретации, чем ЯМР, ИК, УФ, ЭПР и другие типы спектров.
ввод |
|
ионизация |
|
разделение |
|
детекти- |
|
обработка |
|
масс- |
|||||||||
|
|
|
рование |
|
данных |
|
спектр |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
компьютер
Рис. 1.1. Принципиальная схема масс-спектрометра

30 Глава 1. Основные принципы масс-спектрометрии
Интенсивность
9000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
105 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6000 |
|
|
|
|
|
|
|
|
|
77 |
|
|
|
|
|
|
|
|
|
||
5000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2000 |
|
|
|
|
|
51 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1000 |
|
27 |
|
38 |
|
|
62 |
|
|
|
|
85 |
|
|
122 |
|
140 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
0 |
|
|
|
|
|
|
|
|
|
111 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
110 |
120 |
130 |
140 |
150 |
||||||||
m/z
Рис. 1.2. Спектр электронной ионизации бензоилхлорида (NIST 27422)
Существуют определенные правила, определяющие направления фрагментации химических соединений в масс-спектрометре. Поэтому на основе масс-спектра можно установить молекулярную массу, элементный состав, присутствие определенных функциональных групп, а зачастую и полную структуру аналита. Во многих случаях уже новичок может успешно решать задачи даже без использования спектральных баз данных и специального программного обеспечения.
Спектр электронной ионизации бензоилхлорида в классической графической форме представлен на рис. 1.2. Абсцисса соответствует массам ионов (точнее величинам m/z), а ордината — относительным интенсивностям пиков этих ионов. Для новичка проще принимать во внимание только наиболее интенсивные пики в спектре. Менее интенсивные пики, следующие сразу за интенсивными, обусловлены наличием в составе молекул образца природных стабильных изотопов. Они играют важную роль при установлении структуры и далее будут обсуждаться подробнее.
Пик иона с самой большой массой соответствует молекулярному иону аналита. В спектре на рис. 1.2 — это 140. Следует также обратить внимание на ион с m/z 142, интенсивность пика которого составляет 1/3 от интенсивности пика иона с m/z 140. Эти два пика обусловлены существованием двух природных изотопов хлора: 35Cl и 37Cl. Их природное соотношение ~ 3 : 1. Первичный фрагментный ион с m/z 105 образуется при потере 35 единиц массы из молекулярного иона с m/z 140 или 37 единиц мас-
I/%
100 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
237 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
90 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
80 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
295 |
|
|
|
70 |
|
|
|
|
|
|
|
|
|
|
|
208 |
|
|
|
|
|
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
266 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
324 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
40 |
60 |
80 |
100 |
120 |
140 |
160 |
180 |
200 |
|
220 |
240 |
260 |
|
280 |
300 |
320 |
|||||||
m/z
Рис. 1.3. Спектр электронной ионизации тетраэтилсвинца (NIST45993)
1.1. Базовые аспекты |
31 |
сы из изотопного иона с m/z 142. Оба выброса обусловлены атомами хлора (35Cl и 37Cl). Первичный ион с m/z 105 теряет молекулу CO с образованием вторичного фрагментного иона (m/z 77), который, однако, может образоваться и напрямую из молекулярного иона при разрыве связи С-С. Даже человек с минимальным опытом работы по расшифровке масс-спектров знает, что ион с m/z 77 может считаться визитной карточкой фенильной группы (C6H5+). Это стабильный в газовой фазе ион, который указывает на ароматическую природу аналита. Продукт следующей стадии фрагментации, ион с m/z 51, образуется при отщеплении из фенил-катиона молекулы ацетилена (C2H2). Измерение точной массы (см. ниже) может надежно подтвердить сделанные выводы, поскольку дает возможность установить элементный состав всех упомянутых выше ионов.
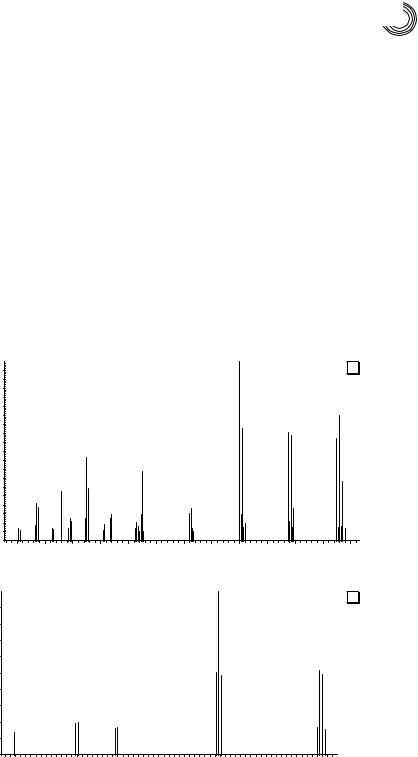
Существование природных изотопов химических элементов облегчает установление структуры и позволяет определить элементный состав анализируемого соединения по его масс-спектру. На рис. 1.3 представлен хороший пример простоты и информативности масс-спектра, демонстрирующий важность учета изотопных пиков. Три основных природных изотопа свинца имеют атомные массы 206, 207 и 208 единиц с распространенностью 25,15 %, 21,11 % и 52,38 % (грубо 1 : 1 : 2) соответственно. Тетраэтилсвинец — топливная добавка. Будучи хорошо известным экотоксикантом, он запрещен в на-
Интенсивность
9500 |
|
|
220 |
a |
9000 |
|
|
|
|
8500 |
|
|
|
|
8000 |
|
|
|
|
7500 |
|
|
|
292 |
7000 |
|
|
|
|
6500 |
|
|
|
|
6000 |
|
|
|
|
5500 |
|
110 |
|
|
5000 |
|
|
|
|
4500 |
|
|
150 |
|
4000 |
|
|
|
|
3500 |
|
92 |
|
|
3000 |
|
|
|
|
2500 |
74 |
|
185 |
|
2000 |
|
128 |
|
|
1500 |
61 |
|
|
|
1000 |
|
|
|
|
500 |
|
|
|
|
0 |
|
|
|
|
60 |
80 |
100 |
120 |
140 |
160 |
180 |
200 |
220 |
240 |
260 |
280 |
300 |
|
|
|
|
|
|
m/z |
|
|
|
|
|
|
Интенсивность
9000 |
|
|
191 |
б |
|
|
|
|
|
8000 |
|
|
|
|
7000 |
|
|
|
|
6000 |
|
|
|
270 |
5000 |
|
|
|
|
|
|
|
|
|
4000 |
|
|
|
|
3000 |
|
81 |
|
|
2000 |
31 |
112 |
|
|
|
|
|||
1000 |
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
40 |
60 |
80 |
100 |
120 |
140 |
160 |
180 |
200 |
220 |
240 |
260 |
|
|
|
|
|
m/z |
|
|
|
|
|
|
Рис. 1.4. Масс-спектры электронной ионизации тетрахлорбифенила NIST 169679 (верх) и трибромфосфина NIST 150824 (низ)

32 Глава 1. Основные принципы масс-спектрометрии
стоящее время в подавляющем большинстве стран. В области высоких масс, начиная с m/z 324, в спектре отчетливо видны 5 триплетов (иногда искаженные) с соотношением интенсивностей 1 : 1 : 2 и отстоящих друг от друга на 29 единиц массы. Эти группы ионов обусловлены последовательными выбросами четырех этильных групп из молекулярного иона Pb(C2H5)4. Детали работы с изотопными пиками представлены в (Lebedev, 2009; Лебедев, 2003).
Хлор и бром часто присутствуют в молекулах приоритетных загрязняющих веществ (пестициды, фармацевтические препараты, побочные продукты дезинфекции, антипирены). Благодаря уникальному соотношению природных изотопов (35Cl:37Cl ~ 3:1; 79Br:81Br ~ 1:1) присутствие этих элементов в анализируемых образцах может быть моментально установлено по масс-спектру. Для этого надо обращать внимание на мультиплеты, пики в которых отстоят друг от друга на две единицы массы. Число атомов этих элементов в молекуле также однозначно определяется по изотопной картинке. Так, два атома хлора в молекуле дадут изотопный кластер (триплет) с относительными интенсивностями (3: 1)2 = 9:6:1; три атома — (3:1)3 = 27:27:9:1 и т.д. Вид мультиплетов ионов в зависимости от числа атомов хлора и брома в молекуле представлен на рис. 12.9 в главе 12. Примеры масс-спектров экологически важных тетрахлорбифенила и трибромфосфина представлены на рис. 1.4. Последовательные выбросы атомов хлора и брома с образованием характеристических изотопных кластеров ионов позволяют легко идентифицировать эти токсиканты. Спектр трибромфосфина особенно прост, поскольку последовательное элиминирование трех атомов брома приводит к иону атомарного фосфора с m/z 31. При этом дублет с m/z 79 и 81 определяется двумя стабильными изотопами брома.
1.2. Ввод образца
Любой масс-спектрометрический эксперимент начинается с ввода образца в прибор. На этой стадии наиболее серьезная проблема связана с тем, что большинство приборов функционирует в условиях глубокого вакуума (10–5—10–6 торр). Существует несколько подходов: прямой ввод, ввод через полупроницаемую мембрану, интерфейсы с многочисленными хроматографами (ГХ, ВЭЖХ, СКФХ, КЭ) и даже самостоятельное натекание молекул или ионов из атмосферы в прибор, работающий в условиях пониженного давления. Последний вариант будет детально рассматриваться в последующих главах, посвященных миниатюризации и современным методам анализа без пробоподготовки (главы 7—9).
В случае прямого ввода жидкий или твердый образец направляется в ионный источник через вакуумный шлюз. Поскольку обычное давление в источнике 10–5—10–6 мм рт. ст., а образец может быть нагрет до 400 °C и более, значительное число органических соединений может быть переведено в газовую фазу и проанализировано. Однако, если образец представляет собой смесь соединений с близкими летучестями, зарегистрированный масс-спектр будет представлять собой суперпозицию спектров компонентов. Этот факт может существенно усложнить процесс идентификации, причем как компьютеризованный, так и производимый вручную.
Полупроницаемые мембраны могут с успехом применяться в экологическом мониторинге. Например, пусть вода протекает по трубке из полимерного материала.

1.3. Ионизация |
33 |
He
|
Источникионов |
|
Мембрана |
Выход |
Вход |
|
Рис. 1.5. Вариант мембранного ввода с положением мембраны вне источника ионов
При этом липофильные соединения могут адсорбироваться на поверхности такого материала, просачиваясь через тонкие стенки. С наружной стороны они попадают в поток инертного газа, доставляющего их непосредственно в ионный источник, где и происходит их детектирование. Подобные устройства успешно используются в онлайн-ре- жиме для определения конкретных соединений в реках, промышленных сбросах и т. д. (глава 9). Аналогичные системы используются для детектирования целевых соединений в биологических жидкостях. К сожалению, метод не универсален и должен несколько модифицироваться для каждого нового аналита. Вариант мембранного ввода представлен на рис. 1.5.
Наиболее популярными являются системы ввода в виде различных интерфейсов между блоком разделения (хроматографы) и масс-спектрометром. Несколько глав (2, 3, 6) посвящены подробному изложению вариантов такого комбинированного метода — хроматомасс-спектрометрии.
1.3. Ионизация
Масс-спектрометрия регистрирует исключительно заряженные частицы. Ни молекулы, ни радикалы не могут быть исследованы в своей исходной нейтральной форме. Следовательно, молекулы образца должны быть ионизированы. Альтернативно ионы целевого вещества, уже существующие в конденсированной фазе, могут быть каким-либо образом переведены в газовую фазу. За столетнюю историю масс-спектрометрии описано несколько десятков методов ионизации, причем следует отметить, что значительное число новых атмосферных методов были предложены совсем недавно, уже в XXI веке. Частота использования того или иного метода с годами изменяется. Одни из них продолжают играть важную роль в современных исследованиях, другие уже прошли свой «золотой период» и заменены более эффективными.
Все существующие методы могут быть грубо разделены на две группы: «мягкие» и «жесткие». Это разделение основано на величине избытка внутренней энергии в образующемся молекулярном ионе. Если эта величина мала, фрагментация незначительна и ион регистрируется как молекулярный. Такой процесс называется «мягкой ионизацией». Определенный избыток внутренней энергии запускает процесс разрыва конкретных химических связей в исходном молекулярном ионе, приводя к появлению различных фрагментных ионов. Иногда молекулярный ион вообще не удается зареги-

34 Глава 1. Основные принципы масс-спектрометрии
стрировать. Подобный процесс называется «жесткой» ионизацией. Оба варианта полезны. Первый дает информацию о молекулярной массе соединения и его элементном составе (масс-спектрометрия высокого разрешения), второй позволяет получить структурную информацию благодаря массам фрагментных ионов.
В этой главе будут рассмотрены только наиболее значимые для экологической массспектрометрии методы ионизации. Несколько новых методов описаны в главах 7 и 8. Для дополнительной информации может быть рекомендована книга (Westman-Brink- malm and Brinkmalm, 2009) и литература, процитированная в ней.
1.3.1. Электронная ионизация
Электронная ионизация (традиционно называвшаяся «электронным ударом»), предложенная Демпстером еще в 1921 году (Dempster, 1921), исторически была первым и до сих пор остается одним из наиболее востребованных методов ионизации. Она особенно важна для масс-спектрометрии образцов объектов окружающей среды. В процессе электронной ионизации (ИЭ) газообразные молекулы образца должны оказаться в ионном источнике, функционирующем в условиях высокого вакуума (10–5—10–6 мм рт. ст.). Испускаемые катодом электроны, пролетая через ионный источник к противоэлектроду, взаимодействуют с этими молекулами. В результате собственные электроны молекул переходят на более высокие орбитали или совсем покидают молекулу с образованием ионов. Процесс может быть представлен следующим уравнением:
M + ē = M+• + 2 ē. |
(1.1) |
Теряя электрон, молекула превращается в катион-радикал. Более 95 % образующихся ионов однозарядные, хотя образуются двух- и даже многозарядные ионы. Их количество зависит от природы молекул образца. Стандартная энергия ионизирующих электронов — 70 эВ, что близко к максимуму сечения ионизации для большинства органических молекул. Внутренняя энергия образующихся молекулярных ионов лежит в диапазоне от 0 до 20 эВ, приводя к интенсивной фрагментации. В условиях высокого вакуума отсутствуют ионно-молекулярные взаимодействия, т. е. перераспределение энергии между частицами за счет их столкновений отсутствует. В результате образовавшиеся молекулярные ионы ведут себя далее исключительно в зависимости от приобретенной в процессе ионизации внутренней энергии. Определенный избыток этой энергии запускает соответствующий процесс фрагментации. Поскольку статистически в результате ионизации образуются миллиарды и триллионы молекулярных ионов с очень широким диапазоном внутренней энергии, активируются все возможные пути фрагментации. Поэтому спектры электронной ионизации предоставляют богатую структурную информацию и характеризуются высокой воспроизводимостью независимо от типа масс-спектрометра. Последняя особенность позволила создать и эффективно использовать библиотеки масс-спектров (глава 5).
Электронная ионизация — это универсальный метод, позволяющий исследовать разные классы химических соединений. Однако у него есть существенный недостаток, связанный с необходимостью перевода молекул образца в газовую фазу. Именно поэтому метод непригоден для полярных, термолабильных и тяжелых молекул. Тем не менее электронная ионизация прекрасно справляется с анализом подавляющего большинства экологически значимых соединений в самых разных матрицах.

1.3. Ионизация |
35 |
Хотя в процессе ионизации электронами образуются и отрицательные ионы, их выходы существенно ниже, что лимитирует использование этого режима на практике.
1.3.2.Химическая ионизация
В1966 г. Мансон и Филд описали «мягкий» метод ионизации (Munson and Field, 1966), названный химической ионизацией (ХИ, chemical ionization, CI). Поскольку внутренняя энергия образующихся в результате ХИ ионов обычно ниже 5 эВ, фрагментация практически отсутствует. Иногда в спектре наблюдается исключительно пик молекулярного иона. Наиболее полное описание процессов ХИ можно найти в книге А. Гаррисона (Harrison, 1992).
Основное различие между ИЭ и ХИ связано со значительно более высоким давлением в источнике (~1 мм рт. ст.) во втором случае. Это давление достигается введением так называемого газа-реагента, в качестве которого можно использовать практически любое вещество (воду, аммиак, метан, бензол, гелий, этилендиамин и т. д.). Взаимодействие молекул газа-реагента с электронами высокой энергии (200—500 эВ) приводит
кионизации. Благодаря высокому давлению образующиеся молекулярные ионы взаимодействуют с нейтральными молекулами. В результате самых разнообразных ион- но-молекулярных реакций создается газовая плазма, существующая в динамическом равновесии. Наиболее распространенные и реакционноспособные ионы в этой плазме называются ионами-реагентами. Это могут быть молекулярные, фрагментные ионы или ионы — продукты реакций исходных молекул газа-реагента. Уравнения (1.2) дают представление о некоторых основных процессах в случае химической ионизации мета-
ном. Два иона (CH5+ — 44 % и C2H5+ — 30 %) являются доминирующими ионами-реаген- тами в образующейся плазме.
CH → CH |
+•, CH +, CH +• |
… |
|||||||||
|
4 |
4 |
|
3 |
|
|
2 |
|
|
|
|
CH |
+• + CH → CH |
+ |
+ CH |
• |
|||||||
|
4 |
4 |
|
5 |
+ + H |
|
3 |
||||
CH + + CH → C |
H |
2 |
(1.2) |
||||||||
|
|
3 |
4 |
2 |
|
5 |
|
|
|
||
CH +• + CH |
→ C |
H + + H |
+ H |
||||||||
2 |
|
4 |
2 |
|
3 |
|
2 |
|
|
|
|
C |
H + + CH → C H |
+ + H |
2 |
|
|||||||
2 |
|
3 |
4 |
3 |
5 |
|
|
|
|||
Когда молекула образца вводится в ионный источник, она взаимодействует с ио- нами-реагентами. Возможны несколько типов реакций. Наиболее значимым является протонирование (перенос протона). Если сродство к протону у аналита M выше, чем у газа-реагента B (например метана в случае CH5+), протекает следующая реакция:
М + ВН+ → MH+ + B. |
(1.3) |
Необходимо подчеркнуть два момента. Во-первых, протонирование приводит к возникновению четноэлектронных катионов (протонированных молекул), которые значительно стабильнее катион-радикалов, образующихся в условиях ионизации электронами. Во-вторых, избыток внутренней энергии MH+ может быть легко вычислен по уравнению
E = СП(M) – СП(B), |
(1.4), |
где СП — сродство к протону M и B соответственно.

36 Глава 1. Основные принципы масс-спектрометрии
Таким образом могут быть генерированы протонированные молекулы аналита с известной внутренней энергией.
Помимо протонирования возможны три других важных процесса ионизации. Перенос заряда. Если молекула газа-реагента не имеет водородных атомов (напри-
мер He), образуются катион-радикалы M+• аналита.
М + X+• → M+• + X |
(1.5) |
В отличие от ИЭ их внутренняя энергия может быть легко рассчитана на основе значений энергии ионизации (ЭИ) аналита и энергии рекомбинации (ЭР) газа-реагента.
Е = ЭР(Х+•) – ЭИ(М) |
(1.6) |
Электрофильное присоединение. Если сродство к протону молекулы аналита недостаточно велико, она может сформировать с ионом-реагентом стабильный комплекс.
М + X+ → MX+ |
(1.7) |
Например, пики ионов [M + NH4]+ и [M + NO]+ весьма интенсивны в условиях ХИ аммиаком и окисью азота соответственно.
Отрыв аниона. Такой процесс протекает при взаимодействии ионов-реагентов переноса протона с аналитами с низким СП.
АВ + Х+ → AX + B+ |
(1.8) |
Наиболее распространенный пример — это образование ионов [M – H]+ в условиях химической ионизации алифатических углеводородов метаном.
В отличие от ИЭ в условиях ХИ образование отрицательных ионов может быть весьма выраженным. Четыре основных процесса образования отрицательных ионов аналита во многом напоминают процессы образования положительных ионов: перенос протона (депротонирование), перенос заряда, нуклеофильное присоединение и нуклеофильное замещение (Лебедев, 2003).
Химическая ионизация отрицательных ионов (ХИОИ, negative ion chemical ionization, NICI) — это эффективный метод анализа соединений с высоким сродством к электрону. В этом случае выигрыш в чувствительности по сравнению с режимом положительных ионов может быть весьма существенным. Хорошим примером использования ХИОИ в экологических исследованиях является качественный и количественный анализ полихлорированных соединений (глава 15).
Недостатками химической ионизации являются необходимость перевода образца в газовую фазу, слабо выраженная фрагментация и быстрое загрязнение источника ионов. Тем не менее комбинация ХИ и ИЭ может быть очень успешной, поскольку первая дает возможность зарегистрировать молекулярный ион, а вторая предоставляет исчерпывающую структурную информацию.
1.3.3. Полевая ионизация
Еще одним популярным «мягким» методом является полевая ионизация (ПИ, field ionization, FI). Само явление было открыто Е. Мюллером в 1951 году. Он создал полевой ионный микроскоп, наблюдая за появлением катионов вблизи металлической поверхности в сильном электростатическом поле (Muller, 1951). Через несколько лет источ-
