
Биохимия_Ответы
.pdf19.Принципи організації та функціонування живої матерії. Біохімічні компоненти клітини. Біохімічний склад, будова, функції біомембран. Компартменталізація
процесів у клітині.
Принципы организации живой материи:
1.Принцип молекулярной экономии – комбинация небольшого числа молекул дает бесконечное множество макромолекул. Например, миллионы белков составлены из набора в 20 аминокислот, а в состав ДНК входят в основном 4 азотистых основания.
2.Принцип простой сложности – все биомолекулы состоят из нескольких элементов – органогенов
(С, Н, О, N, S, P).
3.Принцип комплементарности – необходимость пространственного соответствия отдельных частей биомолекул при их образовании (например, для ДНК – это расположение азотистых оснований по правилам Чаргаффа), а также при взаимодействии макромолекул (например, комплексы антигенантитело, фермент-субстрат и т.д.) по типу «ключ-замок».
Принципы функционирования живой материи
1.Все реакции в живых организмах подчиняются ІІ закону термодинамики и происходят по закону действующих масс
2.Большинство реакций в живых организмах являются ферментативными, то есть протекают при участии ферментов – катализаторов белковой природы
3.Все реакции в живых организмах протекают в водной среде, в том числе и реакции окисления, при относительно невысоких температурах.
4.Энергия в организмах выделяется при окислении питательных веществ (углеводов, белков, жиров) и значительная ее часть аккумулируется в виде макроэргических связей АТФ.
Методы используемые в биохимии: химические; физические; ферментативные методы – есть только в биохимии; молекулярно-генетические и другие. Материал для биохимических исследований * кровь, моча, желудочный сок, спинномозговая жидкость, синовиальная жидкость, слюна, биоптаты органов.
Биохимические компоненты клетки. Живые организмы и клетки – самовоспроизводящиеся химические системы,требующие связи разных групп, потому основа клеточной химии -соединения углерода (способного соединятся в прочные цепи -С-С-Э, с легкими элементами, 99% занимают СНОNPS, 70% - вода), предмет органической химии, включая общие для всех четыре основных типа молекул (с группами ОН,NН2, СН3 и С=О, Мг 100-1000):
1.Сахара как пища для клеток, с формулой (СН2О)п- моно- и полисахариды, бывающие и скелетом и запасом энергии, при окислении(1У.Е)как и, из-за связи восстановления с гидрофобностью, (СН2)п-цепей,
2.Жирные кислоты - компоненты клеточных мембран, границ, в связи через остатки глицерина, с Ф- и +азотсодержащими,
3.Аминокислоты - субъединицы белков (сNН3+ и СООполюсами,источники разнообразных групп, зарядов и биоактивных веществ), 20 их кодируют(2х2)3также содержащие N+основание и Ф-
4.Нуклеотиды - субъединицы ДНК и РНК, носитель и информации и энергии-полифосфатов, способные к автокатализу и воспроизводству, основы жизни.

20. Структура і роль ДНК.
Азотистые основания ДНК обычно варьируют у разных видов организмов, однако почти не претерпевают изменений у одного и того же вида в процессе развития или в зависимости от изменений окружающей среды либо характера питания. Показано также, что ДНК, выделенная из разных тканей одного и того же вида, имеет одинаковый состав азотистых оснований. Полученные количественные соотношения были названы правилами Чаргаффа. При анализе состава очищенной ДНК, выделенной из разныхисточников, были сделаны следующие выводы:
1)молярная доля пуринов равна молярной доле пиримидинов:
А + Г = Ц + Т или (А + Г)/(Ц + Т)= 1
2)количество аденина и цитозина равно количеству гуанина и тимина:
А+ Ц = Г + Т или ( А + Ц)/(Г + Т)= 1;
3)количество аденина равно количеству тимина, а количество гуанина равно количеству цитозина: А = Т и Г = Ц;
4)существенным для характеристики вида (таксономическое значение) оказался так называемый коэффициент специфичности, отражающий отношение
(Г + Ц)/(А + Т)
структурными единицами нуклеиновых кислот являются мономерные молекулы – мононуклеотиды. Следовательно, нуклеиновые кислоты представляют собой полинуклеотиды. Это продукты полимеризации мононуклеотидов, число и последовательность расположения которых в цепях ДНК и РНК определяются в строгом соответствии с программой,заложенной в молекуле матрицы. Мононуклеотиды легко образуются при гидролизе ДНК и РНК в присутствии нуклеаз, состоят из трех специфических компонентов: азотистого основания, углевода и фосфорной кислоты. В этой триаде мононуклеотида углевод занимает среднее положение. Соединения азотистого (любого) основания и углевода(рибозы или дезоксирибозы), получившие название нуклеозидов, легко образуются из мононуклеотида при гидролитическом отщеплении фосфорной кислоты в присутствии щелочи или при участии специфических ферментов – нуклеотидаз.
Первичная структура нуклеиновых кислот
Под первичной структурой нуклеиновых кислот понимают порядок, последовательность расположения мононуклеотидов в полинуклеотидной цепиДНК и РНК. Такая цепь стабилизируется 3',5'-фосфодиэфирными связями. Поскольку молекулярная масса нуклеиновых кислот колеблется в широких пределах (от 2•104 до 1010–1011), установить первичную структуру всех известных РНК и особенно ДНК весьма сложно. Тем не менее во всех нуклеиновых кислотах (точнее, в одноцепочечной нуклеиновой кислоте) имеется один и тот же тип связи – 3',5'-фосфодиэфирная связь междусоседними нуклеотидами. Эту общую основу структуры можно представить следующим образом:
Основание |
|
Основание |
|
Основание |
Пентоза |
P |
Пентоза |
P |
Пентоза |
Установлено, что в образовании межнуклеотидной связи участвуют гидроксильные группы в 3'- и 5'- положениях остатков углевода.
Три варианта схемы нуклеотидной последовательности ДНК( рис.) В последнее время о первичной структуре ДНК (точнее, отдельных ее фрагментов) судят по ряду
косвенных данных, например, по степени сплоченности нуклеотидных звеньев в молекуле ДНК (определение сводится в конечном счете к выяснению числа и структуры отдельных фракций нуклеотидов, так называемых изоплитов), также по кинетике реассоциации ДНК (метод позволяет выяснить наличие в молекуле повторяющихся последовательностей нуклеотидов). О первичной структуре ДНК судят,кроме того, по
распределению минорных оснований (имеются данные о существовании подобной закономерности) и обнаружению в ДНК и определению последовательности палиндромов ( обратно бегущие последовательности, или перевертыши), которые обнаруживаются главным образом в местах рестрикции . Большие надежды в определении первичной структуры ДНК исследователи возлагают на физические, химические (синтез генов), генетические и другие методы, а также на методы выделения некоторых генов (или их фрагментов) из природных источников и синтеза генов на мРНК при участии фермента обратной транскриптазы.Для установления первичной структуры ДНК недавно предложен экспрессметод, включающий применение двух ДНК-полимераз (из E.coli и из
бактериофага Т4). Однако во всех этих случаях определяется структуранебольшого участка ДНК, поэтому полная расшифровка первичной структуры ДНК генома человека ждет своего решения.
Вторичная структура нуклеиновых кислот
В соответствии с моделью Дж. Уотсона и Ф. Крика, предложенной в 1953 г.на основании ряда аналитических данных, а также рентгеноструктурного анализа молекула ДНК состоит из двух цепей, образуя правовращающую спираль, в которую обе полинуклеотидные цепи закручены вокруг одной и той же оси. Удерживаются цепи благодаря водородным связям, образующимся между их азотистыми основаниями (рис. 3.1). Обе цепи полинуклеотидов в биспиральной молекуле ДНК имеют строго определенное пространственное расположение, при котором азотистые основания находятся внутри, а фосфорильные и углеводные компоненты – снаружи.
Детальный анализ всевозможных вариантов образования водородных связей между основаниями показал, что в биспиральной молекуле ДНК основания уложены парами: пурин из одной цепи и пиримидин из другой в соответствии с правилами Чаргаффа. Поскольку ориентация оснований на плоскости не является, очевидно, произвольной, и основания в полинуклеотидах представлены в лактамной форме, наиболее вероятными были признаны пары аденин–тимин и гуанин–цитозин. Этот способ спаривания получил в дальнейшем экспериментальное подтверждение. Избирательность взаимодействия пар А–
Т и Г–Ц принято выражать термином комплементарность , а соответствующие азотистые основания называют комплементарными. Стабильность А–Т оснований обеспечивается двумя водородными связями, а пар Г–Ц – тремя, что в свою очередь определяется особенностями расположения функциональных групп азотистых оснований.
Длина водородных связей между основаниями составляет около 0,3 нм. Таким образом, комплементарными оказываются не только отдельные основания, но и дезоксирибонуклеотидные цепи ДНК в целом, способствующие образованию весьма компактной структуры и стабилизации всей молекулы *.
Обе цепи в молекуле ДНК имеют противоположную полярность. Это означает, что межнуклеотидная связь в одной цепи имеет направление 5'–>3', а в другой – 3'–>5'. Подобная направленность цепей имеет важное биологическое значение при репликации и транскрипции молекулы ДНК.
На модели ДНК видно, что расстояние между витками(шаг спирали) равно 3,4 нм. На этом участке укладываются 10 нуклеотидных остатков, размер одного нуклеотида составляет 0,34 нм; диаметр биспиральной молекулы равен 1,8 нм.
Необходимо указать, что конфигурация двойной спирали ДНК сильно меняется в зависимости от количественного содержания воды и ионной силы окружающей среды. Методами рентгеноструктурного анализа доказано существование по крайней мере 6 форм ДНК, названных А-, В-, С-, D-, Е- и Z-формами. Конфигурация двух из них в простейшей форме представлена на рис. 3.1, б и в. Можно увидеть, что у А-формы наблюдается некоторое смещение пар оснований от оси молекулы к периферии, что отражается на размерах (2,8 нм – длина одного витка, в котором вместо 10
содержится 11 мононуклеотидов; меняется расстояние между нуклеотидами
и др.). Если А- и В-формы представляют собой правозакрученную двойную спираль, то Z-форма (зигзагообразная) ДНК имеет левозакрученную конфигурацию, в которой фосфодиэфирный остов располагается зигзагообразно вдоль оси молекулы. Параллельно фосфодиэфирному остову в структур А- и В-форм ДНК имеются большая и малая бороздки (желобки) –сайты, где присоединяются белки, выполняющие, очевидно, регуляторные функции при экспрессии генов. В настоящее время есть основание считать, что между А- и В-формами ДНК осуществляются взаимные переходы при изменении концентрации
соли и степени гидратации. В-форма ДНК больше всего подходит к модели Уотсона и Крика. В этих переходах, которые могут быть вызваны растворителями или белками, очевидно, заключенопределенный биологический смысл. Предполагают, что в А-форме ДНК выполняет роль матрицы в процессе транскрипции (синтез РНК на молекуле ДНК), а в В-форме – роль матрицы в процессе репликации (синтез ДНК на молекуле ДНК).
В структуре ДНК, как и в структуре РНК, открыты нуклеотидные последовательности, получившие название палиндромы , или перевернутые повторы. Они встречаются как внутри одной цепи, так и в двойной спирали. Например, как слово ротатор, которое одинаково читается как справа налево, так и обратно. Подобные обратные повторы могут служить основой для образования структуры шпилек или других вариаций с измененным внутрицепочечным и межцепочечным спариванием и формированием на отдельных участках тройной спирали. Возможно, эти палиндромные структуры имеют определенный биологический смысл в регуляции экспрессии отдельных генов, выполняя роль сайтов для ДНК-связывающих белков. Предстоит, однако, приложить немало усилий для установления как точной структуры этих вариаций, так и для определения их функциональной роли.
Третичная структура нуклеиновых кислот
Выделить нативную молекулу ДНК из большинства источников,в частности хромосом, чрезвычайно трудно из-за высокой чувствительности молекулы ДНК к нуклеазам тканей и гидродинамической деструкции *.Удалось выделить в интактном (неповрежденном) виде только некоторые ДНК вирусов, митохондрий и хлоропластов. Исследования этих молекул при помощи физических (в частности, кристаллографических) и физико-химических методов показали, что двойная спираль ДНК на некоторых участках может подвергаться дальнейшей спирализации с образованием суперспирали или открытой кольцевой формы. Оказалось также, что линейная ДНК может образоваться из кольцевой формы или существовать как таковая в природе. В некоторых вирусах обнаружены, кроме того, одноцепочечные ДНК линейной и кольцевой форм . Образование кольцевой формы молекулы ДНК у бактерий или в митохондриях клеток животных часто вызвано ковалентным соединением ихоткрытых концов. Известно, что суперспиральная (суперскрученная) структура обеспечивает экономную упаковку огромной молекулы ДНК в хромосоме: вместо 8 см длины, которую она могла бы иметь в вытянутой форме, в хромосоме человека молекула ДНК настолько плотно упакована, что ее длина составляет 5 нм. Обычно в ДНК встречаются положительные и отрицательные
супервитки, образованные за счет скручивания по часовой (правосторонней) или против часовой стрелки двойной спирали. Образование подобных супервитков катализируется специфическими ферментами,получившими название топоизомераз. Подобные суперспирали соединяются с белками (гистонами), упакованными в бороздках, обеспечивая тем самым стабильность третичной структуры ДНК. Степень суперспиральности (наличие супервитков) молекулы ДНК обычно устанавливают по изменению константы седиментации в определенных условиях. Суперспирализация ДНК может быть нарушена разрывом в одной из цепей или в обеих цепях двойной спирали под действием ДНКазы или при обработке
интеркалирующими соединениями. Под интеркаляцией подразумевают встраивание плоских ароматических колец между стопками пар азотистых оснований ДНК. Интеркаляция может быть вызвана антибиотиками и кра-сителями; в интактных клетках она может быть обусловлена ароматическими кольцами амнокислот, что имеет, очевидно, определенный биологический смысл в проблеме белково-нуклеинового узнавания.
Биологические функции. ДНК является носителем генетической информации, записанной в виде последовательности нуклеотидов с помощью генетического кода. С молекулами ДНК связаны два основополагающих свойства живых организмов — наследственность и изменчивость. В ходе процесса, называемого репликацией ДНК, образуются две копии исходной цепочки, наследуемые дочерними клетками при делении, таким образом образовавшиеся клетки оказываются генетически идентичны исходной.Генетическая информация реализуется при экспрессии генов в процессах транскрипции (синтеза молекул РНК на матрице ДНК) и трансляции (синтеза белков на матрице РНК).Последовательность нуклеотидов «кодирует» информацию о различных типах РНК: информационных, или матричных (мРНК), рибосомальных (рРНК) и транспортных (тРНК). Все эти типы РНК синтезируются на основе ДНК в процессе транскрипции. Роль их в биосинтезе белков (процессе трансляции) различна. Информационная РНК содержит информацию о последовательности аминокислот в белке, рибосомальные РНК служат основой для рибосом (сложных нуклеопротеиновых комплексов, основная функция которых — сборка белка из отдельных аминокислот на основе иРНК), транспортные РНК доставляют аминокислоты к месту сборки белков
— в активный центр рибосомы, «ползущей» по иРНК.

21. Біоенергетика. Утворення АТФ та інших макроергічних сполук.
Энергия известна нам в разных формах. Мы знаем электрическую, механическую, химическую, тепловую и световую энергию. Мы знаем также, что энергия может переходить из одной формы в другую. Известно, что любой переход энергии сопровождается некоторыми потерями. Многочисленные количественные исследования по взаимопреврвщении различных форм энергии, выполненные физиками и химиками, позволили сформулировать два фундаментальных закона термодинамики.
Первый закон. При любом физическом или химическом изменении общее количество энергии во Вселенной остается постоянным.
Первый закон – это закон сохранения энергии, его можно сформулировать и так: Энергия не появляется и не исчезает. Всякий раз, когда энергия используется для выполнения работы или же переходит из одной формы в другую, общее количество энергии остается неизменным.
Второй закон. Все физические или химические процессы стремятся идти в направлении, соответствующем необратимому переходу полезной энергии в хаотическую, неупорядоченную форму. Мерой такого перехода служит величина, которая носит название энтропии. Процесс останавливается, когда наступает состояние равновесия, при котором энтропия имеет максимально возможное при данных условиях значение.
Необходимо более точно определить понятия «полезная энергия» и «энтропия». Есть 2 вида полезной энергии: 1) свободная энергия, которая может производить работу при постоянной температуре и постоянном давлении, и 2)тепловая энергия, способная производить работу только при изменении температуры и давления. Энтропия является количественной характеристикой или мерой неупорядоченности энергии в данной системе.
Есть и другой аспект второго закона, который следует учитывать для понимания того, как действует этот закон, особенно в биологических системах. Введем прежде всего понятие реакционной системы, под которой подразумевается совокупность веществ, обеспечивающих протекание данного химического или физического процесса. Такой системой может быть, например, организм животного, отдельная клетка или два реагирующих друг с другом соединения. Далее мы должны ввести понятие окружающей среды, с которой реакционная система может обмениваться энергией. Совокупность реакционной системы и окружающей среды составляет то, что мы называем «Вселенной» и что вообще говоря, включает в себя земной шар и космическое пространство. Некоторые химические или физические процессы могут, конечно, протекать в замкнутых системах, не способных к обмену энергией с окружающей средой. Однако в реальном мире, и особенно в мире биологическом, системы, в которых протекают химические и физические процессы, обмениваются энергией с окружающей средой. Мы скоро убедимся, насколько важно это разграничением между системой и окружающей средой, когда речь идет об обмене энергией. Изменения свободной энергии, теплоты и энтропии в химических реакциях, протекающих при постоянной температуре и постоянном давлении, т.е. в условиях, характерных именно для биологических систем, связаны друг с другом количественно следующим уравнением:
По мере того как химическая реакция стремится к состоянию равновесия, энтропия Вселенной (система + окружающая среда) возрастает. В принципе в некой идеальной системе
реакция может протекать и без увеличения энтропии. Увеличению энтропии Вселенной при какойлибо реакции должно, согласно уравнению соответствовать уменьшение свободной энергии реакционной системы. Поэтому величина AG реакционной системы имеет всегда отрицательное значение. Изменение энтальпии АН определяется как количество тепла, которое данная реакционная система отдает окружающей среде или получает от нее при постоянной температуре и постоянном давлении.
Если реакционная система теряет (т. е.отдает) тепло, то величина 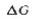 имеет отрицательное значение; если же система получает тепло от окружающей среды, то АН выражается положительной величиной. Для биологических систем существенна еще одна важная особенность изменений энтропии. Согласно второму закону термодинамики, при химических реакциях или физических процессах энтропия Вселенной увеличивается. Из этого закона, однако, не следует, что возрастание энтропии должно происходить обязательно в самой реакционной системе; оно может произойти в
имеет отрицательное значение; если же система получает тепло от окружающей среды, то АН выражается положительной величиной. Для биологических систем существенна еще одна важная особенность изменений энтропии. Согласно второму закону термодинамики, при химических реакциях или физических процессах энтропия Вселенной увеличивается. Из этого закона, однако, не следует, что возрастание энтропии должно происходить обязательно в самой реакционной системе; оно может произойти в
любом другом участке Вселенной. В живых организмах метаболические процессы, т. е. те превращения, которым подвергаются в них пищевые вещества, не ведут к возрастанию внутренней неупорядоченности, или энтропии самих организмов. Из повседневных наблюдений мы знаем, что любой организм, будь то муха или слон (т. е. в нашем понимании «система»), при всех процессах жизнедеятельности сохраняет присущую ему сложную и упорядоченную структуру. В результате процессов жизнедеятельности возрастает энтропия не самих живых организмов, а окружающей среды. Живые организмы сохраняют внутреннюю упорядоченность, получая свободную энергию в виде пищевых веществ (или солнечного света) из окружающей среды и возвращая в нее такое же количество энергии в менее полезной форме, главным образом в форме тепла, которое рассеивается во всей остальной Вселенной. В заключение следует подчеркнуть, что сам по себе рост энтропии, или увеличение степени неупорядоченности, нельзя считать совершенно бесполезным. Поскольку увеличение энтропии Вселенной при биологических процесах необратимо, оно создает движущую силу и задает направление всем видам биологической активности. Живые организмы непрерывно повышают энтропию в окружающей среде, и этим Вселенная расплачивается за поддержание в них внутреннего порядка. Тепло не является для клеток существенным источником энергии, так как тепло способно производить работу лишь в том случае, если оно переходит от более нагретого тела к более холодному или из зоны с более высокой температурой в зону с более низкой температурой. Кроме того, к. п. д. теплового двигателя зависит, как известно, от разности температур между нагретым и холодным телом; чем эта разность больше, тем большая доля тепловой энергии может быть превращена в работу. Поскольку в живых клетках температура в любой точке практически одинакова, они не способны использовать тепловую энергию. Тепло служит им лишь для поддержания оптимальной рабочей температуры. Пригодная для клеток форма энергии, т.е. та форма, которую они и могут, и должны использовать, -это свободная энергия, способная производить работу при постоянной температуре и постоянном давлении. Гетеротрофные клетки извлекают необходимую им энергию из богатых энергией пищевых веществ, а для фотосинтезирующих клеток ее источником служит улавливаемая ими энергия солнечного света. Полученная свободная энергия переводится теми и другими клетками в одну и ту же форму – в химическую энергию, которая затем используется для выполнения работы в процессах, не связанных со сколько-нибудь заметным перепадом температур. Попросту говоря, клетки - это химические двигатели, работающие в условиях постоянства температуры и давления.
Теперь, познакомившись с некоторыми основными законами, которые регулируют обмен энергии в химических системах, мы можем обратиться к рассмотрению энергетического цикла в клетках. Для гетеротрофных клеток источником свободной энергии, получаемой в химической форме, служит процесс расщепления, или катаболизм, пищевых молекул (в основном углеводов и жиров). Эту энергию клетки используют в следующих целях: 1) для синтеза биомолекул из молекул предшественников небольшого размера; 2) для выполнения механической работы, например мышечного сокращения, 3) для переноса веществ через мембраны против градиента концентрации и 4) для обеспечения точной передачи информации. Главным связующим звеном между клеточными реакциями, идущими с выделением и с потреблением энергии, служит аденозинтрифосфат(АТФ).
При расщеплении высокоэнергетического клеточного топлива часть содержащейся в этом топливе свободной энергией улавливается, в том смысле что она используется для синтеза АТФ из аденозиндифосфата и неорганического фосфата - процесса, требующего затраты свободной энергии. Позже АТФ, распадаясь в АДФ и фосфат отдает значительное количество своей химической энергии тем процессам, для которых энергия необходима. Таким образом АТФ выступает в роли переносчика химической энергии, связывающего клеточные процессы, сопровождающиеся выделением энергии, с теми главными видами клеточной активности, в которых энергия потребляется. АТФ поставляет энергию и для таких процессов жизнедеятельности, как люминисценция, которая у светляков служит сигналом для привлечения особей противоположного пола.
22. Біохімія крові. Кров як внутрішнє середовище організму. Хімічний склад крові. Діагностичне значення загального аналізу крові.
Кровь — жидкая ткань, наполняющая сердечно-сосудистую систему позвоночных животных, в том числе человека, некоторых беспозвоночных. Состоит из плазмы (межтканевой жидкости), клеток: эритроцитов, лейкоцитов и тромбоцитов. Циркулирует по системе сосудов под действием силы ритмически сокращающегося сердца и непосредственно с другими тканями тела не сообщается ввиду наличия гистогематических барьеров. У всех позвоночных кровь имеет чаще красный цвет (от бледнодо тѐмно-красного), которым она обязана гемоглобину, содержащемуся в специализированных клетках, эритроцитах.
Биохимический анализ крови — это лабораторный метод исследования, использующийся в медицине, который отражает функциональное состояние органов и систем организма человека. Он позволяет определить функцию печени, почек, активный воспалительный процесс, ревматический процесс, а также нарушение водно-солевого обмена и дисбаланс микроэлементов. Биохимический анализ помогает поставить диагноз, назначить и скорректировать лечение, а также определить стадию заболевания. Для биохимического анализа крови нужно подготовиться. Не следует принимать пищу примерно за 6 - 12 часов до исследования. Из жидкости не следует употреблять соки, молоко, алкоголь, сладкий чай или кофе. Можно пить воду. Любые продукты влияют на показатели крови, они могут привести к неверным данным, что может повлечь за собой неправильное лечение. Взятие крови производится как правило в положении сидя или лежа. На руку выше локтя накладывается специальный жгут. Место забора крови предварительно обрабатывается антисептиком для предотвращения инфицирования. В вену вводится игла и осуществляется забор крови. Кровь переливается в пробирку и отправляется с направлением в биохимическую лабораторию.
Параметры
Гемоглобин - Белок эритроцитов. Функция: транспорт кислорода, уровень у мужчин: 130 - 160 г/л, у женщин: 120 - 150 г/л. Снижение гемоглобина в крови, чаще бывает по причине анемии.
Гаптоглобин —гликопротеин плазмы крови, специфически связывающий гемоглобин. Содержание его в различных возрастных группах колеблется в достаточно широких пределах. При расшифровке анализа крови различают три наследственных фенотипа гаптоглобина: Нр 1
— 1, Нр 2—1, Нр 2—2.
Глюкоза — норма 3,30-5,50 миллимоль на литр. Повышенный уровень глюкозы свидетельствует об угрозе сахарного диабета или нарушении толерантности к глюкозе, что требует консультации эндокринолога.
Мочевина — норма мочевины — 2,5-8,3 миллимоля на литр. Повышение нормы говорит о плохой выделительной работе почек и нарушении фильтрации. Нарастание содержания мочевины в крови до 16—20 ммоль/л (в расчете на азот мочевины) классифицируется как нарушение функции почек средней тяжести, до 35 ммоль/л — как тяжелое; свыше 50 ммоль/л — очень тяжелое, с неблагоприятным прогнозом.
Остаточный азот крови (небелковый азот крови) — азот веществ, остающихся после удаления белков плазмы крови. В норме содержание остаточного азота в сыворотке крови колеблется от 14,3 до 28,6 ммоль/л.
Креатинин — рассматривается в комплексе с мочевиной. Норма креатинина — 44-106 микромиллилитров на литр. Как и мочевина, креатинин говорит о работе почек.
Общие липиды - содержание в крови 4 - 8 г/л.
Холестерин — норма — от 3,64 - 6,76 ммоль/л. Высокий уровень холестерина сигнализирует об угрозе атеросклероза.
Триацилглицерины - содержание в крови 0,44 - 1,82 ммоль/л, повышение уровня ТАГ наблюдается при гипотиреозе, сахарном диабете. Снижение при гипертиреозе.
Фосфолипиды - содержание в крови 2,52 - 2,91. Повышение наблюдается в тех же случаях, что и ТАГ.
Общий билирубин — является продуктом распада гемоглобина, в норме содержание в крови 8.5-20.55 мкмоль/литр.
Общий белок — определяет уровень белка в сыворотке крови. Его норма — 65-85 грамм на литр. Если человек плохо питается, истощен, уровень белка резко понижается.

АлАт (Аланинаминотрансфераза) — фермент используемый для оценки функции печени. Содержание в крови 28 - 178 нкат/л.
АсАТ (Аспартатаминотрансфераза) — фермент используемый для оценки функции печени. Содержание в крови 28 - 129 нкат/л, повышение его уровня - говорит о заболеваниях печени.
Липаза — фермент секретируемый в основном поджелудочной железой. Его уровень в крови повышается при воспалении/повреждении поджелудочной железы.
Амилаза — фермент секретируемый в основном поджелудочной железой и слюнными железами. Его уровень в крови повышается при воспалении/повреждении поджелудочной железы.
Гамма-ГТП — Гамма-глутамилтранспептидаза, фермент используемый для оценки функции печени. (Норма: у муж = 15-106 мкмоль на литр, у жен = 10-66 мкмоль на литр)
Антистрептолизин-О — АСЛ-О представляет собой антитела к антигену (стрептолизину) бета-гемолитического стрептококка группы А. Используется в диагностике ревматизма.
Ревмофактор (ревматоидный фактор) — вид антител, находящийся в крови многих больных аутоиммунными заболеваниями (ревматизм, ревматоидный артрит, системная красная волчанка, склеродермия и др.).
СРБ (С-реактивный белок) — неспецифичный индикатор воспаления в организме.
Щелочная фосфатаза — катализирует отщепление фосфорной кислоты от ее органических соединений. Самая высокая концентрация ЩФ обнаруживается в костной ткани (остеобластах), гепатоцитах, клетках почечных канальцев, слизистой кишечника и плаценте.
Через кровь осуществляется взаимосвязь обмена веществ разных органов тела. Кровь переносит питательные вещества из тонкого кишечника в печень и другие органы, а отработанные шлаки транспортирует в почки для последующего выведения их из организма. Кровь доставляет также кислород от легких к тканям и переносит СО2, образующуюся в качестве конечного продукта дыхания тканей, в легкие. Кроме того, гормоны, функционирующие как химические посредники транспортируются кровью от эндокринных желез к специфическим органам-мишеням. Химический состав крови очень сложен, так как она содержит большое число разнообразных питательных веществ, промежуточных продуктов обмена, отработанных шлаков и неорганических ионов, но именно это и позволяет ей координировать взаимодействие процессов метаболизма в различных органах и объединять их в единую систему. Объем крови в кровеносной системе взрослого человека составляет приблизительно 5-6 л. Почти половина этого объема приходится на долю эритроцитов (красньк кровяньк клеток), значительно меньшая часть-на долю лейкоцитов (белых кровяных клеток) и тромбоцитов.Жидкая часть крови, плазма, состоит на 90% из воды и на 10% из растворенных веществ. Свыше 70% сухого остатка составляют белки плазмы. Приблизительно 20% приходится на долю органических промежуточных продуктов обмела (метаболитов), транспортируемых от одних органов к другим, и на конечные продукты обмена-мочевину и мочевую кислоту, которые, попадая в почки, выделяются из организма с мочой. Остальные 10% сухого остатка плазмы составляют неорганические соли. В нормальных условиях концентрацииряда компонентов в крови когут колебаться в определенных пределах в зависимости от характера питания, а также от того, в какой момент времени взята кровь для анализа. Так, концентрація глюкозы в крови достигает максимума сразу же после еды, особенно если пища была богата углеводами, а спустя несколько часов этот показатель может быть ниже среднего уровня. Аналогичным образом, концентрація кронов в крови подвержена колебаниям в промежутках между приемами пиши. Содержание отдельных компонентов в плазме крови поддерживается наотносительно постоянном уровне спомощью различных регуляторных систем.
Система крови
Кровь это часть жидкой внутренней среды организма, которая циркулирует по системе сосудов. Кровь состоит из плазмы и форменных элементов (эритроциты, лейкоциты и тромбоциты). Все многочисленные функции крови можно разделить на 2 группы:
І. Транспортная функция
1.дыхательная - перенос газов (от легких к тканям кислород, от тканей к легким углекислый газ)
2.питательная или трофическая (перенос продуктов распада питательных веществ - аминокислоты, глюкоза, жирные кислоты - и минеральных веществ от кишечника к тканям)
3.выделительная или экскреторная (перенос продуктов обмена от тканей к органам выделения)
4.терморегуляторная (усредняет температуру сердцевины -внутренние органы, продуцирующие тепло- и оболочки -кожа, отдающая тепло)
5.гуморальная регуляция (переносит биологически активные вещества - гормоны, ферменты, витаминыот места продукции к органам мишеням)
6.поддержание рН внутренней среды (за счет работы буферных систем)
7.обеспечение водно-солеваго баланса в организме (обмен обеспечивается за счет осмотического давления)
8.поддержание целостности тканей и их регенерации (перенос веществ, обеспечивающих креаторные связи, т.е. несущие генетическую информацию о строение ткани)
ІІ. Защитная функция:
1.обеспечение иммунитета · клеточный иммунитет (нейтрофилы и лимфоциты)
· гуморальный иммунитет (выработка лимфоцитами антител)
2.свертывание крови или гемостаз - образование тромбов в местах повреждения сосудов. Химический состав крови в норме относительно постоянен. Это объясняется наличием в организме мощных регулирующих механизмов (ЦНС, гормональная система и др.), обеспечивающих взаимосвязь в работе таких важных для жизнедеятельности органов и тканей, как печень, почки, легкие и сердечно-сосудистая система. Все случайные колебания в составе крови в здоровом организме быстро выравниваются. Напротив, при многих патологических процессах отмечаются более или менее резкие сдвиги в химическом составе крови.

23. Метаболізм ксенобіотиків. Детоксикаційна функція печінки. Біотрансформація ксенобіотиків. Мікросомальне окислення. Цитохром Р-450.
Метаболизм ксенобиотиков в организме идет в основном по пути окисления. Большое распространение имеет также связывание токсических веществ с белками, аминокислотами, глюкуроно-вой, серной кислотами. В большинстве случаев ядовитое соединение подвергается последовательным превращениям, завершающимся реакцией коньюгации. Метаболизм ксенобиотиков чаще приводит к снижению их активности—дезактивации, которую в случае токсичных веществ называют детоксыкацыей. Однако в ряде случаев метаболиты ксенобиотиков,
наоборот, |
становятся |
более |
|
активными |
и |
более |
токсичными. |
||
В |
метаболизме |
ксенобиотиков |
участвуют |
около 30 ферментов. В нем различают две фазы: |
|||||
• |
модификации, |
создающей |
или |
освобождающей |
|
функциональные |
группы; |
||
• конъюгации — присоединения к последним других групп или молекул, окисления ксенобиотиков (превращение фенолов в хи-ноны у растений).
Обе фазы приводят к увеличению гидрофильное, снижению активности и токсичности молекулы ксенобиотика. Третьей фазой можно считать связывание и выведение самих ксенобиотиков и их метаболитов из клетки, а затем из организма.
Многие ксенобиотики, попав в организм, подвергаются биотрансформации и выделяются в виде метаболитов. В основе биотрансформации по большей части лежат энзиматические преобразования молекул. Биологический смысл явления - превращение химического вещества в форму, удобную для выведения из организма, и тем самым, сокращение времени его действия.
Метаболизм ксенобиотиков проходит в две фазы:
Входе первой фазы окислительно-восстановительного или гидролитического превращения молекула вещества обогащается полярными функциональными группами, что делает ее реакционно-способной и более растворимой в воде. Во второй фазе проходят синтетические процессы конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, в результате чего образуются полярные соединения, которые выводятся из организма с помощью специальных механизмов экскреции. Разнообразие каталитических свойств энзимов биотрансформации и их низкая субстратная специфичность позволяет организму метаболизировать вещества самого разного строения. Вместе с тем, у животных разных видов и человека метаболизм ксенобиотиков проходит далеко не одинаково, поскольку энзимы, участвующие в превращениях чужеродных веществ, часто видоспецифичны.
Следствием химической модификации молекулы ксенобиотика могут стать: 1. Ослабление токсичности; 2. Усиление токсичности;
3. Изменение характера токсического действия;
4. Инициация токсического процесса.
Метаболизм многих ксенобиотиков сопровождается образованием продуктов существенно уступающих по токсичности исходным веществам. Так, роданиды, образующиеся в процессе биопревращения цианидов, в несколько сот раз менее токсичны, чем исходные ксенобиотики. Гидролитическое отщепление от молекул зарина, зомана, диизопропилфторфосфата иона фтора, приводит к утрате этими веществами способности угнетать активность ацетилхолинэстеразы и существенному понижению их токсичности. Процесс утраты токсикантом токсичности в результате биотрансформации обозначается как "метаболическая детоксикация". В процессе метаболизма других веществ образуются более токсичные соединения. Примером такого рода превращений является, в частности, образование в организме фторуксусной кислоты при интоксикации фторэтанолом.
Вряде случаев в ходе биотрансформации ксенобиотиков образуются вещества, способные
