
ПЕРФОРАТИВНЫЕ ГАСТРОДУОДЕНАЛЬНЫЕ ЯЗВЫ
Перфорация - тяжелое, угрожающее жизни осложнение, занимающее ведущие позиции в структуре летальности при язвенной болезни. Снизившаяся к 50-м гг. прошлого века летальность при этом состоянии уже в течение многих лет составляет от 5 до 18%. Определяющие летальность факторы - тяжелое общее состояние пациента, обусловленное развитием перитонита, нередко выраженной сопутствующей патологией, а также время, прошедшее с момента возникновения осложнения. Так, у больных, оперированных через сутки после перфорации, летальность возрастает в 3-5 раз по сравнению с пациентами, которым операцию провели в течение первых 6 ч. Современная статистика последнего десятилетия подчеркивает рост доли этого грозного осложнения, при этом перфорации язв стали возникать гораздо чаще, чем стеноз, приближаясь к частоте язвенных кровотечений.
Как правило, осложнение возникает преимущественно у мужчин, в основном молодого возраста, с кратким язвенным анамнезом (до 3 лет) и периодическими обострениями, чаще в весенний и осенний периоды. У 25% больных жалоб в прошлом не было.
Перфоративные язвы чаще бывают локализованы в двенадцатиперстной кишке (90%). Примерно в 10% случаев перфорация язвы сопровождается кровотечением или стенозом.
Классификация
По локализации перфорации:
• язва желудка;
• язва двенадцатиперстной кишки.
По клинической форме перфорации:
• типичная (в свободную брюшную полость), в том числе прикрытая;
• атипичная (в сальниковую сумку, малый или большой сальник, забрюшинную клетчатку, изолированную спайками полость);
• в сочетании с желудочно-кишечным кровотечением;
• в сочетании со стенозом выходного отдела желудка. По клинической фазе течения перитонита:
• химический перитонит (период первичного шока);
• бактериальный перитонит (период мнимого благополучия);
• разлитой гнойный перитонит (период абдоминального сепсиса).
Основные черты патологии
Перфорация язвы приводит к поступлению гастродуоденального содержимого в свободную брюшную полость, воздействуя на брюшинный покров как химический, физический, а затем и бактериальный раздражитель. Перитонит, возникающий при перфорации, - один из факторов, влияющих на тактику хирургического лечения. Следует отметить некоторые особенности перитонита при перфорации. Начальная реакция организма на прободение язвы ярко клинически окрашена в связи с воздействием кислого желудочного сока на брюшину (по сути, является ее химическим ожогом). В дальнейшем развивается серозно-фибринозный перитонит, а затем и гнойный. Как правило, через 6-12 ч от момента перфорации в брюшной полости выявляют прозрачный или мутный экссудат с нитями и хлопьями фибрина, париетальная и висцеральная брюшины ярко гиперемированы. Степень контаминации при этом не превышает 103-105бактериальных тел в 1 мл экссудата. Бактериальный пейзаж в большинстве случаев представлен грамположительными кокками, лактобациллами, грибами родаCandida. Следует отметить, что в 30% случаев в эти сроки бактериальное обсеменение отсутствует. Указанные изменения позволяют выбрать радикальный способ оперативного вмешательства у этой группы больных.
В более поздние сроки с момента перфорации в брюшной полости появляются гноевидный экссудат, фиксированные наложения фибрина, паралитическая кишечная непроходимость с увеличением бактериальной контаминации. В период разлитого гнойного перитонита следует избрать минимально травматичный способ вмешательства, включающий санацию брюшной полости.
Диагностика Симптоматика
Перфорация язвы развивается остро, хотя у 20% больных удается выявить продромальный период - усиление болей за 3-4 дня,
появление тошноты, рвоты. Перфорация сопровождается классической триадой признаков: кинжальной болью (95%), доскообразным напряжением мышц живота (92%), предшествующим язвенным анамнезом (80%).
Физикальное обследование
В течение заболевания различают три фазы шока, мнимого улучшения и гнойного перитонита, имеющие свои характерные клинические проявления.
В первой фазе перфорации (до 6 ч) при физикальном обследовании выявляютшок. Обращают внимание на внешний вид больного: он лежит неподвижно на спине или правом боку с приведенными к животу ногами, охватив руками живот, избегает перемены положения тела. Лицо больного осунувшееся и бледное, с испуганным выражением. Дыхание частое и поверхностное. Характерна начальная брадикардия: пульс нередко снижается до 50-60 в минуту (так называемыйвагусный пульс) вследствие ожога брюшины и нервных окончаний кислотой. АД может быть уменьшено. Язык в первые часы после перфорации остается влажным и чистым. Обращают внимание на резчайшую перкуторную и пальпаторную болезненность живота, напряжение мышц передней брюшной стенки сначала в верхних отделах, а затем и по всему животу. Положителен симптом Щеткина-Блюмберга. Уже в первые часы заболевания удается обнаружить резкую болезненность тазовой брюшины при пальцевом ректальном или вагинальном исследовании.
Описанная картина, характерная для фазы шока, через 6-12 ч после перфорации стирается. Наступает период мнимого благополучия. Лицо больного приобретает нормальную окраску. Пульс и АД нормализуются. Дыхание перестает быть поверхностным. Язык становится сухим и обложенным. Напряжение мышц брюшной стенки уменьшается, при пальпации сохраняются болезненность и положительные симптомы раздражения брюшины. Перистальтика не выслушивается, печеночная тупость отсутствует. При ректальном исследовании можно обнаружить нависание передней стенки прямой кишки и ее болезненность. Затем, через 12-24 ч после перфорации, состояние больных начинает прогрессивно ухудшаться - наступаетфаза гнойного перитонита. Появляется рвота. Больной ведет себя беспокойно. Температура тела повышается. Учащается дыхание, падает пульсовое давление, возникает вздутие живота, перистальтика отсутствует. Налицо развернутая клиническая картина абдоминального сепсиса.
Диагностические методы исследования
При обзорной рентгенографии органов брюшной полости при перфорации полого органа выявляют свободный газ под куполом диафрагмы в 80% случаев. Точность рентгенологического метода находится в прямой зависимости от количества газа, поступившего в свободную брюшную полость. В сомнительных случаях следует прибегать к пневмогастрографии, повышающей достоверность метода до 95%. Установив в желудок зонд, в его просвет с помощью шприца Жане вводят 150-200 мл воздуха и тотчас выполняют обзорную рентгенографию брюшной полости. Тяжело больным целесообразно проводить рентгенографию в положении лежа на боку, при этом свободный газ локализуется у места прикрепления диафрагмы к боковой стенке живота.
Эзофагогастродуоденоскопия (ЭГДС) позволяет уточнить диагноз в сложных случаях, дать точную картину локализации язвы и ее размеров, обнаружить сочетанные осложнения (наличие второй язвы с кровотечением или угрозой его развития, признаки стеноза). ЭГДС необходима также при планировании лапароскопического ушивания прободной язвы.
Лапароскопия помогает уточнить диагноз и выбрать адекватный план лечения при неясной клинической картине (в тех ситуациях, когда другие вышеперечисленные методы не позволяют распознать прикрытую или атипичную перфорацию), а в части случаев позволяет убедиться в возможности проведения того или иного вида операции.
При лабораторном исследовании крови констатируют быстронарастающий лейкоцитоз со сдвигом лейкоцитарной формулы влево. В анализах мочи при перитоните отмечают появление форменных элементов крови, белка и цилиндров.
Дифференциальная диагностика
Дифференциальную диагностику перфоративной язвы нередко проводят с острым аппендицитом, особенно если больного осматривают через 6-7 ч после перфорации, когда желудочное содержимое и экссудат скапливаются в правой подвздошной ямке, вызывая симптомы, характерные для аппендицита. В части случаев диагностические затруднения могут возникнуть при других острых хирургических заболеваниях органов верхнего этажа брюшной полости. Прежде всего, это острый холецистит, острый панкреатит, почечная колика и острая кишечная непроходимость. Нельзя также забывать о возникающих иногда чрез-
вычайных трудностях диагностики терапевтических заболеваний, таких как инфаркт миокарда, базальный плеврит, пневмония. В заключение следует подчеркнуть, что вопросы точной диагностики причины острого живота становятся непреодолимыми при уже развившемся разлитом гнойном перитоните, тогда их решают при экстренной срединной лапаротомии.
Лечение
Консервативный способ ведения больных с перфоративными язвами (так называемый метод Тейлора) предполагает постоянную аспирацию желудочного содержимого, голод, назначение больших доз антибиотиков, а также придание телу больного положения Фаулера (с приподнятым головным концом). Сегодня очевидно, что этот метод несовершенен и поэтому применим только как вынужденная мера при предельно тяжелом состоянии больного либо отсутствии возможности проведения операции.
Хирургическое лечение
Характер и объем хирургического вмешательства определяют строго индивидуально в зависимости от вида язвы, ее локализации, характера и распространенности перитонита, наличия сопутствующих перфорации других осложнений язвенной болезни, а также с учетом степени операционно-анестезиологического риска. Различают радикальные операции, направленные не только на спасение жизни больного, но и на профилактику дальнейших рецидивов образования язв (резецирующие методы, ваготомию с иссечением язвы и пилоропластикой), а такжепаллиативные - различные способы ушивания перфорации, устраняющие только угрожающее жизни осложнение болезни.
Ушивание дуоденальной или желудочной перфоративной язвы остается спасительным методом лечения, особенно у больных с распространенным поздним перитонитом или высокой степенью операционно-анестезиологического риска. На рис. 9-1 и 9-2 представлены наиболее распространенные способы ушивания перфоративной язвы. Подчеркнем, что зачастую при желудочной язве перфоративное отверстие составляет более 1 см, с хрящевидной плотности краями. В этой ситуации целесообразно применить прием Оппеля-Поликарпова, тампонируя перфоративное отверстие прядью большого сальника с последующей его фиксацией отдельными швами к стенке желудка. Летальность зависит, прежде всего, от условий, в которых выполняют вмешательст-
Рис. 9-1. Ушивание перфоративной язвы двенадцатиперстной кишки. Швы накладывают в поперечном по отношению к продольной оси кишки направлении. Ко второму ряду швов фиксируют прядь сальника
Рис. 9-2. Ушивание перфоративной язвы желудка по Оппелю-Поликарпову с тампонадой перфоративного отверстия прядью большого сальника
Рис. 9-3. Лапароскопическое ушивание перфоративной дуоденальной язвы (эндофото). Наложение 8-образного серозно-мышечного шва.
во, распространенности и формы перитонита; она составляет от 5 до 60%.
Лапароскопическое ушивание (или ушивание из абдоминального доступа) показано у больных, у которых перфорируется так называемая немая язва, а выполненная дооперационная диагностическая программа свидетельствует об отсутствии других сочетанных осложнений язвенной болезни. На рис. 9-3 представлена техника лапароскопического ушивания перфоративной дуоденальной язвы.Стволовая ваготомия с иссечением язвы и пилоропластикой - «золотой стандарт» хирургического лечения перфоративной дуоденальной язвы. Она позволяет ликвидировать другие осложнения заболевания, сопутствующие перфорации и создать условия для профилактики дальнейших рецидивов. Послеоперационная летальность после этих операций составляет 1,8-2,5%. На рис. 9-4 представлены схема операции и техника выполнения стволовой ваготомии с иссечением язвы и пилоропластикой по Джадду. Кроме того, довольно часто выполняют пилоропластику по Финнею.
Ваготомию с антрумэктомией используют при перфорации, если выявлены другие осложнения (поздняя стадия пилородуоденального стеноза), а также при сочетанной форме язвенной болезни.
Резекцию желудка (гемигастрэктомию) проводят при прободной желудочной язве у больных с невысоким операционно-анестезиологическим риском, когда перфорирована длительно существующая каллезная язва или существуют сочетанные с перфорацией другие осложнения (кровотечение, различной степени выраженности стеноз). Летальность при этом достигает 4-9%.
Послеоперационный период
Ведение послеоперационного периода у больных, оперированных по поводу прободных гастродуоденальных язв, необходимо соотносить с характером проведенного вмешательства.
Так, при ушивании прободных язв, когда операция фактически не влияет на патогенез заболевания, дальнейшее благополучие больного зависит от противорецидивного лечения, которое начинают сразу после операции. Оно должно быть комплексным, состоящим из антисекреторных препаратов (блокаторов Н2-гистаминовых рецепторов, блокаторов протонного насоса) и антихеликобактерной терапии препаратами висмута в комбинации с антибиотиками (амоксициллином). После выписки из стационара больной переходит под наблюдение гастроэнтеролога для последующей поддерживающей и противорецидивной терапии.
Хирургические операции, имеющие патофизиологическое обоснование (ваготомия с пилоропластикой, ваготомия с антрумэктомией, резекция желудка), по современным представлениям, также должны сопровождаться поддерживающей и противорецидивной терапией. Ее начинают сразу в послеоперационном периоде.
После окончательной оценки непосредственного эффекта противоязвенного лечения в условиях диспансерного наблюдения больных, когда амбулаторно определяют состояние секреторной и эвакуаторной функций оперированного желудка и эрадикацию Helicobacter pylori, больные окончательно переходят под наблюдение врача-гастроэнтеролога.
Прогноз
Показатели летальности были указаны в начале этого раздела. Среди погибших после операций по поводу перфоративной язвы превалируют пациенты с исходным предельно тяжелым состоянием, обусловленным либо сопутствующей патологией, либо терминальной фазой перитонита. Неблагоприятный исход чаще всего становится следствием поздней обращаемости больного за медицинской помощью и несвоевременной диагностики.
У части больных возможны хирургические осложнения, наиболее типичные из них: несостоятельность ушитой язвы или сформированного анастомоза с развитием перитонита, абсцессы различной локализации на фоне недостаточной санации брюшной полости при первичной операции, паралитическая кишечная непроходимость, послеоперационная спаечная кишечная непроходимость, острый послеоперационный панкреатит.
Одна из особенностей состояния больных после операций с ваготомией - нарушение моторно-эвакуаторной функции желудка и двенадцатиперстной кишки. Ниже, в разделе, посвященном язвенному стенозу выходного отдела желудка, об этом сказано более детально.
Одна из задач современной хирургической гастроэнтерологии - не только обеспечение хороших непосредственных результатов, но и создание условий для быстрейшей реабилитации пациентов в раннем послеоперационном периоде и предотвращение рецидивов язвенной болезни. В качестве неблагоприятных факторов в отдаленном периоде рассматривают органические (рецидив язвы, дефект сформированных ранее анастомозов) и функциональные (нарушение желудочной эвакуации функциональной природы, ранний и поздний демпинг-синдромы, синдром приводящей петли, диарею и т.д.) расстройства.
Очевидно, что органосохраняющие операции с ваготомией имеют свои преимущества: в отдаленном послеоперационном периоде у большинства пациентов (90%) отмечают хорошие результаты, а качество жизни соответствует таковому у здорового человека. И все же следует иметь в виду, что доля рецидивов язвенной болезни достигает 10%. Строгое определение группы больных, которым показано ушивание прободной язвы (в том числе и лапароскопическое) с последующей медикаментозной терапией, позволяет достичь хорошего качества жизни.
Частота развития перфораций язв, по данным разных авторов, колеблется от 3 до 34% от числа больных, страдающих язвенной болезнью желудка и двенадцатиперстной кишки. По литературным данным, в нашей стране по поводу перфоративных гастродуоденальных язв производится в среднем 12 операций на 100 000 населения. Преобладающее число больных с прободными гастродуоденальным язвами - пациенты в возрасте 20-50 лет. Больные в возрасте до 50 лет составляют 82% всех оперированных с перфоративной гастродуоденальной язвой. Перфоративные язвы гораздо чаще встречаются у мужчин, чем у женщин. Соотношение лиц мужского и женского пола составляет 7:1-10:1.
В структуре всех острых хирургических заболеваний органов брюшной полости прободные гастродуодельные язвы составляют около 1,6-3%. Большинство авторов приводят цифры, говорящие о преимущественной локализации перфораций в двенадцатиперстной кишке. Перфорация острых и так называемых немых язв, впервые манифестирующих картиной прободения, наблюдается, по литературным данным, в 12-20% случаев. Частота прободения в большинстве случаев в определенной степени совпадает с сезонностью обострений язвенной болезни.
Сохраняющаяся высокая летальность при перфоративных гастродуоденальных язвах остается основным критерием, характеризующим спектр проблем как в диагностике, так и в выборе метода лечебной тактики у этих больных. Так, послеоперационная летальность среди больных, оперированных по поводу перфоративных гастродуоденальных язв, составляет 0,5-8,9%. При этом обращает на себя внимание зависимость исходов оперативного лечения больных с перфоративной гастродуоденальной язвой от сроков обращения за помощью, своевременности диагностики и оперативного вмешательства от момента прободения. Согласно данным большинства авторов, оказывается, что фактор времени можно считать основным фактором риска, влияющим на исходы лечения больных с прободными гастродуоденальными язвами. По данным большинства литературных источников, в первые 6 ч с момента прободения язвы в стационары госпитализируются 67,8- 88,7% больных, а летальность у оперированных в первые 6 ч с момента перфорации не превышает 0,6-1,6%. Основной причиной летальных
исходов у этих больных становится, как правило, тяжелая интеркуррентная соматическая патология. В то же время причиной летальных исходов у больных, оперированных позже 12-24 ч с момента прободения гастродуоденальной язвы, служит чаще всего полиорганная недостаточность, развивающаяся на фоне прогрессирующего перитонита.
Позднее обращение за помощью, а также поздняя госпитализация становятся основными причинами диагностических ошибок и неблагоприятных исходов оперативных вмешательств, достигающих, по литературным данным, 29,5-50%.
Одним из факторов риска, оказывающих существенное влияние на показатели послеоперационной летальности, считается возраст оперированных больных. Приводимые в литературе данные свидетельствуют о том, что прободение гастродуоденальной язвы у пациентов старше 60 лет сопровождается высокой летальностью и значительным числом послеоперационных осложнений. Бесспорно, главными причинами летальных исходов у этих больных выступают осложнения сопутствующих заболеваний. Летальность среди оперированных больных старше 60 лет достигает в зависимости от объема оперативного вмешательства от 15,3 до 80%.
Особенно высокая летальность отмечается среди пациентов с перфоративной гастродуоденальной язвой, сочетающейся с кровотечением из язвы. Одновременно два осложнения язвенной болезни - перфорация и кровотечение - наблюдаются в 1,3-7% случаев. Сочетание прободения с кровотечением из язвы нередко служит причиной диагностических ошибок. Чаще всего не диагностируется одно из этих осложнений. Нередко у ослабленного кровотечением больного прободение язвы протекает атипично, со сглаженностью болевого синдрома. Кровотечение, возникающее на фоне ярко выраженной клинической картины прободения (в особенности язвы двенадцатиперстной кишки), также может быть не диагностировано и становится неожиданной интраоперационной находкой, влекущей за собой необходимость изменения выбора не только объема оперативного вмешательства, но и всей лечебной тактики.
Среди факторов, способствующих прободению язвы, следует иметь в виду употребление алкоголя, обильную еду, физическое напряжение, приводящее к резкому сокращению брюшного пресса и повышению внутрибрюшного давления, эмоционально-нервное перенапряжение.
Нельзя отрицать в развитии осложненного перфорацией течения язвенной болезни и фактор социально-экономического статуса больного.
Существующие точки зрения на патогенез перфораций гастродуоденальных язв не приводят к окончательному мнению о механизмах развития этого тяжелого и опасного осложнения язвенной болезни. Ряд авторов связывают этот процесс с проникновением в гастродуоденальную стенку высоковирулентных инфекционных агентов. Другие объясняют возникновение перфорации сосудистой реакцией гиперэргического типа, приводящей к тромбозу вен желудка. Именно поэтому тромбоз гастродуоденальных сосудов относится к основному патогенетическому звену в остром прободении гастродуоденальной стенки.
Не отрицая роль неврогенного фактора в патогенезе язвенной болезни, большинство авторов считают, что расстройство венозного кровообращения с развитием венозного тромбоза играет основную роль в патогенезе острых гастродуоденальных перфораций. Местная гиперсенсибилизация сосудов желудка рассматривается как манифестация аутоиммунного конфликта. Иммуноморфологические изменения в гастродуоденальной стенке в области язвы, характеризующиеся фибриноидными изменениями стенок сосудов с накоплением кислых мукополисахаридов по периферии язвы, высоким коэффициентом плазматизации слизистой оболочки, большим количеством тучных клеток, могут служить доказательством влияния такой гиперсенсибилизации сосудистой стенки и развития тромбоза. Таким образом, считают, что в патогенетической цепочке (инфекция -- местная гиперсенсибилизация сосудов - тромбоз и тромбофлебит гастродуоденальных вен - перфорация) все звенья неразрывно связаны в единый последовательно развивающийся процесс, ведущий к деструкции гастродуоденальной стенки.
На особенностях клинической картины перфоративной язвы сказывается анатомическая локализация прободения гастродуоденальной стенки, величина перфоративного дефекта, степень наполнения желудка в момент прободения, а также характер желудочного содержимого, кислотность желудочного сока.
Многочисленные классификации прободных гастродуоденальных язв, основанные в основном на клинико-анатомических принципах, подразделяют все перфорации на:
> классическую перфорацию;
> атипичную перфорацию;
> прикрытую перфорацию.
Чаще в практической хирургии используют классификацию прободных язв, на основе которой возможно осуществление выбора оптимального варианта алгоритма диагностики и лечебной тактики. Выделяют:
> перфорацию в свободную брюшную полость (классический вариант);
> перфорацию в сальниковую сумку (атипичная перфорация в замкнутое пространство - большую и малую сальниковые сумки, в печеночно-двенадцатиперстную связку, медиастинум, плевральную полость);
> перфорацию в забрюшинную клетчатку (разновидность атипичной перфорации);
> перфорацию в соседние органы (желчный пузырь, поперечную ободочную кишку);
> прикрытые перфорации.
В клиническом течении перфоративных гастродуоденальных язв выделяют три периода:
> первый (первые 6 ч) - внезапное возникновение резких болей в животе с развитием шокообразного состояния (так называемый период шока);
> второй (6-12 ч) - период затишья, или период мнимого благополучия;
> третий (от 12 ч и позже) - период перитонита.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Клиническая картина перфорации язв характеризуется внезапной «кинжальной» мучительной болью в надчревной области или правом подреберье (симптом Дьелафуа) и выраженным в различной степени напряжением мышц передней брюшной стенки. Боль, вызванная перераздражением концевого нервного аппарата брюшины излившимся в свободную брюшную полость гастродуоденальным содержимым (химический ожог кислым содержимым желудка), приобретает настолько интенсивный характер, что может вызвать кратковременную потерю сознания и не купироваться болеутоляющими средствами. Появление острых болей нередко сопровождается иррадиацией их в правое плечо, надплечье или лопатку (симптом Элекера) вследствие распространения желудочного содержимого в правый боковой канал и раздражения нервного аппарата диафрагмы. Симптом не имеет строгого специфического значения, так как нередко может встречаться при остром холецистите, травмах печени и ряде заболеваний, сопровождающихся вовлечением в воспалительный процесс диафрагмы.
Стадия шока, характеризующаяся резчайшей болью, вынуждает больного лежать неподвижно, чаще на спине. Больной, как правило, бледен, с легким цианозом губ, лицо выражает страх и страдание. Кожный покров покрыт холодным липким потом. Пациент отвечает на вопросы неохотно, с трудом, шепотом, отмечается поверхностное дыхание. Кашель и глубокое дыхание резко усиливают боли в животе. Живот не участвует в акте дыхания, ладьевидно втянут, доскообразно напряжен. У худых больных нередко видно напряжение брюшных мышц с четкой конфигурацией на передней брюшной стенке межсегментарных мышечных перемычек (inscriptiones tendineae - симптом Дзбановского- Чугуева). Иногда наблюдается подтягивание яичек к наружным отверстиям паховых каналов, расположение полового члена параллельно брюшной стенке, головкой кверху - генитальный симптом Берштейна. Достаточно часто наблюдаемым в фазе абдоминального шока клиническим признаком перфоративной гастродуоденальной язвы становится брадикардия - «вагусный пульс» - симптом Грекова.
Период «мнимого благополучия» характеризуется постепенным сглаживанием ярко выраженных кардинальных симптомов шоковой фазы перфоративной гастродуоденальной язвы.
IN.B. Следует помнить, что стадия «мнимого благополучия» - период высокой вероятности диагностических и тактических ошибок. В этой фазе отмечается постепенное улучшение состояния больных. Боли приобретают сглаженный характер, больные успокаиваются, нередко наблюдается психоэмоциональная эйфория. Дыхание становится более свободным, сглаживаются явления сосудистого коллапса. Нет той бледности кожного покрова и холодного пота, которые наблюдаются в шоковом периоде заболевания. Часто уже в начале этого периода (6-12 ч) доскообразное напряжение брюшных мышц сменяется умеренной ригидностью и болезненностью при пальпации в правой половине эпигастральной области. Иногда отмечается перемещение боли и болезненности из эпигастральной области в правую подвздошную область, что связано с затеканием содержимого желудка и двенадцатиперстной кишки по правому боковому каналу в правую подвздошную область. Нередко такое явление трактуется как «классический Кохеровский» вариант острого аппендицита, что ведет к серьезной диагностической ошибке.
При внимательном клиническом анализе состояния больного в периоде «мнимого благополучия» достаточно четко выявляются клинические признаки развивающегося перитонита. Появляются симптомы развивающегося пареза кишечника, общей интоксикации: тошнота,
рвота, учащение пульса, повышение температуры тела, снижение артериального давления. Перкуторно определяется тимпанит над вздутыми петлями кишечника и притупление перкуторного звука в отлогих областях брюшной полости. Период «мнимого благополучия» продолжается в среднем 8-12 ч и без четких временных границ переходит в третий период, характеризующийся типичными признаками разлитого перитонита. Состояние больного вновь ухудшается. У больного заостряются черты лица, глаза западают, кожа лица бледнеет, покрывается холодным потом. Губы становятся сухими и трескаются. Язык сухой, обложен грязнокоричневым налетом, иногда покрыт корочками. Психоэмоциональное состояние больных в периоде перитонита чаще всего подавленное, у некоторых наступает эйфория, у части - возбуждение с явлениями неадекватной оценки своего состояния и поведения. Боли становятся мучительными, появляется выраженное вздутие живота, а напряжение брюшной стенки почти не определяется. При аускультации кишечные шумы не выслушиваются. Перкуторно по мере накопления выпота увеличивается площадь притупления перкуторного звука в отлогих местах живота. Отмечаются задержка газов, отсутствие стула. Со стороны сердечно-сосудистой системы по мере развития перитонита отмечается учащение пульса на фоне прогрессирующей артериальной гипотонии. N.B. Следует помнить, что клиническая картина прободных гастродуоденальных язв может варьировать в зависимости от многих причин: времени от начала перфорации, возраста, реактивности организма, сопутствующих заболеваний, анатомического варианта перфорации в свободную брюшную полость, сальниковые сумки, забрюшинное пространство, соседние полые органы, а также варианта прикрытой перфорации, величины прободного отверстия гастродуоденальной стенки.
Атипичные перфорации
Клиническая картина атипичных вариантов и прикрытых гастродуоденальных перфораций существенно отличается от перфораций в свободную брюшную полость. Одним из вариантов атипичной перфорации может быть перфорация гастродуоденальной язвы в забрюшинную клетчатку. Диагностика таких перфораций представляет серьезные трудности. Чаще это касается язв, располагающихся на задней стенке двенадцатиперстной кишки или в кардиальном отделе желудка, то есть язв в местах, не прикрытых брюшиной.
Перфорация язвы задней стенки двенадцатиперстной кишки в забрюшинную клетчатку встречается крайне редко. Как правило, этот вид
перфорации проявляется внезапным возникновением резких болей в эпигастральной области, иррадиирующих в спину, повышением температуры. Затем боли в эпигастральной области уменьшаются и приобретают постоянный характер в поясничной области. Быстро развивающаяся забрюшинная флегмона манифестирует клинической картиной гнойно-септического заболевания. При объективном обследовании обнаруживается болезненная припухлость справа от позвоночника на уровне Th X-Th XII. Нередко здесь же обнаруживается локальная или распространенная крепитация. Часто при объективном обследовании больных с атипичной перфорацией язвы задней стенки двенадцатиперстной кишки остается незамеченным весьма характерный для этого вида перфораций симптом локальной подкожной эмфиземы в области пупка вследствие распространения газа по круглой связке печени - симптом Вигиацо. Достаточно часто при перфорации язв кардиального отдела желудка можно наблюдать появление подкожной эмфиземы в области левой половины грудной клетки, шеи, лица, реже мошонки - симптом Кораха, а также появление подкожной эмфиземы в левой подключичной области - симптом Подлаха.
Отсутствие язвенного анамнеза создает колоссальные трудности в постановке правильного диагноза, так как клинические проявления атипичных перфораций часто могут быть слабо выражены.
N.B. Необходимо помнить, что мнение об отсутствии язвенного анамнеза у большей части больных с перфорацией отражает не истинную частоту «немых» язв, а частоту неумело собранных анамнестических данных.
Прикрытые перфорации
Прикрытые перфорации встречаются в 5-8% случаев всех перфораций и считаются наиболее благоприятным вариантом осложненного течения язвенной болезни. Чаще всего прикрытая перфорация наблюдается при локализации язв на передней стенке двенадцатиперстной кишки или передней стенке желудка. Прикрытая перфорация наблюдается в тех случаях, когда перфоративное отверстие в силу тех или иных обстоятельств может вскоре после образования «прикрыться»: участком сальника, стенкой соседнего органа, петлей кишки, остатками непереваренной пищи. В этих случаях в брюшную полость попадает незначительное количество желудочного содержимого, или оно не изливается совсем. Именно на этом основан консервативный метод лечения перфоративной язвы - метод Тейлора.
Клиническая картина прикрытой перфорации имеет ряд особенностей и нередко представляет значительные диагностические трудности. Начало периода прободения ничем не отличается от обычной клинической картины прободной гастродуоденальной язвы. Момент перфорации клинически проявляется «классическим» болевым синдромом в эпигастральной области (симптом Дьелафуа). Иногда боли носят менее выраженный характер и быстро проходят. Несмотря на то что вся картина остро протекающего процесса перфорации постепенно стихает, достаточно долго сохраняется выраженная болезненность в эпигастральной области и нечетко выраженный локально сохраняющийся симптом Щеткина-Блюмберга. Характерной клинической особенностью прикрытых гастродуоденальных перфораций служит стойкое, длительно сохраняющееся напряжение мышц брюшной стенки (симптом Ратнера) в правом верхнем квадранте живота, соответствующее чаще расположению прободной язвы. Самой частой причиной диагностических ошибок при прикрытых гастродуоденальных перфорациях становится позднее обращение больных за медицинской помощью. В этих случаях прикрытые перфорации часто принимают за обострение язвенной болезни. Нередко при быстром стихании болевого синдрома клиническая картина принимает форму вялотекущего локального воспалительного процесса. Местный отграниченный перитонит редко заканчивается самоизлечением. Чаще исходом недиагностированной прикрытой перфорации становятся ограниченные абсцессы или разлитой гнойный перитонит.
Перфорация гастродуоденальной язвы в полые органы представляет вид образования межорганных внутрибрюшных свищей. Встречаются такие перфорации крайне редко. Клинические проявления таких перфораций не имеют четко очерченных симптомов. Чаще клинические проявления перфораций с образованием межорганных свищей анамнестически могут указывать на наличие язвенной болезни. Как правило, прободению гастродуоденальной язвы в соседние полые органы (желчный пузырь, поперечную ободочную кишку) предшествуют клинические признаки хронической пенетрирующей язвы. Для пенетрации наиболее характерными клиническими признаками являются упорные, нередко интенсивные боли в эпигастральной области с иррадиацией в ту или иную область, характерную для поражения соседнего органа.
Болевой синдром для периода прободения стенки соседнего органа, куда пенетрировала гастродуоденальная язва, нехарактерен. Наиболее серьезную ситуацию перфорации гастродуоденальной язвы в результате пенетрации представляет образование желудочно-ободочного свища.
Клиническая картина образования желудочно-ободочной фистулы весьма характерна. Как правило, больные отмечают уменьшение или даже полное исчезновение наблюдавшихся болей и появление синдрома диареи, не поддающегося проводимой медикаментозной терапии. Частота стула нередко доходит до 10-15 раз в сутки и более. Отмечается прогрессирующая потеря массы тела, нередко достигающая 40-60%. Появление калового запаха изо рта и отрыжки с каловым запахом свидетельствует о попадании каловых масс и газов из кишечника в желудок. Как правило, отмечаются серьезные нарушения водно-электролитного и белкового обмена. Вследствие прогрессирующего похудания у больных появляются безбелковые отеки, иногда асцит, гидроторакс, анасарка.
При объективном обследовании таких больных обращает на себя внимание бледность и сухость кожного покрова, приобретающего землистый оттенок, снижение его тургора и эластичности. Отмечается также отечность и пастозность нижних конечностей. Кишечные перистальтические шумы нередко слышны на расстоянии.
Основным методом в диагностике перфорации гастродуоденальных язв в полые органы служит контрастное рентгенологическое исследование. Попадание контрастного вещества из желудка в желчный пузырь, ободочную или тонкую кишку свидетельствует о наличии желудочноорганного или дуоденально-органного свища.
Нередко с серьезными диагностическими трудностями сталкиваются при диагностике прободных гастродуоденальных язв у детей, подростков и пожилых людей.
Течение перфоративных гастродуоденальных язв у лиц пожилого и старческого возраста отличается значительной стертостью клинических симптомов. По литературным данным, более чем у 50% больных отсутствует кардинальный симптом перфорации гастродуоденальной язвы - внезапное появление «кинжальной» боли в животе (симптом Дьелафуа). У пожилых лиц отмечается постепенное нарастание этой боли. Нередко клиническая картина перфорации гастродуоденальной язвы у пожилых людей манифестирует появлением болевого синдрома в эпигастральной области с последующей локализацией его в правой подвздошной области. Достаточно часто напряжение мышц передней брюшной стенки в эпигастральной области бывает гораздо менее выраженным, чем в правой подвздошной области, что и становится при поверхностно собранном анамнезе и объективном обследовании больного причиной серьезных диагностических ошибок. Ряд авторов, аргументируя высокую частоту стертого течения перфоративных гастродуоденальных язв у пожилых пациентов, приводят данные о высокой частоте (до 41,2%)
прикрытых перфораций именно у этой категории больных. Сам факт высокой частоты прикрытых перфораций гастродуоденальных язв у пожилых больных свидетельствует об атипичности течения этой патологии, клинической стертости и поздней обращаемости данного контингента пациентов за медицинской помощью.
Клиническое течение прободных гастродуоденальных язв в детском и юношеском возрасте, так же как и у пожилых лиц, имеет ряд существенных особенностей. В первую очередь это относится к периоду течения язвенной болезни, предшествующему перфорации. Чаще всего заболевание до перфорации протекает совершенно бессимптомно или с клиническими симптомами, не привлекающими к себе внимания больных. При более тщательном сборе анамнеза у пациентов с бессимптомным течением заболевания удается, как правило, выявить клинические признаки, характерные для торпидного течения язвенной болезни. У лиц детского и юношеского возраста нередко удается установить за несколько дней до прободения язвы весьма характерный клинический признак - появление продромальных явлений в виде болевого синдрома в эпигастральной области, потери аппетита, диспепсических симптомов (изжога, отрыжка, повышенная саливация, тошнота, иногда рвота).
Большинство авторов указывают на то, что болевой синдром у лиц детского и юношеского возраста при прободении гастродуоденальных язв носит менее выраженный характер по сравнению со взрослыми. Боль появляется внезапно, не имеет «кинжального» характера, локализуется в эпигастрии и часто иррадиирует в плечо, лопатку, шею (симптом Элекера). Сглаженность болевого синдрома большинство авторов объясняют преобладанием прободения в этом возрасте язв двенадцатиперстной кишки. Поступающее в брюшную полость щелочное дуоденальное содержимое вызывает гораздо меньшее раздражение рецепторов брюшины. Отсюда и менее выраженные явления абдоминального шока, напряжения мышц брюшной стенки, тяжести общего состояния больного.
N.B. Редкость наблюдений перфоративных гастродуоденальных язв у детей и подростков считается одним из серьезных факторов риска диагностических ошибок.
Клиническая картина перфоративных гастродуоденальных язв может считаться классическим примером в развитии триады клинических признаков острой патологии органов брюшной полости. Выраженность напряжения брюшной стенки, болезненности, симптомов раздражения брюшины зависит в первую очередь от сроков с момента перфорации (стадии течения заболевания). Фазность развития клинической картины
перфорации гастродуоденальных язв ярчайшим образом характеризует не только клиническую картину этого грозного осложнения язвенной болезни, но и темпы развития воспалительной реакции брюшины.
Перфоративные гастродуоденальные язвы - патология, демонстрирующая один из самых ярких вариантов последовательности развития «пожара обмена» на уровне морфологического и биохимического единства структуры и функции. В диагностике перфоративных гастродуоденальных язв (как, впрочем, и других заболеваний) не должны присутствовать понятия второстепенной значимости тех или иных жалоб, анамнеза заболевания, жизни, общего состояния больного и локальных клинических проявлений остро развивающегося воспалительного процесса в брюшной полости. Клиническая картина перфоративных гастродуоденальных язв демонстрирует важность тщательного анализа всех звеньев как клинико-анамнестической, так и лабораторно-инструментальной диагностики. В жалобах, анамнезе заболевания и жизни, общих и локальных клинических признаках заболевания целесообразно выделить спектр главных и побочных симптомов.
Жалобы
В абсолютном большинстве случаев (по данным разных авторов, от 96,6 до 98%) основными жалобами, предъявляемыми пациентами в первые 6 ч с момента заболевания, были жалобы на внезапную острую боль в животе (симптом Дьелафуа). Иногда (около 17%) пациенты предъявляют жалобы на иррадиацию болей в правое надплечье, лопатку, ключицу (при перфорации язвы, расположенной в пилородуоденальной зоне) или левую (при язве дна или тела желудка) (симптом Элекера). Достаточно частой жалобой, предъявляемой больными с перфоративными гастродуоденальными язвами, но нередко оставляемой без должного внимания, становится жалоба на сильную жажду и сухость во рту. Нередко именно жалобы на жажду и сухость слизистых оболочек, развивающуюся из-за нарастающей интоксикации, связанной с перитонитом и шоком, - основные жалобы, предъявляемые больными с перфоративными гастродуоденальными язвами. Жалобы на рвоту, задержку газов и стула непостоянны, характерны больше для поздних сроков заболевания и требуют при сборе анамнеза заболевания внимания, акцентированного на длительности болевого синдрома с момента появления острых болей.
Anamnesis morbi
Выяснение в анамнезе заболевания данных о продолжительности болевого синдрома позволяет в определенной мере оценить особенности
клинических проявлений, характерных для того или иного периода заболевания. Часто у больных, поступивших в стационар позже 6 ч с момента заболевания (период «мнимого благополучия») именно сведения о продолжительности болевого синдрома и субъективное улучшение состояния, отмечаемое больными, позволяют избежать диагностической и тактической ошибки. Указания больных на желудочный дискомфорт или наличие язвенной болезни, даже при атипичной клинической картине заболевания, должны ориентировать врача на исключение в первую очередь перфоративной гастродуоденальной язвы. Нередко выяснение язвенного анамнеза, позволяющего с высокой степенью достоверности поставить правильный диагноз у таких больных, затруднено из-за тяжести их состояния. Указания больных на разлитой характер болей в животе, сопровождающихся тошнотой и рвотой, свидетельствует о развитии перитонита и общей интоксикации. Если пациента доставляют в стационар позже 10-12 ч с момента перфорации язвы, часто возникают большие трудности при установлении диагноза. N.B. При выяснении анамнеза заболевания нельзя забывать, что у больных пожилого и старческого возраста нередко отсутствует симптом внезапного возникновения резких болей, а также и то, что у большей части этих больных отсутствует язвенный анамнез.
Все это представляет серьезные трудности в клинической диагностике перфоративных гастродуоденальных язв у этой категории больных.
Anamnesis vitae
Основное внимание при выяснении анамнеза жизни в алгоритме диагностики у больных с клинической картиной перфорации гастродуоденальной язвы должно быть обращено на выяснение язвенного анамнеза. Получение от больного анамнестических сведений о выявляемых ранее заболеваниях желудка и двенадцатиперстной кишки при клинико-инструментальном исследовании имеет важное диагностическое значение. Нельзя забывать о том, что ряд возможных сопутствующих заболеваний у больных с перфоративной гастродуоденальной язвой требует серьезной предоперационной коррекции с привлечением врачей смежных специальностей.
Status praesens communis
Общее состояние и клиническая картина больного перфоративной гастродуоденальной язвой зависят от стадии течения заболевания и степени распространенности перитонита. В первые часы перфорации (стадия шока - 6-8 ч) при осмотре обращает на себя внимание вынужденное
положение больных (на спине или правом боку) с приведенными к туловищу коленями; пациенты избегают малейшего движения. Часто больные стараются держать руки на животе в эпигастральной области, надавливая на брюшную стенку. Больной бледен, безучастен, на вопросы отвечает нехотя, шепотом. Лицо больного выражает страх и страдание. Кожный покров бледный, покрыт холодным липким потом, губы цианотичные, конечности холодные на ощупь. Обращает на себя внимание тип дыхания этих больных. Почти всегда можно наблюдать на вдохе происходящее одновременно с подъемом грудной клетки втяжение напряженной брюшной стенки. Это так называемый извращенный торакоабдоминальный ритм - симптом Бейли. Дыхание частое, поверхностное, нередко со стоном. Пульс часто замедлен (симптом Грекова), удовлетворительного наполнения. Артериальное давление нормальное или несколько снижено. Температура тела нормальная.
В период «мнимого благополучия» (последующие 8-10 ч) субъективное улучшение становится фактором высокой вероятности диагностической ошибки. Самочувствие несколько улучшается в связи с уменьшением боли в животе, что связано с парезом нервных окончаний брюшины. Больные, как правило, несколько эйфоричны. Дыхание становится более глубоким, но частым, живот в акте дыхания участия не принимает. Нередко можно отметить появление умеренного метеоризма в связи с парезом кишечника. Учащение пульса, повышение температуры, появление тошноты и рвоты свидетельствуют о нарастании признаков перитонита и общей интоксикации.
В периоде перитонита состояние больного прогрессивно ухудшается и становится крайне тяжелым, угрожающим жизни. Больные, как правило, заторможены, в контакт вступают с трудом. Кожа лица мертвенно-бледная, с синюшным оттенком, заострившиеся черты лица с глубоко запавшими тусклыми глазами. Отмечается появление мучительной гримасы - лица Гиппократа. Изменяется характер дыхания. Оно становится частым, иногда появляется раздувание крыльев носа. Изменение характера дыхания связано с высоким стоянием диафрагмы и выраженным парезом кишечника. В этой стадии паралич кишечника может выступать как одно из важных звеньев патологического процесса, играя ведущую роль в нарастании эндотоксикоза и являясь одной из причин высокой летальности. Со стороны сердечно-сосудистой системы отмечаются явления нарастающей сосудистой недостаточности. Пульс становится частым, малого наполнения, отмечается тенденция к неуклонному падению артериального давления.
Status praesens localis
Яркость выявляемых при физикальном обследовании симптомов перфоративной гастродуоденальной язвы зависит в первую очередь от локализации места перфорации, распространенности воспалительного процесса и инфицирования брюшины.
Одним из первых симптомов, выявляемых при визуальном осмотре и обнаруживаемом при пальпации, становится симптом напряжения мышц брюшной стенки. Ладьевидно втянутая в эпигастральной области брюшная стенка приобретает доскообразную ригидность. Ригидность эта бывает настолько сильно выражена, что у худых пациентов можно увидеть сегментарность рельефа прямых мышц живота и межмышечных перемычек (inscriptiones tendineae) - симптом Дзбановского-Чугуева. Гораздо реже (чаще при атипичных прикрытых перфорациях гастродуоденальных язв и достаточно длительном периоде со времени перфорации) можно обнаружить смещение пупка и белой линии живота в сторону ограниченного патологического воспалительного процесса - симптом Котена-Майера, обусловленного длительным локальным напряжением мышц брюшной стенки над областью локализации патологического процесса.
N.B. Нельзя забывать, что у лиц пожилого возраста с дряблой и атрофич-
ной брюшной стенкой ригидность мышц выражена, как правило, слабо, а
нередко вовсе не обнаруживается.
При аускультации брюшной полости у больных перфоративными гастродуоденальными язвами можно выявить ряд характерных клинических симптомов. Нередко в первые часы шокового периода заболевания при аускультации, проводимой в сидячем положении больного, удается услышать металлический шум трения над XII ребром слева, обусловленный выходом пузырьков воздуха в поддиафрагмальное пространство - симптом Бреннера. Иногда удается также выслушать шум трения над реберной дугой - симптом Бруннера. Значительно реже выявляется симптом Гефтера-Щипицына, характерный для перфораций с образованием значительных дефектов гастродуоденальной стенки и излиянием в брюшную полость значительного количества желудочного содержимого. На более поздних стадиях заболевания аускультация брюшной полости позволяет выявить ряд признаков триады Гюстена, характерных для перфорации гастродуоденальных язв:
> распространение сердечных тонов через растянутую брюшную стенку до уровня пупка. Феномен обусловлен резонирующими свойствами свободного воздуха усиливать звукопроводность;
> нередко удается выслушать перитонеальное трение в области реберной дуги или эпигастральной области, напоминающее шум трения плевры;
> выслушиваемый в эпигастральной области на вдохе металлический звон обусловлен выходом из желудка через перфорационное отверстие в окружающую жидкость свободного газа.
Перкуторно в абсолютном большинстве случаев можно выявить характерные для раздражения брюшины симптомы Менделя и Раздольского. Перкуторное обследование позволяет выявить также наличие свободного газа в брюшной полости. О наличии пневмоперитонеума свидетельствует исчезновение печеночной тупости и появление высокого тимпанита над печенью - симптом Спижарного-Кларка.
Пальпация живота у больных перфоративными гастродуоденальными язвами вызывает резкое усиление болевого синдрома. Выраженность симптома Щеткина-Блюмберга зависит от вида перфорации: в свободную брюшную полость, в забрюшинное пространство или атипичная прикрытая перфорация. При перфорации язвы в свободную брюшную полость симптом Щеткина-Блюмберга носит всегда ярко выраженный характер. Весьма характерным симптомом, выявляемым при перфоративных гастродуоденальных язвах, становится симптом Крымова - усиление боли и болезненность при обследовании области пупочного кольца кончиком пальца. Иногда при нежной поверхностной пальпации передней брюшной стенки в эпигастральной области удается ощутить легкие толчки газов, проникающих в брюшную полость через прободное отверстие гастродуоденальной стенки - симптом Юдина- Якушева.
При пальцевом обследовании per rectum достаточно часто выявляется болезненность передней стенки прямой кишки в области дугласова пространства - симптом Куленкампфа - вследствие скопления желудочного содержимого и перитонеального экссудата.
Несмотря на то что для постановки правильного диагноза большое значение имеет правильно и тщательно собранный анамнез, клинико-лабораторные и инструментальные методы исследования служат методами, дающими прямое или косвенное подтверждение наличия перфоративной гастродуоденальной язвы.
Важную роль в установлении диагноза перфоративной гастродуоденальной язвы играют рентгенологическое, эндоскопическое, ультразвуковое исследования брюшной полости. Использование всего комплекса диагностических (в особенности инвазивных) методов исследования при перфорации гастродуоденальных язв, конечно же, не является
диагностической доктриной и требуется лишь в случаях исключительной трудности постановки диагноза и выбора лечебной тактики.
Лабораторно-инструментальное исследование
Лабораторная диагностика при типичной клинической картине не вносит существенных корректив в постановку диагноза. При любом варианте перфорации гастродуоденальных язв в период шока отмечается умеренный лейкоцитоз с нейтрофильным сдвигом. В периоде «мнимого благополучия» и перитонита отмечается высокий лейкоцитоз, сдвиг формулы белой крови влево до юных форм и миелоцитов, снижение количества лимфоцитов, моноцитов, эозинофилов, нарастание СОЭ и индекса лейкоцитарной интоксикации Кальф-Калифа. Повышение лейкоцитарного индекса интоксикации выше 1,5 усл.ед. свидетельствует о присоединении бактериального компонента в процессе эндогенной интоксикации развивающегося перитонита.
Рентгенологическое исследование
В большинстве случаев (до 90%) обзорной рентгеноскопии или рентгенографии брюшной полости бывает вполне достаточно для подтверждения клинического диагноза перфоративной гастродуоденальной язвы. Рентгенологическое исследование, предпринимаемое для обнаружения пневмоперитонеума, при наличии которого диагноз перфоративной язвы в сочетании с характерной клинической картиной становится бесспорным, служит основным методом диагностики перфоративных гастродуоденальных язв. Частота выявляемого пневмоперитонеума колеблется в широких пределах: от 42 до 85%. Чаще наличие свободного газа в брюшной полости обнаруживается под правым куполом диафрагмы в виде серповидной полоски шириной 3-7 см, расположенной между диафрагмой и печенью. Гораздо реже скопление свободного газа выявляется в левой поддиафрагмальной области. Обнаружение свободного газа в брюшной полости, как правило, свидетельствует о наличии перфорации полового органа. Сочетание перкуторного исчезновения печеночной тупости и обнаружения свободного газа в поддиафрагмальных пространствах брюшной полости при рентгенологическом исследовании можно считать патогномоничным признаком перфорации гастродуоденальных язв. Отсутствие сочетания этих клинических симптомов не всегда свидетельствует об отсутствии перфорации. Если свободный газ при обследовании больного в вертикальном положении в брюшной полости не определяется, в ряде случаев газ определяется при латероскопии.
N.B. При этом необходимо помнить, что наличие свободного газа в брюшной полости между передней поверхностью печени, диафрагмой и передней брюшной стенкой может симулировать интерпозиция толстой кишки -синдром Чилайдити.
При исследовании больного в положении на правом боку можно обнаружить возникающую за счет имеющегося в брюшной полости свободного газа деформацию дугообразного контура желудка - симптом Юдина.
Пневмогастрография
Пневмогастрография, несмотря на то что в последнее время используется в диагностике перфоративных гастродуоденальных язв гораздо реже, не утратила своей диагностической значимости. Принудительное введение воздуха в желудок с последующей рентгенографией может использоваться в случаях обоснованного подозрения на прободную язву. Для этого в желудок через тонкий желудочный зонд вводят 400-500 мл3 воздуха, производят обзорную рентгенографию. Обнаружение свободного газа в брюшной полости свидетельствует о наличии перфорации гастродуоденальной стенки.
Наличие в арсенале диагностических средств фиброгастродуоденоскопа позволяет изменить алгоритм инструментальных диагностических исследований. Сама по себе ФЭГДС дает прямое подтверждение наличия прободной гастродуоденальной язвы при ее визуальном обнаружении. Однако в ряде случаев визуализировать язвенный локус со стороны слизистой гастродуоденальной оболочки не удается. В этих случаях отрицательное заключение об отсутствии перфорации не должно служить аргументом для отказа от рентгенологического исследования. Производимые при ФЭГДС инсуфляция воздуха и последующая обзорная рентгенография брюшной полости становятся, по сути, вариантом пневмогастрографии, позволяющим с высокой степенью достоверности диагностировать варианты перфорации гастродуоденальных язв.
Высокая степень достоверности рентгенологической диагностики перфорации гастродуоденальных язв отмечается при использовании методов контрастной гастрографии и метода двойного гастродуоденального контрастирования.
Контрастная гастрография
Метод осуществляется введением в желудок с помощью желудочного зонда или приемом per os 40-60 мл водорастворимого контрастного вещества (кардиотраст, урографин, верографин). После этого производят полипозиционное рентгенологическое исследование (чаще
латероскопию на правом и левом боках). Обнаружение затекания контрастного вещества в область правого латерального канала, в подпеченочное пространство, обнаружение его следов в забрюшинном пространстве свидетельствует о прободении гастродуоденальной язвы.
Ультразвуковое исследование
Является методом непрямой визуализации вторичных признаков перфорации полых органов. Обнаружение в брюшной полости свободной жидкости и свободного газа служит косвенным признаком перфорации полого органа.
Лапароскопия
Из инвазивных методов диагностики перфоративных гастродуоденальных язв в настоящее время широкое распространение получил метод лапароскопии. Выполнение лапароскопии при подозрении на перфорацию гастродуоденальной язвы позволяет не только визуализировать анатомический вариант перфорации гастродуоденальной стенки, но и, по мере обнаружения перфорации, выполнить лапароскопическое ушивание перфоративного дефекта.
Лапароскопическая картина прободных гастродуоденальных язв характеризуется обнаружением признаков воспалительных изменений гастродуоденальной стенки в области перфорации, а также в соседних органах (сальник, печень, желчный пузырь). Обнаружение слизеподобного мутного выпота с признаками желудочного содержимого, желчи свидетельствует о наличии перфорации гастродуоденальной язвы. Как правило, при лапароскопии обнаруживается картина изменения обычного анатомического соотношения органов в зоне перфорации. Чаще всего над областью перфоративного дефекта гастродуоденальной стенки обнаруживается участок рыхло спаянного с ней инфильтрированного и отечного сальника.
Лапароцентез
Как метод диагностики перфорации гастродуоденальных язв лапароцентез до настоящего времени не утратил своего клинического значения. Хотя диагностическая ценность данного метода уступает методам визуальной диагностики, использование его в условиях отсутствия технических возможностей применения других инструментальных методов необходимо признать вполне оправданным. Опасность развития осложнений при использовании данного метода диагностики при подозрении на перфорацию гастродуоденальной язвы не превышает диагностическую эффективность исследования. Простота и доступность выполнения
лапароцентеза при отсутствии других технических возможностей диагностики, становится основным показанием к выполнению данного метода исследования при подозрении на перфорацию гастродуоденальной язвы. Техника выполнения лапароцентеза сводится к троакарной пункции передней брюшной стенки, выполняемой на 2-3 см ниже пупка. После прокола брюшной стенки тубус троакара направляется в правое подреберье. Через тубус троакара в брюшную полость вводится перфорированная полихлорвиниловая трубка, через которую при подтягивании ее из брюшной полости аспирируется экссудат. При сомнениях в характере экссудата используют диагностическую пробу с 10% йодной настойкой (проба И.И. Неймарка). К 2-3 мл экссудата, полученного из брюшной полости, добавляют несколько капель йодной настойки. При наличии в экссудате желудочного содержимого под воздействием йодной настойки она приобретает грязно-синюю окраску (из-за наличия остатков крахмала в желудочном содержимом).
Вариантом диагностики при лапароцентезе может считаться проба с приемом 200-300 мл жидкости, окрашенной метиленовой синью (Эванса). Появление окрашенного экссудата становится абсолютным доказательством наличия перфорации гастродуоденальной стенки.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПРОБОДНОЙ ЯЗВЫ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
Острый панкреатит
Тесное топографо-анатомическое расположение желудка, двенадцатиперстной кишки и поджелудочной железы - одно из условий затруднительной диагностики заболеваний указанных органов. Сложности в диагностике обусловлены еще и тем, что, как правило, изолированного поражения одного органа при какой-либо патологии не происходит, а наблюдается содружественное вовлечение их в патологический процесс с соответствующими клиническими проявлениями. Наиболее сложными при проведении дифференциальной диагностики становятся случаи прикрытой прободной язвы при быстрой блокаде прободного отверстия кусочком пищи изнутри или прилежащими органами и фибрином, при которых классическая картина прободной язвы может быть весьма искажена.
Жалобы
Наиболее ярким проявлением прободной гастродуоденальной язвы служит острая «кинжальная» боль в эпигастрии - симптом Дьелафуа. При остром панкреатите болевые ощущения в большинстве случаев менее выражены. Не следует забывать, что при этом заболевании в ряде случаев боль может быть настолько интенсивной, что доводит пациента до коллапса. Отличительным признаком боли при остром панкреатите становится опоясывающий характер. При прободной язве рвота бывает только у 10% больных, а при остром панкреатите рвота многократная, встречается значительно чаще (более чем у 70% больных).
Anamnesis morbi
Из анамнеза заболевания устанавливается факт, что возникновению острого панкреатита способствовал прием алкоголя, обильной жирной, острой пищи. В качестве этиологического фактора может выступать и обострение желчнокаменной болезни, хронического холецистита. Возникновению прободения язвы предшествуют: обострение язвенной болезни, обильный прием пищи и/или алкоголя, рвота, внезапное повышение внутрибрюшного давления.
При остром панкреатите перед болевым синдромом возможны продромальные явления в виде тяжести в надчревной и правой подреберной областях, тошноты, слабости. В большинстве случаев происходит нарастание интенсивности боли. Однако и при остром панкреатите возможно начало заболевания с выраженного болевого синдрома. Прободная гастродуоденальная язва начинается с внезапной острейшей боли в эпигастральной области.
При прогрессировании рассматриваемых заболеваний (без лечения) также можно установить ряд отличительных признаков. У больных острым панкреатитом, как правило, отмечается нарастание субъективных признаков заболевания, в том числе и болевого синдрома. При прободной язве, особенно в случаях ее прикрытия, возможен период стихания болевого приступа (период «мнимого благополучия»).
Anamnesis vitae
Из анамнеза жизни больных острым панкреатитом выясняются характерные признаки: злоупотребление алкоголем, а также наличие желчнокаменной болезни.
Для дифференциальной диагностики прободной гастродуоденальной язвы с острым панкреатитом необходимы сведения об имевшейся в прошлом или имеющейся у больного язвенной болезни. Следует помнить,
что прободная язва часто возникает у лиц молодого возраста; язвенный анамнез у них отсутствует.
Большое значение для диагностики имеет информация о наличии у пациента язвы двенадцатиперстной кишки, пенетрирующей в головку поджелудочной железы.
Status praesens communis
При рассматриваемых заболеваниях состояние чаще всего тяжелое. Следует отметить, что при прободной язве оно прогрессивно ухудшается, при остром панкреатите указанные явления растянуты во времени. Положение больного прободной язвой вынужденное - на спине или на правом боку с приведенными нижними конечностями к животу, при этом даже малейшее движение пациента приводит к резкому усилению боли в животе. Такое положение больного может быть и при остром панкреатите, но тогда изменение положения тела не вызывает серьезных беспокойств.
Состояние кожного покрова и слизистых оболочек при прободной язве в начале заболевания не отличается от таковых при остром панкреатите. При прогрессировании заболевания быстро нарастает сухость языка и слизистых оболочек полости рта. Однако при этой болезни кожный покров может быть с цианотичным оттенком.
При остром панкреатите отмечается увеличение живота за счет вздутия вследствие пареза желудка и поперечной ободочной кишки. При прободной язве живот втянут из-за резкого напряжения мышц брюшной стенки.
Status praesens localis
При обследовании больного острым панкреатитом в начальные сроки заболевания регистрируется только болезненность. При пальпации живота возможно определение инфильтрата по ходу толстой кишки (не следует принимать за защитное напряжение мышц брюшной стенки).
У больных прободной язвой, как ни при одном заболевании, классическая триада признаков острого живота (болезненность, напряжение мышц брюшной стенки и симптомы раздражения брюшины) выявляется фактически во всех случаях.
N.B. Следует помнить, что у пациентов с дряблой брюшной стенкой, находящихся в состоянии алкогольного опьянения, у тучных людей, а также у лиц старших возрастных групп напряжение мышц не выражено.
При прикрытой прободной язве только в самом начале заболевания возможно доскообразное напряжение мышц, а далее оно становится незначительным и локализуется только в правом верхнем квадранте
живота (симптом Ратнера-Виккера). Характерными для прободной язвы служат следующие симптомы: симптом Кларка - исчезновение притупления перкуторного звука над печенью, симптом Спижарного - исчезновение печеночной тупости, высокий тимпанит над печенью. Указанные симптомы при остром панкреатите не определяются.
N.B. Следует помнить, при прикрытой прободной язве количество свободного газа в брюшной полости может быть небольшим или отсутствовать вовсе. Именно поэтому вышеуказанные симптомы могут быть отрицательными.
Лабораторно-инструментальное исследование
При остром панкреатите - ферментемия и ферментурия. Отмечается лейкоцитоз, возможен сдвиг формулы белой крови влево.
У больных прободной язвой при рентгенологическом исследовании определяется свободный газ в брюшной полости. В случаях отсутствия свободного газа - рентгенологический повтор после ФЭГДС. При эндоскопии обнаружение язвенного дефекта в гастродуоденальной стенке. По УЗИ - наличие свободной жидкости в животе. При остром панкреатите при ФЭГДС возможны косвенные признаки воспаления поджелудочной железы. В начале заболевания свободная жидкость в животе не определяется.
Острый аппендицит
При кохеровском или кюммелевском начале острого аппендицита боли локализуются в эпигастральной или околопупочной области, затем охватывают весь живот, а после перемещаются в правую подвздошную область. Указанная миграция болей возможна и при перфоративной язве. Это обстоятельство служит одним из предрасполагающих моментов ошибочной диагностики указанных заболеваний.
Жалобы
При остром аппендиците, как указано выше, боль в начале заболевания может быть в надчревье, а затем перемещаться в правую подвздошную область. Следует отметить, что при ее локализации уже в правой подвздошной области болевые ощущения в эпигастрии незначительные или вовсе отсутствуют. Следующей особенностью боли становится то, что при прободной гастродуоденальной язве уже с самого начала заболевания характерен резчайший болевой синдром («кинжальная» боль).
Рвота при остром аппендиците одноили двукратная, бывает более чем у 50% пациентов. При прободной язве она тоже однократная, но встречается реже (до 10%).
Anamnesis morbi
Острый аппендицит возникает на фоне полного здоровья. В большинстве случаев в начале заболевания боли незначительные, по мере прогрессирования воспалительного процесса они нарастают. При прободной гастродуоденальной язве началу заболевания часто предшествует желудочный дискомфорт (изжога, отрыжка, тяжесть и тупые боли в эпигастральной области). Отличительным признаком становится и то, что при перфорации язвы уже в начале заболевания боли очень интенсивные («кинжальные»), и пациент с точностью до минут указывает момент их появления.
Anamnesis vitae
У больных острым аппендицитом в анамнезе жизни нет указаний на какие-либо предрасполагающие заболевания или жизненные обстоятельства, тогда как у пациентов с перфоративной язвой возможно установление желудочного анамнеза, а также ситуаций, сопровождающихся возможным внезапным повышением внутрибрюшного давления.
Status praesens communis
При остром аппендиците общее состояние пациентов страдает мало, особенно в начале заболевания. Кожный покров и видимые слизистые оболочки не изменены. Положение больного вынужденное, с приведенными к животу коленями.
При перфоративной гастродуоденальной язве в абсолютном большинстве случаев состояние больных тяжелое уже в начале заболевания. Больной бледен, с легким цианозом губ, покрыт холодным липким потом, отмечается сухость слизистых оболочек и языка. Положение в постели вынужденное, с приведенными к животу коленями. Дыхание поверхностное, редкое, живот в акте дыхания не участвует, передняя брюшная стенка ладьевидно втянута, доскообразно напряжена.
Status praesens localis
При остром аппендиците классическая триада признаков острого живота (болезненность, напряжение мышц брюшной стенки и симптомы раздражения брюшины) выявляется в большинстве (более 70%) случаев. При прободной гастродуоденальной язве указанные признаки
присутствуют почти у всех больных, причем с максимальной степенью выраженности. Особенностью становится еще и то, что при пальпации живота больных острым аппендицитом эти симптомы выявляются в правой подвздошной области, тогда как при перфоративной язве - в эпигастральной области или по всему животу.
Достаточно часто у больных перфоративной язвой при перкуссии определяется исчезновение печеночной тупости (симптом Спижарного).
Лабораторно-инструментальное исследование
Патогномоничный рентгенологический признак перфоративной гастродуоденальной язвы - обнаружение в правой поддиафрагмальной области свободного газа. При перфоративном аппендиците обнаружение свободного газа в брюшной полости считается казуистической редкостью.
Острый холецистит
Диагностика перфорации гастродуоденальной язвы в свободную брюшную полость не представляет серьезных проблем, и проведение дифференциальной диагностики с острым холециститом требуется крайне редко. Диагностика же атипичных форм (прикрытой перфорации, перфорации в сальниковую сумку и др.) представляет достаточно серьезную дифференциально-диагностическую задачу. Чаще всего прикрытая перфорация наблюдается при локализации язв на передней стенке двенадцатиперстной кишки или передней стенке желудка. В этих условиях клиническая картина не столь яркая, а локализация боли и болезненности может быть не только и не столько в эпигастральной, сколько в правой подреберной области.
Ниже рассматриваются дифференциальные признаки при указанном варианте течения прободной гастродуоденальной язвы.
Жалобы
Основная жалоба больных при рассматриваемых заболеваниях - боль в правом подреберье. Однако следует помнить, что боль при прободной язве вне зависимости от варианта течения возникает внезапно, отличается высокой интенсивностью с самого начала заболевания. При остром холецистите в большинстве случаев она все же нарастает постепенно, и больные могут ее терпеть достаточно продолжительное время. При остром холецистите в начальные сроки боль, как правило, носит приступообразный (из-за камней в желчном пузыре) характер.
При остром холецистите нередко наблюдается многократная рвота, при прободной язве она однократная и встречается крайне редко (до 10%).
Anamnesis morbi
При атипичных формах прободной язвы удается установить факт внезапной острейшей боли в эпигастральной области, которая постепенно стихла и стала носить постоянный, тупой, ноющий характер, занимая эпигастральную область и область правого подреберья. Таким образом, в клинической картине прикрытой перфоративной гастродуоденальной язвы можно выявить период типичной клинической картины перфорации и период стихания и даже полного исчезновения симптомов перфорации. Не следует забывать, что прободению язвы может предшествовать обострение (в случаях ее наличия) язвенной болезни, нарушение диеты, в частности прием больших доз алкогольных напитков.
У больных острым холециститом следует установить факт камненосительства и обострения хронического холецистита, а также выявить провоцирующие агенты (обильный прием жирной, острой, пряной пищи), предшествовавшие заболеванию.
Anamnesis vitae
Язвенный анамнез, даже в виде «малых» признаков желудочного дискомфорта при прикрытых перфорациях, служит важным анамнестическим признаком атипичной формы перфоративной гастродуоденальной язвы.
Получение сведений о наличии у больного хронического холецистита (в особенности калькулезного) или язвенной болезни позволяет выбрать наиболее оптимальный алгоритм диагностических исследований и лечебной тактики. Следует определить, имеются ли у пациента неоднократно повторяющиеся болевые приступы в правом подреберье, имеющие четкую взаимосвязь с погрешностями в диете, с нервными расстройствами, физическим напряжением. Их наличие служит веским основанием для исключения прободной гастродуоденальной язвы.
Status praesens communis
Общее состояние больных острым холециститом по сравнению с прободной язвой (даже прикрытой) страдает меньше. В старших возрастных группах при позднем поступлении в клинику оно может существенно нарушаться. Нередко при выраженном болевом синдроме пациенты с острым калькулезным холециститом ведут себя беспокойно, часто меняют положение в постели.
Общее состояние больных с прикрытыми перфорациями гастродуоденальных язв часто остается средней тяжести и даже удовлетворительным. При внимательном наблюдении за больными с прикрытыми перфорациями гастродуоденальных язв можно отметить некоторую медлительность в движениях, осторожность в перемене положения тела в постели. При осмотре можно отметить незначительное отставание верхних отделов живота в акте дыхания.
Status praesens localis
Для острого холецистита наиболее характерна болезненность в правой подреберной области, особенно в точке проекции желчного пузыря; также выявляется ряд характерных симптомов (Ортнера, Кера, Боаса, Мерфи, Мюсси-Георгиевского, Лепене). В начале заболевания защитного напряжения мышц брюшной стенки, как правило, не бывает.
При прикрытой перфоративной гастродуоденальной язве уже в первые часы заболевания весьма характерным становится стойкое напряжение мышц в правом верхнем квадранте брюшной стенки (симптом Ратнера-Виккера), соответствующее расположению прободной язвы, при удовлетворительном общем состоянии больного. В отличие от острого холецистита при прикрытых перфоративных гастродуоденальных язвах чаще определяются перкуторные симптомы Менделя, Раздольского.
Лабораторно-инструментальное исследование
При лабораторных исследованиях выявляются характерные реакции крови в виде гиперлейкоцитоза со сдвигом лейкоцитарной формулы влево, повышение СОЭ.
Визуальное обнаружение язвенного локуса гастродуоденальной стенки при эндоскопическом исследовании, сопровождающемся инсуфляцией воздуха, даже в случае прикрытой перфорации позволяет при последующем рентгенологическом исследовании обнаружить наличие свободного газа в брюшной полости (чаще в правой поддиафрагмальной области).
Безусловно, важнейшим аргументом в пользу острого холецистита служат признаки воспаления желчного пузыря, особенно при наличии калькулеза, выявленного при УЗИ.
Интраоперационная диагностика
Интраоперационная диагностика типичных гастродуоденальных перфораций не представляет серьезных трудностей. В большинстве случаев диагноз перфоративной гастродуоденальной язвы подтверждается
уже с момента вскрытия брюшины. Нередко, особенно если в процессе диагностики выполнялась ФЭГДС или рентгенопневмография, при рассечении париетальной брюшины можно слышать выхождение газа из брюшной полости. Обнаружение в брюшной полости жидкости зеленовато-серого цвета со слизью и примесью непереваренных фрагментов пищи служит достоверным признаком перфорации гастродуденальной стенки. «Ослизлость» внутрибрюшинного экссудата при прободной гастродуоденальной язве в литературе обозначается как симптом Успенского. Количество обнаруживаемого в брюшной полости экссудата вариабельно и зависит в основном от объема жидкости в желудке в момент перфорации язвы и величины перфоративного отверстия. Иногда жидкость в брюшной полости содержит примесь желчи. Чаще это случается при прободении «низких» постбульбарных дуоденальных язв. Обнаружение перфоративного отверстия на передней стенке желудка и двенадцатиперстной кишки не представляет серьезных технических трудностей. Выявление небольших по величине перфораций («микроперфораций») представляет иногда некоторые трудности. В этих случаях необходимо воспроизвести компрессию желудка путем сдавления его рукой, тогда из визуально не определяемого отверстия начинает выходить газ с жидкостью. Как правило, вокруг таких «микроперфораций» обнаруживаются наслоения фибрина в виде налетов серовато-белого цвета.
N.B. Во время ревизии желудка и двенадцатиперстной кишки необходимо помнить о возможной перфорации задней стенки этих органов, а также о возможности одновременной перфорации двух язв, встречающейся в 0,2-0,5% случаев.
В пользу перфорации задней стенки желудка свидетельствует вытекание желудочного содержимого из отверстия Винслоу и визуально обнаруживаемый пневматоз в полости малого сальника. При обнаружении желто-зеленого пятна на задней париетальной брюшине вокруг двенадцатиперстной кишки (симптом Винивартера), указывающего на перфорацию задней стенки двенадцатиперстной кишки, требуется мобилизация ее по Клерману-Кохеру с тщательной ревизией кишки на протяжении всего внебрюшинного отдела. Элементом обязательной ревизии становится осмотр большой сальниковой сумки. Для исключения атипичных перфораций необходимо обследовать пространство под брыжейкой ободочной кишки, где может быть обнаружена отечность и эмфизема забрюшинной клетчатки.
Таблица к главе 6
Клиническая картина и диагностика прободной язвы желудка и двенадцатиперстной кишки
Симптомы и синдромы перфоративной язвы желудка и двенадцатиперстной кишки
Симптом Бейли (Bailey) (извращенный торакоабдоминальный ритм) - на вдохе брюшная стенка втягивается одновременно с подъемом грудной стенки.
Симптом Берштейна (генитальный симптом) - половой член поворачивается головкой кверху, параллельно брюшной стенке, яички подтягиваются к наружным отверстиям паховых каналов. Возникает в результате рефлекторного сокращения мышцы, поднимающей яичко, и поверхностной фасции живота.
Симптом Бреннера (Brenner) - металлический шум трения, выслушиваемый над XII ребром слева в положении больного сидя, связан с выходом пузырьков воздуха в поддиафрагмальное пространство.
Симптом Бруннера (Brunner) - шум трения под реберной дугой. Возникает в результате воздействия желудочного содержимого на брюшину.
Симптом Вигиацо (Vigyazo) - при перфорации задней стенки двенадцатиперстной кишки подкожная эмфизема может занимать область пупка вследствие распространения газа по круглой связке печени.
Симптом Винивартера (Winiwarter) - желтое пятно на заднем листке париетальной брюшины наблюдается при перфорации внебрюшинного отдела двенадцатиперстной кишки.
Симптом Гефтера-Щипицьша - шум плеска при перфоративных гастродуоденальных язвах.
Симптом Грекова - брадикардия в первые часы после перфорации.
Симптом Гюстена (Guiston) - сердечные тоны выслушиваются до уровня пупка. Феномен обусловлен резонирующими свойствами свободного воздуха, усиливающего звукопроводимость.
Триада Гюстена (Guiston) :
> распространение сердечных тонов через растянутую газами брюшную стенку до уровня пупка;
> перитонеальное трение, напоминающее шум трения плевры в области реберного края или в подложечной области;
> металлический звон или серебристый шум, появляющийся при вдохе и связанный с наличием свободного газа, выходящего из желудка через перфорационное отверстие в окружающую жидкость.
Симптом Дзбановского-Чугуева - поперечные втянутые бороздки на передней брюшной стенке, соответствующие перемычкам прямых мышц живота. Наблюдается в первые часы после перфорации.
Симптом Дьелафуа (Dieulafoy) - острая «кинжальная» боль в животе.
Симптом Кларка (Clark) - исчезновение притупления перкуторного звука над печенью. Выявляется при перфорации желудка или двенадцатиперстной кишки (аналогичен симптому Спижарного).
Симптом Кораха (Corach) - при локализации перфорационного отверстия в области кардии подкожная эмфизема может распространяться на левую половину грудной клетки, лицо и мошонку.
Симптом Крымова - сильная боль, возникающая при исследовании пупка кончиком пальца, связанная с раздражением брюшины.
Симптом Куленкампфа (Kulenkamph) - болезненность прямокишечно-маточного или прямокишечно-пузырного углубления при ректальном обследовании вследствие скопления перитонеального экссудата и желудочного содержимого.
Триада Лаффите (Laffite) - забрюшинная гематома, эмфизема и желто-зеленая окраска заднего листка брюшины, обнаруживаемые во время операции. Характерна для забрюшинного разрыва двенадцатиперстной кишки.
Симптом Подлаха (Podlach) - подкожная эмфизема в левой подключичной области при перфорации язвы кардиального отдела желудка. Характерен для атипичных гастродуоденальных перфораций.
Симптом Потена (Potain) - рефлекторное нарушение гемодинамики в малом круге кровообращения в связи с выраженным болевым синдромом при заболеваниях желудка и желчевыводящих путей.
Симптом Ратнера-Виккера - длительное стойкое напряжение мышц в правом верхнем квадранте брюшной стенки при общем хорошем состоянии больного. Наблюдается при прикрытых перфоративных язвах желудка и двенадцатиперстной кишки.
Симптом Спижарного - высокий тимпанит над печенью - исчезновение печеночной тупости при прободении гастродуоденальных язв.
Симптом Успенского - «ослизнение» внутрибрюшинного экссудата при перфоративной язве желудка.
Острый аппендицит - воспаление червеобразного отростка слепой кишки, одно из самых распространённых хирургических заболеваний. Наиболее часто острый аппендицит встречают в возрасте от 20 до 40 лет, женщины болеют в 2 раза чаще мужчин. Летальность составляет 0,1-0,3%, послеоперационные осложнения встречают в 5-9% случаев.
Этиология
Причины возникновения острого аппендицита до сих пор окончательно не установлены. Определённую роль играет алиментарный фактор. Пиша, богатая животным белком, способствует нарушению эвакуаторной функции кишечника, что следует считать предрасполагающим фактором в развитии заболевания. В детском возрасте некоторую роль в возникновении аппендицита играет глистная инвазия.
Основной путь инфицирования стенки отростка энтерогенный. Гематогенный и лимфогенный варианты инфицирования встречают достаточно редко, они не играют решающей роли в генезе заболевания. Непосредственными возбудителями воспаления становятся разнообразные микроорганизмы (бактерии, вирусы, простейшие), находящиеся в отростке. Среди бактерий чаше всего (до 90%) обнаруживают анаэробную неспорообразующую флору (бактероиды и анаэробные кокки). Аэробную флору встречают реже (6-8%), она представлена кишечной палочкой, клебсиеллой, энтерококками и др.
Классификация
Клинико-морфологические формы аппендицита:
• катаральный;
• флегмонозный;
• гангренозный.
Осложнения:
• перфорация;
• разлитой перитонит;
• аппендикулярный инфильтрат;
• абсцессы брюшной полости (периаппендикулярный, тазовый, поддиафрагмальный, межкишечный);
• забрюшинная флегмона;
• пилефлебит.
Формы острого аппендицита отражают степень (стадию) воспалительных изменений в червеобразном отростке. Каждая из них имеет не только морфологические отличия, но и присущие ей клинические проявления.
Патоморфология
Острый катаральный аппендицит - начальная форма воспаления червеобразного отростка. Макроскопически отросток утолщён, его серозная оболочка тусклая, под ней видно множество наполненных кровью мелких сосудов. На разрезе слизистая оболочка отростка отёчна, серо-красного цвета, в подслизистом слое иногда видны пятна кровоизлияний. В просвете червеобразного отростка нередко содержится сукровичного вида жидкость. Микроскопически выявляют небольшие дефекты слизистой оболочки, покрытые фибрином и лейкоцитами, умеренную лейкоцитарную инфильтрацию подслизисто-го слоя. Иногда в брюшной полости обнаруживают прозрачный стерильный реактивный выпот.
При остром флегмонозном аппендиците отросток значительно утолщён, серозная оболочка и брыжеечка отёчны, ярко гипереми-рованы. Червеобразный отросток покрыт наложениями фибрина, такие же наложения могут быть на куполе слепой кишки, париетальной брюшине и прилегающих петлях тонкой кишки. В брюшной полости почти всегда выявляют выпот, часто мутный из-за большого количества лейкоцитов. Выпот может быть инфицированным. В просвете червеобразного отростка, как правило, содержится жидкий, серого или зелёного цвета гной. Слизистая оболочка червеобразного отростка отёчна, легко ранима, нередко удаётся увидеть множественные эрозии и свежие язвы. Микроскопически во всех слоях червеобразного отростка наблюдают массивную лейкоцитарную инфильтрацию.
Эмпиема червеобразного отростка - разновидность флегмонозно-го воспаления, при котором в результате рубцового процесса или закупорки каловым камнем в просвете отростка образуется замкнутая полость, заполненная гноем. Морфологическая особенность этой формы аппендицита заключается в том, что воспалительный процесс редко переходит на брюшинный покров. Червеобразный отросток при эмпиеме колбовидно вздут и резко напряжён, содержит большое количество зловонного гноя. Наряду с этим серозная оболочка червеобразного отростка выглядит как при катаральной форме острого аппендицита: тусклая, гиперемированная, но без наложений фибрина. В брюшной полости может быть серозный стерильный выпот. При вскрытии червеобразного отростка изливается большое количество зловонного гноя. Микроскопически в слизистой оболочке и подсли-зистом слое выявляют значительную лейкоцитарную инфильтрацию, убывающую по направлению к серозной оболочке.
Гангренозный аппендицит характеризуется некротическими изменениями в органе. Тотальный некроз встречают сравнительно редко, в подавляющем большинстве случаев зона некроза охватывает небольшую часть отростка. Некрозу способствуют располагающиеся в просвете отростка каловые камни и инородные тела. Макроскопически некротизированный участок грязно-зелёного цвета, рыхлый и легко рвётся, остальная часть червеобразного отростка выглядит так же, как при флегмонозном аппендиците. На органах и тканях, окружающих воспалённый червеобразный отросток, видны фибринозные наложения. В брюшной полости часто содержится гнойный выпот с каловым запахом. Посев этого выпота даёт рост типичной толстокишечной флоры. Микроскопически в участке деструкции слои червеобразного отростка не удаётся дифференцировать, они имеют вид типичной некротизированной ткани, в остальных отделах отростка наблюдают картину флегмонозного воспаления.
Катаральная стадия острого аппендицита обычно длится 6-12 ч. Флегмонозный аппендицит развивается через 12 ч от начала заболевания, гангренозный - через 24-48 ч.
Клиническая картина
Острый аппендицит характеризуется определённым симптомоком-плексом, претерпевающим соответствующие изменения по мере развития воспалительного процесса. Вместе с тем, возможны различные
варианты расположения червеобразного отростка (рис. 6-1) в брюшной полости (высокое, низкое, или тазовое, подпечёночное, ретро-цекальное и др.), наличие некоторых симптомов заболевания прямо зависит от локализации отростка.
Катаральный аппендицит
Постоянный симптом начальных стадий острого аппендицита - боли в животе, заставляющие больного обратиться к врачу. Боли возникают чаще всего вечером, ночью или в предутренние часы, что связывают с преобладающим влиянием блуждающего нерва в это время суток. Даже при типичном расположении червеобразного отростка в правой подвздошной области боли очень редко начинаются непосредственно в этом месте. Они, как правило, возникают в эпигастраль-ной области или имеют блуждающий характер (по всему животу без какой-либо определённой локализации). В начальном периоде боли неинтенсивные, тупые, постоянные и лишь иногда могут быть схваткообразными.
Через 2-3 ч от начала заболевания боли, постепенно усиливаясь, перемещаются в правую подвздошную область - зону локализации червеобразного отростка. Такое смещение болей характерно для острого аппендицита и носит название симптома Кохера-Волковича. В дальнейшем после концентрации болей в правой подвздошной области они остаются там постоянно.
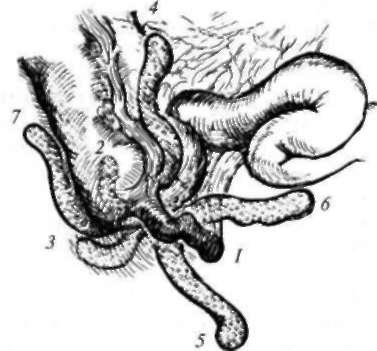
Рис. 6-1.Варианты расположения червеобразного отростка: / - типичное; 2 - позади слепой кишки (ретроцекальное); 3 - ретроперитонеальное; 4 - подпечёночное; 5 - в малом тазу; 6 - медиальное (среди петель тонкой кишки); 7 - в правом латеральном канале.
В первые часы заболевания у 30-40% пациентов может быть однократная рвота, в этой стадии носящая рефлекторный характер;
Общее состояние больного страдает мало, обращает на себя внимание влажный, густо обложенный язык. При осмотре живот не вздут и равномерно участвует в дыхании. Отмечают зону гиперестезии в правой подвздошной области (положительный симптом Раздольско-го). При глубокой пальпации даже в самые первые часы заболевания здесь же удаётся определить явную, иногда довольно значительную болезненность. В этот период можно выявить некоторые специальные симптомы, характерные для острого аппендицита.
• Симптом Ровзинга: левой рукой сквозь брюшную стенку прижимают сигмовидную кишку к крылу левой подвздошной кости, перекрывая её просвет. Правой рукой выше этой зоны производят толчкообразные движения передней брюшной стенки. При этом возникает боль в правой подвздошной области, что связывают с перемещением газов, находящихся в толстой кишке.
• Симптом Ситковского заключается в появлении или усилении болей в правой подвздошной области при положении больного на левом боку.
• Симптом Бартомье-Михельсона: усиление болезненности при пальпации правой подвздошной области в положении больного на левом боку.
Один из ранних объективных симптомов острого аппендицита - повышение температуры тела до 37-37,5 °С илейкоцитоз в пределах10-12- 107л.
Флегмонозный аппендицит
Флегмонозный аппендицит - наиболее частая клиническая форма, с которой больные поступают в хирургический стационар. Боли при флегмонозном аппендиците довольно интенсивны и постоянны. Они чётко локализуются в правой подвздошной области и нередко носят пульсирующий характер. Рвота для этой формы острого аппендицита не характерна, больные жапуются на постоянное чувство тошноты. Из анамнеза выявляют характерное начало заболевания (симптом смешения болей Кохера-Волковича).
Пульс учащён до 80-90 в минуту. Язык обложен. Наряду с описанными симптомами острого аппендицита появляются признаки воспаления брюшины. При осмотре живота отмечают умеренное отставание пои дыхании пеоелней боюшной стенки в поавой подвздошной области.
а при поверхностной пальпации здесь же, кроме гиперестезии, определяют защитное напряжение мышц брюшной стенки и симптомЩёт-кина-Блюмберга. При быстром отдёргивании руки после мягкого надавливания на брюшную стенку больной ошушает внезапное усиление боли вследствие сотрясения брюшной стенки в области воспалительного очага.Симптом Воскресенского (симптом «рубашки», или «скольжения»): через рубашку больного быстро производят скользящее движение рукой вдоль передней брюшной стенки от реберной дуги до паховой связки справа и слева от пупка. При этом отмечают значительное усиление болезненности в правой подвздошной области. Температура тела может достигать 38-38,5 °С, количество лейкоцитов 12-20-10*/л.
Гангренозный аппендицит
Гангренозный аппендицит характеризуется уменьшением или даже полным исчезновением спонтанных болевых ощущений вследствие отмирания нервных окончаний в червеобразном отростке. Наряду с этим всасывание из брюшной полости большого количества бактериальных токсинов приводит к постепенному нарастанию симптомов системной воспалительной реакции. При исследовании живота напряжение брюшной стенки в правой подвздошной области становится менее интенсивным, чем при флегмонозном аппендиците, но попытка глубокой пальпации немедленно вызывает резкое усиление болей. Живот чаще всего умеренно вздут, перистальтика ослаблена или отсутствует. Выражены симптомы Щёткина-Блюмберга и Воскресенского. Положительными также могут быть симптомы Ровзинга, Ситковского, Бартомье-Михельсона.
Температура тела при гангренозном аппендиците нередко бывает или нормальной (ниже 37 °С), или даже пониженной (до 36 °С). Количество лейкоцитов значительно снижается (10- 12109/л) или находится в пределах нормы (6-810ч/л), но воспалительный сдвиг в лейкоцитарной формуле крови может достигать значительной степени (увеличение количества палочкоядерных и появление юных форм нейтрофилов). Для гангренозного аппендицита характерны так называемые«токсические ножницы» - несоответствие выраженной тахикардии (100-120 в минуту) температуре тела на фоне явных признаков тяжёлого воспалительного процесса.
У лиц преклонного возраста иногда развивается так называемый первично-гангренозный аппендицит. Он бывает результатом первичного
нарушения кровотока по артерии червеобразного отростка вследствие тромбоза, т.е. по существу возникает инфаркт червеобразного отростка, непосредственно переходящий в гангрену отростка, минуя катаральную и флегмонозную формы острого аппендицита. В последующем подвергшийся тотальному некрозу червеобразный отросток может полностью отторгнуться от слепой кишки (так называемая самоампутация отростка) и лежать свободно в брюшной полости.
Особенности клинического проявления атипичных форм
Эмпиема червеобразного отростка морфологически похожа на флегмонозный аппендицит, но в клиническом отношении имеет существенные отличия. При эмпиеме боли в животе не имеют характерного смещения (отрицательный симптом Кохера-Волковича), а начинаются непосредственно в правой подвздошной области, достигают максимума лишь к 3-5-му дню заболевания, принимают пульсирующий характер, характерен озноб с повышением температуры тела до 38-39 "С.
При объективном исследовании брюшная стенка не напряжена, отсутствуют симптомы раздражения брюшины. Симптомы Ровзин-га, Ситковского, Бартомье-Михельсона чаще всего положительны. При глубокой пальпации в правой подвздошной области иногда удаётся прощупать резко утолщённый, болезненный червеобразный отросток. Количество лейкоцитов в первые сутки остаётся нормальным, в последующем наблюдают быстрое его увеличение до 20- 109/л и выше с нарастанием сдвига лейкоцитарной формулы влево.
Ретроцекальный аппендицит начинается с болей в эпигастральной области или по всему животу, которые в последующем локализуются в зоне правого бокового канала или поясничной области.
Типичные симптомы аппендицита не выявляют. Симптомы раздражения брюшины также не выражены. Устанавливают напряжение мышц в треугольнике Пти и симптом Образцова (появление болей в правой подвздошной области во время поднимания и последующего опускания больным вытянутой правой ноги).
Тазовый аппендицит встречают у 16% мужчин и 30% женщин. Боли начинаются в эпигастральной области или по всему животу, а через несколько часов локализуются над лобком либо над паховой связкой справа. В связи с близостью прямой кишки и мочевого пузыря нередко возникают частые позывы на стул и дизурические расстройства.
При тазовом аппендиците воспалительный процесс быстро отграничивается окружающими органами, поэтому при исследовании живота далеко не всегда удаётся отметить напряжение мышц передней брюшной стенки и другие симптомы раздражения брюшины. Симптомы Ровзинга, Ситковского, Бартомье-Михельсона нехарактерны. В части случаев оказывается положительным симптом Коупа - болезненное напряжение внутренней запирательной мышцы (в положении больного лежа на спине сгибают правую ногу в колене и ротируют бедро кнаружи, что приводит к появлению боли в глубине таза справа и над лоном). При подозрении на тазовый аппендицит исключительную ценность приобретают пальцевые вагинальное и ректальное исследования, выявляющие болезненность в области дугласова пространства, наличие выпота или воспалительного инфильтрата в полости малого таза, а также позволяющие оценить состояние гениталий и др.
Подпечёночное расположение червеобразного отростка существенно затрудняет диагностику острого аппендицита. Болезненность в области правого подреберья, наличие здесь же напряжения мышц и симптома Щёткина-Блюмберга заставляют думать об остром холецистите. Типичный для приступа острого аппендицита анамнез служит отправной точкой для установления правильного диагноза. При остром холецистите пальпируют увеличенный жёлчный пузырь, при остром аппендиците какое-либо патологическое образование в животе не определяют (исключение составляет аппендикулярный инфильтрат).
Левосторонний острый аппендицит наблюдают при обратном расположении внутренних органов(situs viscerum inversus) или в случае мобильной слепой кишки, имеющей длинную брыжейку. Типичные для аппендицита симптомы выявляют в левой подвздошной области. В случае истинного обратного расположения внутренних органов при аппендэктомии разрез проводят в левой подвздошной области.
Дифференциальная диагностика
Острый аппендицит приходится дифференцировать почти от всех острых заболеваний органов брюшной полости и забрюшинного пространства. Это гастроэнтерит, острый панкреатит, прободная язва желудка или двенадцатиперстной кишки, острый холецистит, правосторонняя почечная колика, правосторонний пиелит (пиелонефрит), терминальный илеит (болезнь Крона) в начальной стадии, дивер-тикулит (воспаление дивертикула Меккеля) и др. Большое подспо-
рье в затруднительных случаях дифференциальной диагностики при острой патологии органов брюшной полости оказывают УЗИ и лапароскопия.
Лечение
Лечебная тактика при остром аппендиците заключается в возможно более раннем удалении воспалённого червеобразного отростка.
Аппендэктомию, как и любое другое полостное вмешательство, предпочтительнее выполнять под обшей анестезией. При невозможности наркоза допустимо выполнение операции под местной анестезией.
Типичную аппендэктомию обычно проводят с помощью косого переменного доступа Волковича-Дьяконова в правой подвздошной области: линию, соединяющую пупок и переднюю верхнюю ость подвздошной кости, делят на три равные части, на границе наружной и средней третей этой линии перпендикулярно к ней проводят кожный разрез. При этом его третья часть должна находиться выше указанной линии, а две трети - ниже неё.
Длина кожного разреза для аппендэктомии составляет обычно 10-12 см. Апоневроз наружной косой мышцы надсекают скальпелем и вскрывают ножницами по ходу волокон. Внутреннюю косую и поперечную мышцы разводят по ходу волокон без их пересечения. После этого рассекают брюшину.
Проникнув в брюшную полость, отыскивают слепую кишку. Она в отличие от тонкой кишки имеет три хорошо выраженные продольные мышечные ленты (taenia coli). Основание червеобразного отростка и начало его брыжеечки находятся в месте слияния всех трёх лент на куполе слепой кишки. В связи с этим чаще всего вместе с куполом слепой кишки удаётся извлечь в рану и червеобразный отросток. После выведения червеобразного отростка в рану перевязывают бры-жеечку, следя за тем, чтобы собственная артерия червеобразного отростка обязательно вошла в лигатуру. Перевязав брыжеечку, отсекают её от отростка на всём протяжении. Вслед за этим пережимают зажимом основание червеобразного отростка и перевязывают его (рис. 6-2, а), используя тонкий кетгут, викрил либо другую быстро рассасывающуюся нить. Червеобразный отросток отводят кверху и, отступя 1 -1,5 см от его основания, накладывают круговой (кисетный) серозно-мышечный шов, для чего используют нерассасываюшуюся
нить на атравматической игле (рис. 6-2, б). Затем на червеобразный отросток накладывают зажим на 0,3-0,5 см выше лигатуры и отсекают его (рис. 6-2, в). Культю червеобразного отростка смазывают 5% спиртовым раствором йода и погружают внутрь кисетного шва (рис. 6-2, г). Поверх кисетного шва аналогичной синтетической нитью на атравматической игле накладывают Z-образный шов. После этого купол слепой кишки погружают в брюшную полость.
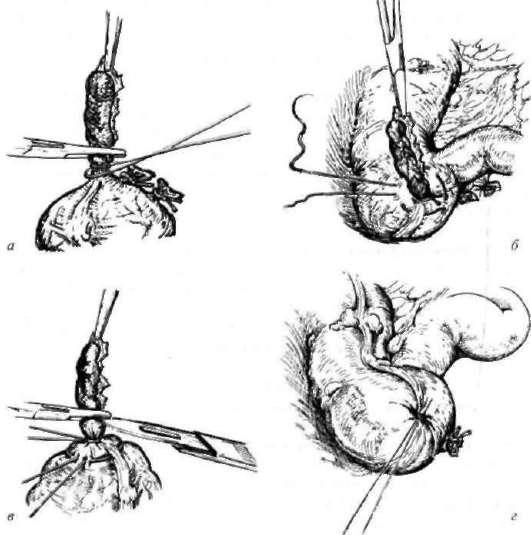
Рис. 6-2. Этапы аппендэктомии: а - перевязка червеобразного отростка у основания; б - наложение кисетного шва на слепую кишку вокруг основания отростка; в - отсечение отростка; г - культя отростка инвагинирована, кисетный шов завязан.
После вправления выведенной для манипуляций слепой кишки тщательно осушают брюшную полость от выпота. Проводят контроль гемостаза. Рану передней брюшной стенки ушивают.
Ретроградную аппендэктомию выполняют при невозможности выведения всего червеобразного отростка за пределы брюшной полости. Под основание червеобразного отростка подводят толстую лигатуру. Затем, используя образовавшееся в брыжеечке отверстие, на основание червеобразного отростка накладывают два зажима, и между ними пересекают отросток. Вскрытый просвет червеобразного отростка смазывают с обеих сторон 5% спиртовым раствором йода. Пол наложенным зажимом перевязывают культю червеобразного отростка и погружают её пинцетом в кисетный шов. Сверху дополнительно накладывают Z-образный шов. Погрузив культю червеобразного отростка, вправляют купол слепой кишки в брюшную полость. Затем, поэтапно накладывая на брыжеечку зажимы, отсекают от неё и удаляют червеобразный отросток. По мере выделения червеобразного отростка рассекают также фиксирующие его сращения, особенно около верхушки. Взятые в зажимы пряди брыжеечки перевязывают, лучше всего с прошиванием. Таким образом, брыжеечка оказывается перевязанной не одной, а несколькими лигатурами. Дальнейший ход оперативного вмешательства не отличается от антеградной аппендэктомии.
Ретроперитонеальная аппендэктомия. В редких случаях червеобразный отросток или его дистальная часть бывает расположена забрю-шинно. В связи с этим удаление забрюшинно расположенного отростка - наиболее трудный вариант аппендэктомии. Расширяют оперативный доступ за счёт максимального разведения внутренней косой и поперечной мышц, а также путём надсечения края влагалища прямой мышцы живота.
Затем под основание червеобразного отростка подводят лигатуру и мобилизуют купол слепой кишки, рассекая париетальную брюшину бокового канала и отодвигая слепую кишку медиально. Проникнув таким путём в позадислепокишечную клетчатку, осторожно выделяют из неё дистальную часть отростка. Особое внимание обращают на гемостаз, так как лишённый серозного покрова червеобразный отросток интимно сращён с окружающей клетчаткой. В этой же клетчатке проходит и артерия червеобразного отростка, её обязательно нужно отыскать и наложить на неё лигатуру. После выделения всего червеобразного отростка и перевязки артерии выполняют аппендэктомию. Вслед за этим ушивают непрерывным швом рассечённую париетальную брюшину.
Особенности хирургического вмешательства при различных формах острого аппендицита
Выполняя вмешательство по поводу катарального аппендицита,
всегда следует придерживаться следующего правила: нельзя удалять червеобразный отросток, не убедившись в том, что изменения в нём первичны, а не вызваны воспалительным процессом в окружающих органах.
Ревизию начинают с осмотра подвздошной кишки. Поэтапно выводя в рану, осматривают не менее 1 м подвздошной кишки, чтобы убедиться в отсутствии терминального илеита, воспалённого дивертикула Меккеля и более редких причин воспаления (массивный аскаридоз, перфорация рыбьей костью и др). Затем осматривают близлежащие отделы толстой кишки с целью исключения рака, язвенного колита, дивертикулита или другого её поражения.
В случае воспаления дивертикула Меккеля в правой подвздошной ямке также нередко находят воспалительный выпот и вторично изменённый, гиперемированный червеобразный отросток. Проводя ревизию подвздошной кишки, можно обнаружить дивертикул, обычно расположенный на расстоянии 40-80 см от илеоцекального угла. Обнаруженный рудимент подлежит удалению. При узком основании дивертикула его перевязывают кетгутом и отсекают, культю погружают в кисетный шов аналогично шву при аппендэктомии. При широком основании выполняют клиновидную резекцию кишки, при деструктивном воспалении дивертикула проводят более обширную резекцию кишки с прилежащей брыжейкой.
У женщин наиболее часто вторичный аппендицит сопутствует воспалению гениталий. Исходя из этого, в каждом случае катаральной формы острого аппендицита у женщин необходимо проводить ревизию внутренних половых органов. Пальпируют и осматривают матку и её правый придаток. Убедившись в отсутствии основного воспалительного очага в окружающих органах, приступают к аппендэктомии.
Флегмонозный аппендицит нередко сопровождается появлением более или менее значительного выпота в правой подвздошной ямке. В связи с этим во время операции необходимо, во-первых, взять экссудат для посева на микрофлору, а во-вторых, тщательно осушить правый боковой канал, подвздошную ямку и малый таз (дугласово пространство) от скопившегося выпота. Обнаружение мутного выпота - прямое показание к дренированию брюшной полости. Дренаж оставляют на 3-4 дня для оттока экссудата и введения антисептиков.
При операции по поводу гангренозного аппендицита оперативный доступ должен быть достаточно широким. После выведения купола слепой кишки в рану осторожно отделяют дистальную часть червеобразного отростка от окружающих органов. Выполняют аппендэктомию, брюшную полость тщательно осушают от выпота. Оставление дренажа в брюшной полости при гангренозном аппендиците обязательно.
Капиллярное кровотечение или неполное удаление некротизиро-ванных тканей - показание для установки дренажа. Антибактериальную терапию при гангренозном аппендиците назначают в обязательном порядке.
Осложнения острого аппендицита Перфорация
Перфорация червеобразного отростка приводит к попаданию в брюшную полость содержимого отростка. Вследствие этого быстро развивается местный перитонит, в последующем способный отграничиться (формирование абсцесса) либо перейти в разлитой перитонит. Макроскопически червеобразный отросток при прободении мало отличается от такового при гангренозной форме острого аппендицита. Участки некроза такого же грязно-зелёного цвета, в одном или нескольких из них видны перфоративные отверстия, из которых изливается зловонный гной. Окружающая брюшина покрыта массивными фибринозными наложениями. В брюшной полости содержится обильный гнойный выпот, иногда - выпавшие из червеобразного отростка каловые камни.
Момент прободения стенки отростка проявляется возникновением резчайшей боли в правой подвздошной области. При осмотре больного обращают на себя внимание тахикардия и сухой обложенный коричневатым налётом язык. Резко выражены все симптомы раздражения брюшины. Живот постепенно становится всё более вздутым, перистальтика отсутствует, что, несомненно, свидетельствует о развивающемся разлитом гнойном перитоните.
Отмечают значительное повышение температуры тела (иногда принимает гектический характер). Количество лейкоцитов в периферической крови значительно повышено, выявляют резкий сдвиг лейкоцитарной формулы крови влево.
Лечение прободного аппендицита по сути не отличается от такового при разлитом перитоните.
Разлитой гнойный перитонит
Разлитой гнойный перитонит осложняет течение острого аппендицита в обшей сложности не более чем в 1% случаев, однако среди прободных аппендицитов частота этого осложнения возрастает до 8-10%. Перитонит - основная причина летальности при остром аппендиците.
Диагностика разлитого перитонита при перфоративном аппендиците не вызывает особых трудностей. Несколько иначе выглядит клиническая картина при перитоните, развивающемся в послеоперационном периоде на фоне медикаментозной терапии. В этих условиях отсутствуют острые боли, соответствующие моменту прободения червеобразного отростка. Боли носят постоянный характер, что до известной степени можно связать с операционной травмой. Генерализованное напряжение брюшной стенки также может отсутствовать, часто живот остаётся умеренно вздутым за счёт пареза кишечника и равномерно болезненным во всех отделах. Тем не менее симптом Щёткина-Блюмберга обычно бывает выражен, как и другие симптомы раздражения брюшины.
Помочь установлению правильного диагноза могут гектический характер температурной кривой, гнойно-токсический сдвиг в формуле крови и другие признаки системной воспалительной реакции. При УЗИ выявляют дилатированные петли тонкой кишки с ослабленной перистальтикой и свободную жидкость в брюшной полости. Некоторую помошь может оказать и сопоставление развивающегося неблагополучия со стороны живота со сроками, прошедшими с момента операции. Симптомы послеоперационного перитонита достигают максимума к 5-7-му дню после хирургического вмешательства. При нормальном течении послеоперационного периода к этому сроку исчезают все болезненные проявления, нормализуются температура тела и ультразвуковая картина.
Разлитой гнойный перитонит - показание к незамедлительному хирургическому вмешательству, проводимому после короткой (не более 2-3 ч) предоперационной подготовки. Под наркозом выполняют широкую срединную лапаротомию. При деструктивном аппендиците проводят аппендэктомию. Тщательно санируют брюшную полость многократным промыванием её большим количеством жидкости. Обязательно следует промыть и осушить полость малого таза, латеральные каналы и поддиафрагмальное пространство. При уверенности в полном удалении гноя и некротизированных тканей полость
брюшины дренируют несколькими дренажами, выводя их через контрапертуры. Операционную рану передней брюшной стенки ушивают наглухо. Если полноценная санация брюшной полости во время одного вмешательства невозможна, накладывают лапаростому, позволяющую купировать явления «запущенного» перитонита путём повторных санационных оперативных вмешательств (см. главу 14).
Аппендикулярный инфильтрат
Аппендикулярный инфильтрат - конгломерат рыхло спаянных между собой органов и тканей, расположенных вокруг воспалённого червеобразного отростка. В его образовании принимают участие слепая кишка, большой сальник, петли тонкой кишки и париетальная брюшина. Возникновение инфильтрата - следствие защитной реакции, отграничивающей воспалительный процесс в брюшной полости. Он чаше всего развивается при флегмонозно изменённом червеобразном отростке, однако иногда в центре воспалительного конгломерата находится отросток, подвергшийся полной деструкции.
Типичная картина аппендикулярного инфильтрата развивается, как правило, через 3-5 дней от начала заболевания. Имевшиеся в начале болезни самостоятельные боли в животе почти полностью стихают, самочувствие больных улучшается, хотя температура тела остаётся субфебрильной. При объективном исследовании живота не удаётся выявить мышечного напряжения и других симптомов раздражения брюшины. В правой подвздошной области, где чаще всего локализуется инфильтрат, можно прощупать довольно плотное, малоболезненное и малоподвижное опухолевидное образование. В диагностике аппендикулярного инфильтрата исключительно важную роль играет анамнез. Если появлению указанного образования в правой подвздошной области предшествовал приступ болей в животе с характерным для острого аппендицита симптомом Кохера-Волкови-ча, однократной рвотой и умеренным повышением температуры тела, то можно быть уверенным в правильной диагностике аппендикулярного инфильтрата.
Аппендикулярный инфильтрат необходимо дифференцировать от опухоли слепой кишки, особенно у лиц пожилого возраста. Для новообразования характерен длительный анамнез с постепенным развитием болевого синдрома без существенного повышения температуры тела. Кроме того, опухоль слепой кишки часто сопровождается анемией, может вызывать явления кишечной непроходимости, чего
почти никогда не наблюдают при аппендикулярном инфильтрате. Динамическое наблюдение за аппендикулярным инфильтратом позволяет отметить уменьшение в размерах опухолевидного образования, при новообразовании этого не бывает.
В диагностике аппендикулярного инфильтрата используют УЗИ, дающее возможность определения внутренней структуры образования, динамики воспалительных изменений с течением времени и под влиянием проводимого лечения, что позволяет уточнить лечебную тактику.
Исходом аппендикулярного инфильтрата может быть либо его полное рассасывание, либо абсцедирование. Это обусловливает консервативно-выжидательную хирургическую тактику. Операция противопоказана при спокойном течении аппендикулярного инфильтрата, когда при динамическом наблюдении регрессирует воспаление и есть явная тенденция к его рассасыванию. Этому способствуют ан-тибиотикотерапия, ограничение физической активности пациента и щадяшая диета, предотвращающая чрезмерную перистальтику кишечника. Поскольку перенесённое воспаление вызывает стойкую деформацию червеобразного отростка и частичную облитерацию просвета с нарушением дренажной функции, вероятность повторного аппендицита очень высока. В связи с этим следует выполнить аппендэктомию в «холодном» периоде - через 3-4 мес после рассасывания инфильтрата.
Если в процессе наблюдения в стационаре у больного вновь появляются боли в правой подвздошной области, развивается системная воспалительная реакция (вновь нарастает лейкоцитоз, температура тела принимает гектический характер), следует предположить абсцедирование аппендикулярного инфильтрата. При этом его размеры могут увеличиваться, возрастает пальпаторная болезненность, в центре иногда определяется размягчение. Развитие периаппендикулярного абсцесса можно подтвердить с помощью УЗИ. Сформированный абсцесс - полостное образование округлой формы с однородным гипо-или анэхогенным содержимым и плотной пиогенной капсулой от 5 до 8 мм толщиной.
Периаппендикулярный абсцесс - показание к хирургическому вмешательству. Вскрытие нагноившегося инфильтрата выполняют под общей анестезией. Проводят разрез Волковича-Дьяконова. Вскрывают полость гнойника, эвакуируют гной, промывают полость раствором антисептика, устанавливают в ней один или два тампона и трубчатый дренаж. Операционную рану ушивают до тампонов. При
латеральной локализации нагноившегося аппендикулярного инфильтрата целесообразно опорожнить гнойник внебрюшинным доступом Пирогова. При вскрытии нагноившегося аппендикулярного инфильтрата не следует стремиться к одновременной аппендэктомии.
В послеоперационном периоде больным назначают дезинтокси-кационную терапию и антибиотики широкого спектра действия. Во избежание рецидива острого аппендицита больным настоятельно рекомендуют плановую аппендэктомию через 3-4 мес после выписки из стационара.
Абсцесс брюшной полости
Абсцессы брюшной полости различной локализации при остром аппендиците бывают следствием осумкования инфицированного выпота, нагноения гематом, несостоятельности швов культи червеобразного отростка. Нередко они возникают при атипичном расположении червеобразного отростка.
Наиболее часто встречают тазовый абсцесс. Это обусловлено, прежде всего, анатомическими причинами, так как воспалительный экссудат в первую очередь скапливается в полости малого таза - самого нижнего отдела брюшной полости. Более того, если во время аппендэктомии в брюшной полости обнаруживают выпот, то в послеоперационном периоде больному в постели специально придают положение с возвышенным головным концом (положение Фовлера), поскольку выявить, вскрыть и санировать абсцесс малого таза легче, чем гнойник любой другой локализации.
Тазовый абсцесс проявляется тупыми болями в нижних отделах живота и промежности, дизурическими расстройствами и учащёнными болезненными позывами к стулу (тенезмами), обычно возникающими на 5-7-й день после операции на фоне вполне благополучного течения. Эти жалобы сопровождаются повышением температуры тела, лейкоцитозом с характерным нейтрофильным сдвигом формулы крови, симптомами интоксикации (слабость, бледность кожных покровов, сухость во рту, тахикардия).
При появлении подобных симптомов следует предпринять пальцевые ректальное и вагинальное исследования, во время которых в области заднего свода влагалища или передней стенки прямой кишки обнаруживают малоподвижный болезненный инфильтрат. Скопление большого количества гноя проявляется пальпаторно определяемой флюктуацией.
Вскрытие абсцесса малого таза у женщин выполняют через задний свод влагалища, а у мужчин - через переднюю стенку прямой кишки. В послеоперационном периоде больному назначают антибиотики и регулярно промывают полость абсцесса антисептиками через дренаж, установленный во время хирургического вмешательства. Системная терапия во всех подобных ситуациях заключается в дезинтоксикации и назначении антибактериальных средств.
Поддиафрагмальный абсцесс встречают гораздо реже тазового. Для него наряду с проявлениями системной воспалительной реакции характерны тупые боли в нижних отделах грудной клетки справа, усиливающиеся при глубоком вдохе, сухой кашель, вызванный раздражением диафрагмы, отставание правой её половины при дыхании, в поздних стадиях - выбухание нижних межреберий. В диагностике поддиафрагмального абсцесса исключительная роль принадлежит рентгенологическому исследованию, УЗИ и (особенно) КТ.
Для вскрытия поддиафрагмального абсцесса используют чресплев-ральные и внеплевральные доступы. В настоящее время предпочтение отдают чрескожному вскрытию и дренированию абсцесса под контролем УЗИ или КТ.
Межкишечный абсцесс - довольно редкое осложнение острого аппендицита. Для него характерен светлый промежуток, продолжающийся 5-7 дней с момента аппендэктомии до первых его симптомов - вялости, потери аппетита, гектической лихорадки, нейтро-фильного сдвига формулы крови. При объективном исследовании живота выявляют плотное, без чётких контуров опухолевидное образование, аналогичное аппендикулярному инфильтрату, но расположенное не в правой подвздошной области, а несколько медиаль-нее её. Симптомы раздражения брюшины отсутствуют, возможен парез кишечника. При отсутствии явных признаков абсцедирова-ния инфильтрата допустима консервативно-выжидательная тактика: покой, холод на область инфильтрата, антибиотики, динамическое наблюдение за картиной крови и температурой тела, ультразвуковой контроль.
Прогрессирование признаков системной воспалительной реакции и обнаружение полости во время УЗИ указывают на необходимость оперативного вмешательства. В проекции пальпируемого инфильтрата делают разрез, вскрывают гнойник и эвакуируют гной. Полость абсцесса промывают, и оставляют в ней тампон и дренаж для введения антисептиков. Возможно «закрытое» (без тампонов) лечение абсцесса, при этом в его полость устанавливают дренажную систему для
постоянного промывания и аспирации содержимого. Эту процедуру продолжают не менее 5-6 дней, до полной санации абсцесса и ликвидации его полости. Обшее лечение аналогично описанному выше.
Пилефлебит
Пилефлебит (септический тромбофлебит воротной вены и её притоков) - крайне редкое и самое тяжёлое осложнение острого аппендицита. Достоверные случаи излечения пилефлебита до настоящего времени неизвестны. Непосредственной причиной возникновения пилефлебита обычно становится гангренозный аппендицит, при котором воспалительный процесс переходит на брыжеечку червеобразного отростка и её вены. После перехода гнойного тромбофлебита на внутрипечёночные ветви воротной вены возникают абсцессы печени и желтуха, прогрессирует печёночно-почечная недостаточность, больные умирают через 7-10 дней от начала заболевания. Профилактика пилефлебита состоит в ранней диагностике и своевременном оперативном лечении острого аппендицита.
Особенности течения заболевания и лечебной тактики у различных категорий больных
Острый аппендицит у беременных
Некоторые признаки аппендицита (боли в животе, тошнота, рвота) присутствуют при обычном течении беременности, что затрудняет диагностику заболевания.
Клинические проявления острого аппендицита в первой половине беременности почти не отличаются от таковых вне беременности. Существенные затруднения в диагностике возникают во второй половине беременности. В этом случае болевой синдром, свойственный аппендициту, иногда отождествляют с болями, часто возникающими во второй половине беременности вследствие растяжения связочного аппарата матки. Внимательный расспрос позволяет установить начало болей в эпигастральной области и постепенное смещение их к месту локализации червеобразного отростка (симптом Кохера-Волковича).
При обследовании живота необходимо учитывать локализацию червеобразного отростка, смещаемого кверху по мере увеличения сроков беременности. Локальная болезненность при остром аппендиците во второй половине беременности определяется не в правой
подвздошной области, а значительно выше. Вследствие растяжения брюшной стенки увеличенной маткой локальное напряжение мышц выражено слабо. На поздних сроках беременности, когда слепая кишка и её отросток находятся позади увеличенной матки, могут быть отрицательными и другие симптомы раздражения брюшины: Щёт-кина-Блюмберга, Воскресенского. В этот период, как правило, хорошо выражены симптомы Образцова и Бартомье-Михельсона, выявляют также и обратный симптом Ситковского (усиление болей при положении на правом боку из-за давления увеличенной матки на воспалённый червеобразный отросток).
Температурная реакция выражена слабее, чем вне беременности. Количество лейкоцитов умеренно повышается, но при этом необходимо учитывать, что лейкоцитоз до 12- 109/л у беременных - распространённое явление.
При любой форме острого аппендицита у беременных для проведения аппендэктомии применяют общую анестезию. В качестве оперативного доступа в первой половине беременности пользуются разрезом Волковича-Дьяконова. Во второй половине беременности этот доступ модифицируют по принципу: чем больше срок беременности, тем выше разрез. В последние недели беременности разрез проводят выше гребня подвздошной кости вследствие значительного смешения слепой кишки и червеобразного отростка кверху. Оперативная тактика при любой форме острого аппендицита у беременных не отличается от общепринятых принципов его лечения.
В послеоперационном периоде, помимо обычной терапии, необходимо назначить лечение, направленное на профилактику преждевременного прерывания беременности.
Острый аппендицит у детей
Острый аппендицит у детей встречают значительно реже, чем у взрослых. Это объясняется тем, что червеобразный отросток у них имеет воронкообразную форму, способствующую хорошему его опорожнению, а также тем, что лимфоидный аппарат органа в этот период жизни недостаточно развит.
Острый аппендицит у детей протекает более бурно, чем у взрослых, что обусловлено малой сопротивляемостью инфекции, слабыми пластическими свойствами брюшины, недостаточным развитием большого сальника, не доходящего до червеобразного отростка и поэтому не участвующего в создании отграничивающего барьера.
Возникшие в животе боли нередко носят схваткообразный характер и не имеют чёткой динамики, характерной для острого аппендицита у взрослых. Дети до 10-летнего возраста не могут точно локализовать боли, что затрудняет распознавание заболевания. Рвота у детей чаще всего бывает многократной, стул не имеет тенденции к задержке, а у детей младшего возраста даже учащён. Характерна поза больного ребёнка. Он лежит на правом боку или спине, приведя ноги к животу и положив руку на правую подвздошную область, защищает её от осмотра врачом. При осторожной пальпации здесь нередко удаётся выявить гиперестезию, напряжение мышц и зону наибольшей болезненности. Даже в первые часы заболевания бывают выражены симптомы Щёткина-Блюмберга, Воскресенского, Бартомье-Михельсона.
Температура тела с самого начала заболевания значительно возрастает, нередко превышая 38 °С. Количество лейкоцитов в периферической крови также увеличено наряду с имеющимся нейтрофильным сдвигом формулы крови.
Острый аппендицит у детей дифференцируют с функциональными расстройствами кишечника, острым гастроэнтеритом, дизентерией, плевропневмонией, геморрагическим васкулитом (болезнью Шёнляйна-Геноха). При затруднениях в дифференциальной диагностике используют лапароскопию.
В связи с тем, что уже в течение первых суток заболевания у детей происходит деструкция отростка, хирургическая тактика должна быть более активной, чем у взрослых. Это в полной мере относится и к аппендикулярному инфильтрату, который у детей нередко образуется уже на 2-й день заболевания. Поскольку у детей червеобразный отросток относительно длинный, а сальник короткий и брюшина не обладает достаточными пластическими свойствами, образующийся инфильтрат «непрочен» и не может служить надёжным препятствием для распространения инфекции по брюшной полости. В связи с этим операция показана даже при пальпируемом инфильтрате, тем более что выделение червеобразного отростка из рыхло спаянных органов не представляет особых трудностей.
Аппендэктомию детям всегда проводят под обшей анестезией. В качестве оперативного доступа используют разрез Волковича-Дьяконова, за исключением случаев разлитого гнойного перитонита, когда показана нижнесрединная лапаротомия.
В большинстве случаев аппендэктомия у детей технически несложна ввиду отсутствия спаечного процесса и сращений червеобразного отростка с окружающими органами. Порядок хирургических мани-
пуляций при этом остаётся тем же, что и у взрослых, за исключением обработки культи отростка, которую у детей до 10-летнего возраста не погружают ввиду опасности сквозного прокола тонкой кишечной стенки при наложении кисетного шва. В связи с этим у детей первых лет жизни применяют так называемый лигатурный (ампутационный) способ аппендэктомии, при котором культю червеобразного отростка перевязывают нерассасываюшейся нитью, прижигают слизистую оболочку электрокоагулятором и оставляют в таком виде в брюшной полости. В связи с тем, что у детей отросток располагается в брюшной полости более свободно, чем у взрослых, в детском возрасте больше оснований для проведения лапароскопической аппендэктомии.
Острый аппендицит у больных пожилого и старческого возрастов
У больных пожилого и старческого возрастов заболевание характеризуется преобладанием деструктивных форм. Это обусловлено, с одной стороны, сниженной реактивностью организма, а с другой - атеросклеротическим поражением сосудов, что становится непосредственной причиной быстрого нарушения кровоснабжения с развитием некроза и гангрены червеобразного отростка. Именно у людей старческого возраста возникает так называемый первично-гангренозный аппендицит, который развивается сразу, минуя стадию катарального и флегмонозного воспаления.
Симптомокомплекс острого аппендицита у больных этой группы нередко имеет стёртую картину. Вследствие физиологического повышения порога болевой чувствительности пациенты часто не фиксируют внимания на эпигастральной фазе абдоминальных болей в начале заболевания. Тошнота и рвота возникают чаще, задержка стула не имеет решающего значения, поскольку в старческом возрасте существует тенденция к замедленному опорожнению кишечника.
При исследовании живота выявляют лишь умеренную болезненность в правой подвздошной области даже при деструктивных формах аппендицита. Вследствие возрастной релаксации мышц брюшной стенки мышечное напряжение в очаге поражения незначительно, но симптом Щёткина-Блюмберга, как правило, выражен. Часто оказываются положительными симптомы Воскресенского и Сит-ковского.
Температура тела даже при деструктивном аппендиците повышается умеренно или остаётся нормальной. Количество лейкоцитов
нормальное или повышено незначительно - в пределах 10-12-10ул, нейтрофильный сдвиг формулы крови не выражен.
У лиц пожилого и старческого возрастов гораздо чаше возникает аппендикулярный инфильтрат, характеризующийся медленным развитием. Больные нередко замечают опухолевидное образование в правой подвздошной области через несколько дней после приступа неинтенсивных болей, что заставляет отнестись с особым вниманием кдифференпиальному диагнозу между аппендикулярным инфильтратом и опухолью слепой кишки.
Своеобразие течения острого аппендицита улиц преклонного возраста приводит к тому, что точное распознавание той или иной клинической формы острого аппендицита до операции затруднено. Это говорит о необходимости активной хирургической тактики, тем более что риск аппендэктомии в старческом возрасте нередко преувеличен. При выборе метода обезболивания отдают предпочтение местной анестезии, особенно у больных с сопутствующими заболеваниями дыхательной и сердечно-сосудистой систем.
Ведение послеоперационного периода у больных пожилого возраста - не менее ответственный этап, чем выполнение самой операции. Необходим динамический контроль функционального состояния важнейших систем организма. Основные мероприятия следует направить на профилактику и лечение нарушений дыхания и кровообращения, метаболических сдвигов и почечной недостаточности. Следует обратить особое внимание на профилактику инфекционных осложнений и ТЭЛА.
Среди острых заболеваний органов брюшной полости острый холецистит занимает второе место после острого аппендицита и имеет тенденцию к увеличению заболеваемости. В последние десятилетия достигнуты значительные успехи в диагностике и совершенствовании методов его лечения, что позволило снизить летальность до 2,5%. Вместе с тем, она остаётся высокой среди больных пожилого и старческого возрастов.
Этиология и патогенез
Возникновение острого холецистита связано с действием нескольких факторов, среди них ведущую роль играют инфекция и застой жёлчи (жёлчная гипертензия). Лишь при их наличии создаются необходимые условия для развития и дальнейшего прогрессирования воспалительного процесса в жёлчном пузыре. В клинической практике в подавляющем большинстве случаев холецистит развивается на фоне ЖКБ. Ему обычно предшествует обтурация камнем шейки жёлчного пузыря или пузырного протока. Внезапное повышение внут-рипузырного давления и растяжение жёлчного пузыря приводят к механическому сдавлению сосудов и нарушениям микроциркуляции в его стенке. Степень сосудистых нарушений находится в прямой зависимости от величины гипертензии. Длительное её сохранение ведёт к ишемии стенки жёлчного пузыря, а возникающие при этом изменения качественного состава жёлчи оказывают повреждающее действие на слизистую оболочку. В этих условиях эндогенная инфекция жёлчного пузыря становится вирулентной. Воспаление жёлчного пузыря сопровождается экссудацией в его просвет, что способствует дальнейшему возрастанию гипертензии и прогрессированию повреждения пузырной стенки.
В жёлчный пузырь микробная флора попадает гематогенным, лимфогенным или энтерогенным путём. В большинстве случаев инфицирование жёлчного пузыря происходит гематогенным путём - из общего круга кровообращения по системе общей печёночной
артерии или из ЖКТ по воротной вене. Редко микробы попадают в жёлчный пузырь восходящим путём - из двенадцатиперстной кишки при зиянии сфинктера Одди и появлении дуодено-билиарного рефлюкса. Обычно микробы обитают в стенке жёлчного пузыря, в ходах Люшка, поэтому в пузырной жёлчи у здорового человека их не обнаруживают.
Бактериальная основа острого холецистита - различные микроорганизмы. Среди них преобладают грамотрицательные бактерии (кишечная палочка, клебсиелла, псевдомонады), в трети случаев обнаруживают их ассоциацию с грамположительными микроорганизмами (бактероиды и анаэробные кокки).
Таким образом, первичным звеном в развитии воспаления жёлчного пузыря становится остро возникающая жёлчная гипертен-зия, а вторичным - инфекция. Прогрессированию патоморфоло-гических изменений в жёлчном пузыре вплоть до некроза способствуют сосудистые заболевания (атеросклероз, гипертоническая болезнь), что часто наблюдают у больных пожилого и старческого возрастов.
Классификация
Клинико-морфологические формы холецистита:
• катаральный;
• флегмонозный;
• гангренозный. Осложнения:
• перфорация;
• разлитой перитонит;
• перипузырный инфильтрат и абсцесс;
• гнойный холангит;
• механическая желтуха;
• жёлчные свищи (наружные и внутренние).
Каждую из неосложнённых форм заболевания следует рассматривать как закономерное развитие воспалительного процесса и поэтапный переход от катарального воспаления к гангрене. Исключением из этой закономерности считают первичный гангренозный холецистит, развивающийся чаще всего вследствие атеротромбоза пузырной артерии.
Патоморфология
• Острый катаральный холецистит морфологически характеризуется гиперемией и отёком жёлчного пузыря, появлением в его просвете серозного экссудата. Микроскопически находят лейкоцитарную инфильтрацию, главным образом слизистой оболочки и подслизи-стого слоя, скопление макрофагов и серозное пропитывание.
• Флегмонозная форма сопровождается резкой гиперемией, кровоизлияниями и отёком тканей жёлчного пузыря, вследствие этого он становится напряжённым и приобретает багровый цвет. На поверхности серозной оболочки появляется фибринозный налёт, слизистая оболочка подвергается очаговому изъязвлению и некрозу. В полости жёлчного пузыря скапливается гнойный или гнойно-геморрагический экссудат. Микроскопическая картина характеризуется лейкоцитарной инфильтрацией всех слоев стенки жёлчного пузыря, иногда обнаруживают абсцессы.
• Деструктивные изменения в тканях жёлчного пузыря находят также при гангренозном холецистите. Очаги некроза захватывают все слои стенки жёлчного пузыря. Они приобретают грязно-зеленоватый или грязно-серый цвет и бывают различной величины, в просвете пузыря - гной.
В 5-10% случаев встречают бескаменный холецистит, в остальных - заболевание носиткалькулёзный характер. Независимо от факта наличия или отсутствия камней клиническая картина заболевания и лечебная тактика практически одинаковы. Относительно редко встречаютферментативный холецистит, развивающийся в результате заброса панкреатического секрета в жёлчные протоки, что может происходить при наличии обшей ампулы жёлчного и панкреатического протоков.
Клиническая картина
Острый холецистит развивается преимущественно у лиц старше 50 лет, больные пожилого и старческого возрастов составляют более 50% заболевших. Соотношение мужчин и женщин среди пациентов составляет 1:5.
Острый холецистит возникает внезапно с появления интенсивных болей в животе. Развитию острых воспалительных явлений в жёлчном пузыре нередко предшествует приступ жёлчной колики. Боли носят постоянный характер, по мере прогрессирования заболевания
их интенсивность нарастает. Они локализуются в правом подреберье и эпигастральной области, иррадиируют в правую надключичную область, плечо или лопатку. Иногда боли иррадиируют в область сердца, что можно расценить как приступ стенокардии (холецистокар-диальный синдром СП. Боткина).
Постоянные симптомы острого холецистита - тошнота и повторная рвота, не приносящая облегчения больному.Повышение температуры тела отмечают с первых дней заболевания, её характер зависит от глубины патоморфологических изменений в жёлчном пузыре. Для деструктивных форм характеренозноб.
Кожные покровы обычной окраски. Умеренная желтизна склер может быть обусловлена переходом воспаления с жёлчного пузыря на печень и развитием локального гепатита. Появление яркой желтухи кожи и склер указывает на механический характер внепечёноч-ного холестаза. Частота пульса колеблется от 80 до 120 в минуту и выше. Частый пульс - грозный симптом, свидетельствующий о тяжёлых воспалительных изменениях в жёлчном пузыре и брюшной полости.
Специфические симптомы заболевания:
• Ортнера - болезненность при поколачивании правой рёберной дуги ребром кисти:
• Мерфи - непроизвольная задержка дыхания на вдохе при пальпации правого подреберья;
• Кера - боль на высоте вдоха во время пальпации правого подреберья;
• Мюсси-Георгиевского (френикус-симптом) - болезненность при надавливании пальцем между ножками правой грудино-ключично-сосцевидной мышцы;
• Щёткина-Блюмберга - в случае вовлечения в воспалительный процесс брюшины.
Частота выявления перечисленных симптомов неодинакова, она зависит от характера морфологических изменений в жёлчном пузыре и перехода воспаления на брюшину. Состояние больного может быть различным, что определяется формой заболевания.
Катаральный холецистит
Катаральный холецистит - наиболее лёгкая форма заболевания, характеризующаяся умеренной постоянной болью в правом подреберье, тошнотой и однократной или двукратной рвотой. Общее состояние больного страдает мало. Пульс может учащаться до 90 в минуту. Язык влажный, обложен белым налётом, при пальпации живота
возникает нерезко выраженная боль в правом подреберье. Знаковые признаки заболевания (симптомы Ортнера, Мерфи, Кера, Мюсси- Георгиевского) выражены слабо или отсутствуют, симптом Щёткина-Блюмберга не определяется. Жёлчный пузырь не пальпируется, но область его проекции болезненна. В анализе крови выявляют умеренный лейкоцитоз (9-1 МО*/л).
Неярко выраженную клиническую картину катарального холецистита можно ошибочно расценить как купировавшийся приступ жёлчной колики, обусловленной холецистолитиазом. Для правильной диагностики следует обращать внимание на признаки воспаления (гипертермия, тахикардия, лейкоцитоз).
При стихании воспалительного процесса, если микробная флора погибает, но сохраняется обтурация пузырного протока, развивается водянка жёлчного пузыря. В этом случае в нём происходит всасывание составных компонентов жёлчи, содержимое его становится бесцветным, носит слизистый характер. При пальпации живота удаётся определить дно увеличенного растянутого и безболезненного жёлчного пузыря.
Флегмонозный холецистит
Флегмонозный холецистит характеризуется более выраженной клинической симптоматикой: боли носят интенсивный постоянный характер, усиливаются при дыхании и перемене положения тела. Больных беспокоят тошнота и многократная рвота. Резко выражены слабость и недомогание, ознобы. Температура тела повышается до 37,8-38 °С и более, сохраняется в течение нескольких дней.
Состояние больных средней тяжести, пульс учащается до 100 в минуту. Язык сухой, живот вздут, значительно болезнен в правом подреберье, здесь же определяются выраженная мышечная зашита и положительный симптом Щёткина-Блюмберга. При нерезко выраженном напряжении брюшной стенки удаётся пальпировать воспалительный инфильтрат или увеличенный болезненный жёлчный пузырь. Как правило, положительны симптомы острого холецистита: Ортнера, Кера, Мерфи. Количество лейкоцитов в крови достигает 12- 15-10'/л со сдвигом лейкоцитарной формулы влево, увеличена скорость оседания эритроцитов (СОЭ).
Возможны различные варианты течения острого флегмонозно-го холецистита. При своевременной госпитализации больного и проведении рациональной консервативной терапии возможны следующие исходы:
• клиническое выздоровление;
• стихание воспалительного процесса в стенке жёлчного пузыря и брюшной полости с последующим развитием эмпиемы жёлчного пузыря;
• распространение воспалительного процесса на соседние органы.
Во втором случае пальпация живота выявляет увеличенный плотный умеренно болезненный жёлчный пузырь, симптом Щёткина- Блюмберга отрицательный. Наличие в полости «отключённого» жёлчного пузыря микробной флоры и гнойного содержимого проявляется периодическими ознобами, сопровождаемыми подъёмом температуры тела до 39-40 °С. В клиническом анализе крови, взятом во время лихорадки, определяют высокий лейкоцитоз с палочкоядерным сдвигом лейкоцитарной формулы.
Третий вариант течения заболевания заключается в распространении воспалительного процесса за пределы жёлчного пузыря на соседние органы: желудок, двенадцатиперстную кишку, большой сальник, поперечную ободочную кишку. Это приводит к плотному их спаянию и образованию воспалительного инфильтрата. Перипузыр-ный инфильтрат формируется на 4-5-й день заболевания. Пальпа-торно он определяется в виде различных размеров плотного неподвижного и болезненного образования в правом подреберье. В случае стихания воспалительного процесса инфильтрат уменьшается в размерах, исчезают боли в животе, нормализуются температура тела и количество лейкоцитов в крови. Если не происходит отграничения воспалительного процесса и спаяния окружающих органов с жёлчным пузырём, развиваетсяразлитой перитонит.
Гангренозный холецистит
Гангренозный холецистит в большинстве случаев бывает результатом прогрессирования воспалительного процесса и расстройства кровообращения в стенке жёлчного пузыря. Эту форму воспаления чаше всего обнаруживают у больных пожилого и старческого возрастов со снижением реактивности организма и у страдающих атеросклерозом висцеральных ветвей брюшного отдела аорты.
В клинической картине заболевания на первый план выступают симптомы выраженной системной воспалительной реакции, тогда как болевые ощущения могут уменьшаться, что связано с гибелью нервных окончаний в жёлчном пузыре. Состояние больных тяжёлое, они вялы, заторможены или, напротив, возбуждены. Температура тела
повышается до 38-39 °С. Пульс учащается до 110-120 в минуту, дыхание поверхностное и частое. Язык сухой. Живот становится вздутым за счёт пареза кишечника, ограниченно участвует в акте дыхания, перистальтика угнетена. Ярко выражены признаки раздражения брюшины - защитное напряжение мышц передней брюшной стенки и симптом Щёткина-Блюмберга. В анализе крови количество лейкоцитов возрастает до 16-18Т0*/л с резким сдвигом лейкоцитарной формулы влево. Иногда можно наблюдать выраженную интоксикацию и тахикардию в сочетании с нормальной температурой тела (симптом «токсических ножниц»), что указывает на глубокие патоморфологи-ческие изменения стенки жёлчного пузыря с образованием участков некроза различной величины, вплоть до его тотальной гангрены.
Для первичного гангренозного холецистита, возникающего вследствие тромбоза или эмболии пузырной артерии, с первых часов заболевания характерно бурное течение. Оно проявляется симптомами выраженной интоксикации и быстро прогрессирующими признаками перитонита.
Некоторые особенности течения острого холецистита наблюдают у больных пожилого и старческого возрастов, состояние которых отягощено сопутствующими заболеваниями. У них нередко отсутствуют интенсивные болевые ощущения, защитное напряжение мышц передней брюшной стенки не выражено, в клиническом анализе крови нет высокого лейкоцитоза, в связи с чем возникают затруднения в диагностике заболевания и выборе метода лечения.
Прободной холецистит
Прободной холецистит развивается у больных с гангренозной формой заболевания в случае неоказания им своевременной хирургической помощи, а также может быть следствием пролежня стенки жёлчного пузыря камнем.
Прободение жёлчного пузыря в свободную брюшную полость ведёт к развитию разлитого перитонита. Клинически момент прободения проявляется резчайшими болями в животе, повторной рвотой. Больной покрывается холодным потом, кожные покровы становятся бледными, происходит снижение пульса и АД. Пальпация живота выявляет резкую болезненность во всех отделах и напряжение мышц передней брюшной стенки, положительный симптом Щёткина-Блюмберга.
Прободение жёлчного пузыря при отграничении его воспалительным инфильтратом протекает с менее выраженными клиническими
проявлениями, так как гнойная жёлчь из пузыря скапливается в под-печёночном пространстве и не поступает в свободную брюшную полость. Нередко это заканчивается образованием подпечёночного абсцесса, который в свою очередь может прорваться в брюшную полость. В момент прободения у больных усиливается боль в правом подреберье, постепенно нарастают симптомы системной воспалительной реакции.
Гнойный холангит
Гнойный холангит, осложняющий течение деструктивного холецистита, чаще всего возникает при наличии камней в жёлчных протоках или рубцовой стриктуры большого дуоденального сосочка. Возможно развитие холангита в результате перехода воспаления с жёлчного пузыря на внепечёночные жёлчные протоки.
Клинические признаки гнойного холангита появляются на 3-4-й день от начала приступа. Для него характерны нарастающая желтуха кожи и склер, фебрильная температура тела, сопровождающаяся ознобами, и боли в правом подреберье (триада Шарко). Состояние больных тяжёлое, они вялы и заторможены, пульс частый, АД снижено. При пальпации живота наряду с симптомами острого холецистита выявляют увеличение в размерах печени и селезёнки, выраженную болезненность в правом подреберье. В анализе крови выявляют высокий лейкоцитоз со сдвигом лейкоцитарной формулы влево, резкое увеличение СОЭ, повышение содержания билирубина, активности трансаминазы, щелочной фосфатазы и у-глутамилтрансферазы. Прогрессирующее течение острого холангита приводит к развитию печёночной и почечной недостаточности. Нередким осложнением острого холангита бывают абсцессы печени и билиарный сепсис. Летальность при гнойном обтурационном холангите достигает 40%.
Клинические проявления механической желтухи, способной осложнять течение острого холецистита, описаны в соответствующей главе учебника.
Диагностика
В типичных случаях диагностика острого холецистита не представляется трудной. Вместе с тем со сходными клиническими симптомами могут протекать прикрытая перфоративная язва желудка или
двенадцатиперстной кишки, острый панкреатит, острый аппендицит при подпечёночном расположении червеобразного отростка, правосторонняя плевропневмония, почечная колика и некоторые другие острые заболевания органов брюшной полости. Правильная и своевременная диагностика острого холецистита - необходимое условие улучшения результатов лечения.
Для уточнения диагноза и принятия адекватной лечебной тактики необходимо в течение первых 24 ч с момента госпитализации больного использовать оптимальный набор лабораторных и инструментальных исследований. Обязательные исследования: клинический анализ крови и мочи, определение содержания билирубина в крови, анализ мочи на диастазу, УЗИ органов брюшной полости, рентгеноскопия органов грудной клетки, ЭКГ. Результаты этих исследований позволяют не только исключить другие острые заболевания, но и оценить тяжесть физического состояния больного, что очень важно для выбора способа лечения.
УЗИ занимает центральное место в диагностике острого холецистита. Значимость УЗИ определяется высокой информативностью метода, неинвазивным характером, возможностью повторного исследования и использования метода для проведения лечебных процедур. Во избежание диагностических ошибок УЗИ необходимо проводить каждому больному с подозрением на острый холецистит, независимо от выраженности клинической симптоматики заболевания.
Ультразвуковые признаки острого холецистита: увеличение размеров жёлчного пузыря, утолщение его стенок, неровность контуров и наличие взвешенных мелких гиперструктур без акустической тени в полости пузыря (рис. 7-1). Выявление жидкости в подпечёночном пространстве и зоны повышенной эхогенности окружающих тканей свидетельствует о выходе воспаления за пределы жёлчного пузыря, перивезикальной воспалительной инфильтрации близлежащих органов и тканей. Фиксированная эхоструктура с акустической тенью в области шейки пузыря - признак вколоченного камня и обтураци-онной формы острого холецистита. По результатам УЗИ судят и о состоянии внепечёночных жёлчных протоков: диаметр общего печёночного протока 9 мм и более указывает на жёлчную гипертензию, которая может быть обусловлена камнем или стриктурой жёлчных протоков. Повторное УЗИ проводят для оценки эффективности проводимого консервативного лечения и выявления признаков прогрес-сирования воспалительного процесса в стенке жёлчного пузыря и брюшной полости.
Диагностировать острый холецистит позволяет лапароскопия, во время которой по визуальным признакам судят о характере воспаления жёлчного пузыря и распространённости перитонита. В настоящее время лапароскопию проводят лишь при неясном диагнозе и невозможности установить причину «острого живота» неинвазивны-ми методами исследования.
При осложнении острого холецистита механической желтухой проводят эндоскопическую ретроградную холангиопанкреатикогра-фию (ЭРХПГ). Она позволяет установить причину внепечёночного жёлчного стаза, локализацию окклюзии общего жёлчного протока, а при наличии стриктуры дистального отдела жёлчного протока - её протяжённость. Рентгеноэндоскопическое исследование необходимо выполнять в каждом случае острого холецистита, осложнённого внепечёночным холестазом, если тяжесть воспалительного процесса в брюшной полости не требует срочного оперативного вмешательства. Кроме того, проведение его целесообразно в тех случаях, когда диагностический этап исследования может быть завершён выполнением лечебной папиллотомии и назобилиарным дренированием для ликвидации жёлчного стаза. В случае устранения причины нарушения желчеоттока в кишечник путём эндоскопического вмешательства в последующем представляется возможность сократить объём операции, ограничивая её только выполнением холецистэктомии, что положительно сказывается на результатах лечения. При срочном выполнении операции у больных с острым холециститом и сопутству-
ющей механической желтухой причину последней устанавливают в ходе самой операции с помощью холангиографии, по её результатам определяют характер вмешательства на внепечёночных жёлчных протоках.
Лечение
Больные острым холециститом подлежат срочной госпитализации в хирургический стационар и должны находиться под постоянным наблюдением хирурга.
Эффективное лечение острого холецистита предполагает соблюдение принципа активной хирургической тактики. Деструктивный холецистит с различными вариантами течения - показание к хирургическому вмешательству в течение первых 24-48 ч пребывания больного в стационаре. Консервативному лечению подлежат больные с катаральным холециститом, при нём лечебные мероприятия в большинстве случаев позволяют купировать воспалительный процесс.
При активной лечебной тактике показания к операции определяют тотчас при постановке окончательного диагноза острого деструктивного холецистита, протекающего как с явлениями перитонита, так и без них. Экстренная операция, выполняемая в ближайшие 6 ч с момента поступления в стационар, показана при всех формах деструктивного холецистита (флегмонозный, гангренозный), осложнённого местным или распространённым перитонитом. Показанием ксрочной операции, предпринимаемой в первые 24 ч с момента госпитализации больного, считают флегмонозный холецистит, не осложнённый перитонитом.
Как поступают, если течение острого холецистита осложняется механической желтухой и обтурационным холангитом? В этом случае хирургическая тактика зависит от двух факторов: выраженности воспалительного процесса в жёлчном пузыре и брюшной полости, а также тяжести состояния больного (степени операционно-анесте-зиологического риска). При наличии показаний к экстренной операции причину механической желтухи устанавливают путём проведения интраоперационной холангиографии и в зависимости от выявленной патологии проводят адекватное вмешательство на вне-печёночных жёлчных протоках. Больным, не нуждающимся в экстренной операции, первоначально выполняют эндоскопическую ретроградную холангиографию и эндоскопическую папиллотомию.
завершая её литоэкстракцией или назобилиарным дренированием для устранения холестаза и холангита. Через 24-48 ч после эндоскопического вмешательства прибегают ко второму этапу лечения - операции холецистэктомии.
Важное место в программе активной лечебной тактики при остром холецистите занимает консервативная терапия, в большинстве случаев позволяющая купировать воспалительный процесс у больных с катаральной формой холецистита и в то же время играющая роль предоперационной подготовки у больных с деструктивным холециститом. Комплекс консервативных мероприятий, основанный на патогенетических принципах, включает следующие лечебные мероприятия: голодание (разрешено щелочное питьё), локальная гипотермия (пузырь со льдом на область правого подреберья), для уменьшения болей и снятия спазма сфинктера Одди назначают ненаркотические анальгетики и холинолитические спазмолитические препараты (метамизолнатрий, метамизолнатрий + питофенон + фен-пиверина бромид,дротаверин, мебеверин, платифиллин). Детокси-кацию и парентеральное питание обеспечивают инфузионной терапией в объёме 2,0-2,5 л в сутки. Критериями адекватного объёма инфузионных сред, вводимых из расчёта 30-50 мл на 1 кг массы тела, служат нормализация гематокрита, ЦВД и диуреза. При осложнении острого холецистита механической желтухой или холангитом дополнительно назначают гемодез, раствор аминокислот, свежезамороженную плазму, витамины С, В(и В6.
Важный компонент консервативной терапии острого холецистита - антибактериальные препараты, назначаемые с целью предотвращения генерализации абдоминальной инфекции. К сожалению, антибиотики не могут ограничить деструктивный процесс в жёлчном пузыре из-за резкого снижения их накопления как в стенке пузыря вследствие сосудистых нарушений, так и в жёлчи в связи с обтурацией камнем шейки пузыря. Между тем, они играют важную роль, блокируя дис-семинацию инфекции и развитие системной воспалительной реакции. Кроме того, использование антибактериальных средств служит средством профилактики послеоперационных гнойных осложнений.
Удаление жёлчного пузыря выполняют от шейки или от дна. Преимущества имеет метод холецистэктомии от шейки: первоначально
выделяют пузырную артерию и пузырный проток, их пересекают и перевязывают (рис. 7-2).
Разобщение жёлчного пузыря с жёлчным протоком предупреждает возможную миграцию камней в протоки, а предварительная перевязка артерии обеспечивает бескровное выделение жёлчного пузыря из ложа печени.
К удалению жёлчного пузыря от дна (рис. 7-3) прибегают при наличии плотного воспалительного инфильтрата в области его шейки и печёночно-двенадцатиперстной связки, поскольку он затрудняет идентификацию важных анатомических элементов этой зоны.
Для выполнения холецистэктомии из мини-лапаротомного доступа проводят транс ректальный разрез длиной 4-5 см ниже реберной дуги и на 3-4 см вправо от срединной линии. Операцию осуществляют с помощью инструментального комплекса «мини-ассистент» (см. рис. 16-5). Удаление жёлчного пузыря из мини-доступа при остром холецистите выполняют в тех случаях, когда ещё не сформировался плотный воспалительный инфильтрат в подпечёночном пространстве, обычно при длительности заболевания не более 72 ч. Если инфильтрат не позволяет идентифицировать анатомические взаимоотношения элементов гепатодуоденальной связки, целесообразен переход на широкую лапаротомию. Операция из мини-доступа отличается от традиционной холецистэктомии малой травматичностью, низкой частотой развития ранних и поздних осложнений, а также быстрым восстановлением трудоспособности больного.
Видеолапароскопическую холецистэктомию при остром холецистите проводят при сроке заболевания 48-72 ч. При большей длительности заболевания эндоскопическая операция часто обречена на неудачу. Более того, она чревата угрозой развития тяжёлых интраоперацион-ных осложнений из-за воспалительного
инфильтрата в подпечёночной области. Применение лапароскопической операции противопоказано при осложнённых формах острого холецистита - распространённом перитоните, механической желтухе, обтурационном холангите. При возникновении технических трудностей в ходе эндоскопической операции и угрозы развития ятрогенных повреждений переходят на открытый способ операции. При остром холецистите подобное случается достаточно часто (до 20% случаев).
Холецистостомия
Холецистостомия - паллиативная малотравматичная операция, позволяющая достичь положительного лечебного эффекта и снизить летальность. Её следует считать стандартом хирургического лечения больных острым холециститом, у которых риск выполнения холецистэктомии чрезмерно велик в связи с тяжёлыми соматическими заболеваниями. Патогенетическим обоснованием целесообразности выполнения холецистостомии служат снятие внутрипузырной гипертензии и отведение наружу инфицированной жёлчи, что устраняет нарушения кровотока в стенке жёлчного пузыря, предотвращая тем самым возникновение и прогрессирование в нём деструктивных изменений.
Холецистостомию выполняют путём чрескожного дренирования жёлчного пузыря под ультразвуковым контролем, лапароскопическим способом или путём открытой лапаротомии. Во всех случаях применяют местное обезболивание при обязательном участии анестезиолога.
Наиболее щадящий способ - пункция и последующее дренирование жёлчного пузыря, проводимое чрескожно и транспечёночнопод УЗИ-контролем (рис. 7-4). В полость жёлчного пузыря устанавливают дренаж, позволяющий отводить наружу гнойную жёлчь и активно осуществлять его санацию. Воздерживаются от применения этого метода при распространённом перитоните, гангрене жёлчного пузыря и в случае заполнения всей его полости камнями.
Лапароскопическую холецистостомию выполняют под контролем видеоэндоскопии после визуальной оценки характера воспалительного процесса в брюшной полости и при условии свободного от сращений с соседними органами дна жёлчного пузыря. Из многочисленных модификаций этого способа хорошо зарекомендовала себя методика прямой пункции жёлчного пузыря троакар-катетером с оставлением в его полости баллонного катетера, благодаря которому обеспечивается герметичность стомы и формируется доступ в полость жёлчного пузыря для его активной санации и удаления конкрементов. Несмотря на малоинвазивный характер и эффективность лапароскопической холецистостомии, применяют её редко, что связано с необходимостью создания пневмоперитонеума и возможным ухудшением состояния больного во время процедуры.
Открытую холецистостомию (рис. 7-5) выполняют под местным обезболиванием из лапаротомного доступа в правом подреберье. Формируют холецистостому подшиванием дна жёлчного пузыря к париетальной брюшине, а в случае невозможности подшить жёлчный
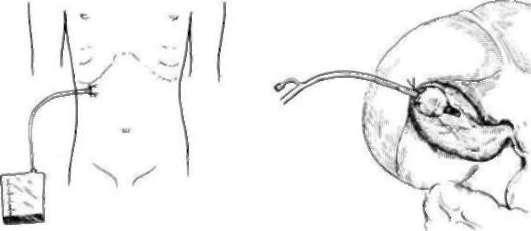
Рис. 7-5. Открытая холецистостомия. В полости жёлчного пузыря установлен баллонный катетер.
пузырь к брюшной стенке его отграничивают тампонами. При открытой холецистостомии образуется широкий канал для доступа в полость жёлчного пузыря и его санации, что важно в профилактике рецидива заболевания. Однако этот способ создания холецистостомии наиболее травматичен в связи с разрезом брюшной стенки.
При наружном дренировании жёлчного пузыря купирование воспалительного процесса и его клинических признаков происходит к 8-10-му дню. Дальнейшая лечебная тактика зависит от тяжести состояния больного и степени операционно-анестезиологического риска. Если он крайне высок, холецистостомия становится основным и окончательным методом лечения. При улучшении общего состояния больного и снижении риска хирургического вмешательства выполняют холецистэктомию с использованием малоинвазивных технологий. Двухэтапное лечение подобных больных с острым холециститом способствует резкому снижению частоты летального исхода.
Операции на жёлчном пузыре и жёлчных протоках, проводимые при остром холецистите, заканчивают установкой в подпечёночном пространстве контрольного дренажа. Дренаж в брюшной полости необходим для оттока наружу жёлчи и крови, подтекающих из ложа пузыря. В случае интенсивного крово- и желчеистечения дренаж позволяет своевременно диагностировать несостоятельность лигатур культи пузырной артерии или протока. При отсутствии отделяемого по дренажу его удаляют на 3-й послеоперационный день.
Тампоны в брюшную полость при остром холецистите вводят исключительно редко. Такая необходимость возникает при осложнении заболевания подпечёночным абсцессом или невозможности остановить кровотечение из ложа пузыря в печени. При абсцессе тампоны подтягивают на 5-й день и удаляют на 9-й, гемостатический тампон извлекают на 4-5-й день после операции.
В послеоперационном периоде продолжают терапию, направленную на коррекцию метаболических нарушений, профилактику инфекционных и тромбоэмболических осложнений. Инфузионную терапию в объёме 2,0-2,5 л жидкости в сутки необходимо проводить не менее 3 дней. Своевременное выполнение операции и рациональная интенсивная терапия в послеоперационном периоде обеспечивают благоприятный исход хирургического лечения больных острым холециститом.
Анатомия желчевыводящей системы необычайно вариабельна. Это нужно учитывать при любом хирургическом вмешательстве в правом верхнем квадранте брюшной полости. В последнее время данное суждение стало особенно актуальным в свете наступления эпохи лапароскопической хирургии желчевыводящих путей. В начале 1990-х гг., лапароскопические хирургические методы были адаптированы для применения в системе желчных протоков, и лапароскопическая холецистэктомия стала стандартом для желчнокаменной болезни. К сожалению, на ранних этапах освоения метода было множество эпизодов повреждения желчных протоков. Они были в значительной степени результатом недостаточного знания хирургами анатомических вариантов системы желчных протоков. Полное понимание типичной и аномальной анатомии - необходимое условие для безопасной хирургии. Стандартная, или классическая, анатомия желчевыводящих путей наблюдается только у одной трети пациентов, поэтому всегда нужно предвидеть возможность анатомических отклонений (рис. 17.1).

Рис. 17.1. Нормальная, или классическая анатомия желчевыводящей системы.
1 - желчный пузырь
2 - общая печеночная артерия
3 - общий желчный проток
4 - воротная вена
5 - верхняя брыжеечная вена и артерия
Желчная система представена организованной совокупностью протоков, по которым проходит желчь от паренхимы печени, где она образуется, в двенадцатиперстную кишку и в конечном итоге рассредоточивается по всему ЖКТ. Чтобы хорошо разобраться в анатомии желчевыводящей системы, полезно рассматривать внутрипеченочную систему отдельно от внепеченочной. Внутрипеченочная система включает мелкие внутрипеченочные протоки, объединенные в правые и левые печеночные протоки. Последние в свою очередь собирают желчь из правой и левой долей печени соответственно. Левый печеночный проток длиннее правого и часто расширяется первым при дистальной обструкции. Правый и левый протоки сливаясь (обычно за пределами паренхимы, в воротах печени) формируют общий печеночный проток. С общим печеночным протоком через пузырный проток соединяется желчный пузырь. Образовавшийся при их слиянии проток называют общим желчным протоком. Дистальнее он подходит к нисходящему отделу двенадцатиперстной кишки.
Нормальный желчный пузырь - это полый грушевидный орган, вмещающий 30-50 мл жидкости. Выпуклый проксимальный отдел называют дном, округлую среднюю часть - телом, а узкий дистальный отдел - шейкой. Иногда выпячивание шейки называют воронкой или карманом Хартмана. Пузырный проток является продолжением шейки желчного пузыря и имеет длину от 3 мм до 3 см. Обычно он соединяется с общим печеночным протоком с боковой стороны, однако бывают и другие варианты. Именно вариатильность слияния пузырного протока с общим желчным протоком, может быть не распознана и привести к ятрогенным повреждениям желчных протоков (рис. 17.2).
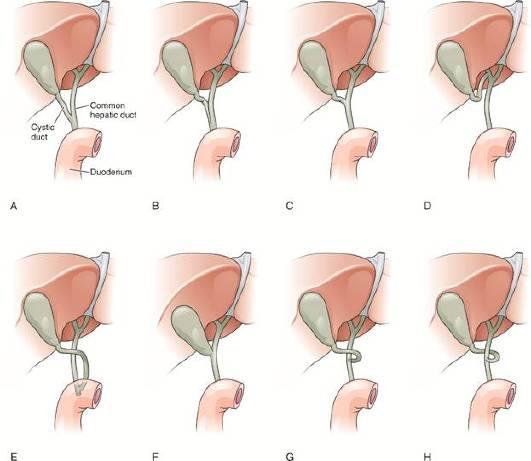
Рис. 17.2. Варианты владения пузырного протока: A - норма; B - параллельный ход пузырного протока общему желчному протоку; C - короткий пузырный проток; D - впадение в правый печеночный проток; E - низкое впадение пузырного протока, пересекающего общий желчныйпроток спереди; F - отсутствие пузырного протока; G - медиальное впадение пузырного протока; H - переднее впадение пузырного протока.
1 - общий печеночный проток
2 - пузырный проток
3 - двенадцатиперстная кишка
Диаметр общего желчного протока у здоровых людей 4-8 мм. Он может стать шире при дистальной обструкции камней или злокачественной опухолью, а также после холецистэктомии и у пациентов преклонного возраста. Как правило, диаметр протока (измеряемый в миллиметрах с помощью УЗИ) у пациентов равен их возрасту разделенному на 10. Например, у 80-летней женщины диаметр протока, вероятно, составит 8 мм. Хотя направление общего желчного протока может изменяться, он обычно проходит позади двенадцатиперстной кишки через головку поджелудочной железы в нисходящий отдел двенадцатиперстной кишки. В конце желчный проток обычно соединяется с протоком поджелудочной железы и впадает в двенадцатиперстную кишку через ампулу фатерова сосочка. В этой области имеется гладкомышечный сфинктер Одди, который окружает оба протока. Ответная реакция на разнообразные раздражители (такие, как холецистокинин) приводит к его расслаблению (часто сопровождаемому сокращением желчного пузыря), что позволяет желчи поступать в кишку. Опухолевая обструкция в этом месте часто дает начало типичному признаку расширения протока при эндоскопической ретроградной холангиопанкреатикографии (рис. 17.3). Необычная форма заболевания, которая затрагивает прежде всего внутрипеченочные желчные протоки, известна как болезнь Кароли и заслуживает отдельного внимания. Хотя она классифицируется как кистозная болезнь печени, данный процесс фактически представляет собой множественные расширения внутрипеченочных желчных протоков, вызывая формирование скоплений желчи, которые при лучевых м етодах диагностики интерпретируют как кисты. Более точно это классифицируется, как кистозная болезнь желчевыводящих протоков. Данный синдром часто сочетается с врожденным фиброзом печени. Иногда развиваются внутрипеченочные камни; у некоторых пациентов может развиться карцинома протоков. Как правило, пациенты преживают периодические приступы холангита, поэтому оказывать помощь лучше всего хирургическим вмешательством и дренированием. Эндоскопическое дренирование желчных протоков также может играть терапевтическую роль в некоторых ситуациях.
Артериальное кровоснабжение желчевыводящей системы осуществляется ветвями артерий, кровоснабжающих печень. Как и в анатомии желчных протоков, изменчивость здесь - правило, а не исключение (рис. 17.4). Отличное от классической анатомии, полное кровоснабжение печени печеночной ветвью чревного ствола выявляют в 25-75% наблюдений. Обычно чревный ствол отходит от передней стенки аорты и в свою очередь, направляясь вперед, делится на левую желудочную, селезеночную и общую печеночную артерии. Общая печеночная артерия, образуя петлю и направляясь вперед и краниально в пределах малого сальника, отдает гастродуоденальную ветвь, кровоснабжающую двенадцатиперстную кишку и поджелудочную железу. Собственная печеночная артерия проходит до ворот печени и делится на правую и левую ветви. Кровоснабжение желчного пузыря осуществляется через пузырную артерию, обычно являющуюся ветвью правой печеночной артерии, но может быть и ветвью «смещенной» правой (5%), левой (10%) или общей печеночной артерией (10%). В некоторых аномальных случаях кровоснабжение может обеспечиваться ветвями, берущими начало от верхней брыжеечной артерии, левой желудочной артерии, аорты и других висцеральных ветвей. Эти отклонения могут быть как сопутствующими (в дополнение к нормальному артериальному кровоснабжению), так и обеспечивать первичное кровоснабжение этой области. Иногда правую печеночную артерию путают (во время операции) с пузырной артерией, когда она проходит параллельно пузырной артерии или в брыжейке желчного пузыря (иногда называют «горб гусеницы»). В такой ситуации путаницы можно ошибочно лигировать или повредить правую печеночную артерию.
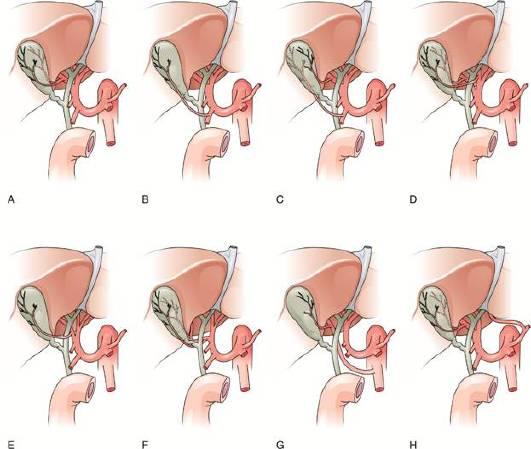
Рис. 17.4. Варианты кровоснабжения желчного пузыря: A - норма; B - H - возможные варианты образования пузырной артерии и ее расположение.
Желчные протоки кровоснабжаются от малых безымянных ветвей печеночной артерии. Венозный отток осуществляется через систему воротной вены. Лимфатические протоки желчного пузыря дренируются в узел пузырного протока (или узел Кало), расположенный между пузырным и общим печеночным протоками. Этот узел служит потенциальным местом метастазирования гепатоцеллюлярного и холангиоцеллюлерного рака и определяет резектабельность.
Треугольник Кало - это критическая анатомическая область, образован пузырным протоком латерально, общим печеночным протоком медиально и печенью сверху[4]. Эта маленькая область содержит многие важные структуры, включая пузырную артерию, правую печеночную артерию, узел Кало; потенциальные варианты сочетания трубчатых структур бесчисленны. Эту область следует тщательно анализировать во время холецистэктомии, чтобы избежать неосторожного повреждения протоков и артерий. При холецистите эта область весьма часто вовлечена в воспаление, таким образом, препарирование может оказаться сложным и опасным. Тем не менее надлежащая идентификация структур в пределах этой и смежных областей - первостепенный фактор безопасной холецистэктомии.
Печеночно-двенадцатиперстная связка включает общий желчный проток, располагающийся спереди и латерально, собственную печеночную артерию, лежащую спереди и медиально и воротную вену сзади. Кроме того, через эту важную структуру проходят нервы и лимфатические сосуды. Доступ к сальниковой сумке осуществляют позади печеночно-двенадцатиперстной связки через сальниковое отверстие, или отверстие Винслоу. При необходимости доступ к сосудам печени может осуществляться посредством захвата печеночно-двенадцатиперстной связки большим и указательным пальцами с пережатием ее сосудистых структур (прием Прингла), помогает избежать кровотечения из паренхимы печени при травмах или во время резекции. Сжатие печеночно-двенадцатиперстной связки при некоторых обстоятельствах может продолжаться до 1 ч, но в этом случае не исключено ишемическое повреждение печени.
Желтуха - синдром, характеризуемый желтушным окрашиванием кожных покровов, слизистых оболочек и склер, обусловленный повышенным накоплением билирубина в сыворотке крови, а также в других жидкостях и тканях организма.
Механическая желтуха - осложнение патологических процессов, нарушающих отток желчи на различных уровнях желчевыводящих протоков.
ПРИЧИНЫ РАЗВИТИЯ ЖЕЛТУХИ
В течение суток печень выделяет в желчь до 250 мг желчного пигмента - билирубина. Он образуется в клетках ретикулоэндотелиальной системы из высвобождающегося гемоглобина зрелых эритроцитов. Схема нормальных биохимических превращений билирубина представлена на рис. 20-1.
Повышение содержания билирубина в сыворотке крови более 40 мкмоль/л вызывает желтушное окрашивание склер, слизистых оболочек и кожных покровов. Билирубин проникает почти во все жидкости и большую часть тканей организма, вызывая желтое прокрашивание экссудатов и транссудатов, секретов различных желез (поджелудочной, слюнных, потовых и др.). У пациентов с анемией и светлой кожей желтуху обнаруживают раньше, в то время как у смуглых больных она дольше остается незамеченной.
В настоящее время известно множество разновидностей желтухи, различающихся по этиологии, механизмам нарушения пигментного обмена и в связи с этим требующих различных лечебно-диагностических мероприятий (рис. 20-2). В повышении концентрации билирубина играют роль три основные причины.
1. Ускоренный распад эритроцитов с избыточным образованием и накоплением непрямого билирубина в сыворотке крови, когда ферментные системы печени неспособны обеспечить дальнейшее превращение
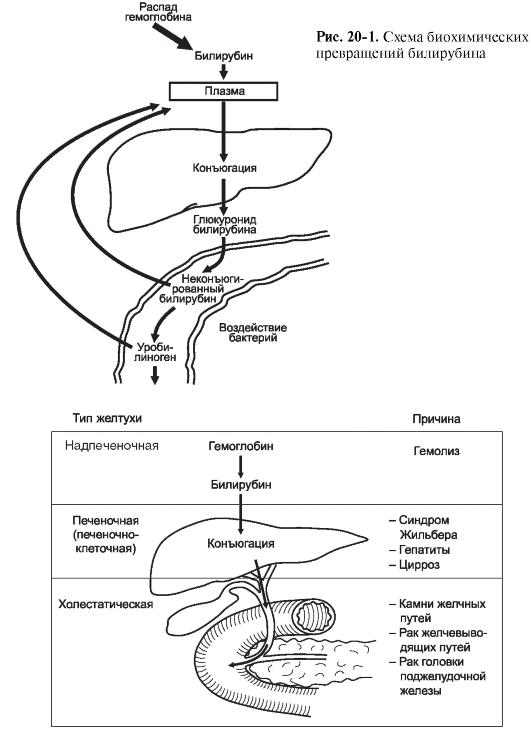
Рис. 20-2. Нарушения пигментного обмена при различных видах желтухи
и выделение избыточного количества пигмента (гемолитическая желтуха). Причиной подобных состояний могут быть интоксикации, отравления, крупные гематомы и др.
2. Поражение печеночных клеток, ведущее к нарушению биохимических превращений билирубина (захвату клетками печени и конъюгации) и проникновению его из крови в желчные капилляры(паренхиматозная желтуха). Такие нарушения развиваются при острых и хронических гепатитах, циррозах печени, гепатозах. Небольшую группу составляют пациенты с различными вариантами наследственно обусловленных нарушений пигментного обмена - так называемыми доброкачественными гипербилирубинемиями (синдромами Жильбера, Криглера-Найяра, Дабина-Джонсона и др.). Как правило, нарушения конъюгации билирубина у этих больных связывают с наследственной недостаточностью ферментов (в частности, глюкуронилтрансферазы). Причиной некоторых форм приобретенной ферментопатии считают использование гепатотоксичных препаратов (парацетамола, экстракта мужского папоротника и др.). Подобные варианты желтухи чаще возникают у лиц молодого возраста, чаще требуют наблюдения без стационарного лечения, однако могут быть причиной диагностических ошибок, обусловливающих неправильную лечебную тактику вплоть до напрасных лапаротомий.
3. Нарушение проходимости желчных путей, ведущее к попаданию билирубина из желчных капилляров в кровеносные и лимфатические сосуды(механическая желтуха).
Механическую желтуху могут вызывать следующие заболевания и состояния.
• Доброкачественные (80%):
- холедохолитиаз;
- стеноз большого сосочка двенадцатиперстной кишки;
- холангит;
- острый папиллит, полипы большого сосочка двенадцатиперстной кишки;
- острый и хронический панкреатит;
- рубцовая стриктура желчевыводящих протоков;
- прочие редкие причины (врожденные аномалии, перихоледохеальный лимфаденит, паразитарные поражения и др.).
• Злокачественные поражения различной локализации (20%):
- рак большого сосочка двенадцатиперстной кишки, поджелудочной железы, желчного пузыря или желчевыводящих протоков;
- первичный и метастатический рак печени.
Синдром механической желтухи следует рассматривать как сложный патофизиологический комплекс, проявляющийся признаками поражения всех органов и систем, преимущественно печени и почек. Несмотря на разнообразие заболеваний, ведущих к развитию механической желтухи, основные патофизиологические звенья синдрома сходны, что позволяет руководствоваться единой лечебно-диагностической тактикой как при доброкачественной, так и при злокачественной его этиологии.
Механизмы развития различных видов желтухи, как правило, сочетаются и редко встречаются в чистом виде. Например, при гемолитической желтухе присоединяется механический компонент в связи со сгущением желчи и обтурацией мелких желчных капилляров. При длительной механической желтухе присоединяется поражение печеночных клеток, и она приобретает некоторые черты желтухи, свойственной гепатиту.
ДИАГНОСТИКА
Диагноз механической желтухи включает два основополагающих момента: подтверждение обтурационного характера желтухи и определение конкретной причины нарушения проходимости желчевыводяших путей.
Решение первой задачи крайне важно, поскольку на догоспитальном этапе возникает до 20% диагностических ошибок, приводящих к госпитализации пациентов в лечебные учреждения, не соответствующие характеру заболевания. Больных с механической желтухой в части случаев ошибочно госпитализируют в инфекционные отделения, несколько реже пациенты с паренхиматозной желтухой первоначально поступают в хирургические стационары. В обоих случаях ошибочная госпитализация приводит к неверной тактике ведения - затягиванию сроков декомпрессии желчных протоков, нарушениям противоэпидемического режима и т.д. Кроме того, следует помнить, что желтое прокрашивание кожи и других тканей организма может происходить и в нормальных условиях при обильном приеме пищи, содержащей красящие вещества, например моркови (каротин), или некоторых лекарственных средств (акрихина).
Механическая желтуха, обусловленная холедохолитиазом, появляется через несколько часов или суток послевыраженного болевого приступа и характеризуется быстрым прогрессированием. Возникновение желтухи сопровождается кожным зудом, вызывающим расчесы, преимущественно на передней брюшной стенке и разгибательных поверхностях конечностей. Для механической желтухи, вызванной опухолью головки поджелудочной железы илибольшого дуоденального сосочка, характерны отсутствие болей и постепенное развитие заболевания. Патогномониченсиндром Курвуазье, характеризуемый пальпируемым увеличенным безболезненным желчным пузырем на фоне желтухи.
Основные клинические проявления, признанные характерными спутниками желтухи, представлены на рис. 20-3. Как правило, выраженность симптомов пропорциональна длительности желтухи.
После оценки клинико-анамнестических и лабораторных данных применяют инструментальные методы исследования. Наибольшее распространение получили следующие способы диагностики:
• УЗИ;
• ЭРХПГ;
• чрескожная чреспеченочная холангиография;
• чреспузырная фистулография (после холецистостомии);
• КТ;
• магнитно-резонансная холангиопанкреатография;
• лапароскопия.
Выбор метода инструментальной диагностики определяется предполагаемой причиной обтурации желчных протоков, возможностью продолжения диагностического исследования в лечебное вмешательство и техническим оснащением лечебного учреждения.
Важную роль в диагностике характера желтухи отводят УЗИ, подтверждающему обтурационный характер заболевания путем выявления дилатации желчных протоков, а в 75% наблюдений позволяющему выявить непосредственную причину механической желтухи (рис. 20-4).
Важнейшие достоинства метода:
• скрининговый характер, неинвазивность, отсутствие осложнений;
• возможность использования при любой степени тяжести состояния пациентов и во время беременности;
• одновременная оценка состояния желчных протоков и других анатомических структур (печени, поджелудочной железы, забрюшинного пространства и т.д.);
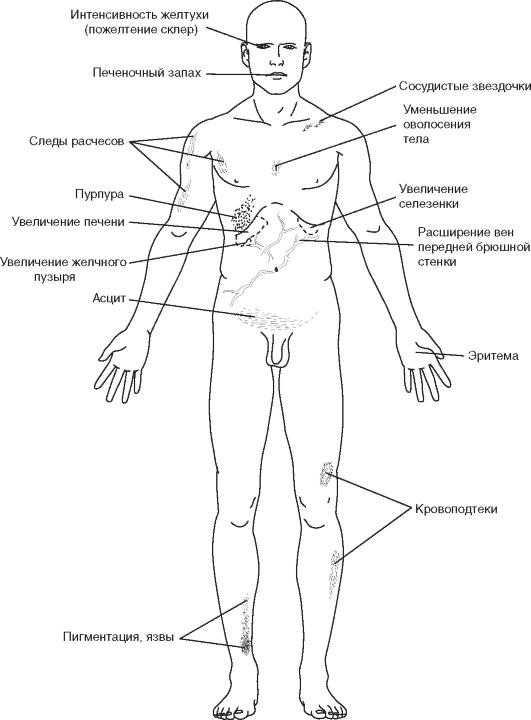
Рис. 20-3. Основные клинические проявления желтухи
• возможность ультразвукового наведения при пункционных методах декомпрессии и биопсии;
• объективный выбор метода декомпрессии желчевыводящих путей.
Несмотря на постоянное совершенствование ультразвуковой диагностики, не всегда с ее помощью удается получить полную информацию о характере патологии желчных путей, достаточную для решения вопроса о методе декомпрессии протоков. Для прогнозирования эффективности вмешательств (в частности, эндоскопической папиллосфинктеротомии) необходимы точные данные о размерах, форме, количестве конкрементов, протяженности и уровне стриктур протоков и других важных деталях.
Наиболее точный способ определения причин механической желтухи - прямое контрастирование желчных путей. Метод выбора - ЭРХПГ (рис. 20-5). Наряду с возможностью контрастирования желчных протоков, метод позволяет визуально оценить состояние желудка и двенадцатиперстной кишки, большого дуоденального сосочка и периампулярной области, а также констатировать факт поступления желчи
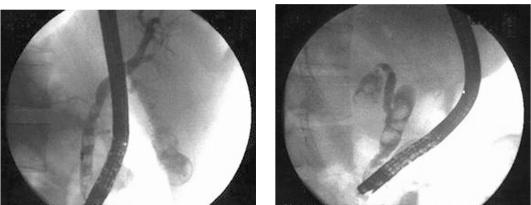
Рис. 20-5. Эндоскопическая ретроградная холангиография при холедохолитиазе
в просвет кишечника. У части больных желтухой возможности эндоскопического ретроградного контрастирования желчных протоков могут быть ограничены рядом обстоятельств, такими как ранее перенесенные операции на желудке, расположение большого дуоденального сосочка в полости крупных дивертикулов, наличие непреодолимого препятствия в устье общего желчного протока (стеноза, вклиненного конкремента, опухоли дистального отдела протока). Подобные трудности встречают приблизительно у 10% больных с обтурационной желтухой.
При неэффективности ретроградного контрастирования желчных протоков используют чрескожную чреспеченочную холангиографию. Для пункции внутрипеченочных желчных протоков применяют специальные тонкие иглы, конструкция которых позволяет избежать свойственных для этого исследования осложнений (крово- и желчеистечения в брюшную полость). Если у больного расширены внутрипеченочные желчные протоки, чрескожная чреспеченочная холангиография позволяет получить информацию об их состоянии в 97% случаев, при отсутствии расширения протоков - в 60% наблюдений.
В части случаев для получения целостного представления о желчевыводящих путях выше и ниже участка сужения (например, при рубцовых или опухолевых стриктурах протоков) целесообразно сочетанное ретро- и антеградное контрастное исследование билиарного тракта. Это позволяет уточнить возможность и характер реконструктивного хирургического вмешательства.
Один из распространенных способов контрастирования билиарного дерева - использование холецистостомы, наложенной прямым (хирургическим) путем либо пункционным под контролем УЗИ или лапароскопии (рис. 20-6). Необходимое условие для подоб-

Рис. 20-6. Чрескожная холецистостомия, выполненная под контролем УЗИ. На холецистохолангиограмме определяются дилатация желчных протоков, отсутствие эвакуации контрастного вещества в двенадцатиперстную кишку, обусловленное опухолью головки поджелудочной железы
ного исследования - проходимость пузырного протока. Об этом, как правило, свидетельствует поступающая по дренажу желчь. Чаще всего необходимость в наружном дренировании желчного пузыря возникает при сочетании механической желтухи с острым деструктивным холециститом или при опухолях головки поджелудочной железы (дистального отдела протоков), когда крайне тяжелое состояние больных не позволяет выполнить паллиативное или радикальное вмешательство традиционным хирургическим способом.
Высокую разрешающую способность имеет КТ, позволяющая наряду с выявлением дилатации протоков и причины их обструкции выполнить прицельную биопсию или декомпрессионное вмешательство. В отличие от УЗИ, диагностические возможности метода не снижаются при метеоризме, асците, ожирении.
В последние годы широкое распространение приобретает магнитно-резонансная холангиопанкреатография, обладающая высокой точностью в диагностике причин механической желтухи, особенно в оценке характера и протяженности стриктур желчных путей, а также внутрипротоковых образований. Вместе с тем этот метод лишен пункционнодренажных лечебных возможностей.
Лапароскопию при механической желтухе в настоящее время применяют редко, в основном для подтверждения опухолевого процесса (первичного или метастатического) в гепатодуоденальной области. Цели исследования - определение операбельности злокачественного заболевания и прицельная биопсия.
ЛЕЧЕНИЕ
Основная задача лечебных мероприятий при механической желтухе - ликвидация холестаза и профилактика печеночно-почечной недостаточности. Учитывая высокую летальность при операциях на высоте желтухи, общепринят этапный лечебный подход.
На первом этапе используют комплексную консервативную терапию и малоинвазивные методы, направленные на ликвидацию холестаза. При неразрешающейся или нарастающей желтухе декомпрессионные вмешательства необходимо выполнить в срочном порядке в течение 2-3 сут с момента поступления больного в стационар.
Если малоинвазивные вмешательства не стали окончательными способами лечения, на втором этапе, по мере разрешения желтухи, в более благоприятных обстоятельствах проводят хирургические операции.
Все диагностические мероприятия с первых суток пребывания больного в стационаре выполняют на фоне консервативной терапии, направленной главным образом на профилактику печеночной и почечной недостаточности. При оценке клинического течения и определении тактики ведения пациентов с механической желтухой важнейшим фактором считают степень печеночной недостаточности. По клиниколабораторным данным выделяют три степени ее выраженности
(табл. 20-2).
Таблица 20-2. Оценочные критерии степени тяжести печеночной недостаточности
Критерии
Степень печеночной недостаточности
I - легкая
II - средняя
III - тяжелая
Длительность желтухи
До 7 дней
7-14 дней
Более 14 дней
Энцефалопатия
Нет
Снижение аппетита, адинамия, бессонница
Отсутствие аппетита, выраженная адинамия, инверсия сна, эйфория
Гемодинамика
Стабильная
Стабильная
Артериальная гипотензия
Диурез
Достаточный
Достаточный
Снижен
Концентрация билирубина, мкмоль/л
До 100
100-200
Более 200
Концентрация мочевины
Не изменена
Не изменена
Повышена
Альбумино-глобулиновый коэффициент
Более 1,2
1,2-0,9
Менее 0,9
Нарушение поглотительновыделительной функции гепатоцитов (радиогепатография, Тmах, мин). Норма - до 25%
До 50
50-60
Более 60
Снижение печеночного кровотока, %
На 25-30
На 30-50
Более 50
При наличии в момент поступления печеночной недостаточности III степени лечебный комплекс проводят в реанимационном отделении. На фоне диеты (стол № 5а), обогащенной углеводными и белковыми продуктами, проводят массивную инфузионную терапию (переливание глюкозы с инсулином, солевых растворов, гемодеза*, реополиглюкина*, белковых препаратов, кровезаменителей) и форсированный диурез. Консервативная терапия включает также ком-
плексную витаминотерапию и препараты, улучшающие функции печени, - кокарбоксилазу, фосфолипиды.
Назначают также аминокислоты (глутаминовую кислоту и метионин), стимуляторы метаболизма (диоксометилтетрагидропиримидин), анаболические гормоны. Целесообразно назначение стероидных гормонов: преднизолона по 60-120 мг/сут, в тяжелых случаях внутрипеченочного холестаза и холангита - до 1000 мг/сут.
Важный компонент лечения - профилактика эрозий, острых изъязвлений и кровотечений из ЖКТ. Для этого назначают антацидные и обволакивающие слизистую оболочку желудка препараты, ингибиторы протонного насоса.
В случаях тяжелого эндотоксикоза используют методы экстракорпоральной детоксикации (плазмаферез, гемодиализ и др.).
Важнейшей задачей ведения больных с механической желтухой следует считать профилактику острого холангита - инфекционно-воспалительного осложнения обтурации желчных путей. Клиническое течение острого холангита характеризуется тремя основными симптомами: болевым синдромом, ознобом, лихорадкой (триадой Шарко). Замедление тока желчи приводит к быстрому распространению микрофлоры на магистральные и внутрипеченочные желчные ходы, что вызывает тяжелую системную воспалительную реакцию, внутрипеченочные абсцессы, острую гепатоцеребральную и почечную недостаточность. Стремительное развитие генерализованного гнойно-септического процесса обусловлено большой площадью поверхности желчных протоков, прямым билиовенозным шунтом токсинов и бактерий, печеночно-почечной недостаточностью. Эти процессы усугубляются при механической желтухе метаболическими нарушениями, связанными с холемией и ахолией: колонизацией микроорганизмов в кишечнике и их транслокацией в кровоток, токсическим воздействием билирубина, коагулопатией, полиорганными нарушениями и др.
Все это обусловливает высокую летальность при остром холангите (до 30%). В целях предотвращения этого осложнения используют антибиотики цефалоспоринового ряда. При появлении клинико-лабораторных признаков острого холангита декомпрессионные вмешательства и комплексную консервативную терапию проводят в экстренном порядке.
Декомпрессия желчных протоков
Выбор способа декомпрессии желчевыводящих протоков зависит от уровня и характера препятствия для оттока желчи. Арсенал этих мето-
дов достаточно велик и продолжает расширяться. Наибольшее распространение получили следующие мотоды:
• эндоскопическая папиллосфинктеротомия;
• чрескожная чреспеченочная холангиостомия;
• хирургическая холецистостомия;
• пункционная холецистостомия под контролем УЗИ или лапароскопии;
• эндопротезирование желчных протоков;
• интраоперационные (прямые) методы декомпрессии желчных протоков.
Для каждого из методов инструментальной декомпрессии желчных протоков существуют показания и ограничения. Как правило, методы декомпрессии становятся продолжением диагностических процедур, что также следует считать одним из факторов, определяющих целесообразность применения того или иного метода.
Инструментальные малоинвазивные методы декомпрессии желчных путей
Среди малоинвазивных методов разрешения холестаза важнейшее место занимает эндоскопическая папиллосфинктеротомия - метод выбора устранения желтухи, обусловленной холедохолитиазом. Показания к выполнению метода и прогнозирование его результативности основываются на точном представлении о характере препятствия для желчеоттока (размерах конкрементов, их расположении и количестве, состоянии устья общего желчного протока и т.д.). Если размеры конкрементов не превышают диаметра общего печеночного протока, их можно удалить с помощью этой эндоскопической манипуляции и тем самым восстановить пассаж желчи в двенадцатиперстную кишку. Подобную ситуацию встречают более чем в 90% наблюдений, что обеспечивает успешную санацию желчных протоков с помощью эндоскопической папиллосфинктеротомии у большинства пациентов.
В случаях, когда размеры конкрементов велики и превышают диаметр просвета нижележащих отделов желчных путей, не происходит спонтанного отхождения конкрементов после эндоскопической папиллосфинктеротомии. Тогда необходимо их насильственное извлечение с предварительной литотрипсией (рис. 20-7). В ряде случаев плотная структура конкремента делает подобное вмешательство весьма травматичным, что создает опасность развития серьезных осложнений (кровотечения, панкреонекроза, ретродуоденальной перфорации). Именно поэтому при наличии крупных фиксированных конкрементов в маги-
стральных желчных протоках, которые можно выявить при УЗИ, не следует прибегать к ретроградному контрастированию билиарного дерева и попыткам извлечения камней путем эндоскопической папиллосфинктеротомии. В подобной ситуации необходимо предпринять билиодуоденальное стентирование (катетер проводят выше уровня конкремента) или антеградное чрескожное чреспеченочное дренирование. В последующем, по мере разрешения желтухи, следует выполнить традиционное хирургическое вмешательство.
При так называемом высоком блоке желчных протоков (опухоль, стриктура, реже конкремент) наряду с ретроградными эндоскопическими методами декомпрессии можно использовать антеградное чрескожное чреспеченочное дренирование желчных протоков. В случаях, когда стент удается провести ниже места препятствия в двенадцатиперстную кишку, осуществляют двойное наружно-внутреннее дренирование желчных путей (рис. 20-8).
Примерно в половине наблюдений при доброкачественной природе обтурационной желтухи малоинвазивные инструментальные
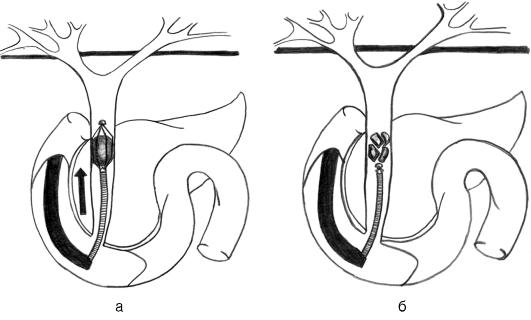
Рис. 20-7. Схема механической литотрипсии при холедохолитиазе с помощью специального инструмента, проведенного в общий желчный проток после эндоскопической папиллосфинктеротомии: а) большой камень захвачен корзинкой литотриптера; б) при затягивании корзинки конкремент разрушается на фрагменты, которые в дальнейшем удаляются или спонтанно мигрируют в двенадцатиперстную кишку
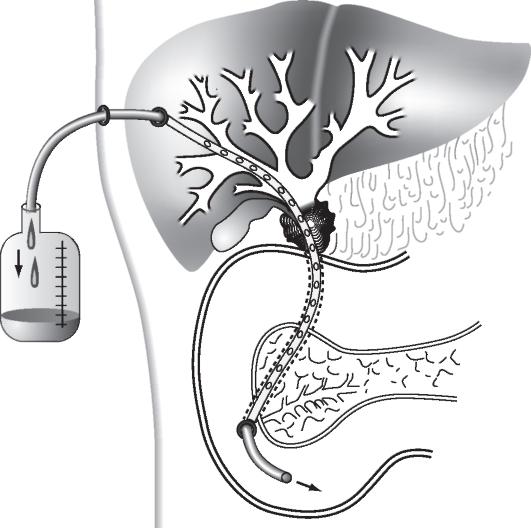
Рис. 20-8. Антеградное наружно-внутреннее дренирование желчных протоков
методы позволяют устранить желтуху и ликвидировать патологию, обусловившую ее появление. Это исключает необходимость традиционного хирургического вмешательства. В остальных случаях после инструментальной декомпрессии желчных протоков по мере разрешения механической желтухи и восстановления функций важнейших органов и систем выполняют прямые операции. Сроки хирургических вмешательств зависят от исходной тяжести печеночной недостаточности и составляют 1-4 нед. Как правило, одним из основных ориентиров, свидетельствующих об очевидной тенденции к разрешению холестаза и возможности выполнения хирургического вмешательства, бывает снижение концентрации общего билирубина менее 50 мкмоль/л. Наряду с этим нормализуются и другие параметры, характеризующие функциональное состояние организма.
Прямые хирургические вмешательства на желчных путях
Выбор метода операции основывают на результатах дооперационной диагностики и данных интраоперационной ревизии желчных протоков с учетом общего состояния больного.
Доступ. Наибольшее распространение при операциях на желчных протоках получили косые разрезы в правом подреберье (Кохера, Федорова). Реже применяют верхнесрединный доступ. При необходимости обширных реконструктивных операций используют двухподреберный доступ. Вмешательства на желчных протоках у больных с ЖКБ обычно выполняют после холецистэктомии (см. главу 15).
Идеальная холедохотомия. После удаления единичного конкремента посредством холедохотомии при отсутствии признаков холангита и хорошей проходимости дистального отдела общего желчного протока отверстие в нем ушивают атравматическим монофиламентным шовным материалом. Это позволяет снизить вероятность формирования послеоперационного лигатурного холедохолитиаза.
Наружное дренирование общего желчного протока - наиболее частый способ завершения холедохотомии. Необходимость во временном на-
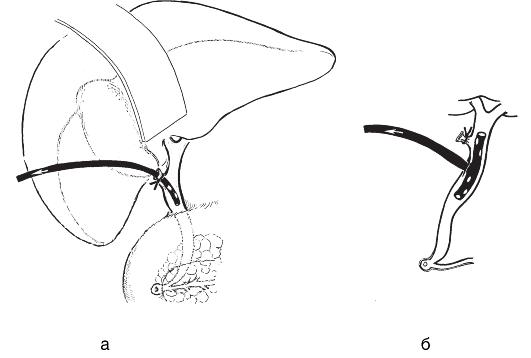
Рис. 20-9. Наружное дренирование общего желчного протока: а - через культю пузырного протока; б - Т-образный дренаж Кера, вводимый через холедохотомию
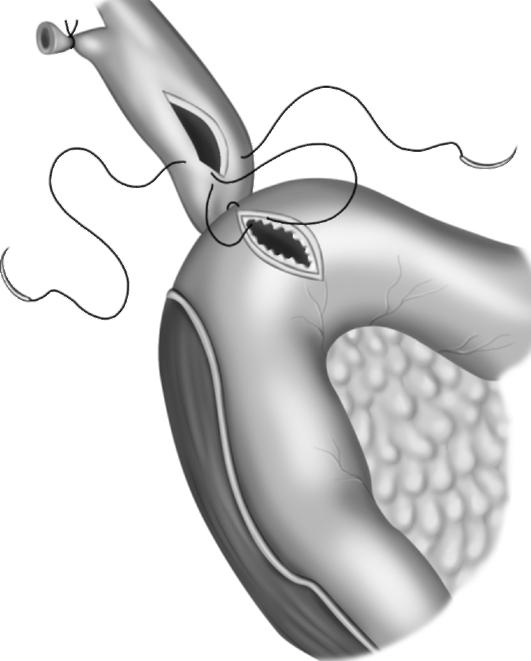
Рис. 20-10. Холедоходуоденостомия (схема операции)
ружном отведении желчи возникает при холангите, панкреатите, папиллите или других обратимых патологических состояниях. Наружное дренирование протоков (рис. 20-9) проводят Т-образным дренажем (по Керу) или через культю пузырного протока (по Холстеду-Пиковскому).
Холедоходуоденостомию (рис. 20-10) илихоледохоэнтеростомию применяют при необратимых препятствиях в дистальном отделе общего желчного протока, которые невозможно устранить с помощью эндоскопической папиллосфинктеротомии (протяженном рубцовом стенозе, индуративном панкреатите, неблагоприятном расположении околососочковых дивертикулов и т.д.).
При высоких рубцовых стриктурах желчных протоков выполняют сложные реконструктивные операции, направленные на восстановление оттока желчи. Среди них наибольшее распространение получили билиодигестивные соустья на различных уровнях желчных протоков с петлей тонкой кишки, выключенной по Ру (рис. 20-11).
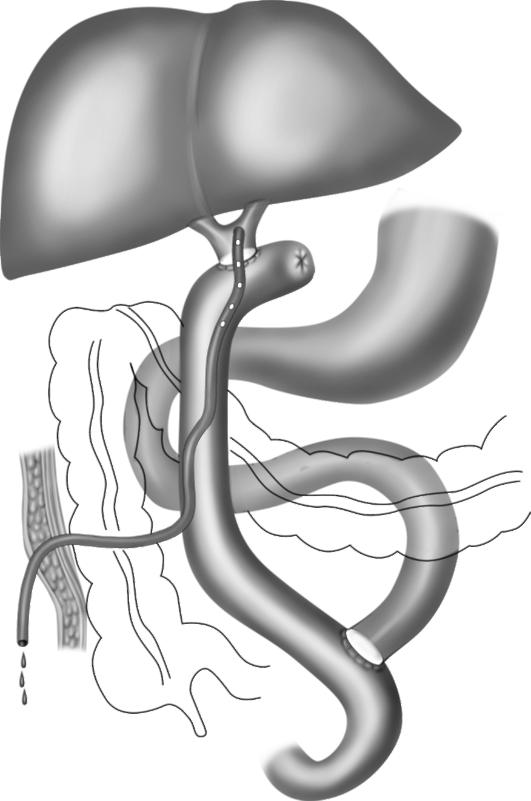
Рис. 20-11. Схема реконструктивной операции на желчных путях. Гепатикоеюностомия с использованием петли тонкой кишки, выключенной по Ру, дополнена наружным дренированием желчных протоков
Операции при желтухе опухолевой природы
Наиболее тяжелую группу составляют больные с обтурацией желчевыводящих путей опухолевого происхождения. После ликвидации желтухи малоинвазивным путем выполняют радикальное или паллиативное хирургическое вмешательство. Возможность выполнения радикальных операций (см. главу 17) у этих пациентов отмечают не более чем в 15-20% случаев.
Паллиативные операции направлены на создание обходных билиодигестивных соустьев. В случае рака головки поджелудочной железы (наиболее частой опухолевой причины механической желтухи) операцией выбора считают холецистоэнтеростомию по Микуличу (рис. 20-12). Условие успешной декомпрессии желчных путей при этой операции - проходимость пузырного протока.
При других локализациях опухоли формируют билиодигестивные соустья либо применяют один из способов эндопротезирования: антеградный чрескожный чреспеченочный или ретроградный эндоскопический. В последние годы методы эндопротезирования желчных протоков расценивают как предпочтительные паллиативные вмешательства при опухолевых поражениях. Это обусловлено их меньшей
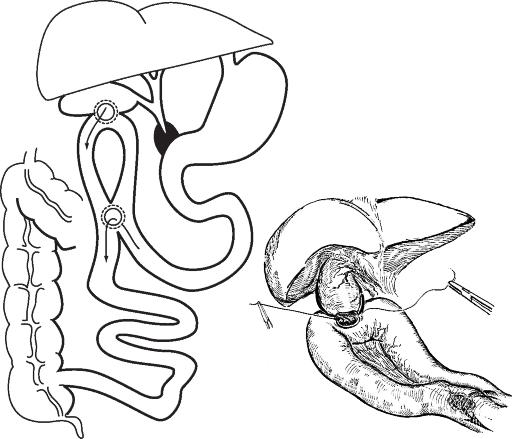
Рис. 20-12. Холецистоэнтеростомия с межкишечным соустьем
травматичностью и сходной продолжительностью жизни по сравнению с результатами обходных билиодигестивных анастомозов. Наибольшее распространение нашли саморасширяющиеся металлические сетчатые стенты с памятью формы или размещаемые в желчные протоки с помощью баллонных дилататоров (рис. 20-13).
ПРОГНОЗ
Летальность при механической желтухе зависит от причины обтурации желчных протоков, длительности заболевания и тяжести состояния больных. Современные технические средства позволяют более чем в 90% наблюдений устранить холестаз малоинвазивным путем и оперировать больных, если это необходимо, в благоприятных условиях - после разрешения желтухи. При соблюдении подобного этапного подхода летальность при доброкачественной природе обтурации желчных путей не превышает 5%.
Наиболее сложную группу составляют больные, у которых с помощью инструментальных методов не удается устранить билиарную гипертензию, и прямое хирургическое вмешательство приходится выполнять на высоте желтухи. В таких ситуациях проводят интенсивную подготовку больных в течение суток в условиях отделения реанимации, направленную главным образом на снижение интоксикации и профилактику печеночно-почечной недостаточности. После кратковременной подготовки выполняют минимальное по объему хирургическое вмешательство, направленное лишь на восстановление оттока желчи. Вынужденные операции на фоне нарастающей механической желтухи, холангита, печеночной недостаточности представляют наибольшую опасность и сопровождаются высокой летальностью.
