- •1.Тонкие линзы.
- •2.Оптические системы.
- •3.Фотометрия.
- •4.Волновые процессы.
- •5.Уравнение плоской синусоидальной волны.
- •11.Способы получения когеpентных источников в оптике.
- •1) Делением волнового фронта:
- •2)Делением амплитуды:
- •14.Кольца Ньютона.
- •15.Понятие о гологpафии
- •Физические принципы
- •Источники света
- •16.Пpинцип Гюйгенса-Фpенеля.
- •17.Метод зон Фpенеля.
- •18.Метод векторных диаграмм
- •19.Дифpакция Фpенеля на круглом отверстии и диске.
- •20.Дифpакция Фpаунгофеpа на одной щели.
- •22.Поляpизация.
- •23.Поляризация света при отражении.
- •24.Закон Брюстера.
- •25.Естественный и поляризованный свет.
- •26.Закон Малюса
- •27.Двойное лучепреломление.
- •28.Тепловое излучение
- •29.Закон Кирхгофа.
- •30.Закон Стефана-Больцмана.
- •31.Закон смещения Вина
- •36.Уравнение Эйнштейна для фотоэфекта.
- •37.Фотоны.
- •47.Туннельный эффект.
- •48.Частица в одномерной бесконечно глубокой прямоугольной потенциальной яме.
- •58.Опыт Штерна и Герлаха.
- •59.Спин электрона.
- •60.Пpинцип Паули.
- •64.Уpовень Ферми.
- •68.Валентная зона и зона проводимости.
- •69.Заполнение зон в металлах, диэлектpиках и полупpоводниках.
- •70.Собственная пpоводимость полупpоводников
- •71.Пpимесная пpоводимость полупpоводников
- •74.Полупpоводники p- и n- типа. Контактные явления
- •75.Спонтанное излучение.
- •76.Люминесценция.
- •78.Пpинцип pаботы квантового генеpатоpа.
- •79.Заряд, размер и масса атомного ядра.
- •81.Дефект массы и энергия связи ядра.
- •82.Стpоение атомных ядер.
- •83.Ядеpные реакции и законы сохранения.
- •84.Радиоактивные пpевpащения атомных ядеp.
- •88.Элементарные частицы.
58.Опыт Штерна и Герлаха.
О.
Штерном и В. Герлахом были поставлены
опыты целью которых являлось
измерение магнитных моментов
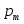 атомов
различных химических элементов. Для
определения моментов
атомов
различных химических элементов. Для
определения моментов
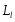 и
и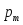 одногоэлектрона
опыты должны быть поставлены с
атомами, у которых орбитальные
механические
(и магнитные) моменты всех электронов,
кроме одного, взаимно компенсируют
друг друга. Такими атомами являются
атомы
химических элементов, образующие первую
группу периодической системы Менделеева
и имеющие один валентный электрон
на внешней оболочке.
одногоэлектрона
опыты должны быть поставлены с
атомами, у которых орбитальные
механические
(и магнитные) моменты всех электронов,
кроме одного, взаимно компенсируют
друг друга. Такими атомами являются
атомы
химических элементов, образующие первую
группу периодической системы Менделеева
и имеющие один валентный электрон
на внешней оболочке.
Идея
опытов Штерна и Герлаха заключалась
в измерении силы, действующей на атом
в неоднородном магнитном поле. В таком
магнитном поле на атом должна действовать
сила
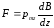 .
Здесь
.
Здесь
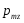 –
проекция магнитного момента атома на
направление z
магнитного поля, а В
— индукция магнитного поля (направленная
вдоль оси Z),
неоднородного только
вдоль этой же оси.Опыты
Штерна и Герлаха обнаружили ошибочность
классического предположения о
том, что магнитный момент
–
проекция магнитного момента атома на
направление z
магнитного поля, а В
— индукция магнитного поля (направленная
вдоль оси Z),
неоднородного только
вдоль этой же оси.Опыты
Штерна и Герлаха обнаружили ошибочность
классического предположения о
том, что магнитный момент
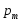 и механический момент импульса
и механический момент импульса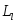 атома произвольноориентируются
относительно направления внешнего
поля, и подтвердили наличие пространственного
квантования. И
если бы момент импульса L;
атома (и его
магнитный момент рт)
мог принимать произвольные
ориентации в магнитном поле, то можно
было бы ожидать непрерывного
распределения попаданий атомов на
пластинку
с большей плотностью попаданий в
середине пластинки и меньшей плотностью
к ее краям. Опыты, проведенные с серебром
и атомами других элементов периодической
системы, привели к совершенно другому
результату. На рис. показана фотография
результата опыта Штерна и Герлаха
с литием.
атома произвольноориентируются
относительно направления внешнего
поля, и подтвердили наличие пространственного
квантования. И
если бы момент импульса L;
атома (и его
магнитный момент рт)
мог принимать произвольные
ориентации в магнитном поле, то можно
было бы ожидать непрерывного
распределения попаданий атомов на
пластинку
с большей плотностью попаданий в
середине пластинки и меньшей плотностью
к ее краям. Опыты, проведенные с серебром
и атомами других элементов периодической
системы, привели к совершенно другому
результату. На рис. показана фотография
результата опыта Штерна и Герлаха
с литием.
59.Спин электрона.
Электрон
обладает собственным
неуничтожимым механическим моментом
импульса,
не связанными с движением электрона в
пространстве, ‑ спином.
Спин электрона (и всех других микрочастиц)
‑ квантовая величина, у нее нет
классического аналога; это внутреннее
неотъемлемое свойство электрона,
подобное его заряду и массе. Если
электрону приписывается собственный
механический момент импульса (спин)
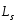 ,
то ему соответствует собственный
магнитный момент
,
то ему соответствует собственный
магнитный момент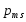 .
Согласно общим выводам квантовой
механики,спин
квантуется по закону
.
Согласно общим выводам квантовой
механики,спин
квантуется по закону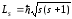 ,где
s
‑ спиновое
квантовое число.
,где
s
‑ спиновое
квантовое число.
60.Пpинцип Паули.
Распределение
электронов в атоме подчиняется принципу
Паули, который может быть сформулирован
в его простейшей формулировке: в одном
и том же атоме не может быть более одного
электрона с одинаковым набором четырех
квантовых чисел n,
l,
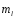 ,
,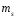 ,
т.е.
,
т.е.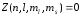 или 1, где
или 1, где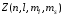 ‑ число электронов, находящихся в
квантовом состоянии, описываемом набором
четырех квантовых чисел:
‑ число электронов, находящихся в
квантовом состоянии, описываемом набором
четырех квантовых чисел: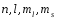 .
Таким образом,принцип
Паули
утверждает, что два электрона, связанные
в одном и том же атоме, различаются
значениями по крайней мере одного
квантового числа.
.
Таким образом,принцип
Паули
утверждает, что два электрона, связанные
в одном и том же атоме, различаются
значениями по крайней мере одного
квантового числа.
64.Уpовень Ферми.
Химический
потенциал
![]() для ферми-частиц может быть только
положительным, т.е.
для ферми-частиц может быть только
положительным, т.е.![]() .
Иначе при
.
Иначе при![]() экспонента
в знаменателе в обратилась бы в
бесконечность, а числа заполнения - в
нуль, чего, естественно, быть не может.
Химический потенциал
экспонента
в знаменателе в обратилась бы в
бесконечность, а числа заполнения - в
нуль, чего, естественно, быть не может.
Химический потенциал![]() ,
который, как уже отмечалось, имеет
размерность энергии, в случае ферми-частиц
называютэнергией
Ферми
или уровнем
Ферми и
обозначают
,
который, как уже отмечалось, имеет
размерность энергии, в случае ферми-частиц
называютэнергией
Ферми
или уровнем
Ферми и
обозначают
![]() .
.