
- •ВВЕДЕНИЕ
- •НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •Вводная часть
- •Традиционные названия сложных соединений
- •Классификация неорганических веществ
- •Вопросы к семинару
- •Общие правила работы с химическими реактивами
- •Ядовитые и вредные вещества
- •Химические ожоги
- •Меры по предупреждению пожаров, возгораний и взрывов
- •Поражение электрическим током
- •Искусственное дыхание
- •Наружный массаж сердца
- •Меры первой помощи при кровотечениях от порезов
- •Меры предосторожности при мытье посуды
- •Вопросы к семинару
- •ПРАВИЛА ОФОРМЛЕНИЯ ОТЧЕТА ПО ЛАБОРАТОРНЫМ РАБОТАМ
- •2. Взвешивание
- •3. Определение концентрации раствора. Фильтрование
- •Вопросы к семинару
- •ЭКВИВАЛЕНТ
- •Вопросы к семинару
- •СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА РАСТВОРА
- •ЛАБОРАТОРНАЯ РАБОТА «Приготовление растворов»
- •Вопросы к семинару
- •ТЕРМОХИМИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Определение тепловых эффектов»
- •Вопросы к семинару
- •ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •ЛАБОРАТОРНАЯ РАБОТА «Равновесие»
- •Вопросы к семинару
- •СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ
- •ЛАБОРАТОРНАЯ РАБОТА «Скорость химических реакций»
- •Вопросы к семинару
- •Вопросы к коллоквиуму I
- •Задачи к коллоквиуму I
- •РАСТВОРИМОСТЬ ЭЛЕКТРОЛИТОВ
- •ЛАБОРАТОРНАЯ РАБОТА «Растворимость и ПР»
- •Вопросы к семинару
- •ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Электролитическая диссоциация»
- •Вопросы к семинару
- •Методика решения задач
- •ГИДРОЛИЗ СОЛЕЙ
- •ЛАБОРАТОРНАЯ РАБОТА «Гидролиз солей»
- •Вопросы к семинару
- •КОЛЛОИДНЫЕ РАСТВОРЫ
- •ЛАБОРАТОРНАЯ РАБОТА «Коллоидные растворы»
- •Вопросы к семинару
- •РЕДОКС-ПРОЦЕССЫ
- •ЛАБОРАТОРНАЯ РАБОТА «ОВР»
- •Вопросы к семинару
- •ЭЛЕКТРОХИМИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Электрохимия»
- •Вопросы к семинару
- •КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Получение и свойства КС»
- •Вопросы к семинару
- •Вопросы к коллоквиуму II
- •ЛАБОРАТОРНАЯ РАБОТА «Очистка веществ»
- •Вопросы к семинару
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- •ОГЛАВЛЕНИЕ

Подчеркнем, что кинетические уравнения, как и выражения K a , записы-
ваются, только исходя из сокращенного ионного вида уравнения. Если бы данный процесс был одностадийным, то кинетическое уравнение для прямой реакции, выраженное через концентрации, имело бы вид:
k C(S O2 |
) C2 (H ) |
. |
|
|
|
2 |
3 |
|
|
|
|
|
|
|
|
||
В действительности это взаимодействие включает как минимум четыре |
|||||
стадии: |
|
|
|
|
|
1) S2 O32 |
H HS 2 O3 , |
2) HS 2 O3 |
H H2S2 O3 , |
||
3) H2S2 O3 |
|
H2SO3 S , |
4) H2SO3 |
SO2 H2 O , |
|
а значит, приведенное выше кинетическое уравнение является фор- мально-кинетическим1. Истинный порядок данной реакции по каждому из реагирующих веществ предлагается оценить экспериментально (опыт 1).
Подчеркнем, что скорость 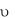 любого обратимого процесса равна разности значений
любого обратимого процесса равна разности значений 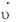 и
и 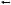 . Но разложение тиосульфата можно условно считать необратимым, т.к. есть продукты, которые выводятся из сферы реакции (S и SO2), поэтому значением
. Но разложение тиосульфата можно условно считать необратимым, т.к. есть продукты, которые выводятся из сферы реакции (S и SO2), поэтому значением 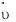 можно пренебречь и считать скорость равной
можно пренебречь и считать скорость равной 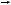 .
.
Кроме того, время окончания наблюдения в опытах 1 и 2 фиксируется по едва заметному появлению мути (начало образования продукта – серы), т.е. на начальной стадии процесса, когда скорость обратной реакции тем более можно не учитывать.
ЛАБОРАТОРНАЯ РАБОТА «Скорость химических реакций»
1. Определение константы скорости и порядка реакции. Налить в че-
тыре пробирки 5%-ный тиосульфат натрия и воду в следующих пропорциях:
Номер пробирки |
V р-ра (Na2S2O3), |
V воды, мл |
|
мл |
|
1 |
1 |
3 |
2 |
2 |
2 |
3 |
3 |
1 |
4 |
4 |
– |
В приготовленные растворы тиосульфата натрия добавить по 1 мл 2,5%-ной серной кислоты и заметить по секундомеру, через какой промежуток времени после сливания появится едва заметная муть. Чем вызвано помутнение? Написать уравнение реакции. Результаты занести в таблицу:
1 Формально-кинетическое уравнение пишется с учетом стехиометрии суммарного уравнения процесса, как если бы он был одностадийным, но это очень грубое приближение.
44

Номер опыта |
ω(Na2S2O3), % |
Время, с |
1 |
|
|
2 |
|
|
3 |
|
|
4 |
|
|
Аналогично описанному выяснить, как зависит скорость реакции от концентрации кислоты (опыты 5 – 8), изменяя ее объем от 1 до 4 мл, а объем воды – от 3 мл до 0 соответственно (лить кислоту в воду!). Объем 5%-го тиосульфата, добавляемый к приготовленным растворам кислот, брать равным 1 мл.
На основании полученных результатов определить порядки реакции по ионам: S2 O23 и H
и H , и оценить значение константы скорости в кинетическом
, и оценить значение константы скорости в кинетическом
уравнении исследуемого процесса: |
k |
Сn (S2 O32 ) |
Cm (H ) , |
|||||||||
считая, что |
1 / |
, где – время от начала реакции до момента по- |
||||||||||
явления мути (в секундах), а |
k k . (Поскольку k – это скорость реакции в |
|||||||||||
стандартных условиях (в частности, при активностях реагентов равных |
||||||||||||
1 моль/л, то по аналогии с равенством: |
|
имеем: k |
k |
k ), но если при- |
||||||||
нять k |
0 (случай кинетически необратимых реакций), то k |
k .) |
||||||||||
Найти n, m и k предлагается следующим способом. Поскольку в первой |
||||||||||||
части эксперимента (опыты 1 – 4) Cm (H ) |
const , то можно записать: |
|||||||||||
|
|
k' |
Cn (S2 O32 ) , где k' |
k Cm (H ) , |
|
|
|
|
|
|
||
или: |
lg |
lg k' n lg C(S2 O32 ) , т.е. получаем уравнение типа: y b ax . |
||||||||||
Рассчитать значения величин, необходимых для определения n, m и k, и |
||||||||||||
представить в виде таблицы: |
|
|
|
|
|
|
||||||
Номер |
|
|
, с-1 |
|
lg |
C(S2 O32 ) |
lg C(S2 O32 ) |
|
C(H ) |
|
lg C(H ) |
|
опыта |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
… |
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
Построив по данным эксперимента (опыты 1-4) график зависимости lg |
||||||||||||
от lg C(S2 O32 |
) , найти величину n (как tg угла наклона полученной прямой к оси |
|||||||||||
lg C(S2 O32 |
) ) |
и lgk' (отрезок, отсекаемый прямой на оси lg ). Обработав анало- |
||||||||||
гично результаты опытов 5 – 8 (при Cn (S2 O32 ) |
const ), определить значения m |
|||||||||||
и k. |
|
|
|
|
|
|
|
|
|
|
|
|
По рассчитанным двум значениям k найти среднее арифметическое ( k ) и написать кинетическое уравнение процесса разложения тиосульфат-ионов,
45
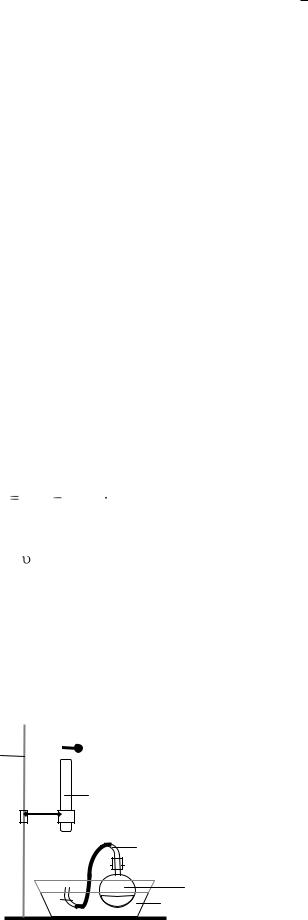
подставив найденные значения n, m и k . Каков общий порядок данной реакции?
2. Определение температурного коэффициента реакции и оценка ее энергии активации. Налить в три сухие пробирки по 1 мл 2,5%-ной серной кислоты, а в три другие – по 1 мл 5%-го тиосульфата натрия. Первый опыт провести при комнатной температуре. Быстро прилить серную кислоту к тиосульфату натрия и отметить время (по секундомеру) до едва заметного помутнения раствора.
Затем провести аналогичный опыт, но при Т на 100С выше комнатной, для чего следующую пару пробирок перед смешиванием растворов нагревать в течение 15 минут на водяной бане, температуру которой контролировать термометром.
Далее, нагревая растворы таким же способом, провести опыт при Т, на 200С превышающей комнатную. Полученные данные записать в таблицу:
Номер опыта |
Температура, 0С |
Время, с |
1 |
|
|
2 |
|
|
3 |
|
|
На основании экспериментальных данных рассчитать значение температурного коэффициента. Выполняется ли правило Вант-Гоффа в данном эксперименте?
|
Используя |
|
формулу Аррениуса в логарифмическом виде: |
||
lg k |
lg A |
Ea |
|
1 |
, |
2,3R |
T |
||||
|
оценить значение E a , построив график зависимости lgk (принять k рав- |
||||
ным |
) от величины 1 / T , где Т – температура раствора по Кельвину. |
||||
|
3. Влияние концентрации гомогенного катализатора на скорость ре- |
||||
акции (на примере разложения H2O2 в присутствии дихромата калия)
Собрать установку (рис. 6). Заполнить бюретку (1) водой до верхнего деления, затем, закрыв большим пальцем отверстие бюретки, перевернуть ее и погрузить в ванну (2) с водой той же температуры (следить, чтобы во время опыта Т в ванне была постоянной). Закрепить бюретку в штативе и отметить
|
|
|
|
|
|
|
|
|
уровень жидкости в ней. |
|
|
|
|
|
|
|
|
|
Отмерить цилиндром 30 мл 0,1%-го ди- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
хромата калия и вылить в колбу (3). В другую |
|
|
|
|
|
|
|
|
|
колбу налить 20-25 мл 10%-го H2O2, поставить |
|
1 |
|
|
|
|
ее в ванну (2) и выдержать 15 мин. Отобрать пи- |
|||
|
|
|
|
|
|
|
|
|
петкой 5 мл H2O2, вылить в колбу с дихроматом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
калия и сразу же закрыть пробкой с газоотвод- |
||
|
|
|
|
|
|
ной трубкой (4), введенной в бюретку Непре- |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
рывно и равномерно встряхивая колбу (не выни- |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
2 |
мая ее из ванны), через каждые 30 с измерять |
|||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Рис.6. Установка для изучения
разложения пероксида водорода
46

объем выделившегося кислорода. При этом один студент, равномерно встряхивая колбу, снимает показания уровня воды в бюретке по сигналу «Внимание, отсчет!» второго студента, который следит за временем и записывает показания.
Отметить окраску раствора в начале процесса и когда он закончится. (Опыт длится 8-10 мин.)1 Результаты занести в таблицу:
w(K2 |
|
|
|
|
Cr2O7), |
|
0,1 |
0,05 |
0 |
|
|
|
|
|
Время |
|
Объем выделившегося кислорода, мл |
||
от начала |
|
|
|
|
опыта, с |
|
|
|
|
30 |
|
|
|
|
60 |
|
|
|
|
90 |
|
|
|
|
… |
|
|
|
|
… |
|
|
|
|
… |
|
|
|
|
Провести аналогичный опыт, используя 0,05%-ный раствор дихромата калия, а затем без раствора дихромата калия, заменив его тем же объемом воды.
Сравнить результаты проведенных экспериментов, построив на одном графике кинетические зависимости для каждого опыта (откладывая на оси абсцисс время, а на оси ординат – объем кислорода, выделившегося за каждые 30 с). Как зависит скорость реакции от концентрации катализатора? Написать уравнения суммарной реакции и ее стадий, включая образование интермедиата.
(Если провести разложение пероксида водорода в присутствии катализатора диоксид марганца, то будет ли от его количества зависеть скорость реакции?)
4. Автокатализ. К 5 каплям 5%-ой щавелевой кислоты добавить 3 капли 1М H2SO4, затем 2 капли перманганата калия, отметить время, за которое произойдет обесцвечивание раствора и снова добавить 2 капли перманганата. Изменилось ли время обесцвечивания после 2-го добавления? А после 3-го? Какой продукт реакции является катализатором данного процесса?
5. Действие ингибитора. В 2 пробирки налить до 1/4 объема 1М H2SO4 и по капле раствора K 3 [Fe(CN)6 ]2 (зачем?). В одну добавить микрошпатель уро-
тропина. Две одинаковые железные проволоки очистить наждачной бумагой и опустить в пробирки. По времени появления достаточно интенсивной синей
1Можно ли на основании наблюдаемых внешних эффектов сделать предположение о механизме действия катализатора? (Учесть, что ассоциат [Cr2O7 H2О2]2- имеет черный цвет).
2Гексациано(III)-феррат калия (K3[Fe(CN)6]) является реактивом на ионы железа(II) , т.к. образует с ними синий продукт состава: KFe[Fe(CN)6].
47
