
- •ВВЕДЕНИЕ
- •НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •Вводная часть
- •Традиционные названия сложных соединений
- •Классификация неорганических веществ
- •Вопросы к семинару
- •Общие правила работы с химическими реактивами
- •Ядовитые и вредные вещества
- •Химические ожоги
- •Меры по предупреждению пожаров, возгораний и взрывов
- •Поражение электрическим током
- •Искусственное дыхание
- •Наружный массаж сердца
- •Меры первой помощи при кровотечениях от порезов
- •Меры предосторожности при мытье посуды
- •Вопросы к семинару
- •ПРАВИЛА ОФОРМЛЕНИЯ ОТЧЕТА ПО ЛАБОРАТОРНЫМ РАБОТАМ
- •2. Взвешивание
- •3. Определение концентрации раствора. Фильтрование
- •Вопросы к семинару
- •ЭКВИВАЛЕНТ
- •Вопросы к семинару
- •СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА РАСТВОРА
- •ЛАБОРАТОРНАЯ РАБОТА «Приготовление растворов»
- •Вопросы к семинару
- •ТЕРМОХИМИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Определение тепловых эффектов»
- •Вопросы к семинару
- •ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •ЛАБОРАТОРНАЯ РАБОТА «Равновесие»
- •Вопросы к семинару
- •СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ
- •ЛАБОРАТОРНАЯ РАБОТА «Скорость химических реакций»
- •Вопросы к семинару
- •Вопросы к коллоквиуму I
- •Задачи к коллоквиуму I
- •РАСТВОРИМОСТЬ ЭЛЕКТРОЛИТОВ
- •ЛАБОРАТОРНАЯ РАБОТА «Растворимость и ПР»
- •Вопросы к семинару
- •ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Электролитическая диссоциация»
- •Вопросы к семинару
- •Методика решения задач
- •ГИДРОЛИЗ СОЛЕЙ
- •ЛАБОРАТОРНАЯ РАБОТА «Гидролиз солей»
- •Вопросы к семинару
- •КОЛЛОИДНЫЕ РАСТВОРЫ
- •ЛАБОРАТОРНАЯ РАБОТА «Коллоидные растворы»
- •Вопросы к семинару
- •РЕДОКС-ПРОЦЕССЫ
- •ЛАБОРАТОРНАЯ РАБОТА «ОВР»
- •Вопросы к семинару
- •ЭЛЕКТРОХИМИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Электрохимия»
- •Вопросы к семинару
- •КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА «Получение и свойства КС»
- •Вопросы к семинару
- •Вопросы к коллоквиуму II
- •ЛАБОРАТОРНАЯ РАБОТА «Очистка веществ»
- •Вопросы к семинару
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- •ОГЛАВЛЕНИЕ

му р, складывается из парциальных давлений водорода и водяного пара. Таким образом, объем водорода при н.у. определяется по формуле1:
|
V |
V(p |
h) |
273 . |
|
|
0 |
(273 |
t) |
760 |
|
|
|
|
|||
|
Затем рассчитать мольную массу эквивалентов металла, соответствую- |
||||
щую 1,008 г водорода (по объему – 11 200 мл H2 ), используя равенство: |
|||||
Mf |
11 200 m / V0 . |
|
|
||
|
Опыт провести два раза, величину Mf найти как среднее из двух опреде- |
||||
лений. Сравнить полученное ее значение с рассчитанным по формуле: |
|||||
Mf |
f M и оценить абсолютную и относительную ошибку эксперимента. Чем |
||||
она обусловлена? |
|
|
|||
Вопросы к семинару
1.Определение моля и эквивалента. Как рассчитать фактор эквивалент-
ности?
2.Закон Авогадро. Мольная масса и мольный объем вещества и его эквивалентов. Для каких соединений они имеют переменные значения? Закон эквивалентов.
3.Как найти практически M и Mf . Формула Клапейрона-Менделеева.
4.При каких условиях реальные газы можно рассматривать как идеаль-
ные?
5.Сколько атомов в моле вещества? а молекул в 100 мл воды при 40С?
6.Решить каждому студенту одну из следующих задач по [6] (№10 и №11), (с №1 по №9), (с №12 по №16).
СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА РАСТВОРА
Состав раствора выражают разными способами: в массовых, объемных или молярных долях, или указывая его молярную концентрацию и др. [8].
Массовая доля соединения ( wi ) показывает, какую часть (т.е. долю) от массы всей системы, состоящей из k компонентов, составляет масса данного вещества.
Объемная доля соединения ( i ) используется для газообразных систем и равна отношению объема данного газа к объему всей системы, состоящей из k газов.
Молярная доля вещества ( i ) равна отношению количества данного соединения к числу молей всей системы, содержащей k компонентов.
Доли рассчитывают по соответствующим формулам:
1 Данная формула не учитывает, что давление пара над раствором меньше, чем над чистой водой. Это тоже может быть причиной неточного определения эквивалента металла].
32

|
wi |
mi |
, |
|
Vi |
|
, |
|
|
ni |
. |
|
k |
i k |
|
i |
k |
||||||
|
|
mi |
|
|
Vi |
|
|
ni |
|
||
|
|
i 1 |
|
|
i 1 |
|
|
|
i |
1 |
|
|
Молярная концентрация показывает количество растворенного веще- |
||||||||||
ства, которое находится в 1л раствора. Ее обозначение – C. Например, запись |
|||||||||||
C(HCl) |
0,1 моль/л означает, что в 1 л раствора – одна десятая моля хлороводо- |
||||||||||
рода; |
а C(1/5 KMnO 4 ) |
1 моль |
указывает на то, что 1 л раствора содержит |
||||||||
1 моль эквивалентов перманганата калия, то есть 1/5 1 или 0,2 моль его. |
|||||||||||
|
Возможна и другая запись молярной концентрации, например: 0,1М |
||||||||||
НСl – децимолярный раствор; |
или 2M (1/5 KMnO 4 ) , т.е. 2н KMnO 4 – это двунор- |
||||||||||
мальный раствор. (Если молярная концентрация выражена через моли эквивалентов, то обозначается Сf и при ее названии используется термин «нормальная».)
Молярная концентрация раствора, который приготовлен из навески растворенного вещества m (г) в мерной колбе объема V (мл), рассчитывается по
формуле: |
C |
m 1000 (моль / л) . (Для расчета Сf вместо М подставляют Mf ). |
|||
|
|
M V |
|
|
|
Рассмотрим на конкретных примерах, как осуществляется переход от |
|||||
одного способа выражения концентрации раствора к другому. |
|
|
|||
Пример 1. Определить массовую долю азотной кислоты в 12M ее рас- |
|||||
творе, плотность которого ( ) равна 1,33 г/мл. |
|
|
|
||
Массовая доля кислоты определяется формулой: |
HNO 3 |
m HNO 3 |
. |
||
|
|||||
|
|
|
|
mр ра |
|
Масса 1 л 12M раствора кислоты равна: а масса растворенного вещества:
mр ра 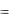 V 1,33
V 1,33  1000 1330 г;
1000 1330 г;
m(HNO 3 ) M n |
63 г / моль |
12 моль |
756 г . |
|
Следовательно, |
(HNO 3 ) |
756 /1330 |
0,567 56,7%, |
а |
(H2O) 43,3% .
Пример 2. Рассчитать молярную и нормальную концентрации фосфорной кислоты с массовой долей кислоты в растворе 3% ( 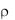 1 г/мл).
1 г/мл).
|
Искомые концентрации определяются формулами: C |
|
n |
и Cf |
nf . |
|||||||||||
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
V |
|
Если взять 100 г раствора, указанного в задаче, то получим: |
|
||||||||||||||
|
V |
mр ра |
|
100 г |
100 мл , n |
m |
|
|
3 г |
0.0306 моль . |
И тогда: |
|||||
|
|
|
1 г/мл |
M 98 г/моль |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
С H |
PO |
4 |
0.0306 |
1000 мл |
0.306 моль , |
а C |
f |
С 1/3H PO |
3C |
0.918 моль . |
||||||
3 |
|
|
|
100 мл |
|
л |
|
|
|
3 4 |
|
|
|
л |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
33
