
молек. биофизика укр.презент
.pdf
Міністерство освіти і науки України
Київський національний університет імені Тараса Шевченка
МОЛЕКУЛЯРНА БІОФІЗИКАІЗИКА
к.б.н., доцент кафедри біофізики Мартинюк Віктор Семенович

Біомолекули – молекулярні конструкції
Молекула білка - молекулярна конструкція
Первинна
Вторинна |
|
Третинна |
|
Четвертинна |
|
|
|
|
|

Біомолекули – молекулярні конструкції
Близькі за структурою, функціями та походженням оксидоредуктази
Різні за структурою та походженням серинові протеази

Біомолекули – молекулярні конструкції
Молекула ДНК - молекулярна конструкція

Стабілізація просторової структури
Зв'язки, які забезпечують стабілізацію просторової структури біомакромолекул:
1.ковалентні зв'язки;
2.електростатичні взаємодії;
3.водневі зв'язки;
4.Ван-дер-Ваальсові взаємодії;
5.гідрофобні зв'язки.
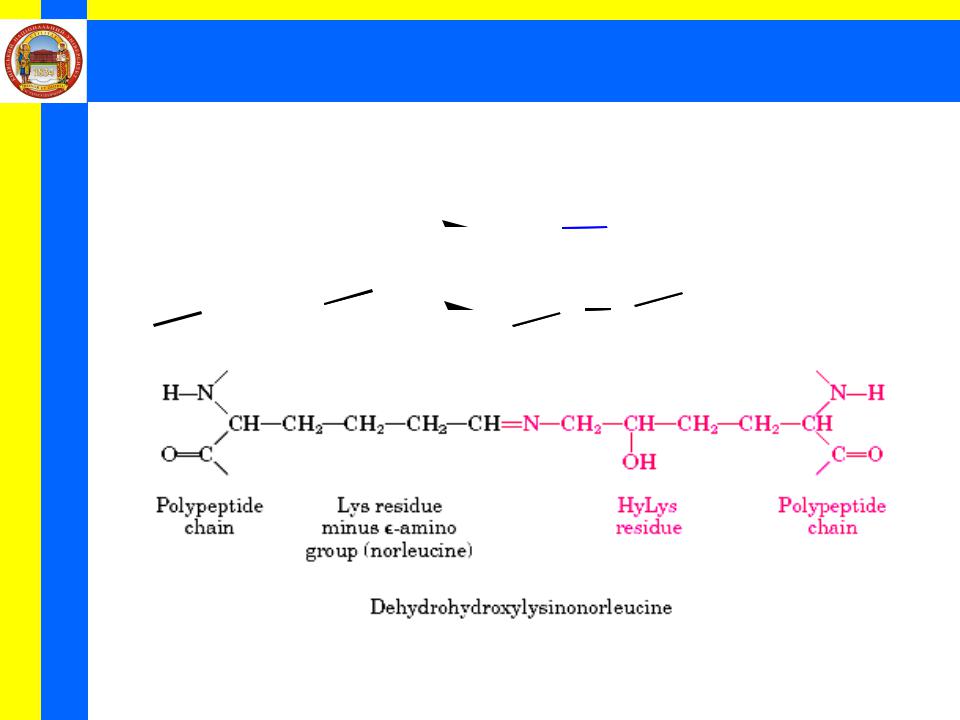
Стабілізація просторової структури
Ковалентні зв'язки
O O
|
|
NH2 + OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Амідний |
R |
|
|
C |
|
R |
|
|
R |
|
N |
C |
|
R |
||||||||
|
|
|
|
|
|
|
зв’язок |
||||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
R |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
SH + |
|
|
|
|
|
|
|
|
H |
|
|
|
|
Дисульфідний |
|||||
|
|
HS |
|
|
|
|
|
|
S |
|
S |
зв’язок |
|||||||||
|
R |
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|||||
Енергія ковалентних зв'язків 170-800 кДж/моль
-С-С- 348 кДж/моль |
-С-N- 336 кДж/моль |

Стабілізація просторової структури
Дисульфидні зв'язки у колагені

Стабілізація просторової структури
Дисульфидні зв'язки в ферментах

Стабілізація просторової структури
Електростатичні взаємодії
Електростатичні взаємодії виникають між молекулами або їх фрагментами, які мають електричний заряд.
Електричний заряд утворюється внаслідок особливостей хімічної
будови молекули:
CH3
R N+
CH3
CH3
або дисоціації хімічних груп у водних розчинах:
R |
|
NH2 + H+ |
|
|
|
R |
|
NH3+ |
|
|
|
||||||
|
|
|
|
|
||||
|
|
|
|
R |
|
COOH |
|
|
|
R |
|
COO- + H+ |
|
|
|
|
|
||||
|
|
|
|

Стабілізація просторової структури
Електричні взаємодії є далекодіючими, тому що сила та енергія взаємодії пропорційна 1/r, тоді як Ван-дер-Ваальсові залежать від відстані пропорційно 1/r6 .
Енергія електричних взаємодій записується як:
|
Wel = |
1 q1q2 |
|||
де |
4πε0 |
|
εr |
|
|
|
|
|
|
|
|
r – |
відстань, |
|
|
|
|
ε – |
діелектрична проникненість середовища, |
||||
q – |
заряд. |
|
|
|
|
Енергія електричних взаємодій складає 40 - 200 кДж/моль.
У водному середовищі, де значення ε ~ 81, енергія електростатичних зв'язків слабше, у порівнянні з гідрофобним оточенням, в якому ε ~ 2-5. Однак вірогідність знаходження зарядженої групи в гідрофобному оточенні дуже мала.
