
Pat_fiziologiya_Ataman
.pdfкровотворних клітин);
г) пов 'язані зі зменшенням плацдарму еритропоезу. Є наслідком заміщення кровотворної тканини лейкозними клітинами, сполучною тканиною (фіброз), метастазами пухлин.
III. Залежно від сутності процесів, що лежать в основі розвитку анемій, виділяють:
а) порушення утворення еритроцитів: дефіцит кровотворних клітин унаслідок їх ушкодження або заміщення, порушення розмноження клітин кровотворення (порушення ресинтезу ДНК), дефекти дозрівання еритроцитів і виходу їх у кровоносні судини (неефективний еритропоезу,
б) порушення синтезу гемоглобіну: дефіцит заліза, порушення синтезу порфіринів (спадкові порушення ферментів, отруєння свинцем, дефіцит вітаміну В6, розлади синтезу білкових ланцюгів молекул гемоглобіну).
26.1.43. Що таке гіпопластична анемія? Які її етіологія й патогенез?
Гіпопластична (апластична) анемія - це захворювання системи крові, що характеризується пригніченням кровотворної функції червоного кісткового мозку і виявляється недостатнім утворенням еритроцитів, гранулоцитів і тромбоцитів (панцитопенією) або одних тільки еритроцитів (парціальна гіпопластична анемія, еритробластофтиз).
Розрізняють набуті і спадково обумовлені форми гіпопластичної анемії. Набуті форми можуть мати такі причини:
1)фізичні фактори (іонізуюча радіація);
2)хімічні агенти (бензол, свинець, пари ртуті, лікарські препарати: цитостатичні засоби, левоміцетин, сульфаніламіди);
3)біологічні фактори (вірус гепатиту).
Крім того, до набутих відносять так звану ідіопатичну форму, причину якої встановити не вдається. На цю форму припадає 50-75 % всіх випадків гіпопластичної анемії.
Усі наведені етіологічні фактори поділяють на дві групи.
I. Фактори з облігатним (обов 'язковим) мієлотоксичним ефектом. До них відносять іонізуючу радіацію, бензол та його похідні, протипухлинні препарати (цитостатики), неорганічні сполуки миш'яку та ін.
II. Фактори з факультативним мієлотоксичним ефектом, що може виявлятися лише в окремих поодиноких випадках (наприклад, апластична постмедикаментозна анемія). У розвитку анемії після прийому лікарських препаратів велике, якщо не вирішальне, значення мають індивідуальні особливості організму. Встановлено, що не існує прямого зв'язку між розвитком гіпопластичної анемії, з одного боку, і дозою, а також тривалістю застосування лікарських препаратів, з другого. Розвиток гіпопластичної анемії може бути пов'язаний з прийманням деяких антибіотиків (левоміцетин), протисудомних, антитиреоїдних, антигістамінних засобів, транквілізаторів.
Прикладом спадково обумовленої форми гіпопластичної анемії є анемія Фан-коні
— захворювання з аутосомно-рецесивним типом спадкування. Сутність дефекту полягає в порушеннях систем репарації ДНК. Унаслідок цього легко виникають невідновлювані ушкодження ДНК під впливом ультрафіолетового випромінювання й хімічних агентів. Порушується кровотворення, часто розвиваються гострі лейкози.

У патогенезі гіпопластичної анемії провідне місце посідають два механізми.
1.Ушкодження стовбурових клітин. Доказом цього є панцитопенія, тобто порушення утворення всіх формених елементів крові, що мають загального попередника (еритроцитів, гранулоцитів, тромбоцитів).
2.Ушкодження клітин мікрооточення - порушення стромальних клітин, які впливають на процеси розмноження й дозрівання клітин крові. Можливість реалізації даного патогенетичного механізму доводиться існуванням чистих ліній мишей ("сталеві" миші) з первинними спадково обумовленими дефектами стромальних клітин. Для всіх представників "сталевих" мишей характерний розвиток гіпопластичної анемії.
26.1.44.Дайте характеристику картини периферичної крові і червоного кісткового мозку при гіпопластичній анемії.
Для картини периферичної крові характерне зменшення вмісту еритроцитів і концентрації гемоглобіну, при цьому колірний показник у межах норми. У мазку крові, як правило, не виявляють регенераторних форм еритроцитів (ретикулоцитів, поліхроматофІлів). Зменшується вміст гранулоцитів (особливо нейтрофілів) і тромбоцитів. Кількість лімфоцитів може залишатися без змін.
У червоному кістковому мозку зменшується кількість кровотворних клітин зі збільшенням вмісту жирової тканини (картина спустошення червоного кісткового мозку). У зв'язку з тим, що залізо не використовується для кровотворення, збільшується його вміст в еритробластах і позаклітинно.
26.1.45.Визначте місце гіпопластичної анемії в різних класифікаціях
анемій.
|
Класифікація |
Гіпопластична анемія |
|
|
|
І. |
За патогенезом |
Анемія, пов'язана з порушеннями |
|
|
еритропоезу |
|
|
|
II. |
За етіологією |
Набута, є спадкові форми |
|
|
|
III. |
За регенераторною здатністю |
Гіпоабо арегенераторна |
|
червоного кісткового мозку |
|
|
|
|
IV. |
За колірним показником |
Нормохромна |
|
|
|
V. |
За типом кровотворення |
3 еритробластичним типом |
|
|
кровотворення |
VI. |
За клінічним перебігом |
Хронічна |
|
|
|
26.1.46. Якими синдромами виявляє себе гіпопластична анемія?
Прояви гіпопластичної анемії пов'язані зі зменшенням утворення трьох видів формених елементів крові: еритроцитів, гранулоцитів і тромбоцитів. Це призводить до розвитку таких клінічних синдромів.
I. Анемія і пов'язаний з нею гіпоксачниїї синдром. II. Геморагічний синдром (див. розд". 26.3).
III. Запальні процеси, обумовлені інфекційними агентами (пневмонія, отит, пієліт та ін.).
26.1.47. Що таке металобластичні анемії? Наведіть приклади.
Мегалобласмичні анемії-це група анемій, в основі яких порушення синтезу нуклеїнових кислот у клітинах і, як наслідок, порушення розмноження останніх. До мегалобластичних відносять:
1) анемію, обумовлену дефіцитом вітаміну В і фолієвої кислоти, - Вп-
фолієводефі-цитну анемію;
2)перніціозну анемію Аддісона-Бірмера (етіологію не встановлено);
3)анемію, пов'язану з порушеннями ферментів синтезу пуринових і піримідинових
основ, — В 12-рефрактерну анемію (стійку до лікування вітаміном В|2).
За походженням мегалобластичні анемії можуть бути набутими (виявляються звичайно у дорослих і осіб літнього віку) і спадково обумовленими. В останньому випадку порушення можуть мати стосунок до системи транспорту речовин (усмоктування в травному каналі) і реакцій метаболізму (ферментопатії).
26.1.48. Яка роль вітаміну В12 і фолієвої КИСЛОТИ В забезпеченні кровотворення?
Вітамін В (ціанокобаламін) надходить в організм у складі харчових продуктів (м'ясо, яйця, сир, печінка) у зв'язаному з білками вигляді. У результаті гідролізу
білків вітамін В]2 вивільняється в шлунку, де утворюється комплекс вітаміну В,2 з
гастромукопротеїном (внутрішнім фактором Кастла). 1 мг гастромукопротеїну
зв'язує 25 мг вітаміну В]2. Комплекс, що утворився, всмоктується в середньому й нижньому відділах клубової кишки.
Транспорт вітаміну В12 кров'ю здійснюється за допомогою специфічних транспортних білків - транскобаламінів. Печінка є важливим депо вітаміну В12. Запаси його тут настільки великі, що потрібно 3-6 років, аби при порушеннях надходження вітаміну В в організмі виникли ознаки його дефіциту.
У клітинах з вітаміну В12 утворюється дві його коферментні форми: метилкобаламін і 5-дезоксиаденозилкобаламін.
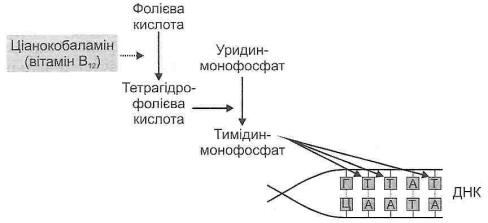
Метилкобаламін необхідний для синтезу ДНК у клітинах, тому він істотно впливає на кровотворення (рис. 105).
Рис. 105. Вплив ціанокобаламіну на кровотворення
Цей кофермент входить до складу ферментного комплексу, що перетворює фолієву кислоту на її коферментну форму — тетрагідрофолієву кислоту. Тетрагідро-
фолієва кислота, у свою чергу, є коферментом ферментного комплексу, що каталізує реакцію перетворення уридинмонофосфату на тимідинмонофосфат, що йде на побудову ланцюгів ДНК.
Друга коферментна форма вітаміну В]2 - 5-дезоксіаденозилкобаламін — необхідна для нормального обміну жирових кислот. Вона бере участь у реакціях перетворення токсичного продукту обміну - метилмалонової кислоти на сукцинат, котрий потім надходить у цикл Кребса.
26.1.49. Назвіть основні причини недостатності вітаміну В12в організмі.
1. Екзогенна (аліментарна) недостатність — недостатнє надходження вітаміну
В12 в організм з продуктами харчування. Може розвиватися у маленьких дітей при вигодовуванні їх козяч им молоком або сухими молочними сумішами.
2. Порушення всмоктування вітаміну BJ2:
а) порушення утворення й секреції гастромукопротеїну (внутрішнього фактора Кастла). Буває при спадково обумовлених порушеннях, атрофії слизової оболонки шлунка, аутоімунних ушкодженнях парієтальних клітин слизової шлунка, після гастректомії або видалення понад 2/3 шлунка; б) порушення функції тонкої кишки: хронічні проноси (целіакія, спру), резекція великих ділянок кишки;
в) конкурентне використання вітаміну В12 гельмінтами й мікрофлорою кишок (дифілоботріоз, синдром "сліпої петлі").
3.Порушення утворення транскобаламінів у печінці.
4.Порушення депонування вітаміну Впу печінці (наприклад, при цирозі).
5.Посилене використання вітаміну Вп (наприклад, при вагітності).
26.1.50.ЯКИЙ патогенез порушень, що розвиваються в організмі при
дефіциті вітаміну В12?
Дефіцит вітаміну В12 призводить до розвитку розладів, пов'язаних з порушенням утворення двох коферментних форм цього вітаміну: метилкобаламіну та 5- дезоксіа-денозилкобаламіну.
Недостатнє утворення метилкобаламіну, як і дефіцит фолієвої кислоти, викликає порушення утворення тетрагідрофолієвої кислоти, у результаті чого не відбувається перетворення уридинмонофосфату в тимідинмонофосфат. Унаслідок дефіциту пуринових основ порушуються синтез ДНК і розмноження клітин, у першу чергу кровотворних і епітелію травного каналу.
У червоному кістковому мозку еритробластичний тип кровотворення змінюється на мегалобластичний, зростає неефективний еритропоез, стає коротшою тривалість життя еритроцитів. Розвивається анемія, при якій клітини патологічної регенерації й еритроцити з вираженими дегенеративними порушеннями з'являються не тільки в кістковому мозку, але й у крові.
Зміни в клітинах мієлоїдного й мегакаріоцитарного ряду виявляються зменшенням кількості лейкоцитів і тромбоцитів, вираженою атипією клітин (гігантські нейтрофіли, мегакаріоцити з дегенеративними змінами в ядрі).
Виникнення при дефіциті вітаміну В]2 і фолієвої кислоти атипового мітозу та поява гігантських клітин епітелію травного каналу призводять до розвитку запальноатрофічних процесів у слизовій оболонці його відділів (глосит, стоматит, езофагіт, ахі-лічний гастрит, ентерит). Це посилює первинні порушення секреції або
всмоктування гастромукопротеїну, а отже, посилює дефіцит вітаміну Вр ("зачароване коло").
У результаті недостатності другої коферментної форми вітаміну В — 5-дезоксіа- денозилкобаламіну в організмі накопичуються пропіонова і метилмалонова кислоти, токсичні для нервових клітин. Крім того, у нервових волокнах синтезуються жирові кислоти зі зміненою структурою, що призводить до порушення утворення мієліну і ушкодження аксонів. Розвивається дегенерація задніх і бічних стовпів спинного мозку (фунікулярний мієлоз), уражаються черепні й периферичні нерви.
26.1.51.Дайте характеристику картини периферичної крові і
червоного кісткового мозку при В 12-фолієводефіцитній анемії.
Найхарактернішою рисою цієї анемії є поява в крові й червоному кістковому мозку

клітин патологічної регенерації — мегалобластів та їхніх без'ядерних форм-
мегалоцитів.
На тлі істотного зменшення вмісту еритроцитів і концентрації гемоглобіну колірний показник збільшений, що пояснюється більшим діаметром еритроцитів. Характерне явище дегенерації еритроцитів: анізоцитоз (макроцитоз), пойкілоцитоз (поява клітин овальної форми), патологічні включення (тільця Жоллі, тільця Кебота).
У крові зменшений вміст гранулоцитів (особливо нейтрофілів) і тромбоцитів. Виявляються гігантські нейтрофіли з гіперсегментованими ядрами.
26.1.52. Визначте місце В 12-фолієводефіцитної анемії в різних класифікаціях анемій.
|
Класифікація |
В^-фолієводефіцитна анемія |
І. |
За патогенезом |
Анемія, пов'язана з порушеннями еритропоезу |
|
|
|
II. |
За етіологією |
Набута, є спадкові форми |
|
|
|
III. |
За регенераторною здатністю |
Гіпорегенераторна |
|
червоного кісткового мозку |
|
|
|
|
IV. |
За колірним показником |
Гіперхромна |
|
|
|
V. |
За типом кровотворення |
3 мегалобластичним типом кровотворення |
|
|
|
VI. |
За клінічним перебігом |
Хронічна |
|
|
|
26.1.53.Якими синдромами виявляє себе В 12-фолієводефіцитна
анемія?
При В -фолієводефіцитній анемії спостерігають:
1. Гематологічний синдром:
а) анемія і пов'язана з нею гіпоксія; б) лейкопенія (нейтропенія), що призводить до зниження резистентності організму до інфекцій;
в) тромбоцитопенія, що викликає розвиток геморагічного синдрому.
2. Ураження травного каналу, що виявляються розвитком запально-атрофічних змін у слизовій оболонці: глосит, стоматит, езофагіт, ахілічний гастрит, ентерит.
3. Ураження центральної й периферичної нервової системи: фунікулярний мієлоз,
дегенерація периферичних нервів.
26.1.54.У чому полягає фізіологічне значення заліза?
В організмі дорослої людини масою 70 кг міститься 4,5 г заліза. Воно в гемовій і негемовій формах входить до складу цілого ряду білків.
I. Білки, які містять залізо в гемовій формі:
а) гемоглобін; б) міоглобін; в) цитохроми; г) каталаза; ґ) лактоферин.
II. Білки, які містять залізо в негемовій формі:
а) феритин; б) гемосидерин;
в) трансферин; г) ферменти: аконітаза, ксантиноксидаза, НАДН-дегідрогеназа.
26.1.55. Як відбувається обмін заліза в організмі?
Залізо надходить в організм у складі харчових продуктів (м'ясо, печінка, риба, рис, горох, курага). Найкраще всмоктується залізо, що входить до складу харчових білків у формі гема. Стінки кишок містять фермент гемоксигеназу, що розщеплює гем харчових продуктів на білірубін, оксид вуглецю (II) та іони заліза, останні і всмоктуються в тонкій кишці. Цьому процесу сприяють аскорбінова кислота, фруктоза, піровиноградна кислота. Системи транспорту заліза в кишках можуть забезпечити всмоктування максимум 2,5 мг заліза за добу, незалежно від потреби організму в цьому елементі.
Транспорт заліза в організмі здійснюється за допомогою білка трансферину, а депонування відбувається у формі іншого білка - феритину. Надходячи в клітини, залізо зв'язується з внутрішньоклітинним білком сидерохіліном, що транспортує залізо в мітохондрії, де синтезується гем.
Фізіологічні втрати заліза невеликі. У чоловіків вони становлять менш ніж 1 мг/ добу (втрати із сечею, потом, злущеним епітелієм шкіри). У жінок вони набагато більші і обумовлені менструаціями, вагітністю, пологами, лактацією.
26.1.56.Назвіть можливі причини розвитку залізодефіцитної анемії.
1. Недостатнє надходження заліза в організм:
а) аліментарна анемія в грудних дітей (вигодовування коров'ячим або козячим молоком); б) порушення всмоктування заліза (резекція шлунка, кишок, гастрити, ентерити).
2. Крововтрати. Це найпоширеніша причина дефіциту заліза в організмі. Найчастіше буває при невеликих, але повторних кровотечах (хронічна постгеморагічна анемія).
3. Посилене використання заліза - вагітність, лактація.
26.1.57.ЯКИЙ патогенез порушень, що розвиваються в організмі у зв 'язку з дефіцитом заліза ?
Недостатність заліза в організмі призводить до порушення синтезу залізовмісних білків, а отже, до розладів функцій, у виконанні яких беруть участь ці білки. Найбільше значення мають такі лінії патогенезу:
1) дефіцит заліза → порушення синтезу гема і гемоглобіну → анемія; 2) дефіцит заліза → порушення синтезу гема → порушення утворення цитохро-мів
→ розлади клітинного дихання (порушення утилізації кисню) → тканинна гіпоксія; 3) дефіцит заліза → порушення синтезу гема → зменшення активності каталази → порушення функції антиоксидантних систем → активація вільнорадикального окиснення → ушкодження клітин → гемоліз еритроцитів і розвиток дистрофічних змін у клітинах; 4) дефіцит заліза → порушення синтезу гема → зменшення синтезу міоглобіну →
зниження пристосувальних можливостей клітин щодо гіпоксії.
26.1.58.Дайте характеристику картини периферичної крові і червоного кісткового мозку при залізодефіцитній анемії.
Для залізодефіцитної анемії характерне зниження концентрації гемоглобіну в периферичній крові і зменшення колірного показника, що свідчить про зменшення насичення кожного окремого еритроцита гемоглобіном. Кількість еритроцитів в одиниці об'єму крові при цьому або трохи зменшується, або залишається без змін. При біохімічних дослідженнях виявляється зниження вмісту заліза в сироватці крові, а також ступеня насичення залізом трансферину.
У мазку крові зменшується кількість регенераторних форм еритроцитів (ретику-

лоцитів, поліхроматофілів) і з'являються дегенеративні форми. Характерні гіпохромія (з'являються анулоцити), анізоцитоз (мікроцитоз), пойкілоцитоз.
У червоному кістковому мозку зменшується вміст сидеробластів і сидероцитів (еритробластів і нормоцитів, що містять гранули заліза), частка яких у нормі становить 20-40 %. У той же час збільшується вміст базофільних і поліхроматофільних форм клітин еритроїдного ряду при одночасному зменшенні оксифільних. Зазначений феномен отримав назву "синього кісткового мозку ".
26.1.59. Визначте місце залізодефіцитної анемії в різних класифікаціях анемій.
|
Класифікація |
Залізодефіцитна анемія |
|
|
|
І. |
За патогенезом |
Анемія, пов'язана з порушеннями еритропоезу |
|
|
|
II. |
За етіологією |
Набута |
|
|
|
III. |
За регенераторною здатністю |
Гіпорегенераторна |
|
червоного кісткового мозку |
|
|
|
|
IV. |
За колірним показником |
Гіпохромна |
|
|
|
V. |
За типом кровотворення |
3 еритробластичним типом кровотворення |
|
|
|
VI. |
За клінічним перебігом |
Хронічна |
|
|
|
26.1.60. Якими синдромами виявляє себе залізодефіцитна анемія?
1.Гематологічний синдром. Охоплює порушення з боку периферичної крові і червоного кісткового мозку.
2.Гіпоксія. Виявляється загальною слабкістю, запамороченнями, серцебиттям, задишкою, непритомностями. Кисневе голодування в умовах дефіциту заліза має два механізми: кров'яний (зменшення кисневої ємності крові) і тканинний (порушення клітинного дихання й утилізації кисню).
3.Синдром трофічних порушень. Виявляється такими ознаками, як сухість і тріщини шкіри, тріщини в кутах рота, ангулярний стоматит, ураження нігтів (зміни форми, стоншення), атрофія сосочків язика (атрофічний глосит), атрофічний гастрит. Вважають, що розвиток зазначених порушень, з одного боку, пов'язаний з гіпоксичним і вільнорадикальним ушкодженням клітин, з другого — з розладами вторинних метаболічних шляхів, у здійсненні яких беруть участь ферменти, що містять залізо.
4.Сидеропенічний синдром. Це специфічний синдром, що виникає при дефіциті заліза. Він виявляється спотвореннями смаку й нюху. Хворі часто їдять крейду, зубний порошок, вугілля, глину, пісок, лід, сирі крупи, тісто, сирий м'ясний фарш. Мають пристрасть до запахів гасу, бензину, ацетону, вихлопних газів автомобілів. Патогенез зазначених порушень досі невідомий.
5.Синдром м'язової слабкості. М'язова слабість, що виникає при дефіциті заліза, завжди більш значна, ніж та, котрої варто було б очікувати, виходячи зі ступеня анемії. Вона виявляється слабкістю і стомлюваністю скелетних м'язів, слабкістю міокарда (міокардіопатія), порушеннями ковтання (дисфагія), порушеннями сечовипускання. Очевидно, що важливе значення в розвитку зазначених симптомів мають гіпоксія (кров'яна і тканинна), а також зменшення вмісту міоглобіну в м'язовій тканині.
26.1.61.Що таке залізорефрактерна анемія? Які її етіологія й патогенез?
Залізорефрактерна анемія-цс анемія, що виникає в результаті порушення
включення заліза в гем при зниженні активності ферментів, що каталізують синтез порфіринів і гема.
Причинами розвитку цієї анемії можуть бути:
1)генетично обумовлене зниження активності декарбоксилази копропорфірииоге-ну - ферменту, що забезпечує один з кінцевих етапів синтезу гема (успадковується рецесивно, зчеплено з Х-хромосомою);
2)зменшення вмісту піридоксальфосфату - активної форми вітаміну В6, унаслідок чого залізо не вилучається з мітохондрій еритробластів і не включається в гем;
3)блокада свинцем сульфгідрильних груп ферментів, що беруть участь у синтезі гема, при побутовому й виробничому отруєнні свинцем.
Зменшення активності ферментів, що беруть участь в утворенні порфіринів і гема, призводить до зниження утилізації заліза й порушення синтезу гема гемоглобіну, що викликає недостатність еритропоезу і розвиток гіпохромної анемії з низьким вмістом гемоглобіну.
Порушення використання заліза супроводжується підвищенням вмісту сироваткового заліза, відкладенням його у внутрішніх органах з вторинним розростанням сполучної тканини (гемосидероз).
26.2. Порушення системи лейкоцитів
26.2.1.Дайте загальну характеристику порушень системи лейкоцитів.
Патологічні зміни лейкоцитів виявляються порушеннями їх утворення в кровотворній тканині, а також кількісними та якісними змінами лейкоцитів крові. Такі порушення можуть бути наслідком первинного ураоїсення клітин гранулоцитарного, лімфоцитарного і моноцитарного рядів під впливом різноманітних патогенних факторів і виявляти себе розладами утворення, дозрівання або ж руйнування лейкоцитів у кровотворній тканині і кровоносному руслі. Вторинні зміни лейкоцитів
виникають як захисна реакція організму у відповідь на патологічні процеси, що відбуваються не [ в самій системі крові, а в органах і тканинах інших систем. Головною ланкою в патогенезі порушень лейкоцитарного паростка крові є зміна реактивності організму, у тому числі імунологічної й алергічної. Це пояснюється розладами основних функції, що їх виконують лейкоцити, беручи участь у процесах фагоцитозу, антитілоутворення, інактивації біологічно активних речовин (гістаміну, брадикініну, серотоніну). Патологічні зміни лейкоцитів можуть супроводжуватися трофічними порушеннями тканин, місцевими мікроциркуляторними розладами. Це обумовлено тим, що одна з функцій лейкоцитів полягає в постачанні тканинам, що регенерують, поживних речовин і стимуляторів поділу клітин. Гранулоцити беруть участь у розвитку судинних порушень як переносники вазоактивних речовин (базофільні, еозинофільні лейкоцити) або ж впливають на їхній синтез і вивільнення з тканинних базофілів (нейтрофільні лейкоцити).
26.2.2.Як розподіляються лейкоцити в організмі?
Лейкоцити містяться в організмі в трьох "відсіках": червоний кістковий мозок, периферична кров, периферичні тканини. І. Червоний кістковий мозок. Тут лейкоцити утворюють 4 пули (рис. 106):

Рис. 106. Emanu лейкопоезу
1)пул стовбурових клітин, що перебувають у стані спокою. Він дуже малий і являє собою резерв кровотворення;
2)мітотичний пул. Це клітини, що перебувають у стані мітотичного поділу. Від стовбурової клітини до утворення клітин, що дозрівають, звичайно проходить від 4 до 11 поділів;
3)пул клітин, що дозрівають. Містить клітини, дозрівання яких триває в середньому 3-5 діб;
4)резервний пул. Складається зі зрілих лейкоцитів, які можуть переходити в кров.
II. Периферична кров:
1)пул циркулюючих лейкоцитів (близько 50 %);
2)пристінковий (маргінальний) пул (близько 50 %).
III. Периферичні тканини:
1)мігруючі лейкоцити,
2)лейкоцити в стані спокою.
Підраховано, що загальна маса лейкоцитів периферичної крові становить близько 10ц червоного кісткового мозку - 500 г, периферичних тканин - 600 г.
26.2.3. Які показники використовують для характеристики стану системи лейкоцитів?
1. Вміст лейкоцитів в одиниці об'єму крові. У нормі цей показник становить від 4 - 109/л до 9 -109/л. Збільшення вмісту лейкоцитів у крові отримало назву
лейкоцитозу, зменшення - лейкопенії.
2. Лейкоцитарна формула. Це кількісне співвідношення різних форм лейкоцитів у периферичній крові.
Для норми характерні такі значення: базофіли — 0—1 %, еозинофіли - 2-4 %, мієлоцити - 0 %, метамієлоцити (юні нейтрофіли) - 0-1 %, паличкоядерні нейтрофіли - 3-5 %, сегментоядерні нейтрофіли 50-70 %, лімфоцити- 20-35 %, моноцити - 2-8 %.
3. Абсолютний вміст кожної форми лейкоцитів в одиниці об'єму крові. Цей показник розраховують, виходячи із загального вмісту лейкоцитів і лейкоцитарної формули.
4. Якісні характеристики лейкоцитів. їх визначають на підставі вивчення мазків периферичної крові. В умовах патології можлива поява різних дегенеративних форм лейкоцитів.
5. Мієлограма. Це показник, що характеризує кількість і якісний склад клітин чер-| воного кісткового мозку.
26.2.4. ЯКИМИ КІЛЬКІСНИМИ І ЯКІСНИМИ змінами лейкоцитів можуть виявляти себе патологічЩ'процеси в організмі?
1. Лейкоцитоз.
2. Лейкопенія.
3. Порушення співвідношення зрілих і незрілих форм лейкоцитів (зміщення лейкоцитарної формули).
4. Дегенеративні зміни лейкоцитів.
26.2.5. Що таке лейкоцитоз? Як класифікують лейкоцитози?
Лейкоцитоз - це збільшення кількості лейкоцитів в одиниці об'єму крові понад) 10
• 109/л. Лейкоцитоз не має самостійного значення, він є всього лише симптомом, що супроводжує розвиток багатьох хвороб.
Класифікація лейкоцитозів.
I. Залежно від причин розвитку виділяють фізіологічний і патологічний лейко-1 цитози.
II. Лейкоцитоз може бути абсолютним і відносним. Для абсолютного лейкоцитозу) характерне збільшення абсолютної кількості лейкоцитів в одиниці об'єму крові. Про відносний лейкоцитоз ідеться в тому випадку, коли зростає відносний вміси окремих форм лейкоцитів у периферичній крові.
III. За механізмом розвитку лейкоцитоз буває:
а) реактивним; б) перерозподільним;
в) пухлинного походження.
IV. Залежно від видів лейкоцитів, вміст яких у крові збільшений, виділяють: а) нейтрофільний лейкоцитоз (нейтрофільоз); б) еозинофільний лейкоцитоз (еозинофілія); в) базофільний лейкоцитоз;
г) лімфоцитарний лейкоцитоз (лімфоцитоз); ґ) моноцитарний лейкоцитоз (моноцитоз).
26.2.6.Наведіть приклади фізіологічного і патологічного лейкоцитозів.
Фізіологічний лейкоцитоз є фізіологічною реакцією організму на ті чи ті впливи. До його різновидів відносять:
а) емоціогенний лейкоцитоз — виникає під час сильних емоцій; б) міогенний — розвивається під час інтенсивної фізичної роботи;
в) статичний — характерний для переходу людини з горизонтального у вертикальне положення; г) аліментарний — розвивається після приймання їжі; ґ) лейкоцитоз у вагітних;
д) лейкоцитоз у новонароджених.
Патологічний лейкоцитоз пов'язаний з перебігом в організмі патологічних процесів. Він, як правило, розвивається при:
а) інфекційних захворюваннях; б) запальних і алергічних процесах;
в) інтоксикації екзо- й ендогенного походження.
26.2.7.Що таке реактивний лейкоцитоз? Які механізми можуть лежати в основі його розвитку?
Реактивним називають лейкоцитоз, що виникає як реакція червоного кісткового мозку на патогенні впливи. Він закономірно розвивається при інфекційних захворюваннях, запаленні, дії низьких доз токсичних речовин.
В основі розвитку реактивного лейкоцитозу можуть лежати два механізми. І.
Посилення проліферації і дозрівання лейкоцитів у червоному кістковому мозку. Це може бути пов'язано або зі збільшенням утворення в організмі лейкопоети-нів -
