
- •Міністерство освіти україни
- •Лабораторна робота №1. Правила роботи в хімічній лабораторії. Знайомство з посудом. Зважування.
- •Лабораторна робота №2. Основні класи неорганічних сполук, генетичний зв’язок між ними
- •Лабораторна робота №3. Швидкість хімічних реакцій
- •Лабораторна робота №6. Приготування розчинів. Способи вираження концентрацій розчинів.
- •Приготування розчинів з заданою масовою часткою речовини в розчині (з твердої речовини та води).
- •Хід роботи
- •Запитання для самоконтролю
- •Завдання для самоконтролю
- •Лабораторна робота №7. Колоїдні розчини
- •Лабораторна робота №8 Теорія електролітичної дисоціації
- •5. Забарвлення індикаторів
- •Завдання для самоконтролю
- •Лабораторна робота №9. Реакції в розчинах електролітів.
- •Завдання для самоконтролю
- •Лабораторна робота №10. Кислотно-основне титрування
- •Хід роботи
- •Лабораторна робота №11. Водневий показник – рН
- •Завдання для самостійної роботи
- •Лабораторна робота №12. Гідроліз солей
- •Завдання для самостійної роботи
- •Лабораторна робота №13. Окисно-відновні реакції
- •Завдання для самоконтролю
- •Лабораторна робота №14. Електрохімічний потенціал. Визначення ерс гальванічного елемента.
- •1. Що таке гальванічний елемент?
- •2. Символічний запис гальванічних ланцюгів.
- •3. Виникнення стрибка потенціалу на межі розділу фаз
- •4. Стандартний водневий електрод. Електродний потенціал. Стандартний (нормальний) електродний потенціал
- •5.Вимірювання ерс гальванічних елементів Вимоги до вхідного опору вольтметра. Похибки вимірювання.
- •6. Електрична схема, що моделює вимірювання ерс гальванічного елемента.
- •6. Абсолютна похибка і відносна похибки
- •Значення ерс гальванічних ланцюгів
- •Лабораторна робота №15.Комплексні сполуки
- •Література Основна
- •Додаткова
6. Абсолютна похибка і відносна похибки
Абсолютна похибка
Різниця між виміряним значенням (Хвим.) і істинним(Хіст.) значенням
Х= Хвим - Хіст.
Якщо говорити про абсолютну похибку вимірювання ЕРС, Е= Евим - Етеор.
Етеор. — теоретичне значення Е.
Евим.— експериментально визначене значення Е.
Відносна похибка
Відношення абсолютної похибки до істинного значення:
 (29)
(29)
![]() (30)
(30)
7. Порядок виконання роботи
Мета роботи:Обчислити ЕРС гальванічних елементів при заданих концентраціях солей та порівняти їх з експериментально виміряними.
Зібрати схему для вимірювання ЕРС за 7
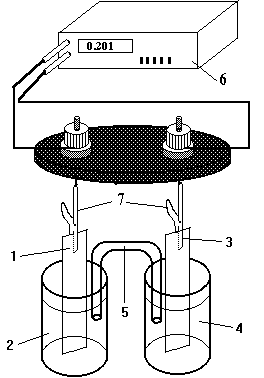
1.Пристрій для вимірювання ЕРС з цифровим вольтметром:
1-пластинка з металу №1,
2-розчин солі металу №1,
3- металічна пластинка №2,
4 розчин солі металу №2,
5- електролітичний місток,
6- вольтметр,
7 - затискачі електродів (крокодили).
Виміряти ЕРС цинк-мідного хімічного елемента (Якобі-Даніеля) при різних концентраціях сульфату міді і сульфату цинку і порівняти їх з обчисленими за формулою
 (розрахувати абсолютну і відносну
похибку).
(розрахувати абсолютну і відносну
похибку).Виміряти ЕРС цинкового та мідного концентраційних елементів, та порівняти з обчисленими за формулою
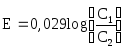 (31) , де С1
- більша концентрація розчину, С2
- менша концентрація розчину,
(31) , де С1
- більша концентрація розчину, С2
- менша концентрація розчину, Виміряти електродні потенціали мідного та цинкового електродів по відношенню до хлор-срібного електроду порівняння. (Стандартний хлор-срібний електрод порівняння при 250С має потенціал 0,201В по відношенню до стандартного водневого електроду) і порівняти їх з обчисленими даними за формулою 24 (розрахувати абсолютну і відносну похибку).
Результати роботи записати в таблицю №1.
Таблиця №1
Значення ерс гальванічних ланцюгів
|
№ |
Схема ланцюгів |
E обчис-лене |
E експери-ментальне |
Абсолют-на похибка |
Відносна похибка | ||||
|
|
— Cu,ZnZnSO4KClCuSO4Cu+ C1=1н нас. C2=1н |
|
|
|
| ||||
|
|
— Cu,ZnZnSO4KClCuSO4Cu+ C1=0,1н нас. C2=1н |
|
|
|
| ||||
|
|
— Cu,ZnZnSO4KClCuSO4Cu+ C1=0,1н нас. C2=0,1н |
|
|
|
| ||||
|
|
— Cu,ZnZnSO4KClCuSO4Cu+ C1=1н нас. С2=0,1н |
|
|
|
| ||||
|
|
—ZnZnSO4KClZnSO4Zn+ C1=0,1н нас. C2=1н |
|
|
|
| ||||
|
|
—CuCuSO4KClCuSO4Cu+ C1=0,1н нас. C2=1н |
|
|
|
| ||||
|
|
— Ag,ZnZnSO4KClAgClAg+ C=1н нас. |
|
|
|
| ||||
|
|
+ Ag,CuCuSO4KClAgClAg— C=1н нас. |
|
|
|
| ||||
Запитання до самопідготовки
Що таке подвійний електричний шар. Яка його природа?
Яка будова гальванічного елемента Якобі-Даніеля?
Дайте визначення електродного потенціалу?
Дайте визначення стандартного (нормального) електродного потенціалу?
Запишіть рівняння Нернста.
Поясніть як записати гальванічний ланцюг.
Поясніть як теоретично розрахувати ЕРС гальванічного елемента.
Дайте визначення аноду і катоду в гальванічному елементі та в електролізері.
Електроди порівняння (водневий, стандартний водневий, хлор-срібний, каломельний).
Принципові схеми пристроїв, вимоги та дія приладів для вимірювання ЕРС.
.
