
- •5.2.3. Виды патологических состояний у человека, связанные
- •1.1. Проявления, механизмы развития и регуляция апоптоза на уровне клетки
- •1.1.2. Многообразие пусковых механизмов апоптоза
- •1.1.3. Пути передачи внутриклеточных сигналов к развитию апоптоза (частные события)
- •1.1.4. Общий путь индукции апоптоза
- •1.1.5. Эндогенные регуляторы апоптоза
- •1.2. Роль апоптоза в многоклеточном организме
- •1.2.1. Апоптоз, процессы формообразования и клеточного гомеостаза на уровне организма
- •1.2.2. Роль апоптоза в иммунных процессах
- •1.3. Место апоптоза в патологии
- •Участие апоптоза а формировании типовых патологических процессов Изменение выраженности апоптоза
- •Повышение вероятности развития злокачественных опухолей
- •1.3.2. Патологические процессы, обусловленные ослаблением апоптоза
- •1.3.3. Патологические процессы,
- •2.1. Словарь сокращений и терминов
- •2.1.3. Цитокины
- •2.1.4. Конкретные иммунологические эффекторные реакции
- •2.2. Определение понятия «иммунитет»
- •2.3. Главные функции иммунной системы
- •2.4.1. Органы лимфопоэза
- •2.4.2. Характеристика лимфоцитов
- •2.5. Гуморальные факторы иммунитета
- •2.6. Стадии развития иммунного ответа
- •2.7. Иммунная подсистема кожи
- •2.8. Иммунная система слизистых оболочек
- •2.9. Патологические процессы с участием иммунной системы
- •2.9.1. Полноценная иммунная система
- •2.9.2. Генетические дефекты в иммунной системе
- •Дефект гуморального звена иммунитета (антитела, комплемент)
- •2.9.2.2. Патологические процессы с участием иммунной системы при общем тяжелом патологическом процессе в организме
- •2.9.3. Иммуностимулирующая терапия, неспецифичная по антигену
- •3.1. Аллергены и аллергенность
- •3.1.1. Номенклатура аллергенов
- •3.1.2. Идентификация и очистка аллергенов
- •3.1.3. Нашивные аллергены как гетерогенная и изменчивая популяция
- •3.2. Иммуноглобулин е:
- •3.2.1. Модель запуска синтеза IgE
- •Связывание аллергена поверхностным иммуноглобулином на в-клетке
- •Процессинг аллергена
- •Активация транскрипции на Запуск.Переключающий специфическом регионе Ig рекомбинации на синтез локуса IgE
- •3.2.2. Сигнал индукции синтеза IgE,
- •3.2.5. Независимая от взаимодействия cd40 с cd154 индукция синтеза IgE
- •3.2.6. Вспомогательные молекулы, усиливающие и сдерживающие влияния
- •Cd28 (т-клетка)
- •Усиление
- •Усиление экспрессии с080 (в-клетка)
- •3.2.7. Избирательность включения тъ2-клеток в IgE-omeem
- •3.2.8. Возможные способы оценки опосредуемого Тп2-клетками аллергического ответа в клинических условиях
- •3.3. Некоторые замечания
- •4.1.1. Классификация
- •4.1.2. Краткие эпидемиологические данные
- •4.1.3. Этиологические факторы канцерогенеза
- •4.1.4. Характерные свойства опухолей
- •4.1.5. Взаимоотношения опухоли и организма
- •4.1.6. Стадии развития
- •4.2.1. Изменения кариотипа
- •4.2.2. Признаки клеточной трансформации в культуре
- •4.2.3. Иммортализация опухолевых клеток
- •4.2.4. Межклеточная кооперация
- •4.3. Молекулярные механизмы опухолевого роста
- •4.3.1. Эндокринная, паракринная и аутокринная регуляция
- •4.3.2. Митогенная «рефлекторная дуга»
- •4.3.3. Клеточный цикл
- •4.3.4. Перенос митогенного сигнала
- •Неактивный Ras
- •I I ядро
- •Мекк мек »► erk
- •4.3.5. Реализация митогенного сигнала
- •4.3.6. Апоптоз
- •4.3.7. Механизмы опухолевой трансформации
- •I Мутантные по р53 клетки I доминируют в опухоли
- •Нормальный эпителий
- •5.1. Феномен стресса
- •5.1.1. Стресс-реакция
- •Стрессор
- •Побочные эффекты стресс-реакции адаптация (восстановление гомеостаза)
- •5.1.2. Стресс-система
- •Периферические и черепные нервы, кровь
- •Стресс-реакция
- •5.1.3. Стресс-лимитирующие системы
- •Стрессор
- •Ограничание высвобождения а и на в цнс и органах
- •I Ограничение cmpecc-реекции и ее повреждающих эффектов I
- •5.1.4. Роль соотношения активностей
- •5.1.5. Адаптивные и повреждающие эффекты стресс-реакции
- •5.2. Эмоциональный стресс и связанные с ним патологические состояния
- •5.2.1. Особенности эмоциональных стрессоров и эмоциональной стресс-реакции
- •5.2.2. Стрессорные патологические состояния и их возможные механизмы
- •5.2.2.1. Роль стресс-системы в формировании эмоционального стресса и патогенезе стрессорных повреждений
- •Субъективная оценка фактора
- •Слабая стресс-реакция или отсутствие стресс-реакции
- •5.2.3. Виды патологических состояний у человека, связанные с эмоциональным стрессом, и их механизмы
- •2 Х е м а 5.7. Патогенез первичного стрессорного повреждения сердца [Meerson f., 1991]
- •Стрессор
- •I | Активация стресс-системы. Стресс-реакция | Действие на сердце избытка катехоламинов и других гормонов. Активация аденилат-циклазы, фосфолипазы с
- •Нарушение функционирования Na -, к*- и Са2*- насосов сарколеммы, Са2* насоса спр
- •5.2.3.1.1. Ишемическая болезнь сердца и инфаркт миокарда
- •Уменьшение периферического сопротивления сосудов
- •5.2.3.1.2. Внезапная сердечная смерть
- •Отличительные признаки
- •Стрессорная аритмическая болезнь сердца
- •5.2.3.1.3. Гипертоническая болезнь
- •IЯзвенное поражение желудка
- •5.2.3.3. Система крови и иммунная система при эмоциональном стрессе
- •Уменьшение синтеза антител
- •5.2.3.4. Психический статус при эмоциональном стрессе и посттравматическое стрессовое расстройство
- •5.2.3.4.1. Нарушения психического статуса
- •5.2.3.4.2. Посттравматическое стрессовое расстройство2
- •5.2.4. Основы предрасположенности и устойчивости к стрессорным повреждениям
- •5.3. Принципы профилактики и коррекции стрессорной патологии
- •5.3.1. Профилактика и коррекция с помощью защитных эффектов адаптации к факторам среды
- •5.3.2. Коррекция с помощью
- •5.3.3. Использование приемов психотерапии при стрессорных психосоматических расстройствах
- •6.1. Характеристика боли
- •6.2. Физиология боли
- •6.2.1. Анатомо-функциональная организация ноцицептивной системы
- •6.2.1.2. Периферические алгогены
- •6.2.1.3. Первое переключение ноцицептивной информации (первичное ноцицептивное реле)
- •6.2.1.6. Обработка ноцицептивной информации в коре больших полушарий
- •6.2.2. Антиноцицептивная система мозга
- •6.3. Патофизиология боли
- •6.3.1. Соматогенные болевые синдромы
- •6.3.1.2. Механизмы развития вторичной гипералгезии
- •6.3.2. Патофизиология нейрогенных болевых синдромов
- •6.3.2.3. Периферические механизмы нейрогенной боли
- •7.1. Современные представления о свертывании крови
- •7.1.1. Механизмы свертывания крови
- •I Сосудистая стенка .
- •|Г* Фосфолипаза Аг
- •3 (Простат
- •I римооксан а2 pgi2
- •7.1.2. Механизмы ингибирования свертывания крови. Фибринолиз
- •7.2. Современные представления о природе тромбозов
- •7.2.1. Основные причины развития тромбозов
- •7.2.2. Лабораторная диагностика вероятности развития тромбозов
- •7.3. Геморрагии
- •7.3.1. Виды и основные причины развития геморрагии
- •7.3.2. Лабораторная диагностика геморрагических состояний
- •7.5. Лекарственная коррекция патологии гемостаза
Мекк мек »► erk
МАР-киназный каскад JNK/SAPK-киназный каскад HOG/рЗв-киназный каскад
Raf, Mos, MEKK1
МЕК1.2
ERK1.2
MEKK1
\
JNKK
I
JNK/SAPK
MEKK1
\
JNKK.MKK3
I
HOG/D38
MAP — киназные модули млекопитающих; ERK — extracellular signal-regulated kinase; MKK — MAP kinase/ERK kinase; МЕК — то же, что и МАРКК; МЕКК — МЕК kinase; JNK/SAPK — Jun-N-terminal kinase/stress-activated protein kinase; JNKK — JNK kinase. Пояснения в тексте.
щие один и тот же путь, способны вызывать абсолютно разные клеточные реакции. Так, активация Ras в клетках линии PC 12 эпидермальным фактором роста вызывает клеточную пролиферацию, а фактором роста нервов — дифференцировку.
Разнообразие сигналов, использующих МАР-киназный путь, свидетельствует о том, что он «служит» разным целям. Конкретные же последствия его активации (иногда диаметрально противоположные) определяются той конкретной ситуацией, в которой оказалась данная клетка. Вместе с тем важно подчеркнуть, что этот сигнальный путь, как и другие, не «линеен», а входит как элемент в сложную сеть конвергирующих и ветвящихся информационных потоков.
Наиболее полно изученный и состоящий из 3 ферментов МАР-киназный каскад является каноническим для ряда других 3-киназных каскадов, обнаруженных в клетках млекопитающих и обладающих иными внутриклеточными мишенями (схема 4.1). Согласно концепции трехкомпонентных МАР-ки-назных модулей, они, будучи во многих отношениях родственными, «обслуживают» разные рецепторы и образуют параллельные информационные потоки. Наряду с каноническим МАР-киназным каскадом (МАРККК -> МАРКК -> МАРК) существуют трехкомпонентные JNK/SAPK (Jun-N-terminal kinase/stress-activated protein kinase) и HOG/p38 каскады (одни и те же киназы известны иногда под разными названиями, что объясняется их независимым обнаружением в разных лабораториях).
Активность ферментов, участвующих в киназных каскадах, уравновешивается активностью противодействующих им и находящихся под столь же строгим контролем фосфатаз.
13—1385
193
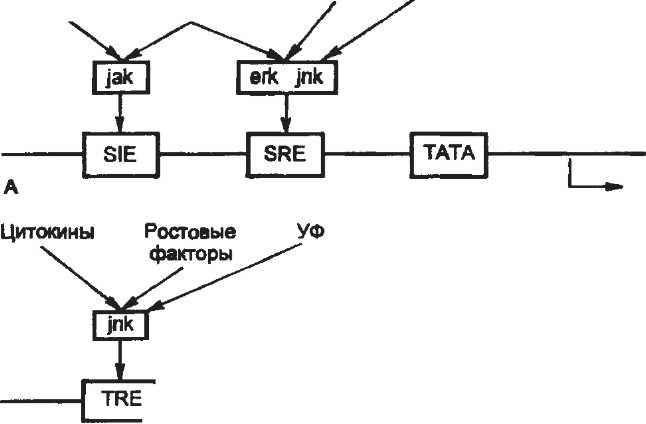
Активация транскрипции. Группа генов, определяющих вхождение клетки в фазу S, активируется транскрипционным фактором АР-1, представляющим собой комплекс белков — членов семейств Jun и Fos (гены, их кодирующие, — c-jun и c-fos, относятся к числу протоонкогенов; с — от cell, обозначает их клеточное происхождение в отличие от вирусных онкогенов v-jun и v-fos). Эти транскрипционные факторы могут взаимодействовать между собой с образованием множества гомо- и гетеродимеров, связывающихся с определенным участком ДНК и стимулирующих синтез РНК на прилежащих к этим участкам генов.
Регуляторные участки (прямоугольники), прилежащие к генам c-fos и c-jun, взаимодействуют с транскрипционными факторами (на схеме не представлены), активированными соответствующими протеинкиназами (последние принадлежат к различным киназным каскадам). SIE (sis-induc-ible enhancer), SRE (serum response element), TRE (TPA response element) — регуляторные участки генов; TATA (так называемый TATA-box) — короткая нуклеотидная последовательность, играющая важную роль в формировании транскрипционного комплекса; Jak, Jnk, Erk — последние члены разных киназных каскадов; А — активация c-fos (стрелка показывает начало считывания РНК); Б — активация c-jun.
|
1 1 |
TATA |
|
|
J 1 |
1 |
МАР-киназы повышают активность АР-1 двояким образом: а) опосредованным, активируя соответствующие гены и увеличивая тем самым содержание комплекса в клетке, и б) прямым, фосфорилируя входящие в их состав сериновые и треониновые остатки. В первом случае (схема 4.2) МАР-киназы фосфорилируют в строго определенных сайтах соответст-
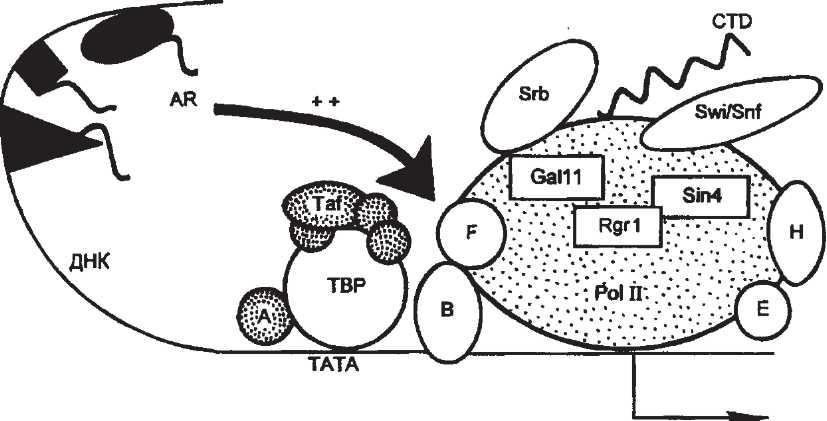
Рис.
4.9. Транскрипционная триада — типичный
эукариотический транскрипционный
комплекс в промоторном участке гена.
Белки-активаторы (Аг) «садятся» на
участок энхансера (регуляторная
последовательность ДНК, усиливающая
транскрипцию) и стимулируют (++) синтез
РНК посредством белок-белкового
взаимодействия своих активирующих
доменов (волнистая линия) с компонентами
базового аппарата транскрипции. Последний
состоит из двух основных компонентов
— ТВР
(TATA-binding protein)
и РНК-полимеразы II
(Pol II).
С ТВР взаимодействует около 10
дополнительных
белков —
Taf (TBP-associated factors)
и транскрипционный фактор
TFIIA
(А). В состав комплекса с РНК-полимеразой
входят транскрипционные факторы
TFIIB
(В),
TFIIE
(Е),
TFIIF (F), TFIIH
(Н) и ряд дополнительных белков,
способствующих правильной посадке
комплекса и точной транскрипции, —
Srb, Gall
1,
Sin4, RgrI,
а также мультифермент-ный комплекс
Swi/Snf
(ДНК-стимулируемая АТФаза), вызывающий
разрушение структуры нуклеосом и
движение РНК-полимеразы по нити хроматина.
вующие транскрипционные факторы (в частности, TCF — ternary complex factor). Последний взаимодействует с так называемым базовым аппаратом транскрипции — мультифермент-ным комплексом, формирующимся на промоторном участке гена (в частности, на последовательности так называемого ТАТА-бокса), в состав которого входит РНК-полимераза, и активируют его (рис. 4.9).
Активация гена, таким образом, обеспечивается триадой: а) транскрипционные белки-активаторы, связывающиеся с энхансерами; б) транскрипционные факторы, взаимодействующие с ТАТА-боксом; в) РНК-полимераза II в комплексе со вспомогательными белками. Гены c-jun и c-fos относятся к числу генов немедленного реагирования (immediate-early genes), чья активность зависит от синтеза новых бел-
13*
195
ков и очень быстро возрастает вслед за клеточной стимуляцией.
Другой путь активации комплекса АР-1 — непосредственное фосфорилирование Fos (треонина в положении 232) и Jun (серины в положении 73 и 63). Эти события способствуют, с одной стороны, формированию активного комплекса Fos/Jun, а с другой — усилению его активирующего воздействия на базовый аппарат транскрипции. В фосфорилировании Jun участвует JNK (Jun N-terminal kinase), а в фосфорилировании Fos — FRK (Fos regulating kinase), входящие в семейство МАР-киназ.
В результате активации генов продуцируются белки, необходимые для синтеза ДНК и последующего митоза. Некоторые из новообразованных белков (Fos, Jun, Мус), известные как белки раннего ответа (immediate-early proteins), выполняют регуляторные функции; связываясь со специфическими участками ДНК, они активируют прилежащие гены. Другую группу составляют ферменты, такие как тимидинкиназа, рибонуклео-тидредуктаза, дигидрофолатредуктаза, тимидилатсинтаза, ор-нитиндекарбоксилаза, ДНК-полимеразы, топоизомеразы и множество других, которые имеют непосредственное отношение к синтезу ДНК. Усиливается, кроме того, общий белковый синтез, поскольку при каждом цикле удвоения воспроизводятся все клеточные структуры.
Нормальное прохождение клеткой отдельных фаз клеточного цикла обеспечивается строгой последовательностью и упорядоченностью во времени многочисленных ферментативных процессов. Роль «водителя ритма» при этом играют белки циклины, закономерным образом сменяющие друг друга на протяжении цикла.
