
- •Электролиз растворов
- •10. Содержание отчета
- •11. Контрольные вопросы.
- •Взаимодействие азотной кислоты с металлами.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Свойства серной кислоты.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Взаимодействие оксидов щелочных и щелочноземельных металлов с водой и кислотами
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Взаимодействие гидроксида кальция с оксидом углерода (IV).Получение и свойства оксида фосфора (V).
- •7. Содержание отчета
- •8. Контрольные вопросы.
- •Влияние температуры и разбавления на степень гидролиза.
- •7. Содержание отчета
- •8. Контрольные вопросы.
- •Качественные реакции на неорганические соединения. Обратимость химических реакций.
- •8. Содержание отчета
- •9. Контрольные вопросы.
- •Горение щелочных и щелочноземельных металлов на воздухе.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Конструирование молекул алканов и циклоалканов.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Предельные углеводороды.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Спирты.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Конструирование моделей структурных звеньев полимеров.
- •9. Содержание отчета
- •10. Контрольные вопросы.
- •Моделирование построения Периодической таблицы химических элементов
- •7. Содержание отчета
- •5. Содержание отчета
- •Решение экспериментальных задач на идентификацию органических соединений
- •4. Задания
- •5. Содержание отчета
8. Содержание отчета
8.1. Наименование и цель работы.
8.2. Выполненное задание (уравнения реакций, наблюдения, выводы)
8.3. Ответы на контрольные вопросы.
9. Контрольные вопросы.
1. От каких факторов зависит скорость реакции? Приведите примеры.
2. Почему скорость многих химических реакций с течением времени уменьшается? Приведите примеры, когда скорость реакции с течением времени увеличивается?
3. Могут ли отличаться скорости прямой и обратной реакций до достижения равновесия? Приведите примеры.
4.
![]()
5.
![]()
6. Изменится ли состояние равновесия в следующей системе, если смесь газов сжать:
![]()
7.В какую сторону смещаются равновесия при повышении температуры в следующих системах:
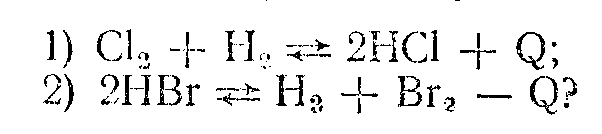
8.В какую сторону сместятся равновесия при повышении давления в системах:
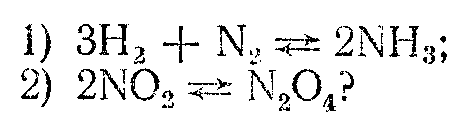
9. Как изменятся равновесия при понижении температуры в системах:
![]()
10. Как повлияет: А) повышение давления; Б) повышение температуры; В) увеличение концентрации кислорода на равновесие системы:
![]()
Лабораторная работа №8
Горение щелочных и щелочноземельных металлов на воздухе.
Цель работы
Изучить горение щелочных и щелочноземельных металлов на воздухе.
Подготовка к работе
Изучить материал по указанной литературе.
Ответить на контрольные вопросы.
Литература
Габриелян О.С. Химия. 11 класс. Базовый уровень: учеб. для обще- образоват. учреждений.- М.,2009,стр. 180-187.
Глинка Н.Л. Общая химия.-М.,2003, стр.382 - 393.
Перечень необходимых материалов
Программа «Виртуальная химическая лаборатория».
Задание
Используя методические указания и программу «Виртуальная химическая лаборатория» изучить горение щелочных и щелочноземельных металлов на воздухе.
Порядок выполнения работы
Получить допуск к работе.
Выполнить задание.
Методические указания
Запустить программу «Виртуальная химическая лаборатория». Выбрать панель «Свойства неорганических веществ», затем тему «Щелочные и щелочноземельные металлы и их соединения». Для получения допуска к работе выполнить тест по технике безопасности. После прохождения тестирования выбираем опыт «Горение щелочных и щелочноземельных металлов на воздухе».
Перед началом работы ознакомьтесь с порядком выполнения опыта.
Оформить отчет о проделанной работе.
9. Содержание отчета
9.1. Наименование и цель работы.
9.2. Выполненное задание (уравнения реакций, наблюдения, выводы)
9.3. Ответы на контрольные вопросы.
10. Контрольные вопросы.

2. Запишите определение коррозии. Объясните, в чем заключается вред, наносимый коррозией.
3.

4.
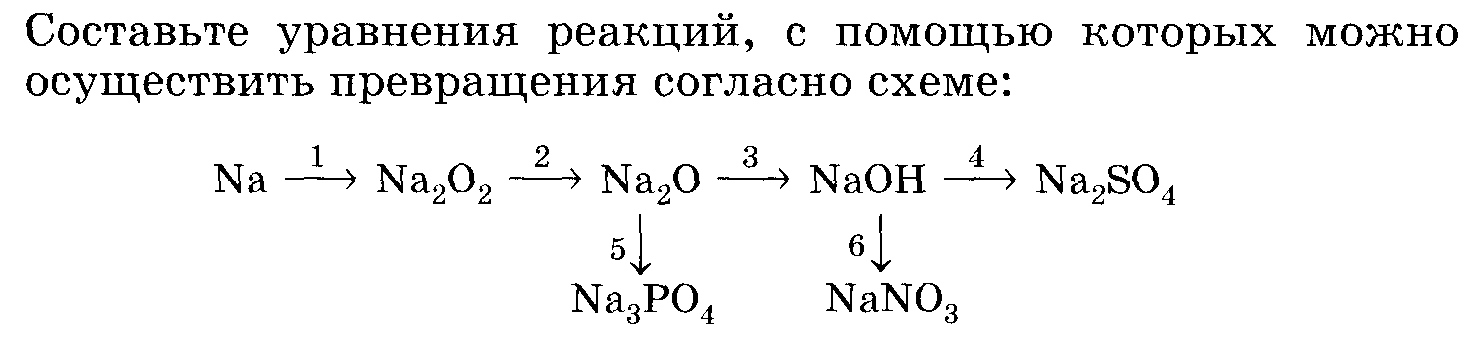
5.
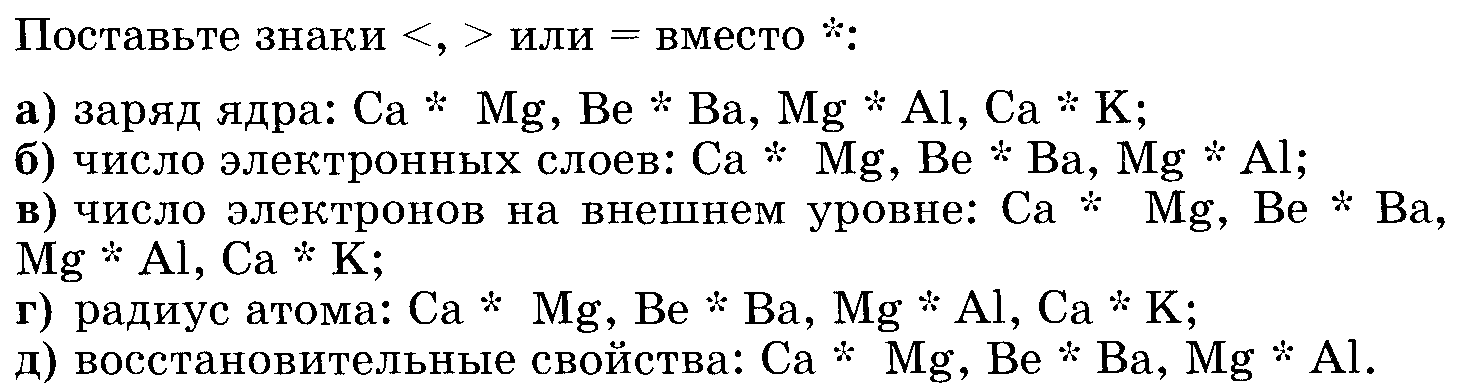
6. Какой объем водорода получится при действии на воду сплава, содержащего 4,6 г натрия и 3,9 г калия.
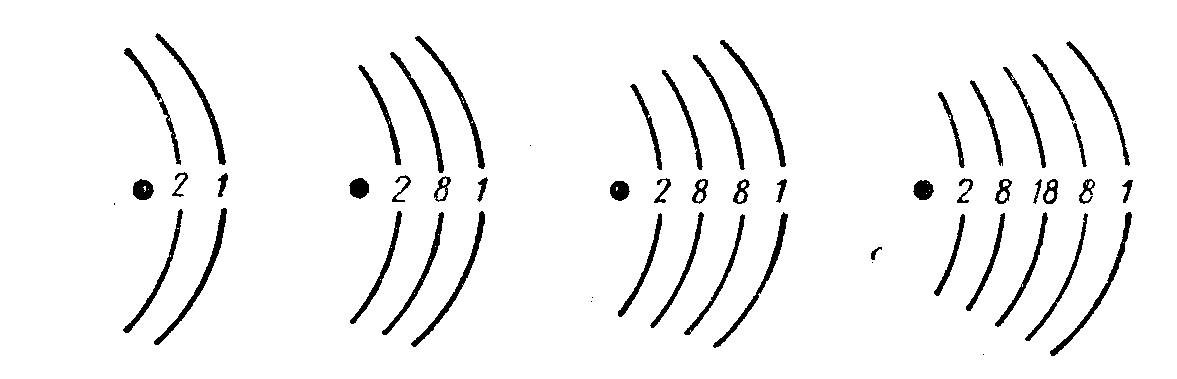
7. Напишите формулы оксидов и гидроксидов элементов, строение атомов которых схематически представлено на рисунке. Назовите эти элементы. Укажите, какой из гидроксидов должен быть наиболее сильным основанием:
Лабораторная работа №9
