
Работа 86
Измерение соотношения cр/cv воздуха изучение адиабатного процесса
Цель работы: Изучение закономерностей изменения параметров газа при адиабатном сжатии и измерение отношения теплоемкостей газа при постоянном давлении и постоянном объёме на основании проведенных измерений.
Приборы
и оборудование:
установка для изучения адиабатного
процесса ,USB-адаптер с кабелем, компьютер
(рис.1).
Рис. 1
Установка для изучения адиабатного процесса представляет собой пластиковый шприц объемом 50 мл (3), соединенный короткой трубкой с датчиком абсолютного давления. Установка содержит толкатель поршня шприца, который приводится в движение в горизонтальном направлении с помощью клина(1), движущегося вертикально. Влияние теплообмена газа со стенками сосуда, поршнем и окружающей средой можно минимизировать, осуществляя сжатие газа максимально быстро. Это достигается при ударе молотком по клину. За счет остановки толкателя в крайнем положении происходит фиксация конечного объема системы.
Давление газа в сосуде постоянно регистрируется на протяжении опыта с помощью датчика давления, подключенного к компьютеру через кабель с переходником(2). В результате процесса температура газа повышается, а затем он остывает, возвращаясь к комнатной температуре. Это проявляется в плавном уменьшении давления после скачкообразного повышения его при сжатии.
Регистрация данных во время сжатия газа производится с высокой скоростью (точки на экране следуют через 0,5 мс). На медленных стадиях процесса программа увеличивает интервал между выводимыми на экран точками до 20 мс.
Клапан (4) предназначен для возвращения поршня в исходное состояние.
Введение
При медленном сжатии газа в сосуде, при котором за время перемещения поршня газ успевает обмениваться энергией с окружающей средой, температура газа в сосуде остается равной температуре внешней среды. Такой процесс будет описываться моделью изотермического процесса, в котором
pV const. (1)
Соотношение (1) называют законом Бойля - Мариотта.
В общем случае термодинамическое состояние газа, характеризуемое термодинамическими параметрами p, V и T, описывается уравнением
p V n const, (2)
где п – произвольное число, как положительное, так и отрицательное, а также равное нулю. Таким образом, любой процесс, уравнение которого можно свести к этому виду, является политропическим. Термодинамические процессы, описываемые таким уравнением это политропические процессы, а соответствующие графики – политропы. Политропическими являются, в частности, процессы изохорический, изобарический, изотермический и адиабатический. На рис. 2 представлены политропы изотермического и адиабатического термодинамических процессов.
Отличительной особенностью всех политропических процессов является то, что в ходе этих процессов теплоемкость газа остается постоянной:
Сп const (3)
Если
п
,
то Сп
0 (это следует и из определения
адиабатического процесса). При п
1, как и должно быть, Сп
→
 при изотермическом процессе.
при изотермическом процессе.
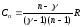 (4)
(4)
Выражение, определяющее п через теплоемкости имеет вид
 (5)
(5)
Предельным случаем сжатия ( или расширения) газа с учетом теплообмена является процесс, в котором вообще нет теплообмена с окружающей средой адиабатический или адиабатный процесс. Соответствующее уравнение (6) называют уравнением адиабаты или уравнением Пуассона.
pV γ = const (6)
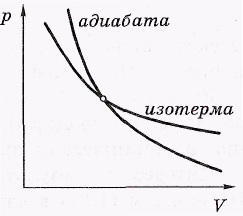
Рис.2
Уравнение (7) связывает значение показателя в уравнении (6) с теплоемкостями газа при постоянном давлении и объеме с числом степеней свободы i. В этом уравнении γ – постоянная адиабатического процесса, равна
=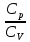 =
= ,(γ
>1) (7)
,(γ
>1) (7)
В данной работе реализуется процесс, в котором газ, заключенный в шприце, быстро сжимается за счет надавливания на поршень при вбивании клина молотком. Быстрые изменения давления регистрируется датчиком давления. На рисунке 3 представлены последовательные состояния воздуха под поршнем, возникающие при перемещении поршня
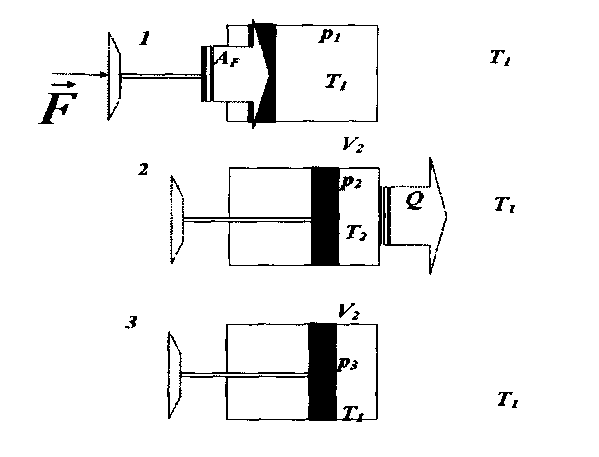
Рис.3
1 – воздух под поршнем не сжат, 2 − воздух под поршнем частично сжат , 3 − воздух под поршнем сжат.
Находящийся в сосуде при комнатной температуре газ сначала сжимается, переводится из состояния 1 в состояние 2, а затем при неизменном объеме остывает до комнатной температуры (переводится из состояния 2 в состояние 3).На рисунке 4 представлено изменение давления газа под поршнем в зависимости от времени.
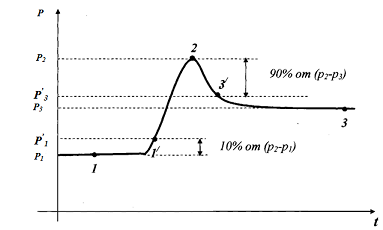
Рис.4
Исходное
давление газа (р1)
и его объем (V1)
связаны с
![]() параметрами,
характеризующими систему по завершении
адиабатического процесса (р2,
V2),
уравнением Пуассона:
параметрами,
характеризующими систему по завершении
адиабатического процесса (р2,
V2),
уравнением Пуассона:
p1V1γ =p2V2γ (8)
Следующее выражение можно использовать для получения значения показателя в уравнении адиабаты, если процесс является адиабатическим:
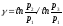 (9)
(9)
