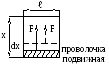II.Поверхностно натяжение.Адсорбция.
До сих пор мы рассматривали тепловые свойства и явления, имевшие объемный характер; в них участвовала вся масса тела. Наличие у тел свободных поверхностей приводит к существованию явлений, называемых поверхностными.
В поверхностных явлениях участвуют лишь молекулы, находящиеся у самой поверхности тел.
Молекулы, расположенные вблизи поверхности (в тонком поверхностном слое), находятся в условиях, отличных от условий внутри тела.
|
|
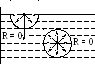
Молекулы внутри тела окружены со всех сторон молекулами жидкости, действие сил с их стороны – R= 0. Радиус действия молекулярных сил r= 10–7см. Молекулы вблизи поверхности имеют одинаковых соседей лишь с одной стороны, R≠ 0. Молекулы как бы втягиваются в жидкость за счет избыточного молекулярного давления, направленного по нормали внутрь жидкости. |
Различное положение молекул приводит к тому, что энергия молекул в поверхностном слое и внутри различна.
Разность между энергией всех молекул вблизи поверхности и той энергией, которой обладали бы эти молекулы внутри жидкости, называется поверхностной энергией U.
∆U=α∆S, (5)
где S– поверхность раздела;
α – коэффициент поверхностного натяжения
Мерой поверхностной энергии служит работа, которую нужно затратить, чтобы создать единицу поверхности жидкости.
Тогда α можно выразить как:
![]() (6)
(6)
Поверхностное натяжение проявляет себя как сила натяжения между молекулами, действующая по поверхности жидкости.
Силы, действующие по поверхности и стремящиеся сократить (сжать) её, называются силами поверхностного натяжения.
Силовое проявление поверхностного натяжения рассмотрим на примере:
|
|
Пленка, сокращаясь, перемещает проволочку на dX. Тогда силаF, действующая на проволочку:
|
Т.к. поверхностей у жидкости 2, имеем:
F= –2αℓ
![]() (8)
(8)
“ – “ показывает, что сила направлена внутрь поверхности пленки.
|
Коэффициент поверхностного натяжения численно равен силе поверхностного натяжения, приходящейся на единицу длины граничной линии на поверхности жидкости. |
Следствие:
Сила Fперпендикулярна границе линии, касательная к поверхности, направлена внутрь её.
Силы действуют так, чтобы привести тело в состояние с наименьшей энергией, поэтому и силы поверхностного натяжения направлены внутрь поверхности, стремясь её сократить, т.е. придать возможное наименьшее значение.
П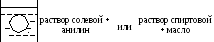 ример:
ример:
Опыт:
Коэффициент поверхностного натяжения зависит от химического состава жидкости и температуры.
Поверхностным натяжением обладают любые свободные поверхности жидкости, а так же и твердого тела.
При растворении твёрдого или жидкого вещества в жидком растворителе силы притяжения между молекулами растворённого вещества и растворителя обычно не равны силам взаимного притяжения между молекулами чистого растворителя.
Рассмотрим случай, когда силы притяжения между молекулами растворённого вещества и растворителя меньше сил притяжения между молекулами растворителя. Такие растворённые вещества называются поверхностно-активными. К ним принадлежит мыло при растворении в воде, ряд жирных кислот и многие другие. Так как молекулы растворённого вещества притягиваются молекулами растворителя слабее, чем молекулы самого растворителя, то из поверхностного слоя внутрь жидкости преимущественно втягиваются молекулы растворителя и в поверхностном слое увеличивается концентрация молекул растворённого вещества, уменьшая тем самым поверхностное натяжение раствора. Равновесие наступает тогда, когда число молекул растворённого вещества, втягиваемых из поверхностного слоя вглубь жидкости, будет равняться числу молекул, приходящих вследствие диффузии из глубинных слоёв на поверхность. Поверхностный слой оказывается обеднённый молекулами растворителя и обогащённым молекулами растворённого вещества. Это явление носит названиеадсорбиции, им объясняется устойчивость жидких плёнок, пены и т.д.
Плёнка из чистой жидкости неустойчива при действии постоянной силы:
а) либо сжимается, если приложенная сила меньше сил поверхностного натяжения
б) либо растягивается, если приложенная сила больше сил поверхностного натяжения.
При растворении поверхностно-активного вещества, например мыла, его молекулы концентрируются в поверхностном слое растворителя, понижая поверхностное натяжение. При растяжении такой плёнки её поверхность увеличивается и часть растворённого вещества из остального объёма жидкости переходит на новую поверхность. Этот процесс вызывает уменьшение концентрации растворённого вещества на остальной поверхности плёнки, т.е. увеличение её поверхностного натяжения. Чем сильнее растягивается плёнка, тем больше становится поверхностное натяжение.
При сокращении плёнки имеет место противоположный процесс. Таким образом, плёнка раствора поверхностно-активного вещества ведёт себя подобно упругой плёнке, она является устойчивой. Аналогично объясняется устойчивость пены.
При растворении таких веществ, как кислоты и соли, происходит диссоциация молекул – распадение их на ионы.
Процесс адсорбиции– это электрический процесс, поэтому ионы особенно активно участвуют в нём.
Можно подобрать такое адсорбирующее твёрдое вещество, которое будет интенсивно поглощать из раствора ионы определённого знака, выделяя в раствор другие ионы. Такой процесс называется ионным обменом.
Например, некоторые вещества адсорбируют из раствора ионы металлов, заряженные положительно, выделяя вместо них ионы водорода. Такие адсорбирующие вещества или адсорбенты называются катионитами.
Другие адсорбенты собирают отрицательные ионы кислотных остатков, заменяя их гидроксильными ионами ОН. Такие адсорбенты называются анионитами.
В большинстве случаев используются адсорбенты типа смол, называемые ионнообменными смолами. Процесс ионного обмена получил большое практическое применение для очистки воды. В обычной воде всегда содержатся ионы различных растворённых солей, кислот и щелочей. Пропуская воду через две так называемые ионнообменные колонны, содержащие одна катионит, а другая – анионит, можно очень хорошо очистить воду от ионов, что заменяет процесс дистилляции.
Адсорбция на поверхности твёрдых тел может протекать весьма интенсивно, особенно в случае значительной поверхности твёрдого тела. Особенно большой поверхностью обладает измельчённый уголь, хорошо адсорбирующий различные вещества, например вредные газы. В угольном противогазе путём обработки (активации) угля соответствующими веществами его адсорбирующая способность может быть ещё повышена. Один грамм такого угля имеет поверхность до 1000 м2и может поглотить несколько десятых грамма вредных газов.
Адсорбция зависит:
а) от температуры;
б) давления;
в) взаимодействия молекул адсорбента и адсорбирующего вещества (адсорбата);
г) от взаимодействия молекул адсорбируемого вещества между собой.
При адсорбции могут образоваться не только мономолекулярные слои. При определённых условиях (при смачивании поверхности твёрдого тела) с повышением давления адсорбируется несколько слоёв молекул и количество адсорбированного вещества резко возрастает.
Процесс адсорбиции сопровождается выделением теплоты адсорбиции. По величине последняя близка к теплоте конденсации, если процесс адсорбции не сопровождается химическими реакциями. В последнем случае выделяющееся тепло может быть на порядок больше.