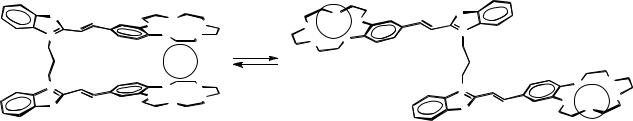Методичка_Громов
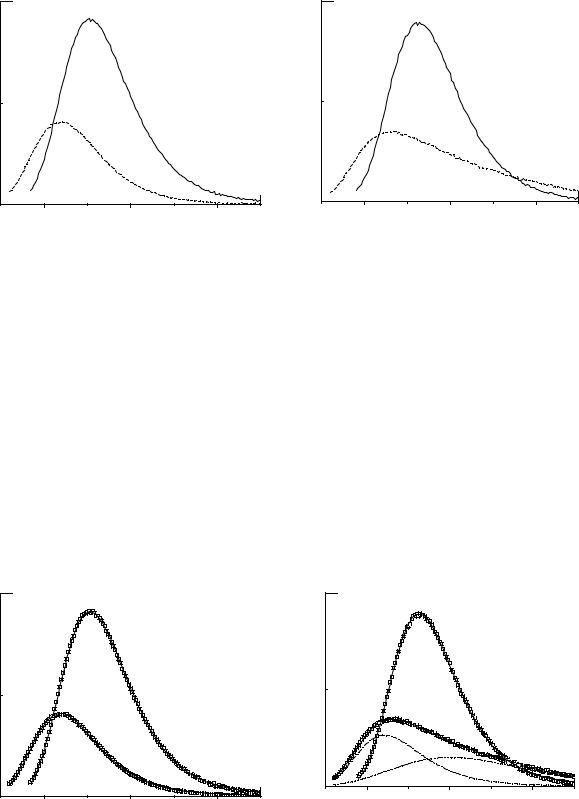
.pdfОтличительной особенностью спектрофлуориметрии является то, что регистрируемая спектральная зависимость является функцией двух переменных – длины волны возбуждения
λex и длины волны испускания λem. Если λex фиксирована, а λem сканируется, то измеряется спектр флуоресценции I(λem). Если сканируется λex при постоянной λem, то получается спектр возбуждения флуоресценции I(λex), который называют также спектром действия флуоресценции.
Как уже говорилось, флуоресценция обычно происходит из нулевого колебательного уровня нижнего возбужденного состояния S1. Поэтому спектр возбуждения флуоресценции, как правило, совпадает со спектром поглощения. Прежде чем измерить спектр флуоресценции вещества, следует вначале получить истинный спектр возбуждения флуоресценции и сравнить его со спектром поглощения. Соответствие этих спектров будет означать, что флуоресцирует исследуемое вещество, а не примеси. Флуориметры, не способные измерять спектры возбуждения, малопригодны для научных исследований.
Чувствительность фотоприемников зависит от длины волны света. Поэтому для получения истинного спектра флуоресценции измеренные зависимости интенсивности от длины волны должны быть исправлены с учетом спектральной чувствительности фотоприемника. Существуют разные способы калибровки фотоприемников, например, можно использовать известные истинные спектры флуоресценции стандартных веществ. Спектры, полученные на разных приборах, можно сопоставлять только в том случае, если вы уверены, что они исправлены с учетом спектральной чувствительности аппаратуры.
Интенсивность возбуждающего света также зависит от длины волны. Для получения истинного спектра возбуждения флуоресценции прибор должен иметь канал сравнения, в который помещают вещество, играющее роль счетчика фотонов.
Эффект внутреннего фильтра. Если оптическая плотность исследуемого образца мала (< 0.1), то интенсивность флуоресценции примерно одинакова в любой точке вдоль пути возбуждающего света через образец. Это оптимальные условия для измерения. При увеличении оптической плотности раствора интенсивность флуоресценции, регистрируемой под прямым углом, вначале растет, затем ее рост замедляется и, наконец, падает, поскольку флуоресцирует только очень тонкий слой вблизи передней стенки кюветы. Это явление называют эффектом внутреннего фильтра.
Вторичное поглощение. Еще один эффект, который может приводить к ошибкам измерения флуоресценции – вторичное поглощение (реабсорбция). Эффект реабсорбции возникает, если спектры поглощения и флуоресценции перекрываются и оптическая плотность образца в области перекрывания значительна. Реабсорбция приводит не только к
191
ошибкам измерения интенсивности флуоресценции, но и к искажению формы спектра флуоресценции. В результате нарушается зеркальная симметрия спектров поглощения и флуоресценции. Искажения становятся тем больше, чем больше оптическая плотность образца в области перекрывания спектров. Если оптическая плотность образца в области перекрывания не превышает 0.05, то эффектом реабсорбции можно пренебречь.
Современные методы обработки спектроскопических данных
Супрамолекулярная химия – это химия сравнительно слабых нековалентных взаимодействий. Супрамолекулярные системы часто представляют собой равновесную смесь реагентов и продуктов. Поэтому важной задачей является определение числа компонентов в исследуемой системе. Эту задачу можно решить, используя современные методы глобального анализа спектроскопических данных, например, абстрактный факторный анализ. Методы глобального анализа, такие как параметрическое моделирование спектров, незаменимы в тех случаях, когда нужно определить неизвестные спектры отдельных компонентов реакционной смеси.
Абстрактный факторный анализ
Этот метод применяется для определения числа линейно независимых компонентов в системе. Рассмотрим его в применении к электронным спектрам поглощения.
Допустим, что спектры поглощения реакционной системы изменяются в зависимости от определенного фактора, например, от концентрации реагентов. Спектры, измеренные при разных концентрациях реагентов в фиксированном спектральном диапазоне с одинаковым шагом, можно представить в виде матрицы данных Dexp размерности n × m, где n – число значений оптической плотности в спектре, m – число измеренных спектров.
Чтобы определить число поглощающих свет компонентов в системе, матрицу Dexp подвергают разложению по сингулярным числам и сингулярным векторам. Такое разложение удобно проводить с помощью программы Matlab (версия 6 или 7, MathWorks), встроенные функции которой позволяют легко оперировать с матрицами данных. Например, операция сингулярного разложения матрицы данных Dexp размерности n × m выполняется с помощью функции ‘svd’, генерирующей три матрицы
[V,S,U] = svd(Dexp),
где V – матрица размерности n × n с искомыми векторами сингулярного разложения в порядке убывания значимости, S – матрица размерности n × m с неотрицательными
192

диагональными элементами в порядке убывания (сингулярными значениями), U – унитарная матрица размерности m × m такая, что
Dexp = V×S×U',
где U' – транспонированная матрица U.
Сингулярные векторы обладают замечательным свойством – если реакционная система содержит k поглощающих свет компонентов, то спектры поглощения этой системы, измеренные при разных концентрациях реагентов, можно представить в виде линейной комбинации первых k векторов сингулярного разложения матрицы данных Dexp. Остальные векторы описывают погрешности измерения спектров.
Наилучшая аппроксимация матрицы данных Dexp с помощью первых k векторов сингулярного разложения находится по формуле
Dsvd = V(1:n,1:k)×S(1:k,1:m)×U',
где V(1:n,1:k) – матрица, составленная из первых k столбцов матрицы V, а S(1:k,1:m) – матрица, составленная из первых k строк матрицы S.
Погрешность, с которой теоретическая матрица Dsvd воспроизводит матрицу данных Dexp, определяется среднеквадратичным отклонением
|
|
n m |
|
|
|
åå(Dexpij − Dsvdij )2 |
|
σsvd |
(k) = |
i=1 j=1 |
|
(n − k)m |
|||
|
|
Количество поглощающих свет компонентов в системе определяется по минимальному значению k, при котором величина стандартного отклонения σsvd снижается до уровня инструментальной погрешности измерения спектров.
Если речь идет о спектрофотометрических данных, то инструментальная погрешность обычно очень мала: ~ 10–4 ед. оптической плотности.
Реализация абстрактного факторного анализа в программе Matlab
%Загружаем матрицу экспериментальных спектров, находящуюся,
%например, в файле “spectra.dat”
load spectra.dat -ascii; [a,b]=size(spectra);
% Берем из файла “spectra.dat” столбец со значениями длины волны
%и столбцы со значениями оптической плотности
Wavelength=spectra(1:a,1:1); Dexp=spectra(1:a,2:b); [n,m]=size(Dexp);
%Выводим спектры на экран
plot(Wavelength, Dexp);
% Производим сингулярное разложение
193
[V,S,U]=svd(Dexp);
%Находим теоретическую матрицу спектров Dcal, воспроизводящую
%матрицу Dexp с помощью первых k векторов сингулярного разложения
%(k = 1–5), а также стандартное отклонение между Dexp и Dcal
for i=1:5; Dcal=V(:,1:i)*S(1:i,:)*U'; Standard_Deviation(i)=(sum(sum((Dcal-Dexp).^2))/(n-i)/m)^0.5; end;
% Выводим на экран стандартное отклонение
Standard_Deviation
Параметрическое моделирование спектров
Метод параметрического моделирования спектров (ПМC) незаменим при количественном исследовании сложных многокомпонентных систем, в частности, супрамолекулярных систем. Допустим, что для данной системы мы измерили спектры поглощения в зависимости от определенных факторов, например, от концентрации реагентов. Параметрическое моделирование экспериментальных спектров производится на основе предполагаемой реакционной модели. Метод ПМС дает возможность проверить справедливость модели и, если она верна, определить неизвестные спектры отдельных компонентов системы, а также количественные характеристики реакций. Рассмотрим этот метод в применении к данным спектрофотометрического титрования (СФТ) для системы лиганд/катион металла.
Обычно данные СФТ представляют собой набор спектров поглощения, измеренных при постоянной общей концентрации лиганда (CL) и переменной общей концентрации катиона металла (CM).
Экспериментальные спектры поглощения представляются в виде матрицы Dexp, которая может включать данные сразу нескольких экспериментов, проведенных при разной величине CL в кюветах разной длины l. Допустим, что для исследуемой системы применима реакционная модель, включающая две равновесные реакции:
K
L + M ¾¾¾1® LM ¬¾¾
K
LM + M ¾¾¾2 ® LM
¬¾¾ 2
где L – молекула лиганда, M – катион металла, K1 и K2 – константы равновесия. Допустим, что поглощающими свет компонентами в данной системе являются только L, LM и LM2. Используя закон действующих масс и принцип материального баланса, составляем систему уравнений:
194
[LM] = K1 [L] [M]
[LM2] = K2 [LM] [M]
CL = [L] + [LM] + [LM2]
CM = [M] + [LM] + 2 [LM2]
Процесс ПМС начинается с постулирования значений констант равновесия K1 и K2 и решения вышеуказанной системы уравнений, которая легко сводится к уравнению третьей степени для [L],
K1(4K2 – K1)[L]3 + K1(K1CL – K1CM – 8K2CL + 4K2CM)[L]2 + (4K1K2CL2 – 4K1K2CLCM + K1K2CM2 +
K1CM + 1)[L] – CL=0.
Это уравнение имеет аналитическое решение. Правильный корень кубического уравнения выбирается, исходя из физических ограничений для концентраций компонентов. В более сложных случаях концентрации компонентов можно рассчитать численным методом.
Найденные величины концентраций [L], [LM] и [LM2] умножаются на соответствующее значение длины кюветы l и составляется матрица "концентраций" C
размерности 3 × m, первую строку которой составляют значения [L]l, вторую – значения [LM]l, и третью – значения [LM2]l.
Затем путем решения матричного выражения закона поглощения света
D = E×C
генерируется теоретическая матрица коэффициентов молярного поглощения компонентов Ecal размерности n × 3
Ecal = Dexp×C'×(C×C')–1,
где C' – транспонированная матрица C. Теоретическая матрица Dcal, воспроизводящая матрицу Dexp, вычисляется по формуле
Dcal = Ecal×C.
Константы равновесия K1 и K2, а также коэффициенты молярного поглощения всех трех поглощающих свет компонентов, то есть L, LM и LM2, находятся путем минимизации стандартного отклонения σD(K1,K2) между теоретической матрицей Dcal и матрицей экспериментальных данных Dexp. Выражение для σD аналогично выражению для погрешности σsvd. Величина σD является критерием справедливости реакционной модели. Помимо инструментальных погрешностей она включает погрешности, связанные со случайными и систематическими ошибками измерения концентраций реагентов, и, следовательно, зависит не только от точности оборудования, но и от методики эксперимента.
Обычно, величина σD не должна превышать 0.002 ед. оптич. плотности.
195
Метод ПМС очень легко реализуется с помощью программы Matlab
Примеры применения электронной спектроскопии для исследования свойств супрамолекулярных систем
Комплексообразование молекулярного пинцета с ионами металлов
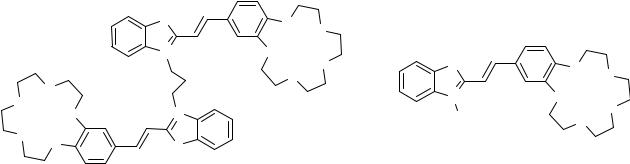
С помощью спектрофотометрии и спектрофлуориметрии в сочетании с методами глобального анализа спектроскопических данных мы изучили комплексообразование краунсодержащего бисстрилового красителя БК и его моностирилового аналога МК с ионами Ca2+ и Ba2+ в ацетонитриле. Предполагалось, что два краун-эфирных фрагмента бисстирилового красителя будут кооперативно захватывать большие ионы металлов типа Ba2+. Такие молекулы называют молекулярными пинцетами.
|
S |
O |
O |
|
|
|
|
|
|
|
|
|
|
|
N+ |
O |
O |
S |
O |
|
|
|
O |
O |
|||
|
O |
|
|
|
||
|
|
|
N+ |
O |
|
|
O |
|
N+ |
|
O |
||
O |
|
ClO – C2H5 |
|
|||
|
|
O |
||||
O |
|
2ClO4– |
|
4 |
|
|
O |
|
|
|
|
||
|
S |
|
|
МК |
|
|
|
|
|
|
|
|
БК
На рисунке показаны спектры поглощения молекулярного пинцета БК при разных концентрациях иона Ba2+. Наличие изобестической точки в спектрах указывает на то, что в данной системе присутствуют только два поглощающих свет компонента, т.е. свободный краситель и комплекс красителя с ионом Ba2+. Факторный анализ спектров подтвердил это предположение.
Методом ПМС было установлено, что спектральные изменения, наблюдаемые для этой системы, описываются одной равновесной реакцией:
K
L + M ¾¾¾1® LM ¬¾¾ ,
где L – молекула лиганда, M – катион металла, K1 – константы равновесия.
196

0.8 |
|
|
|
|
|
|
0 |
|
|
|
CM/CL |
D |
|
|
|
|
|
|
10 |
0.4 |
|
|
|
0.0 |
|
|
λ / нм |
350 |
400 |
450 |
|
Спектры поглощения бискраун-эфира БК (2.0×10−6 М, кювета 5.5 см) в MeCN/0.01 M |
|||
Et4NClO4 при разных концентрациях Ba2+. |
|||
Таким образом, эксперимент показал, что в данной системе образуется единственный комплекс состава 1:1. Этому комплексу приписана структура типа внутримолекулярный сэндвич.
|
S |
|
|
O |
O |
|
S |
|
O |
|
|
|
|
|
|
|
O |
O |
|||
|
|
|
|
|
|
|
|
|
||
|
N |
+ |
O |
|
O |
Ba2+ |
N+ |
O |
|
O |
|
|
O |
Ba2+ |
|
||||||
|
O |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
O |
O |
N+ |
|
|
|
|
N+ |
O |
|
O |
|
|
|
|
|
|
O |
O |
O |
||
|
|
|
|
|
|
|
S |
|||
O |
|
|
|
|
|
|
|
|
||
O |
S |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
БК |
|
|
|
|
|
БК ·Ba2+ |
|
|
|
Образование комплекса типа внутримолекулярный сэндвич между красителем БК и катионом Ba2+.
Комплексообразование с ионом Сa2+
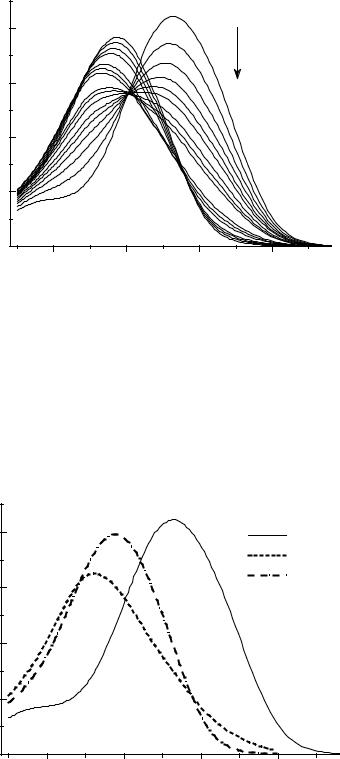
Более сложная спектральная картина наблюдается при комплексообразовании молекулярного пинцета БК с ионами Ca2+. Ясно, что в данной системе присутствует более двух поглощающих свет компонентов. Факторный анализ спектров показал, что система включает три поглощающих свет компонента. С учетом структуры красителя наиболее вероятной реакционной моделью для этой системы является следующая:
197
|
|
K1 |
|
|
|
|
|
¾¾¾® |
LM |
|
|
|
L + M ¬¾¾ |
|
|
||
|
|
K2 |
|
|
|
|
|
¾¾¾® |
LM2 |
|
|
|
LM + M ¬¾¾ |
|
|||
D |
|
|
|
0 |
|
0.8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CM/CL |
|
0.6 |
|
|
|
400 |
|
|
|
|
|
|
|
0.4 |
|
|
|
|
|
0.2 |
|
|
|
|
|
0.0 |
|
|
|
|
нм |
350 |
400 |
450 |
500 |
||
Спектры поглощения бискраун-эфира БК (2.0´10−6 М, кювета 5.5 см) в MeCN/0.01 M Et4NClO4 при разных концентрациях Ba2+.
Обработка спектров поглощения методом ПМС для системы БК/Ca2+ показала, что указанные две равновесные реакции адекватно описывают наблюдаемые спектральные изменения. На рисунке ниже пунктирными линиями показаны рассчитанные спектры поглощения комплексов состава 1:1, т.е. БК · Ca2+, и 1:2, т.е. БК · (Ca2+)2.
D |
|
|
|
|
0.8 |
|
|
|
L |
|
|
|
|
LM |
0.6 |
|
|
|
LM2 |
|
|
|
|
|
0.4 |
|
|
|
|
0.2 |
|
|
|
|
0.0 |
|
|
|
нм |
350 |
400 |
450 |
500 |
|
Спектры поглощения красителя БК и чистых комплексов БК · Ca2+ и БК · (Ca2+)2. |
||||
198