
1. Введение
В последней главе рассматривались некоторые особые случаи, для которых количественные термодинамические данные можно получить из диаграмм состояния. Цель настоящей главы — исследовать равновесие сосуществующих фаз с более общей точки зрения. Такие исследования не дают количественных результатов, но часто позволяют делать важные полуколичественные выводы.
Сначала исследуем общую форму кривой свободная энергия—состав для обычного раствора вблизи любого конца бинарной системы. Свободная энергия смешения при каком-либо данном составе будет выражена уравнением

если не важен ближний порядок. Дифференцируя ΔGсм по Хв
при постоянных температуре и давлении, находим
 (10.2)
(10.2)
Рассматривая
разбавленный раствор компонентов В
в
А, можно сказать, что![]() и
и![]() равны
нулю и (1—
Хв)~1.
Таким
образом,
равны
нулю и (1—
Хв)~1.
Таким
образом,
 (10.3)
(10.3)
В
уравнении (10.3)![]() и
и![]() не
будут зависеть от состава в области
разбавленного раствора, а следовательно,
значение
не
будут зависеть от состава в области
разбавленного раствора, а следовательно,
значение![]() будет
зависеть от состава только благодаря
второму члену в правой части уравнения
при любом знаке у величии
будет
зависеть от состава только благодаря
второму члену в правой части уравнения
при любом знаке у величии![]() и
и![]() .
Отношение
.
Отношение![]() будет
всегда отрицательной величиной при
достаточно малых значениях
будет
всегда отрицательной величиной при
достаточно малых значениях
![]() поскольку
поскольку![]() ,
когда
,
когда![]()
Таким образом, растворение вещества в кристалле всегда приводит к уменьшению свободной энергии системы, следовательно, чистая фаза всегда термодинамически неустойчива.
=======================================
Этот вывод имеет важное значение для процесса изготовления сверхчистых материалов, поскольку из него следует, что чистый материал будет всегда стремиться к загрязнению за счет поглощения примесей из окружающей среды. Таким образом, если чистый материал находится в тигле, материал тигля будет иметь тенденцию растворяться в чистом материале (по крайней мере в ограниченной степени).
2. Зависимость свободная энергия — состав для случая, когда а и в имеют одинаковую кристаллическую структуру
Теоретически возможно образование компонентами А и В непрерывного ряда твердых растворов, если оба эти компонента имеют одинаковую кристаллическую структуру. Если же А и В имеют различные структуры, непрерывный ряд твердых растворов невозможен.
Известно,
что![]()
при
данной температуре. Если ΔHсм
отрицательная,![]() как
как
функция![]() будет
отрицательной при всех составах, так
как
будет
отрицательной при всех составах, так
как
![]() всегда
отрицательно (рис. 58, а), но если
всегда
отрицательно (рис. 58, а), но если![]() положительна,
положение осложняется. Форма кривой
свободная энергия—состав может сильно
изменяться с температурой. При высоких
температурах выражение
положительна,
положение осложняется. Форма кривой
свободная энергия—состав может сильно
изменяться с температурой. При высоких
температурах выражение![]() будет
иметь большее значение, чем при низких,
следовательно, возможно, что при высоких
температурах кривая
будет
иметь большее значение, чем при низких,
следовательно, возможно, что при высоких
температурах кривая![]() будет вогнута вниз при всех составах,
как показано на рис. 58, а. Однако с
понижением температуры член
будет вогнута вниз при всех составах,
как показано на рис. 58, а. Однако с
понижением температуры член![]() начнет
преобладать в выражении свободной
энергии, а кривая
начнет
преобладать в выражении свободной
энергии, а кривая![]() будет
стремиться стать положительной.
будет
стремиться стать положительной.
Как
обсуждалось ранее, вблизи концов бинарной
системы
![]() будет
всегда отрицательной, так что полностью
кривая будет иметь вид, как на рис. 58, б.
Если
раствор регулярный, минимумы
симметричны относительно
будет
всегда отрицательной, так что полностью
кривая будет иметь вид, как на рис. 58, б.
Если
раствор регулярный, минимумы
симметричны относительно![]() и
связаны с тем же значением
и
связаны с тем же значением![]()
Для
сплава состава а
величина![]() будет
отрицательной
будет
отрицательной
и
равной![]() .
Поэтому этот раствор устойчив по
отношению
.
Поэтому этот раствор устойчив по
отношению
к
чистым А и В. То же справедливо и для
сплава с.
Теперь
рассмотрим сплав х.
Он
может иметь отрицательное значение![]()
но
мы должны поставить под вопрос возможность
снижения
![]() за
счет распада раствора. Предположим, что
он распадается
на два раствора, составы которых due
соответственно.
Тогда свободная
энергия системы будет выражаться суммой
произведений свободной энергии
раствора состава d,
равной
величине В, умноженной на количество
этого состава, и свободной энергии
раствора состава е,
равной
величине С, умноженной на количество
раствора состава е.
Долю
раствора состава d
получаем
по
за
счет распада раствора. Предположим, что
он распадается
на два раствора, составы которых due
соответственно.
Тогда свободная
энергия системы будет выражаться суммой
произведений свободной энергии
раствора состава d,
равной
величине В, умноженной на количество
этого состава, и свободной энергии
раствора состава е,
равной
величине С, умноженной на количество
раствора состава е.
Долю
раствора состава d
получаем
по

правилу
рычага; она равна
![]() .
Подобным образом
.
Подобным образом
доля
раствора состава е
равна
![]() .
Таким образом,
.
Таким образом,
значение![]() всей
системы равно
всей
системы равно
![]()
Значение
D
меньше
А—исходного
значения![]() до
распада;
до
распада;
но![]() будет
еще более снижаться при обогащении
раствора
будет
еще более снижаться при обогащении
раствора
состава
d
компонентом
А,
и
раствора состава е
—
компонентом В.
Самым
низким устойчивым значением![]() ,
которое можно
,
которое можно
достичь за счет распада, является величина (J при составах соответственно у и г. Эти растворы находятся в равновесии друг с другом, поскольку компонент В будет иметь одинаковый химический потенциал в обеих растворах.
Следует
отметить, что составы у
и
z
не
обязательно связаны с минимумами
кривой![]() ;
свободные энергии Е
и
F
могут
;
свободные энергии Е
и
F
могут
в
значительной степени отличаться от
минимальных значений, поскольку важным
критерием равновесия является одинаковый
химический потенциал данного компонента
в обеих фазах, а не минимальное значение
свободной энергии каждой фазы. Очевидно,
этот критерий нельзя удовлетворить,
проведя касательные при минимальных
значениях кривой![]() ,
если только они случайно не совпадут
при одинаковых значениях
,
если только они случайно не совпадут
при одинаковых значениях![]()
Таким образом, растворы слева и справа соответственно от у и z устойчивые, а растворы состава между у и Z неустойчивые и будут распадаться на две сосуществующие фазы.
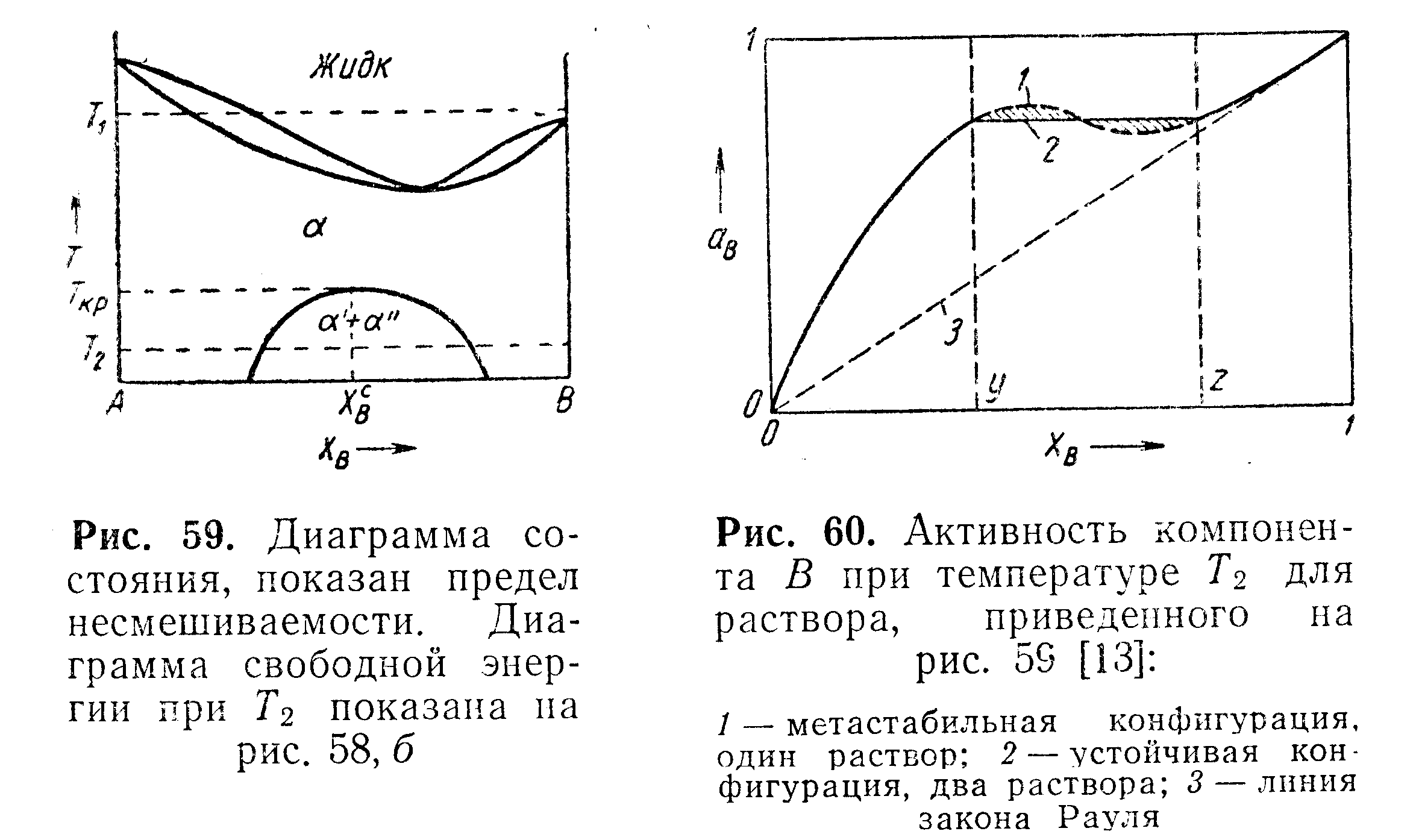
Рассмотренная кривая свободной энергии связана с пределом несмешиваемости на диаграмме состояния. При более высоких температурах минимумы приближаются друг к другу по составу и, наконец, полностью исчезают при критической температуре
![]() ,
Тип
диаграммы состояния, относящийся к рис.
58, б,
показан
на рис. 59. При температуре
,
Тип
диаграммы состояния, относящийся к рис.
58, б,
показан
на рис. 59. При температуре![]() диаграмма
свободная энергия — состав была бы
сходной с представленной на рис. 58, б.
На рис.
58, б
можно
видеть, что между у
и
г
существуют
две точки перегиба,
называемого спинодами,
играющие
важную роль в кинетике разложения фаз.
диаграмма
свободная энергия — состав была бы
сходной с представленной на рис. 58, б.
На рис.
58, б
можно
видеть, что между у
и
г
существуют
две точки перегиба,
называемого спинодами,
играющие
важную роль в кинетике разложения фаз.
Рассмотрим
теперь активность компонентов A
и В, характерную для типа кривой,
показанной на рис. 58, б.
Беря
в качестве примера компонент В,
находим![]() для
любого состава, экстраполируя наклон
кривой при определенном составе до
для
любого состава, экстраполируя наклон
кривой при определенном составе до![]() .
Значение ав
можно
легко получить, поскольку
.
Значение ав
можно
легко получить, поскольку
![]()
Кривая![]() ,
полученная из рис. 58, показана на рис.
60.
,
полученная из рис. 58, показана на рис.
60.
При
составах у
и
г
компонент
В
будет
иметь одинаковую активность в
соответствии с требованием равновесия.
Максимум и минимум ав
соответствуют
спинодным точкам диаграммы![]()
![]() .
Как
можно видеть, площади
заштрихованных частей равны'.
.
Как
можно видеть, площади
заштрихованных частей равны'.
