
Лекция 4.
Сополимеризация.
Сополимеризацией называется процесс совместной полимеризации двух или нескольких мономеров с образованием макромолекул, содержащих в основной цепи звенья различных исходных мономеров. Соответствующим подбором исходных мономеров полимерным материалам придаются определённые физико-механические свойства. Соотношение компонентов в составе сополимера зависит от реакционной способности мономеров и радикалов.
Сополимеризация может протекать по ионному и радикальному механизму. При простейшем случае радикальной сополимеризации двух мономеров М1 и М2 возможно протекание четырёх элементарных реакций роста цепи:
Реакция роста Скорость реакции роста
~R1· + M1 → ~R1· k11[R1·][M1]
~R1· + M2 → ~R2· k12[R1·][M2]
~R2· + M1 → ~R1· k21[R2·][M1]
~R2· + M2 → ~R2· k22[R2·][M2]
где Mi – мономер i-го типа; ~Ri· -макрорадикал, оканчивающийся звеном Mi; kij – константа скорости присоединения Mi мономера к ~Ri· радикалу.
Кинетическая обработка приведённой реакционной схемы в квазистационарном приближении позволяет установить связь между составом сополимеров и составом исходной смеси мономеров. В квазистационарном состоянии концентрации радикалов ~R1· и ~R2· постоянны, т.е. скорости перекрёстного роста цепи равны между собой:
k12[R1·][M2] = k21[R2·][M1] (1)
Скорости превращения мономеров при сополимеризации описываются уравнениями
d[M1]/dt = k11[R1·][M1] + k21[R2·][M1]
d[M2]/dt = k22[R2·][M2] + k12[R1·][M2]
Для отношения скоростей этих реакций получим:
d[M1] k11[R1·][M1] + k21[R2·][M1]
—— = ———————————
d[M2] k22[R2·][M2] + k12[R1·][M2]
Исключая из этого уравнения стационарные концентрации радикалов [r1·] и [r2·] с помощью условия квазистационарности (1), получим выражение
d[M1] [M1](r1[M1] + [M2])
—— = ————————
d[M2] [M2](r2[M2] + [M1])
где r1 = k11/k12 и r2 = k22/k21 – так называемые константы сополимеризации. Величины r1 и r2 представляют собой отношения констант скоростей присоединения к данному радикалу «своего» и «чужого» мономеров. Значения r1 и r2 зависят от химической природы реагирующих мономеров. На начальных стадиях превращения, когда без большой ошибки можно положить концентрации мономеров [M1] и [M2] постоянными, состав сополимера будет определяться уравнением
[m1] [M1] r1[M1] + [M2]
—— = —— · —————— (2)
[m2] [M2] r2[M2] + [M1]
Где [m1] и [m2] – концентрации мономерных звеньев в макромолекуле.
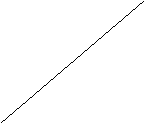
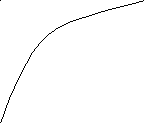
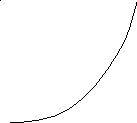
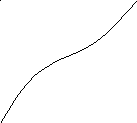
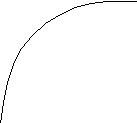
Зависимость состава сополимеров от состава смеси мономеров удобно характеризовать диаграммой состав мономерной смеси – состав сополимера (рис. 1). Форма получаемых кривых зависит от значений r1 и r2. При этом возможны следующие случаи: 1) r1=r2=1, т.е. для всех соотношений концентраций мономеров в реакционной смеси состав сополимера равен составу исходной смеси; 2) r1 > 1, r2 < 1, т.е. для всех соотношений концентраций мономеров в реакционной смеси сополимер обогащён звеньями М1; 3) r1 < 1, r2 > 1, т.е. для всех исходных соотношений концентраций мономеров сополимер обогащён звеньями М2; 4) r1 < 1 и r2 < 1, т.е. при малых содержаниях М1 в исходной смеси мономеров сополимер обогащён звеньями М1, а при большом – звеньями М2. Случай r1 > 1 и r2 > 1, которому должна соответствовать тенденция к раздельной полимеризации мономеров в смеси, на практике не реализуется.
[m2], мол. доли [st] в сополимере, мол. доли








3
1 1
2
4 2
3

 [M2],
мол. доли [St]
в смеси мон., мол. доли
[M2],
мол. доли [St]
в смеси мон., мол. доли
Рис.1. Зависимость состава сополимера Рис. 2. Зависимость состава сополимера
от состава смеси мономеров М1 и М2. от состава смеси стирол-метилметакрилат.
1) r1=r2=1; 2) r1>1, r2<1; 1) SnCl4 (r1 = 10, r2 = 0,1; 2) пероксид
3) r1<1, r2>1; 4) r1<1, r2>1. бензоила (r1 = 0,52, r2 = 0,46); 3) Na
(r1 = 0,1, r2 = 6)
Произведение r1·r2 определяет склонность звеньев к чередованию. При r1·r2 = 1 звенья обоих типов присоединяются к полимерной цепи по закону случая. При r1·r2 < 1 вероятность чередования звеньев увеличивается. В пределе, когда r1·r2 = 0, можно получить регулярно чередующийся сополимер.
При радикальной сополимеризации значения констант сополимеризации определяются практически целиком реакционной способностью мономеров и не зависят от типа инициирующей системы. При ионной сополимеризации сильное влияние на константы r1 и r2 оказывают тип каталитической системы и полярность среды. Эти особенности обусловлены неодинаковым изменением реакционной способности каждого из сомономеров при замене одного активного центра другим.
Различие между ионной и радикальной сополимеризацией наиболее заметно проявляется в составе сополимеров, образующихся из одних и тех же мономеров, например, стирола и метилметакрилата, способных сополимеризоваться по трём различным механизмам (рис. 2). Различный ход кривых объясняется тем, что одни и те же структурные особенности по-разному отражаются на способности мономерной молекулы присоединяться к свободному радикалу, аниону или катиону. Так как фенильная группа притягивает электроны слабее, чем группа –СООСН3, электронная плотность у двойной связи винильной группы стирола больше, чем у метилметакрилата. По той же причине при радикальной сополимеризации (инициировании пероксидом бензоила) электронная плотность на активном конце растущей цепи выше, если там находится стирольный остаток, а не звено метилметакрилата. В связи с тем, что частицы с повышенной электронной плотностью стремятся прежде всего реагировать с такими, у которых электронная плотность меньше, радикал со стирольным концевым звеном будет предпочтительно присоединять метилметакрилат, а радикал с остатком метилметакрилата на конце цепи – стирол. Следовательно, в макромолекуле сополимера будет соблюдаться более или менее правильное чередование стирольных и метилметакрилатных звеньев, что находится в соответствии со значениями r1 = 0,52 и r2 = 0,46 (r1 < 1, r2 < 1).
Кроме того, скорости присоединения каждого мономера к тому или другому растущему радикалу хотя и не одинаковы, но всё же близки друг к другу. Это значит, что оба мономера расходуются почти с одной и той же скоростью, а состав сополимера мало отличается от состава мономерной смеси.
При катионной сополимеризации с хлоридом олова в качестве катализатора растущий катион, будучи заряженным положительно, всё время предпочтительно реагирует со стиролом, обладающим повышенной электронной плотностью, и содержание стирольных остатков в сополимере составит почти 100% (r1 = 10, r2 = 0,1); только при резком увеличении количества метилметакрилата в мономерной смеси эта тенденция к присоединению одного стирола ослабляется вследствие возрастания вероятности столкновения растущего иона с молекулами метилметакрилата, в результате чего сополимер обогащается остатками этого мономера.
При анионной сополимеризации с металлическим натрием в качестве катализатора, наоборот, будет реагировать почти исключительно метилметакрилат (r1 = 0,1, r2 = 6) , так как сравнительно низкая электронная плотность у двойной связи его молекул благоприятствует присоединению к аниону.
Таким образом, при анионной полимеризации более активным мономером является метилметакрилат, а при катионной – стирол, при радикальной полимеризации эти активности почти одинаковы.
