
- •1. Определение гидросферы
- •3. Температура максимальной плотности пресной воды.
- •4. Диаграмма агрегатных состояний.
- •5. Изменение температуры плавления льда при повышении давления
- •6. Число Рейнольдса
- •7. Гидрологический режим
- •8. Гидрология как наука (схема)
- •9. Изотопный состав воды.
- •11.График Хелланд-Хансена
- •12. Изменение температуры максимальной плотности при уменьшении солёности
- •14. Закон сохранения тепловой энергии и уравнение теплового баланса
- •16. Изменение объема воды в диапазоне температур от 0 до 4°c
- •17. Диаграмма агрегатных состояний воды
- •18. Расход воды. Определение. Формула. Единицы измерения.
- •19. Прямая и обратная плотностная стратификация
- •21. Задача общей гидрологии
- •22. Минерализация и солёность.
- •23. Скорость звука в воде и воздухе (больше, меньше)
- •24. Работа воды (формула)
- •25. Причины вертикальной расслоенности вод
- •26. Методы изучения водных объектов
- •27. Классификация подземных вод по залеганию
- •27.1 Классификация подземных вод по залеганию (с рисунком, есть в ваших лекциях, а в данном документе рисунок взят из интернета)
- •27.2 Артезианский бассейн (с рисунком ( есть в учебнике на стр. 148)
- •28. Виды подземных вод (по происхождению)
- •29. Движение подземных вод.
- •32. Классификация рек по типам питания
- •33. Русловые деформации (классификация, схема переката с объяснением)
- •34. Определение подземных вод
- •36. Водный баланс бассейна реки.
- •37. Водные свойства грунтов.
- •38. Речные наносы
- •39. Водный режим грунтовых вод.
- •40. Термический режим рек
- •41. Зоны грунтов по отношению к подземным водам
- •42.Морфометрия реки и её бассейна
- •43. Гидравлическая связь
- •44. Водный баланс грунтовых вод
- •45. Водный режим рек
- •46. Роль подземных вод в физико-географических процессах
- •48. Водный баланс озера.
- •49. Колебания уровня воды в озерах
- •50. Течения, волнения и перемешивание воды в озерах.
- •51. Термический и ледовый режим озер
- •52. Водохранилища. Классификация. Морфометрия.
- •54. Ледник. Определение.
- •55. Понятие снеговой линии и хионосферы.
- •56. Типы ледников
- •57. Аккумуляция и абляция. Баланс льда и воды в леднике.
- •59. Водные массы озера.
11.График Хелланд-Хансена
- это график зависимости температуры замерзания воды и температуры наибольшей плотности от солености.
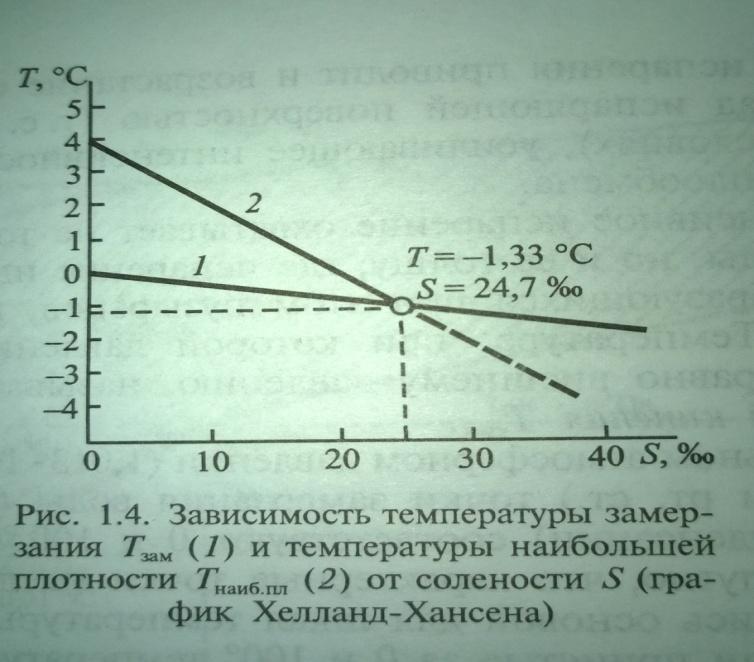
Увеличение солёности воды приводит к понижению температуры наибольшей плотности.
В пресных или солоноватых водах зимой в придонных горизонтах температура воды оказывается выше, чем на поверхности, и, согласно данному графику, всегда выше температуры замерзания.
12. Изменение температуры максимальной плотности при уменьшении солёности
Температура максимальной плотности также убывает с увеличением солености от максимального значения 4 С для пресной воды. Вода имеет самую высокую теплоемкость ( за исключением водорода и аммиака), что способствует сглаживанию температурных градиентов в атмосфере. Вследствие высокой теплоемкости воды до 30 % солнечной энергии расходуется на ее испарение, а это приводит к стабилизации температуры на Земле. Вода обладает низкой сжимаемостью. Высокое значение поверхностного натяжения воды позволяет воде подниматься по капиллярам на несколько метров и играет важную роль в образовании капель.
13. Число Фруда Число Фруда характеризует соотношение между силой инерции и внешней силой, в поле которой происходит движение, действующими на элементарный объём жидкости или газа:
![]()
где ![]() —
характерный масштабскорости,
—
характерный масштабскорости, ![]() —ускорение,
характеризующее действие внешней
силы,
—ускорение,
характеризующее действие внешней
силы, ![]() —
характерный размер области, в которой
рассматривается течение.
—
характерный размер области, в которой
рассматривается течение.
Например, если рассматривается
течение жидкости в трубе в поле силы
тяжести, то под
величиной ![]() понимаетсяускорение
свободного падения,
под величиной
понимаетсяускорение
свободного падения,
под величиной ![]() —
скорость течения, а за
—
скорость течения, а за![]() можно
принять длину трубы или её диаметр.
можно
принять длину трубы или её диаметр.
14. Закон сохранения тепловой энергии и уравнение теплового баланса



15. pH
Водоро́дный показа́тель, — мера активности(в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, количественно выражающая его кислотность. Равен по модулю и противоположен по знаку десятичному логарифму активности водородных ионов, выраженной в молях на один литр:
![]()
pH измеряется в степенях числа 10. Концентрация ионов водорода в растворесс pH 1.0 в 10 раз выше, чем концентрация ионов водорода в растворе с pH 2.0. Чем выше концентрация ионов водорода, тем ниже pH.
при pH > 7 раствор щелочной (основной)
при pH < 7 раствор кислый, или кислотный
16. Изменение объема воды в диапазоне температур от 0 до 4°c
При повышении температуры плотность воды, как и любого другого вещества, в большей части диапазона изменения температуры уменьшается, что связано с увеличением расстояния между молекулами при росте температуры. Эта закономерность нарушается лишь при плавлении льда и при нагревании воды в диапазоне от 0 до 4°C (точнее 3,98 °C). Здесь отмечаются еще две очень важные «аномалии» воды: 1) плотность воды в твердом состоянии (лед) меньше, чем в жидком (вода), чего нет у подавляющего большинства других веществ, 2) в диапазоне температуры воды от 0 до 4°C плотность воды с повышением температуры не уменьшается, а увеличивается. Особенности изменения плотности воды связаны с перестройкой молекулярной структуры воды. Эти две аномалии «аномалии» воды имеют огромное гидрологическое значение: лед легче воды и поэтому «плавает» на ее поверхности; водоемы обычно не промерзают до дна, так как охлажденная до температуры ниже 4°C пресная вода становится менее плотной и поэтому остается в поверхностном слое.
