
- •от ХХ УУУУ 20007 г. МГУП
- •Учебник подготовлен в рамках Инновационной образовательной программы
- •ISBN 978-5-7262-0821-3
- •ISBN 978-5-7262-0822-0 (т.1)
- •Глава 1. ФИЗИЧЕСКАЯ КРИСТАЛЛОГРАФИЯ
- •Предисловие к тому 1
- •Глава 1. ФИЗИЧЕСКАЯ КРИСТАЛЛОГРАФИЯ
- •1.1. Кристаллическое состояние
- •1.1.3. Решетка и структура кристаллов
- •1.2. Основы кристаллографии
- •1.2.1. Кристаллографические проекции
- •1.2.2. Пространственная решетка
- •1.2.3. Кристаллографические символы
- •1.2.4. Обратная решетка
- •1.2.5. Матрица ортогонального преобразования
- •1.2.6. Преобразование индексов направлений
- •1.3. Симметрия кристаллов
- •1.3.1. Поворотные оси симметрии
- •1.3.2. Инверсионные оси
- •1.3.3. Зеркально-поворотные оси
- •1.3.4. Элементы теории групп
- •1.3.5. Точечные группы симметрии
- •Бравэ
- •Бравэ
- •Распределение ячеек Бравэ по сингониям показано в табл. 1.4.
- •1.3.6. Пространственные группы
- •1.3.7. Предельные группы симметрии
- •1.4. Структура кристаллов
- •1.4.1. Плотнейшие упаковки в структурах
- •1.4.3. Структурные типы соединений типа АВ
- •1.4.4. Структурные типы соединений типа АВ2
- •1.4.5. Структурные типы соединений типа АmВnCk
- •1.4.7. Структура фуллеренов, фуллеритов
- •1.4.8. Структура поверхности
- •1.5. Физические свойства кристаллов
- •1.5.1. Принцип симметрии в кристаллофизике
- •1.5.4. Упругие свойства кристаллов
- •1.6. Кристаллография пластической деформации
- •1.6.1. Геометрия пластической деформации
- •1.6.2. Кристаллографическая текстура
- •1.7. Кристаллография границ зерен
- •1.7.1. Малоугловые границы
- •1.7.2. Высокоугловые границы
- •1.8. Кристаллография мартенситных превращений
- •1.8.1. Морфология мартенситных превращений
- •1.8.2. Кристаллография мартенситных превращений
- •Контрольные вопросы, задачи и упражнения
- •Глава 2. ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОЙ СТРУКТУРЫ
- •2.1. Точечные дефекты
- •2.1.1. Вакансии и межузельные атомы
- •2.1.2. Энергия образования точечных дефектов
- •Контрольные вопросы
- •Список использованной литературы
- •Глава 3. ФИЗИКА ТВЕРДОГО ТЕЛА
- •3.1. Строение атомов и межатомные взаимодействия
- •3.1.1. Классификация конденсированных систем
- •3.1.4. Энергия связи кристаллов
- •3.1.5. Типы связи в твердых телах
- •Металлическая связь. В отличие от ковалентной связи, которая образуется между двумя соседними атомами в результате коллективизации двух валентных электронов, металлическая связь появляется вследствие коллективизации всех валентных электронов. Эти электроны не локализуются у отдельных атомов, а принадлежат всему коллективу атомов. Поэтому они называются свободными электронами, перемещающимися по всему объему металла и в каждый момент времени равномерно распределенными в нем. Классическим подтверждением наличия таких свободных электронов в металлах является опыт Мандельштама и Папалекси, когда при резкой остановке вращающейся катушки, сделанной из металлической проволоки, в ней возникал электрический ток. Ярким подтверждением этому являются высокие электро- и теплопроводность металлов.
- •Ионная связь. Атомы, стоящие в периодической системе Д. И. Менделеева рядом с инертными газами, обладают склонностью принимать их конфигурацию либо путем отдачи, либо путем принятия электронов. У атомов щелочных металлов, стоящих непосредственно за инертными газами, валентный электрон слабо связан с ядром, так как движется вне заполненного слоя. Поэтому этот электрон может быть легко удален от атома. У галоидов, стоящих непосредственно перед инертными газами, недостает одного электрона для заполнения устойчивого слоя благородного газа. Поэтому галоиды обладают высоким сродством к дополнительному электрону.
- •Изоморфизм и морфотропия. Рассмотрим несколько ионных соединений щелочных металлов с галоидом бромом: LiBr, NaBr, KBr, RbBr и CsBr. Первые четыре соединения имеют решетку типа NaCl, а пятое соединение CsBr кристаллизуется в решетке типа CsCl.
- •3.2. Основы электронной теории кристаллов
- •3.2.1. Квантовая теория свободных электронов
- •3.2.2. Зонная теория металлов
- •3.3. Теория фаз в сплавах
- •3.3.1. Классификация фаз в сплавах
- •3.3.2. Твердые растворы
- •3.3.3. Промежуточные фазы
- •1B3.4. Диффузия и кинетика фазовых превращений
- •2Bв металлах и сплавах
- •4B3.4.1. Линейные феноменологические законы
- •5B3.4.2. Макроскопическое описание явления диффузии
- •6B3.4.3. Атомная теория диффузии в металлах
- •9B3.4.5. Диффузия и фазовые превращения в металлах
- •10Bи сплавах
- •3B3.5. Электрические свойства твердых тел
- •11B3.5.1. Основы электронной теории электропроводности
- •14B3.5.3. Эффект Холла
- •15B3.5.4. Связь электросопротивления со строением сплавов
- •20B3.5.7. Сверхпроводимость
- •3.6. Магнитные свойства твердых тел
- •3.6.1. Основные определения. Классификация веществ по магнитным свойствам
- •3.6.2. Магнитные свойства свободных атомов
- •3.6.3. Физическая природа диамагнетизма
- •3.6.4. Физическая природа парамагнетизма
- •3.6.5. Магнитная восприимчивость слабых магнетиков
- •3.6.6. Основы теории магнитного упорядочения
- •3.6.7. Доменная структура ферромагнетиков
- •3.6.8. Магнитные свойства ферромагнетиков
- •3.6.9. Антиферромагнетики и ферримагнетики
- •3.7. Тепловые свойства твердых тел
- •3.7.2. Теплоемкость кристаллических твердых тел
- •3.7.3. Теплопроводность твердых тел
- •3.7.4. Термическое расширение твердых тел
- •3.8. Упругие свойства твердых тел
- •3.8.1. Основные характеристики упругости
- •3.8.2. Упругость чистых металлов и сплавов
- •3.8.3. Ферромагнитная аномалия упругости
- •3.8.5. Внутреннее трение
- •Контрольные вопросы
- •Список использованной литературы

θк = 2zk (cA2 AAA + cB2 ABB + cAcB AAB ) ,
где z – координационное число; k – постоянная Больцмана.
Как видно, зависимость квадратичная. Результаты расчетов влияния легирования никеля другими переходными металлами на температуру Кюри, приведенные на рис. 3.120, показали хорошее соответствие с экспериментальными данными. Отметим, что точка Кюри ферромагнетиков почти всегда понижается при растворении в них неферромагнитных компонентов.
3.6.9. Антиферромагнетики и ферримагнетики
Как было показано выше, отрицательное обменное взаимодействие (A < 0) вызывает антипараллельное расположение спиновых магнитных моментов. Если магнитные моменты соседних узлов решетки кристалла одинаковы, то мы имеем дело с антиферромагнетизмом. Если противоположно направленные моменты не компенсируют друг друга, то вещество является ферримагнетиком. Антиферромагнетиками при комнатной температуре являются как чистые металлы (Mn, Cr, легкие редкоземельные металлы − Ce, Pr, Nd, Pm, Sm, Eu), так и большое число соединений переходных металлов. Магнитная восприимчивость антиферромагнетика постепенно повышается с температурой до максимального значения в точке Нееля ТN, в которой упорядоченное расположение спинов полностью утрачивается, и антиферромагнетик становится парамагнетиком. Дальнейшее повышение температуры выше точки Нееля приводит к уменьшению величины магнитной восприимчивости.
Так как спиновые магнитные моменты локализованы вблизи узлов кристаллической решетки, то удобно ввести понятие магнитной структуры тела. Экспериментальное изучение магнитных структур оказалось возможным с помощью дифракции нейтронов, имеющих, как известно, собственный магнитный момент.
Магнитную структуру антиферромагнетика в наиболее простых случаях можно представить себе как суперпозицию двух или более вставленных друг в друга подрешеток, в каждой из которых маг-
557
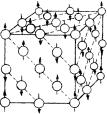
нитные моменты направлены параллельно, а магнитные моменты различных подрешеток компенсируют друг друга. Пример магнитной структуры антиферромагнетика приведен на рис. 3.121.
Оксид марганца МnО имеет кристаллическую структуру типа NaCl. Магнитная структура выражается в последовательном чередовании в семействе {111} плоскостей с параллельной и антипараллельной ориентацией спиновых моментов вдоль одного из
ребер куба. В результате период маг- Рис. 3.121. Магнитная структура нитной структуры удваивается по срав- антиферромагнетика MnO нению с периодом атомной структуры.
Магнитное взаимодействие между плоскостями {111} приводит к небольшому искажению кубической решетки, что устанавливается рентгенографически.
Наиболее типичными ферримагнетиками являются ферриты –
двойные оксиды металлов состава MeO.Fe2O3: где Me – двухвалентный металл (Mg2+, Zn2+, Cu2+, Ni2+, Fe2+, Mn2+). Ферриты имеют
кубическую структуру типа шпинели. В элементарной ячейке структуры содержится восемь формульных единиц, т. е. 32 атома кислорода, 8 ионов двухвалентного металла Мe2+ и 16 ионов трехвалентного железа Fe3+. Атомы кислорода образуют плотную кубическую упаковку. Восемь октаэдрических пустот в элементарной ячейке заняты ионами Fe3+, а в 16 тетраэдрических пустотах располагаются 8 ионов двухвалентного металла Мe2+ и 8 ионов трехвалентного железа Fe3+. Магнитные моменты трехвалентных ионов Fe3+, расположенные в октаэдрических и тетраэдрических пустотах, попарно антипараллельны друг другу, а наблюдаемый магнитный
момент обусловлен нескомпенсированными спиновыми моментами ионов Мe2+.
Оценим магнитный момент, приходящейся на один атом железа в соединении Fe3O4 = FeO.Fe2O3. Поскольку один ион Fe2+ на молекулу дает четыре магнетона Бора, то по расчету на один атом железа в этом соединении приходится средний момент Мср 4/3МБ = 1,33МБ, что близко к экспериментальному значению – 1,33МБ.
558
