
20120316103426operiser
.pdfМинистерство здравоохранения Республики Беларусь Минский государственный медицинский институт
С.И. Корсак, А.А. Баешко, Е.В. Крыжова
ОПЕРАЦИИ НА СЕРДЦЕ
Учебно-методическое пособие для студентов 4-го курса лечебнопрофилактического факультета
Минск – 1998

2
Цель настоящего учебного пособия - отразить принципы и некоторые особенности хирургического лечения основных врожденных и приобретенных пороков, ишемической болезни сердца, болезней перикарда, ранений сердца, дать понятие о трансплантации сердца.
Врожденные ПОРОКИ сераиа (ВПС)
Дефект межпредсердной перегородки (ДМПП)
Наличие отверстия в перегородке приводит к сбросу крови из левого предсердия в правое. Анатомическая характеристика порока определяется количеством, величиной и локализацией отверстий. По эмбриологическому происхождению выделяют первичные (рис. 1а) и вторичные (рис. 2а) дефекты.
Рис. 1. Первичный дефект межпредсердной перегородки: а) дефект; 6) ушивание щели митрального клапана; в) устранение дефекта.
Естественное течение и прогноз. В раннем детском возрасте порок, как правило, протекает доброкачественно, первые клинические симптомы появляются к 2-3 годам. Средняя продолжительность жизни больных с ДМПП не превышает 37-40 лет. Лечение. Больным с 1-ой степенью сброса (нет легочной гипертензии) операция не показана. Всем остальным пациентам показания к хирургическому вмешательству явля- ются абсолютными.
Техника операции. Операция выполняется с использованием аппарата искусственного кровообращения (АИК) на "сухом" сердце. Оперативный доступ - срединная стерно- томия. Атриотомия (вскрывается правое предсердие). Дефект менее 3 сантиметров в диа- метре подлежит ушиванию (рис. 26). При большем диаметре производят пластику перего- родки заплатой из аутоперикарда или синтетической ткани (рис. 1б,в).
б |
в |
а
Рис. 2. Вторичный дефект межпредсердной перегородки:
а) дефект; б) ушивание дефекта;
в) пластика лоскутом синтетического материала
Дефект межжелудочковой перегородки (ДМЖП)
Приводит к сбросу крови в правый желудочек через дефект в мышечной или мембранозной части перегородки. Самый частый из ВПС: выявляется у 9-25% детей,

3
родившихся с пороками сердца.
Естественное течение и прогноз. При небольших (до 1 см в диаметре) дефектах течение благоприятное; в возрасте 4-5 лет спонтанно закрываются до 25-40% ДМЖП
Лечение. В настоящее время больные с малыми ДМЖП хирургическому лечению не подлежат. При больших дефектах (диаметр более 1 см
\
Рис.3. Паллиативная операция при ДМЖП
или более 1/2 диаметра устья аорты) больных относят к IIIA гемодинамической группе, и они нуждаются в оперативном лечении. Хирургическое вмешательство при ДМЖП может быть радикальным и паллиативным. Радикальная операция заключается в закрытии де- фекта; паллиативная - в сужении легочной артерии манжеткой, в результате чего умень-
шается сброс крови через дефект и снижается объем легочного кровотока и давление в легочной артерии, дистальнее манжетки (рис. 3). Паллиативная операция выполняется при критических состояниях детей первых месяцев жизни, при безуспешности консерва- тивных мероприятий. Она также рекомендуется детям с множественными ДМЖП, а также с сопутствующими тяжелыми врожденными внутрисердечными аномалиями.
Техника операции. Выполняется с использованием аппарата искусственного крово- обращения (АИК) на "сухом" сердце. Оперативный доступ - срединная стернотомия. Ис- пользуются доступы через правое предсердие, правый желудочек, иногда через левый желудочек или легочный ствол. При небольшом дефекте его ушивают отдельными швами; при больших - накладывают заплату из синтетической ткани или биологических материалов (ауто-, ксеноперикард) (рис. 4).
Незаращенный артериальный (Боталлов) проток (НЛП)
Артериальный проток (ductus arteriosus) соединяет чаще всего общий ствол легочной ар- терии с нижней полуокружностью дуги аорты на уровне устья левой подключичной арте- рии. По частоте является одним из наиболее часто встречающихся (11-20% от всех ВПС) и почти в 2 раза чаше встречается у женщин. При незаращении артериального протока часть оксигенированной крови из аорты попадает в легочный ствол, далее в легкие; из сосудов малого крута кровообращения она опять поступает в левую половину сердца и аорту. Все это приводит к перегрузке прежде всего левого предсердия и желудочка, вызывая их ги- пертрофию.
Естественное течение и прогноз. Средняя продолжительность жизни больных с НАП не превышает 25 лет. Спонтанное закрытие НАЛ возможно крайне редко.

4
Рис. 4 Устранение дефекта наложением П-образных швов или заплатой
Лечение. При установлении диагноза НАЛ показания к операции абсолютны. Оп- тимальный возраст для операции 2-5 лет. Иногда эффективным является назначение в первые дни после рождения индометацина, что, по данным некоторых авторов, способст- вует ликвидации порока в 18-20% случаев при оральном применении и в 88-90% случаев при внутривенном введении (0,2 мг/кг в сутки).
Техника операции. Производится без использования АИКа. Выполняется левосторонняя торакотомия (рис. 5а). Вскрывается медиастинальная плевра между диафрагмальным и блуждающими нервами. С помощью диссектора между аортой и легочной веной обеспе- чивается доступ к Боталлову протоку 6 (рис. 56). Последний перевязывается
двумя лигатурами. Иногда проток пересекают с последующим ушиванием обо их отверстий.
Рис. 5. Незаращенный артериальныйпроток:
а) место торакотомии; 6) схема операции
Коарктация аорты (КА)
Врожденное сегментарное сужение аорты, располагающееся в области ее перешейка (рис. 6а). Довольно часто КА встречается в сочетании с другими ВПС. Среди детей первого года жизни с ВПС КА занимает четвертую позицию по частоте и встречается в 7,5% случаев. Заболевание в 2-2,5 раза чаще встречается у лиц мужского пола.
Естественное течение и прогноз. КА характеризуется крайне неблагоприятным естественным течением. До 56% больных умирают в течение первого года жизни. Еще более неблагоприятно протекает КА в сочетании с другими ВПС. В возрасте от 2 до 10 лет смертельные исходы наблюдаются редко. Средняя продолжительность жизни около 30 лет, 70% больных умирают в возрасте до 40 лет, и лишь незначительная часть больных доживает до 60-70 лет.
Лечение. Наличие КА является абсолютным показанием к операции, риск которой неодинаков в различные возрастные периоды и зависит от тяжести состояния больных, анатомии порока и расстройств кровообращения. У детей грудного возраста, особенно в первые 3 месяца жизни, операцию выполняют в экстренном порядке для предупреждения прогрессирования сердечной недостаточности и развития декомпенсации. При отсутствии осложнений оптимальным возрастом для операции следует считать период между 3 и 5 годами. У взрослых больных (старше 19-20 лет) вопрос о показаниях решается строго ин-
5
дивидуально.
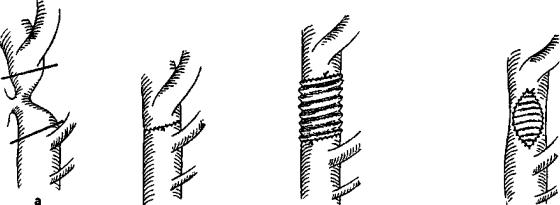
Техника операции. АИК, как правило, не используют. У детей грудного возраста широко используется операция пластики перешейка аорты (истмопластика) лоскутом левой подключичной артерии для профилактики рекоарктации. В более поздние сроки используются операции резекции аорты с наложением анастомоза "конец в конец" (рис. 66), протезирование иссеченного участка синтетическим протезом (рис. 6в), непрямая истмопластика аорты заплатой (рис. 6г).
Рис. 6. Коарктация аорты:
а) наиболее характерный уровень коарктации и линии пересечения аорты; б) резекция и наложение анастомоза «конец в конец»; в) устранение дефекта аорты протезом;
г) непрямая истмопластика синтетической заплатой.
Тетрада Фалло (ТФ)
ТФ характеризуется недоразвитием выходного отдела правого желудочка и смещением конусной перегородки кпереди и влево, что обуславливает стеноз выходного отдела правого желудочка, как правило, с нарушением развития фиброзного кольца легочного ствола, его клапанного аппарата и очень часто ствола и ветвей. То есть признаками порока являются стеноз выходного отдела правого желудочка, ДМЖП, декстропозиция аорты и гипертрофия правого желудочка. Встречается у 14% детей, родившихся с ВПС.
Естественное течение и прогноз. Течение болезни и прогноз определяются степенью легочного стеноза; 25% детей с ТФ умирают в течение первого года жизни, большинство из них - на первом месяце. Как правило, это больные, имеющие тяжелейшую обструкцию выходного отдела правого желудочка и легочной артерии; 40% больных погибают к 3 годам, 70% - к 10 годам и 95% - к 40 годам жизни.
Лечение. Показания к операции при ТФ носят абсолютный характер. Все больные подлежат хирургическому лечению. Прежде всего, следует оперировать больных с ранним цианозом. Применяются операция радикальной коррекции или паллиативные операции (операции типа Блелока-Тауссиг).
Техника операции. Операция Блелока-Тауссиг. Выполняется широкая торакото-мия в 4, 5 межреберье справа. Вскрывают перикард в продольном направлении на 1,5-2 см ниже диафрагмального нерва, выделяют легочную артерию. Над непарной веной рассекают медиастинальную плевру. Блуждающий нерв отводят латеральнее, выделяют и подтя- гивают из-под блуждающего нерва подключичную артерию. После перевязки подключич- ную артерию рассекают проксимальнее места деления ее на ветви и накладывают анасто- моз с легочной артерией в наиболее верхнем ее отделе (рис. 7).
Методы радикальных операций при ТФ еще нельзя считать окончательно разработанными. Объем хирургического вмешательства зависит от типа стеноза выходного отдела правого желудочка, состояния кольца и клапанов легочной артерии,

6
диаметра ствола последней и состояния устьев и ветвей легочной артерии, а также от расположения ДМЖП. При выполнении радикальной операции используют АИК с холодовой кардиопле-гией, после чего должны решаться две задачи: во-первых, должен быть устранен или, хотя бы, уменьшен стеноз начального отдела легочного ствола; во- вторых, должен быть ликвидирован ДМЖП.
Рис. 7. Схема операции по Blalock-Taussig с правой стороны.
ПРИОБРЕТЕННЫЕ ПОРОКИ СЕРДЦА (ППС) Пороки аортального клапана
Стеноз аортального клапана. Изолированные аортальные стенозы встречаются в 1.5-2% случаев ППС. В сочетании с той или иной степенью аортальной недостаточности он встречается примерно в 23% случаев.
Естественное течение и прогноз. Особенностью аортального стеноза является длительный период компенсации, после которого быстро развивается сердечная недоста- точность. После появления выраженных симптомов прогноз резко ухудшается. Средняя продолжительность жизни после появления выраженного ишемического синдрома - 3 года 11 месяцев, при левожелудочковой недостаточности - 1 год 11 месяцев, при общей сер- дечной недостаточности - 7 месяцев.
Недостаточность аортального клапана. Составляет около 14% от всех ППС, причем 3,7% -
визолированном виде, а 10,3% - в сочетании с другими пороками (стеноз аорты, пороки митрального и трикуспидального клапанов).
Естественное течение и прогноз. Недостаточность кровообращения при этом пороке длительное время не возникает вследствие компенсаторной функции левого желудочка, являющегося самым мощным отделом сердца. Но, при появлении первых симптомов аортальной недостаточности, процесс быстро прогрессирует (при внезапной недоста- точности средняя продолжительность жизни составляет 7 месяцев). Анализ естественного течения болезни с использованием актуарного метода показал, что 45% больных умирают
втечение 2 лет.
Лечение. Показанием к оперативному лечению является появление одного или нескольких признаков из так называемой триады симптомов - обмороки, сердечная астма, ишемические боли (III - IV функциональный класс по NYHA).
Пороки митрального клапана
Недостаточность митрального клапана. Частый порок сердца: встречается у 50% больных с различными пороками сердца, причем у детей он наблюдается гораздо чаще, чем у взрослых.
Естественное течение и прогноз. При умеренной недостаточности трудоспособность сохраняется длительное время. Выраженная недостаточность довольно быстро приводит к развитию тяжелой недостаточности кровообращения и смерти больных. Консер-
вативное лечение бесперспективно. При естественном течении митральных пороков к 12 годам после появления первых симптомов заболевания умирает 86% больных с недоста- точностью митрального клапана.

7
Стеноз митрального клапана. Митральный стеноз является наиболее частым ревматическим пороком сердца и встречается в 90% случаев от всех ППС. Порок обычно формируется в молодом возрасте и чаще наблюдается у женщин (80%).
Рис. 8. Механические и биологические протезы клапанов сердца
Естественное течение и прогноз. Течение процесса определяется степенью вы- раженности стеноза, наличием легочной гипертензии и состоянием сократительной спо- собности правого желудочка. Среднестатистические данные наблюдений за естественным течением заболевания показали, что после появления симптомов нарушения кровообра- щения при лекарственном лечении к 5 годам умирает 50% больных.
Лечение. Хирургическое лечение показано в зависимости от функционального класса NYHA. В I (обычная физическая нагрузка переносится так же, как и до болезни) -операция не показана; во И (незначительное ограничение физической активности, в покое жалоб нет) - показания к операции относительны; в Ш (заметное ограничение физической нагрузки; обычная физическая активность вызывает боль, усталость, одышку, сердцебие- ние) и IV (субъективные симптомы недостаточности кровообращения имеются даже в покое) - показания абсолютные. В настоящее время практически во всех случаях операци-
ей выбора при всех клапанных пороках является замещение клапана механическим или биологическим протезами (рис.8) или т.н. клапаносохраняющие операции: открытая ко- миссуротомия и аннулопластика.
Техника операции при клапанных пороках сердца. Замещение пораженных клапанов сердца механическими или биологическими протезами производится на "открытом" сердце с использованием ИК. Операции в условиях ИК, за исключением внутрисердечного этапа, вьшолняются по следующей схеме: оперативный доступ - сре- динная стернотомия. Выделяют аорту, полые вены и правые отделы сердца. Для подклю- чения АИК вводят венозные канюли в обе полые вены, а артериальную - высоко в восхо- дящую часть аорты. После начала ИК с холодовой кардиоплегией, после появления фиб-

8
рилляции сердца восходящую аорту пережимают. Разгрузка сердца осуществляется за счет канюляции левого желудочка через верхушку сердца или левое предсердие. Иногда каню-лируется легочный ствол. При протезировании митрального клапана дренаж проводят в левый желудочек через протез. После этого выполняется внутрисердечный этап операции, заключающийся в иссечении измененного естественного клапана и замене его механическим или биологическим протезом (рис. 9). После окончания этого этапа, герметизации и заполнения кровью полостей сердца снимают зажим с аорты. При необходимости восстанавливают деятельность сердца дефибрилляцией. После стабилизации гемодинамики прекращают ИК и производят деканюляцию. Операция заканчивается дренированием полостей перикарда и средостения, наложением редких швов на перикард, ушиванием грудины, мягких тканей.
Рис. 9. Схематическое изображение имплантации дискового протеза в митральную
позицию
Аннулопластика при митральной недостаточности предполагает восстановление запира- тельной функции митрального клапана с помощью жесткого опорного кольца. Метод основан на том, что в механизме развития недостаточности митрального клапана важным фактором является дилатация фиброзного кольца в области комиссур и задней створки,
тогда как часть фиброзного кольца в основании передней створки является единым целым с корнем аорты и не вовлекается в процесс. Преимуществом аннулопластики является
сохранение нормальной площади отверстия и функции клапана, создаются условия
для предотвращения рецидивирования дилатации фиброзного кольца.
Иногда, по строгим показаниям, используя АИК, выполняют открытую комиссу-ротомию. Рассекают стенку левого предсердия или левое ушко, разъединяют створки клапана под контролем зрения, что позволяет избежать их чрезмерной травматизацни и при необходимости выполнить протезирование клапана.
Болезни перикарда
Сдавливающий перикардит. В большинстве случаев является следствием туберкулезного процесса. Происходит срастание перикарда с эпикардом с нередким отложением в этой рубцовоизмененной ткани извести ("панцирное сердце").
Сущность сдавливающего перикардита состоит в том, что сердце в период диастолы неспособно расширяться и поэтому прогрессивно снижается его диастолическое на- полнение или приемная способность.
Техника операции. Срединная стернотомия. Производят надрез, по возможности, в необызвествленном участке перикарда до сокращающегося сердца. Отыскивается стой, расположенный между измененным перикардом и мягкой, неизмененной сердечной мыш- цей. Затем продвигаются по этому слою во всех направлениях, стремясь, по возможности, наиболее полно удалить измененный (особенно обызвествленный) перикард. Следует
стремиться к ликвидации всех кольцеобразных сращений для обеспечения свободного наполнения сердца в диастолу. Часть перикарда, расположенного сзади, как правило, ос- тавляют. При удалении измененного перикарда следует остерегаться повреждения диа- фрагмального нерва.
9
Ише.нпческая болезнь сердца (ИБС)
ИБС - острая или хроническая дисфункция сердца, возникшая вследствие относительного или абсолютного уменьшения снабжения миокарда артериальной кровью.
Естественное течение и прогноз. Прогноз у больных с ИБС в значительной мере зависит от состояния коронарных артерий и миокарда, а также от многих других факто- ров. Следует отметить, что смертность больных ИБС в 2-3 раза выше, чем лиц данной возрастной группы, не страдающих ИБС-
Лечение. При неэффективности консервативного медикаментозного лечения показано хирургическое лечение, включающее в себя закрытые (баллонная дилатация, стенти- рование коронарных артерии) и открытие (маммарно-коронарный анастомоз - М-КА, аор- токоронарное шунтирование-АКШ) методы.
Ангиопластика венечных артерий. Показанием служит поражение коронарной артерии в ее проксимальных отделах при условии отсутствия выраженного кальциноза и поражения дистального русла этой артерии. Необходимым условием выполнения ангио-
пластики является наличие готовой операционной бригады для выполнения экстренной операции аортокоронарного шунтирования в случае появления осложнений при выполне- нии процедуры.
Техника операции. Используется система двух катетеров: катетер-проводник (более широкого диаметра) и дилатадионный катетер (более узкий). После выполнения коро- нарографии обычным методом аягяографический катетер заменяют катетером- проводником, через который проводят дилатационный катетер в стенозированную арте- рию. Максимальный диаметр наполненного баллончика - 3-3,7 мм, в спавшемся состоянии - 1,2-1,3 мм. При достижении баллончиком стенозированного сегмента он (баллончик) заполняется 30% раствором контрастного вещества. В таком состоянии баллончик находится в течение 5-60 секунд. При необходимости процедуру повторяют несколько раз. Успешным считается вмешательство, при котором степень стеноза уменьшается более чем на 20%. Суммарный положительный результат баллонной дилатации достигается примерно у 65% больных.
Основными осложнениями ангиопластики являются: острый инфаркт миокарда (5,3%), окклюзия коронарной артерии (4,6%), спазм коронарной артерии (4,5%). Клиниче-
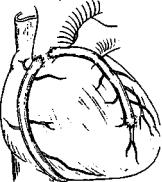 Рис. 10. Схема АКШ
Рис. 10. Схема АКШ
ский эффект ангиопластики заключается в исчезновении или значительном урежении приступов стенокардии примерно у 80% больных. Эффективность процедуры через 3 года составляет 67%. В последнее время баллонную дилатацию коронарных артерий стали до- полнять стентированием (каркасированием) суженого участка с помощью механических изделий с эффектом памяти (стентов), что позволило улучшить отдаленные результаты. Аортокоронарное шунтирование. В настоящее время основой для определения пока- заний к хирургическому лечению являются следующие факторы: выраженность стенокардии и устойчивость ее к медикаментозному лечению; степень и локализация, а также количество пораженных сосудов; сократительная функция миокарда. Только на
10
основании этих факторов ставятся показания к АКШ, которое может быть дополнено при необходимости маммарно-коронарным анастомозом.
Техника АКШ. Операция осуществляется в несколько этапов: 1) доступ к сердцу, обычно срединная стернотомия; 2) забор аутотрансплантатов, выполняемый другой бригадой хирургов одновременно с производством стернотомии; 3)
канюляция восходящей части аорты и полых вен и подключение ИК; 4) пережатие восхо- дящей аорты с кардиоплегией; 5) наложение дистальных анастомозов с коронарными ар- териями; 6) снятие зажима с восходящей аорты; 7) профилактика воздушной эмболии; 8) восстановление сердечной деятельности; 9) наложение проксимальных анастомозов; 10) отключение ИК; 11) деканюляция; 12) ушивание торакотомной раны с дренированием полости перикарда (рис. 10).
В качестве трансплантата используют: реверсированный (повернутый на 180°) участок большой скрытой вены голени, а в последнее время — нижняя надчревная, лучевая, левая желудочная, обе желудочносальниковые и внутренняя грудная артерии.
Маммарно - коронарный анастомоз (рис. 11). Впервые выполнен В.И.Колесовым в 1964 году. Преимущества метода: - может выполняться без использования АИК: - большее соответствие диаметров внутренней грудной и коронарной артерий; - анастомоз на- кладывается между однородными тканями; - выше линейная скорость кровотока, что тео- ретически должно снизить частоту тромбозов; - накладывается только один анастомоз, что сокращает время операции и уменьшает вероятность технической ошибки; - внутренняя грудная артерия редко поражается атеросклерозом; в ней не развивается субинти-мапьная гиперплазия, как в аутовенозных шунтах.
Ограничениями к применению М-КА следует считать следующее: 1) диаметр правой внутренней грудной артерии значительно меньше, чем правой коронарной артерии, а диаметр левой внутренней грудной артерии меньше, чем передней межжелудочковой ветви левой коронарной артерии; 2) имеются только две внутренние
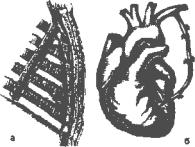 Рис. 11. Схема МКШ:а) выделение внутренней грудной
Рис. 11. Схема МКШ:а) выделение внутренней грудной
артерии; 6) анастомоз
грудные артерии, что ограничивает возможность реваскуляризации нескольких артерий; 3) выделение внутренней грудной артерии является более сложным, чем забор аутовены; 4) наложение анастомоза технически более сложно из-за меньшего диаметра и тонкой стенки внутренней грудной артерии.
Ранения сердца
Среди проникающих ранений грудной клетки ранения сердца и перикарда встречаются в 10-15% случаев. Основным патофизиологическим моментом при ранениях сердца является поступление крови в полость перикарда, что затрудняет деятельность сердца (тампонада сердца). При этом вследствие одновременного сдавления коронарных сосудов резко нарушается питание сердечной мышцы. Кроме того, тампонада сердца может соче- таться со смещением средостения, перегибом сосудистого пучка и т.д.
Лечение. При ранениях сердца показана операция.
Техника операции. Под интубационным эндотрахеальным наркозом выполняется торакотомия, чаше всего переднебоковая в IV-V межреберьях, что обеспечивает необхо- димые условия для ревизии органов грудной клетки. Перикард вскрывают продольно кнутри от диафрагмального нерва. Рану сердца прикрывают пальцем для остановки кро-
