
- •Глава 1. Структура и свойства жидких кристаллов…………………………… 4
- •Глава 2. Применение жидких кристаллов……………………………………..13
- •Введение
- •Глава 1. Структура жидких кристаллов.
- •1.1Структура жк
- •1.2 Термотропные жк
- •1.3. Лиотропные жк
- •Глава 2. Применение жидких кристаллов
- •2.1. Управление жк
- •2.2. Жк-индикаторы
- •2.3. Управление холестерической спиралью
- •2.4. Tft-lcd дисплей
- •2.5. 3D tft-lcd монитор
- •2.6. Lcd-проекторы
- •2.7. Lcos-проекторы Рис. 11. Lcos-проектор
- •2.8. Электронная бумага
- •Заключение
- •Список использованной литературы
Министерство образования и науки РФ
Государственное образовательное учреждение
высшего профессионального образования
«ТУЛЬСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Кафедра физики металлов и материаловедения
Контрольно – курсовая работа
по дисциплине «Кристаллография»
Тема работы: «Жидкие кристаллы. Структура, свойства и применение»
Выполнила
Ст. гр. 430391 Новосветлова Е. Э.
Роспись ____________________
Проверил
Троицкий И. В.
Роспись____________________
Тула 2011
Содержание………………………………………………………………… …….. 2
Введение………………………………………………………………………..… 3
Глава 1. Структура и свойства жидких кристаллов…………………………… 4
1.1. Структура ЖК………………………………………………………………... 4
1.2. Термотропные ЖК………………………………………………………...… 6
1.3. Лиотропные ЖК…………………………………………………………….10
Глава 2. Применение жидких кристаллов……………………………………..13
2.1. Управление ЖК……………………………………………………………..13
2.2. ЖК-индикаторы…………………………………………………………..…15
2.3. Управление холестерической спиралью………………………………..…17
2.4. TFT-LCD дисплей………………………………………………………...…20
2.5. 3D TFT-LCD монитор………………………………………………………21
2.6. LCD-проекторы………………………………………………………….….21
2.7. LCOS-проекторы……………………………………………………………21
2.8. Электронная бумага………………………………………………….……..22
Заключение ………………………………………………………………….…..23
Список использованной литературы…………………………………...………24
Введение
Жидкие
кристаллы открыл в 1888 г. австрийский
ботаник Ф. Рейнитцер. Он обратил внимание,
что у кристаллов холестерилбензоата
и холестерилацетата было две точки
плавления и, соответственно, два разных
жидких состояния — мутное и прозрачное.
Однако, учёные не обратили особого
внимания на необычные свойства этих
жидкостей. Долгое время физики и химики
в принципе не признавали жидких
кристаллов, потому что их существование
разрушало теорию о трёх состояниях
вещества: твёрдом, жидком и газообразном.
Учёные относили жидкие кристаллы то к
коллоидным растворам, то к эмульсиям.
Научное доказательство было предоставлено
профессором университета Карлсруэ Отто
Леманном (нем. Otto Lehmann) после многолетних
исследований, но даже после появления
в 1904 году написанной им книги «Жидкие
кристаллы», открытию не нашлось
применения.[1]
Рис.1.Ф. Рейнитцер.
В 1963 г. американец Дж. Фергюсон (англ. James Fergason) использовал важнейшее свойство жидких кристаллов — изменять цвет под воздействием температуры — для обнаружения невидимых простым глазом тепловых полей. После того как ему выдали патент на изобретение (U.S. Patent 3 114 836), интерес к жидким кристаллам резко возрос.
В 1965 г. в США собралась Первая международная конференция, посвящённая жидким кристаллам. В 1968 г. американские учёные создали принципиально новые индикаторы для систем отображения информации. Принцип их действия основан на том, что молекулы жидких кристаллов, поворачиваясь в электрическом поле, по-разному отражают и пропускают свет. Под воздействием напряжения, которое подавали на проводники, впаянные в экран, на нём возникало изображение, состоящее из микроскопических точек. И всё же только после 1973 г., когда группа английских химиков под руководством Джорджа Грея (англ. George William Gray) получила жидкие кристаллы из относительно дешёвого и доступного сырья, эти вещества получили широкое распространение в разнообразных устройствах.[1]
Глава 1. Структура жидких кристаллов.
1.1Структура жк
Сейчас известно уже около сотни тысяч органических веществ, которые могут находиться в ЖК-состоянии, и число таких соединений непрерывно растет. Если в первые десятилетия после открытия жидких кристаллов основными представителями этих соединений являлись только вещества, состоящие из асимметричных молекул стержнеобразной формы, – так называемые каламитики (от греческого “каламис” – тростник), то впоследствии было обнаружено, что в ЖК-состояние могут переходить самые разнообразные вещества, имеющие молекулы более сложной формы (диски, пластины и др.) Молекулы ЖК-соединений очень часто называют мезогенами, а группировки или фрагменты молекул, способствующие формированию ЖК-фазы, – мезогенными группами.[2]
В таблице 1 приведены примеры стержнеобразных мезогенов – каламитиков, а также химические формулы доскообразных (дискотики) и планкообразных мезогенов (санидики) (от греческого “sanidis” –планка).
Таблица
1. Типичные примеры химических соединений.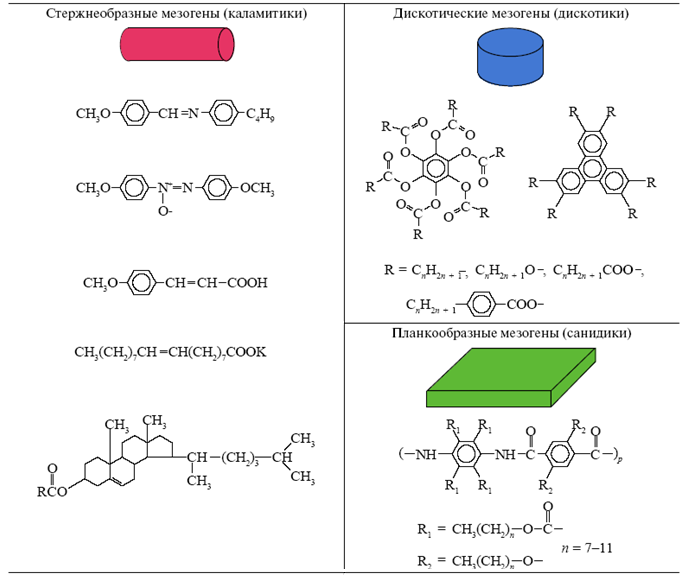
Как видно из таблицы 1, среди мезогенных групп чаще всего встречаются бензольные кольца, связанные непосредственно друг с другом или с помощью различных химических группировок (–CH=CH–, –CH=N–, –NH–CO– и др.). Характерной особенностью всех ЖК-соединений является асимметричная форма молекул, обеспечивающая анизотропию поляризуемости и тенденцию к расположению молекул преимущественно параллельно друг другу вдоль их длинных (каламитики и санидики) и коротких (дискотики) осей.[2]
По своим общим свойствам ЖК можно разделить на две большие группы:
1) термотропные ЖК, образующиеся в результате нагревания твердого вещества и существующие в определенном интервале температур и давлений;
2) лиотропные ЖК, которые представляют собой двух- или более компонентные системы, образующиеся в смесях стержневидных молекул данного вещества и воды (или других полярных растворителей).
