
- •Методические указания
- •1. Цель работы.
- •2. Возникновение горения
- •3. Горение (взрыв) газовых и пылевых смесей
- •4. Параметры, определяющие пожарную опасность веществ
- •Общие сведения о пожаре и пожарной опасности
- •1. Пожарная опасность
- •2. Причины пожаров
- •3. Распространение пожаров
- •Огнестойкость и возгораемость строительных конструкций
- •1. Строительные конструкции и противопожарная защита
- •2. Возгораемость строительных материалов и конструкций
- •3. Перекрытия
- •4. Экраны
- •5. Водяные завесы
- •6. Противопожарные зоны
- •2. Понятия и определения вынужденной эвакуации
- •4. Параметры движения людей
- •5. Нормирование процесса эвакуации
- •6. Расчет продолжительности эвакуации
- •7. Конструктивно-планировочные решения
- •Организация пожарной охраны и тушение пожаров
- •1. Государственный пожарный надзор
- •2. Пожарная охрана на новостройках
- •3. Огнегасительные вещества и средства пожаротушения
- •4. Средства тушения пожаров
- •5. Средства извещения 0 пожарах
- •Противопожарная защита новостроек
- •1. Пожарная опасность новостроек
- •2. Строительный генеральный план (стройгенллан)
- •3. Производство строительно-монтажных работ
- •Библиографический список рекомендуемой литературы
2. Возникновение горения
Тепловое и цепное самовоспламенение. Горению веществ всегда предшествует медленный процесс окисления. Согласно теории цепных реакций Н. Н. Семенова процесс окисления начинается с активации горючего вещества.
Реакция окисления экзотермическая и при определенных условиях имеет возможность самоускоряться. Процесс самоускорения реакции окисления и переход ее в горение называется самовоспламенением.
Самовоспламенение может быть тепловое и цепное. При тепловом самовоспламенении причиной ускорения реакции окисления является превышение скорости тепловыделения над скоростью теплоотвода, а при цепном — превышение скорости разветвления цепей над их обрывом. Наиболее распространенным является тепловое самовоспламенение.
Предположение о том, что ускорение реакции окисления обусловлено преобладанием скорости тепловыделения над скоростью теплоотвода, высказывалось еще Вант-Гоффом. Однако только в 1928 г. Н. Н. Семеновым была дана детальная количественная теория теплового самовоспламенения.
Сущность тепловой теории самовоспламенения сводится к следующему.
Скорость выделения
тепла при окислении горючей системы
![]() в сосуде объемом
в сосуде объемом![]() равна
равна
![]() (18.6)
(18.6)
где Q — теплота горения системы;
![]() —предэкспоненциальный
множитель;
—предэкспоненциальный
множитель;
Е — энергия активации;
с — концентрация реагирующего вещества;
![]() —суммарный порядок
реакции;
—суммарный порядок
реакции;
Т — температура горючей системы;
е — основание натуральных логарифмов;
R— газовая постоянная.
Выделившаяся
теплота передается горючей системе,
которая нагревается выше температуры
стенки сосуда. Это вызывает теплоотвод
от горючей системы, скорость которого
![]() равна
равна
![]() (18.7)
(18.7)
где ![]() -коэффициент
теплоотдачи от горючей системы к стенкам
сосуда;
-коэффициент
теплоотдачи от горючей системы к стенкам
сосуда;
S — общая поверхность стенок сосуда;
![]() —температура
стенок сосуда.
—температура
стенок сосуда.
Если в процессе
окисления
![]() =
=![]() то реакция будет происходить при
постоянной температуре, при которой
возникло это соотношение, если же
то реакция будет происходить при
постоянной температуре, при которой
возникло это соотношение, если же
![]() >
> ![]() то горючая система будет самонагреваться
до возникновения горения. Следовательно,
условием самовоспламенения горючей
системы является превышение скорости
тепловыделения при окислении над
скоростью теплоотвода.
то горючая система будет самонагреваться
до возникновения горения. Следовательно,
условием самовоспламенения горючей
системы является превышение скорости
тепловыделения при окислении над
скоростью теплоотвода.
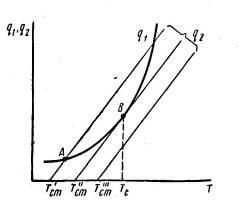
Рис. 18-2. Изменение скорости
тепловыделения и теплоотвода
от температуры
Представим процесс теплового самовоспламенения графически (рис. 18-2) . По оси абсцисс отложим температуру стенки сосуда и горючей смеси, а по оси ординат — скорость тепловыделения и теплоотвода. На графике зависимость скорости тепловыделения от температуры выразится кривой линией (18.6), а теплоотвода — прямой (18.7). Местоположение прямой теплоотвода в координатах q— Т зависит от температуры стенки сосуда Тст.
При температуре
стенки сосуда Тст линия теплоотвода
пересекает линию тепловыделения в точке
А. До точки А скорость тепловыделения
горючей системы превышает скорость
теплоотвода, поэтому происходит
самонагревание системы. В точке А
скорость тепловыделения становится
равной скорости теплоотвода, и дальнейшее
самонагревание горючей системы
прекращается, так как при температуре
выше, чем в точке А, скорость тепловыделения
ниже скорости теплоотвода. Таким образом,
при нагреве стенки, а следовательно, и
горючей системы до температуры ![]() горение
не возникает. Оно может возникнуть, если
стенки сосуда будут нагреты до более
высокой температуры
горение
не возникает. Оно может возникнуть, если
стенки сосуда будут нагреты до более
высокой температуры ![]() .
При этой температуре кривая скорости
выделения тепла
.
При этой температуре кривая скорости
выделения тепла ![]() не пересекается с прямой теплоотвода
не пересекается с прямой теплоотвода
![]() ,
поэтому при всех температурах горючей
системы скорость выделения тепла
превышает скорость теплоотвода и горючая
система самонагревается до температуры
горения, т. е. самовоспламеняется. Понижая
температуру стенки сосуда ниже
,
поэтому при всех температурах горючей
системы скорость выделения тепла
превышает скорость теплоотвода и горючая
система самонагревается до температуры
горения, т. е. самовоспламеняется. Понижая
температуру стенки сосуда ниже ![]() ,
можно достигнуть предельной температуры
стенки, при которой еще возможно
самовоспламенение. Такой температурой
является температура
,
можно достигнуть предельной температуры
стенки, при которой еще возможно
самовоспламенение. Такой температурой
является температура ![]() ,
при ней прямая теплоотвода касается
кривой теплоотвода в точке В. Температура
горючей системы в точке В является
предельной температурой самовоспламенения
Тс. Однако эту температуру трудно
замерить и практически за температуру
самовоспламенения принимают температуру
стенки сосуда
,
при ней прямая теплоотвода касается
кривой теплоотвода в точке В. Температура
горючей системы в точке В является
предельной температурой самовоспламенения
Тс. Однако эту температуру трудно
замерить и практически за температуру
самовоспламенения принимают температуру
стенки сосуда ![]()
Следовательно,
температура самовоспламенения есть та
наименьшая температура горючего
вещества, при которой оно способно
самонагреваться до возникновения
горения, т. е. при которой ![]() .Так
как скорости тепловыделения и теплоотвода
в горючей системе зависят от многих
факторов, то температура самовоспламенения
ее не является величиной постоянной.
Она особенно сильно изменяется от
концентрации горючего вещества в
системе, объема и формы горючей системы
и давления.
.Так
как скорости тепловыделения и теплоотвода
в горючей системе зависят от многих
факторов, то температура самовоспламенения
ее не является величиной постоянной.
Она особенно сильно изменяется от
концентрации горючего вещества в
системе, объема и формы горючей системы
и давления.
В табл. 19 приведены температуры самовоспламенения некоторых горючих веществ и материалов.
Таблица 19
|
Наименование веществ и материалов |
Температура самовоспламенения, °С
|
Наименование веществ н материалов |
Температура самовоспламенения, °С
|
|
Бензин А-66 |
255 |
Линолеум резиновый |
410 |
|
Винипласт |
580 |
Линолеум хлорвиниловый |
410 |
|
Войлок строительный |
370 |
Опилки сосновые |
306 |
|
Гранитоль |
165 |
Плита древесноволокнистая |
345 |
|
Древесина сосновая |
399 |
Руберойд |
400 |
Н. Н. Семенов первым показал, что в горючих системах, в которых возможна разветвленная цепная реакция, самоускорение реакции, приводящее к самовоспламенению, может происходить при постоянной температуре. Такое самовоспламенение было названо цепным.
Чисто цепное самовоспламенение — довольно редкое явление, так как оно протекает при таких низких давлениях и температурах, до которых у немногих горючих веществ простирается область самовоспламенения. Так, например, цепное самовоспламенение смеси водорода с кислородом при температуре 485° происходит при давлении от 5,8 до 8,2 мм рт. ст.
Сущность цепного самовоспламенения состоит в следующем.
При нагревании
горючей системы в ней образуются активные
центры (радикалы, атомы), которые, имея
свободные валентности, легко вступают
в соединения с кислородом воздуха.
Допустим, при нагревании горючей системы
образуется n
активных центров. Некоторые из них
погибнут, а остальные прореагируют.
Образовавшиеся в результате реакции
активные центры могут опять частично
прореагировать и дать новые активные
центры, остальные погибнут. Отношение
числа обрывов к общему числу активных
центров называется вероятностью обрыва
цепи и обозначается буквой ![]() .
В разветвляющихся цепях при реакции
одного активного центра может получаться
два или больше центров. Если из активного
центра образуются два, то один считается
продолжением цепи, а другой — разветвлением.
Отношение числа всех разветвлений к
общему числу активных центров называется
вероятностью разветвления цепи и
обозначается буквой 8. Ускорение цепной
реакции возможно, если вероятность
разветвления цепи превысит вероятность
обрыва, т. е.
.
В разветвляющихся цепях при реакции
одного активного центра может получаться
два или больше центров. Если из активного
центра образуются два, то один считается
продолжением цепи, а другой — разветвлением.
Отношение числа всех разветвлений к
общему числу активных центров называется
вероятностью разветвления цепи и
обозначается буквой 8. Ускорение цепной
реакции возможно, если вероятность
разветвления цепи превысит вероятность
обрыва, т. е. ![]() .
Это условие и является условием цепного
самовоспламенения.
.
Это условие и является условием цепного
самовоспламенения.
Самовозгорание. Температура самовоспламенения горючих веществ очень разнообразна. У некоторых веществ она превышает 600°, у других — ниже обычной.
На основании температуры самовоспламенения все горючие вещества разбиты на две группы: вещества, имеющие температуру самовоспламенения выше температуры окружающей их среды, и вещества, имеющие температуру самовоспламенения ниже температуры окружающей среды. Вещества первой группы способны самовоспламеняться только в результате нагрева извне. Вещества же второй группы могут самовоспламеняться без нагрева, так как окружающая их среда уже нагрела их до температуры самовоспламенения. Такие вещества представляют большую пожарную опасность и называются самовозгорающимися веществами, а процесс самонагревания их до возникновения горения — самовозгоранием.
Как видно из изложенного, самовозгорание и самовоспламенение — одно и то же явление, но только первый термин относят к процессу возникновения горения веществ, имеющих температуру самовоспламенения ниже температуры окружающей среды, а второй — выше.
Самовозгорающиеся вещества по причинам выделения тепла подразделяются на три группы.
Вещества, самовозгорающиеся от воздействия на них воздуха. К этой группе самовозгорающихся веществ относятся: растительные масла и животные жиры, нанесенные тонким слоем на волокнистые и порошкообразные материалы, бурые и каменные угли, сульфиды железа, фрезерный торф, растительные продукты (сено, опилки, листья), желтый фосфор, цинковая и алюминиевая пыли, сажа,
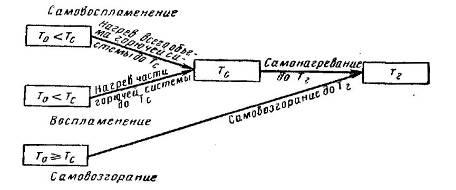
Рис. 18-3. Схема процесса возникновения горения
свежеприготовленный древесный уголь, металлоорганичёские соединения, порошок эбонита и др.
2. Вещества, вызывающие горение при соприкосновении с водой. К этой группе относятся: щелочные металлы (калий, натрий и др.), карбид кальция и карбиды щелочных металлов, негашеная известь, гидросульфит натрия, сесквихлорид и др.
3. Химические вещества, самовозгорающиеся при смешении друг с другом. В эту группу веществ входят газообразные, жидкие и твердые окислители: кислород сжатый, галоиды, азотная кислота, перекись натрия и бария, марганцевокислый калий, хромовый ангидрид, селитры, хлораты и др. Перечисленные окислители в большинстве случаев вызывают самовозгорание органических веществ при смешении или соприкосновении.
Воспламенение. Процесс возникновения горения, происходящий в результате нагрева источником воспламенения небольшой части горючего вещества, называется воспламенением.
Физическая сущность процесса воспламенения не отличается от процесса самовоспламенения, так как условия самоускорения реакции окисления у них одни и те же. Основное отличие между ними заключается в том, что процесс воспламенения пространственно ограничен частью объема горючего вещества, в то время как процесс самовоспламенения происходит во всем его объеме.
На рис.18-3 показана
схема процесса возникновения горения.
На ней можнo
видеть, что вне зависимости от положения
температуры горючих веществ ![]() относительно их температуры
самовоспламенения Тс(То<Тс,
относительно их температуры
самовоспламенения Тс(То<Тс, ![]() )
в процессе возникновения горения
существует общая для всех их стадия
самонагревания, которая начинается с
температуры самовоспламенения Tс
и заканчивается температурой горения
)
в процессе возникновения горения
существует общая для всех их стадия
самонагревания, которая начинается с
температуры самовоспламенения Tс
и заканчивается температурой горения
![]() .
.
Следовательно, тепловой процесс возникновения горения в природе один и назван он самовоспламенением. Самовозгорание же и воспламенение являются частными случаями этого общего процесса.
