
Лекция 9
.docxВТОРАЯ ФАЗА МЕТАБОЛИЗМА - КОНЪЮГАЦИЯ
Основные функции этой фазы те же, что и первой: увеличение гидрофильности и снижение токсичности ксенобиотиков.
Превращение молекул в первой фазе биотрансформации усиливает их полярность, уменьшает способность растворяться в липидах. Уже только благодаря этому целый ряд чужеродных соединений лучше выделяется с мочой.
Эффект еще более усиливается, когда к образовавшимся в ходе 1 фазы метаболизма продуктам присоединяются такие эндогенные вещества, как ацетат, сульфат, глюкуроновая кислота, глутатион (важен в качестве гидрофильной молекулы, которая присоединяется ферментами печени к гидрофобным токсическим веществам в процессе их биотрансформации с целью выведения из организма (в составе желчи). Как часть глиоксалазной ферментативной системы глутатион участвует в реакции детоксификации метилглиоксаля, токсического побочного продукта метаболизма).
Как и ферменты l фазы метаболизма ксенобиотиков, ферменты ll фазы обладают слабой субстратной специфичностью и участвуют в превращениях большой группы химических веществ.
Рассматриваемую группу энзимов можно классифицировать следующим образом:
1. Энзимы, формирующие эфирные или амидные связи с промежуточными метаболитами:
- ацетил КоА: амин N-ацетилтрансфераза;
- сульфотрансфераза;
- УДФ-глюкуронозилтрансфераза (уридиндифосфат).
2. Энзимы, активирующие конъюгацию веществ с глутатионом:
- глутатион S-трансферазы.
3. Энзимы, активирующие конъюгацию веществ с цистеином:
-
цистеин-конъюгирующие
![]() -лиазы.
-лиазы.
Конъюгация включает реакции двух типов: I тип реакций - активируется конъюгирующее вещество, которое затем взаимодействует с ксенобиотиком. Происходит во всех тканях. II тип реакций - активируется ксенобиотик, который взаимодействует с конъюгирующим веществом. Происходит в печени и почках. Встречается редко.
Общая характеристика реакций конъюгации ксенобиотиков представлена в таблице :
|
Реакция |
Присоединяемый агент |
Функциональная группа ксенобиотика |
|
А. Реакции, протекающие при участии активированных форм присоединяемых агентов |
||
|
Конъюгация с глюкуроновой кислотой |
УДФ-глюкуроновая кислота |
-ОН; -СООН; NH2; -NR2; -SH; -CH |
|
Конъюгация с глюкозой |
УДФ-глюкоза |
-ОН; -SH; COOH; =NH |
|
Сульфатация |
ФАФС (3'-фосфоаденозин-5'-фосфосульфат) |
-ОН; -NH2; -SH |
|
Метилирование |
S-аденозилметионин |
-ОН; -NH2 |
|
Ацетилирование |
Ацетил КоА |
-ОН; -NH2 |
|
Детоксикация цианида |
Сульфон-сульфид |
-CN- |
|
Б. Реакции, протекающие при участии активированных форм ксенобиотиков |
||
|
Конъюгация с глутатионом |
Глутатион |
Ареноксиды; эпоксиды; галогенированные алкильные и арильные углеводороды |
|
Конъюгация с аминокислотами |
Глицин; глутамин; орнитин; таурин; цистеин |
-СООН |
Первый тип реакций конъюгации.
1) Конъюгация с глюкуроновой кислотой; источником является УДФ-глюкуроновая (уридиндифосфат) кислота. Глюкуронидной конъюгации подвергаются природные соединения (билирубин, стероидные гормоны и др.), ксенобиотики (фенолы, стероиды, морфин, левомицетин, зидовудин – лекарство от СПИДа). В реакцию вступают субстраты, которые имеют гидроксильную, карбоксильную или аминогруппу. Процесс конъюгации приводит к образованию эфиров глюкуроновой кислоты - глюкуронидов. Ферменты - УДФ-глюкуронилтрансферазы локализованы в эндоплазматической сети клеток печени, в меньшей степени - в почках, пищеварительном тракте, коже.
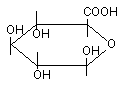 глюкур
к-та
глюкур
к-та
RXH
+ УДФ-глюкуронат —► RX-глюкуронид + УДФ
2) Сульфатная конъюгация; активной формой серной кислоты является 3'-фосфоаденозин-5'-фосфосульфат (ФАФС). Сульфатной конъюгации подвергаются эндогенные токсические продукты гниения белков в кишечнике (индол, скатол, фенолы), а также стероиды, йодтиронины, токоферолы, нафтохиноны и др. Как правило, вещества должны быть циклическими соединениями, имеющими свободные аминные или гидроксильные группы. Происходит, в основном, в печени. Ферменты - сульфотрансферазы.
RXH
+ ФАФ~S03Н
-> RX-SO3H
+ ФАФ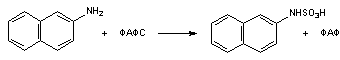
Запасы ФАФС в печени незначительны, легко истощаются, что при высоких токсических нагрузках приводит к переключению метаболизма на другие пути, в частности в сторону образования продуктов глюкуронидирования. Сульфатация, таким образом, является системой с "высоким сродством, но малой мощностью", глюкуронидирование, напротив - с "малым сродством, но высокой мощностью".
3) Ацетильная конъюгация. Происходит в печени, а также в слизистой пищеварительного тракта и в ретикулоэндотелиальных клетках селезенки и легких. Источник ацетильных групп - ацетил-КоА. Ферменты -ацетилтрансферазы. Этому типу конъюгации подвергаются вещества, имеющие свободную аминогруппу (серотонин, гистамин, сульфаниламиды, гидразиды изоникотиновой кислоты и др.).
R-NH2 + ацетил-КоА -> R-NH-CO-CH3 + HS-KoA.
4) Метильная конъюгация; В качестве донора метильной группы выступает метионин в форме S-аденозилметионина (SАМ), ферменты - метилтрансферазы. Метильной конъюгации подвергаются фенолы, амины, тиоловые соединения. Образуются соответственно О-, N- и S-метиловые конъюгаты. Процесс наиболее интенсивен в печени.
R-OH + СНз-SAM -> R-O-CH3 + SАМ
Среди эндогенных веществ, таким образом, метаболизируют адреналин, норадреналин, дофамин. При этом образуются малоактивные 3-метоксипроизводные катехоламинов.
5) Тиосульфатная конъюгация используется при обезвреживании
цианидов. Конъюгирующим веществом является сера тиосульфата. Источником тиосульфата в тканях являются серосодержащие аминокислоты. Конъюгация происходит с цианидами неорганического (синильная кислота, цианиды натрия, калия) и органического (ацетонитрил, акрилонитрил, бензилцианид и др.) происхождения.
Второй тип реакций конъюгации
1) Конъюгация с глутатионом и цистеином. Алифатические и ароматические соединения, содержащие в молекуле атомы галогенов, в организме могут взаимодействовать с SH-содержащими эндогенными соединениями: цистеином, ацетилцистеином, глутатионом и т.д.
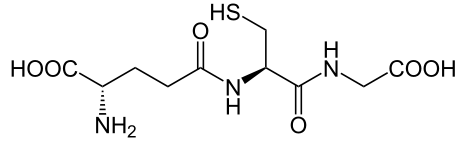 глутатион
глутатион
Реакции
конъюгации глутатиона с ксенобиотиками
катализируют ферменты глутатион-S-трансферазы
(GST). Хотя GST обнаружены практически во
всех тканях организма млекопитающих,
их уровень в печени - максимален. В этом
органе GST составляет до 10% общего
количества ферментов. Их активность
индуцируется при поступлении в организм
различных ксенобиотиков. В подавляющем
большинстве случаев взаимодействие
ксенобиотиков с глутатионом приводит
к их детоксикации.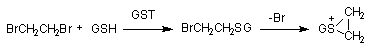
Однако известны примеры активации. Так, конъюгация глутатиона с 1,2-дигалогеналканами (дихлорэтан, дибромэтан) приводит к образованию продукта: S-(2-галогеналкан), который в дальнейшем превращается в активный циклический эписульфониум-ион:
Рисунок Биоактивация дибромэтана при участии глутатион-S-трансферазы
2) Реакции конъюгации с аминокислотами. Предварительно происходит активация ксенобиотика (ароматических и гетероциклических карбоновых кислот). Глициновые конъюгаты обозначают как «гиппуровые» кислоты.
Аналогичным образом происходит взаимодействие ксенобиотиков с цистеином и ацетилцистеином:
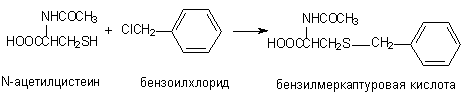
Функционирование всех ферментов второй фазы ограничивается тем, что они метаболизируют только те вещества, которые имеют функциональные группы. Именно поэтому эти ферменты чаще включаются после образования или освобождения функциональных групп ферментами первой фазы, то есть во второй фазе метаболизма ксенобиотиков.
Однако трансферазы имеют важные достоинства: 1) они есть во всех клетках, 2) функционируют при любых путях поступления ксенобиотиков в организм, 3) осуществляют или завершают детоксикацию, а иногда исправляют ошибки первой фазы. Так, они обезвреживают токсичные метаболиты ПАУ (канцерогены), хлороформа (фосген), парацетамола. Правда, теперь обнаружено, что и эти ферменты могут токсифицировать некоторые ксенобиотики, но это встречается реже, чем для системы цитохрома Р-450.
Элиминация - связывание, транспорт и выведение ксенобиотиков.
Эти процессы чаще носят физический характер. В плазме крови огромное количество как эндогенных (жирные кислоты, свободный билирубин), так и экзогенных веществ (сульфаниламиды, антибиотики, салицилаты, сердечные гликозиды, противосвертывающие) связывается и транспортируется альбумином. Некоторые вещества (жирорастворимые витамины, анаболические стероиды) переносят липопротеины. В клетках, особенно печени, многие ксенобиотики (ПАУ, канцерогены, нитропроизводные, антибиотики) связываются (некоторые ковалентно) глутатионтрансферазами. Металлы связываются SH-группами глутатиона и небольшого белка металлотионеина, очень богатого остатками цистеина. Связанные ксенобиотики неактивны, постепенно они освобождаются, метаболизируются и выводятся.
Очень важный механизм выведения из клетки ксенобиотиков — функционирование Р-гликопротеина. Когда гидрофобное вещество, в том числе противораковое лекарство, проникает в клетку, то оно удаляется из нее Р-гликопротеином за счет энергии гидролиза АТФ. Это снижает эффективность химиотерапии рака.
Большинство ксенобиотиков в результате метаболизма становятся более гидрофильными, поступают в плазму крови, откуда они удаляются почками с мочой. "Кооператив" печень — почки играет важнейшую роль в обезвреживании и выведении из организма большинства ксенобиотиков. Вещества более гидрофобные или с большой молекулярной массой (>300) чаще выводятся с желчью в кишечник и затем удаляются с калом.

Возможны и другие пути: через кожу (пот, кожное сало), легкие (выдыхаемый воздух), молочные железы (молоко), слюнные железы (слюна). Ксенобиотики выводятся из организма: 1) в неизменном виде; 2) в виде метаболитов; 3) в виде конъюгатов; 4) в комплексе с биомолекулами.
Элиминационное время полужизни - это время, которое требуется для уменьшения концентрации ксенобиотика на 50%. Обычно требуется 7 элиминационных времен полужизни для выведения 99% ксенобиотика и 10 элиминационных времен полужизни для выведения 99,9% ксенобиотика.
Факторы, влияющие на метаболизм ксенобиотиков:
генетические, физиологические, средовые и патологические факторы.
Генетические факторы включают конститутивные особенности метаболизма ксенобиотиков и наследуемые ферментопатии, связанные с метаболизмом лекарств. Особи одного и того же вида живых существ порой значительно различаются по способности метаболизировать ксенобиотики. Это во многом детерминировано генетически. Так, в популяции людей выявляются лица, обладающие пониженной активностью цитохромР-450 зависимых оксидаз. "Слабые метаболизанты" могут отличаться отсутствием некоторых изоэнзимов, необходимых для катализа ряда превращений ксенобиотиков.
Физиологические факторы (возраст, пол, состояние нейрогуморальной регуляции, циркадные ритмы) влияют на метаболизм ксенобиотиков. Возраст: до 2-месячного возраста метаболизм ксенобиотиков практически не происходит. В старческом возрасте замедляются и снижаются. Поэтому у детей чаще проявляются побочные и токсические эффекты лекарств, а у стариков повышена чувствительность к ряду лекарств. Пол: андрогены являются индукторами микросомального окисления и ферментов конъюгации; у мужчин лекарства обезвреживаются быстрее. Питание: голодание угнетает ферменты микросомального окисления и повышает вероятность интоксикации; при гиповитаминозах В1 и В2 снижаются гидроксилирование ксенобиотиков в печени. Биологические ритмы: днем активность ферментов микросомального окисления снижается, а в ночное время - увеличивается.
Факторы внешней среды (стресс, ионизирующая радиация, химические вещества и др.) оказывают влияние на метаболизм лекарств. Многие химические вещества-лекарства взаимодействуют между собой, а также способны индуцировать ферменты метаболизма ксенобиотиков. Ионизирующее излучение и эндотоксины снижают обезвреживающую способность монооксигеназной системы и глутатионтрансферазы. Стресс посредством глюкокортикоидов способен увеличивать активность ферментов метаболизма ксенобиотиков.
Патологические факторы, которые связаны с повреждением почек, печени, сердца (травмой, повреждением пищеварительного тракта, шоком).


