
- •1.Які елементи називаються біогенними елементами?
- •9.Яка реакція середовища у водному розчині ch3cooNa? Відповідь аргументувати.
- •10.Яка реакція середовища у водному розчині Na3po4? Відповідь аргументувати.
- •11. Яка реакція середовища у водному розчині ZnSo₄? Відповідь аргументуйте.
- •12. Яка реакція середовища у водному розчині (ch₃coo)₂Mg? Відповідь аргументуйте.
- •13. Яка реакція середовища у водному розчині nh₄Cl? Відповідь аргументуйте.
- •14. Яка реакція середовища у водному розчині k₂co₃? Відповідь аргументуйте.
- •15. Яка реакція середовища у водному розчині Fe(no₃)₂? Відповідь аргументуйте.
- •16. Яка реакція середовища у водному розчині AlCl₃? Відповідь аргументуйте.
- •17. Яка реакція середовища у водному розчині Na₂s? Відповідь аргументуйте.
- •18.Де краще розчиняється кисень: у воді чи у крові? Відповідь аргументуйте.
- •46.Що таке водневий показник? За якою формулою його обчислюють?
10.Яка реакція середовища у водному розчині Na3po4? Відповідь аргументувати.
1.Na₃PO₄ - це розчинна сіль, утворена слабкою кислотою H₃PO₄ та сильною основою NaOH → дана сіль зазнає гідролізу.
2.У водному розчині сіль дисоціює на іони:
Na₃PO₄ → 3Na⁺ + PO₄³⁻
З водою буде реагувати аніон PO₄³⁻, оскільки саме йому відповідає слабкий електроліт.
3.Перша стадія гідролізу:
PO₄³⁻ + Н₂О ↔ HPO₄ + ОН⁻ - скорочене іонне рівняння
Na₃PO₄ + H₂O ↔ Na₂HPO₄ + NaOH - молекулярне рівняння
Відповідь: Середовище розчину фосфату натрію лужне, оскільки в результаті гідролізу солі в розчині збільшується кількість іонів ОН⁻.
11. Яка реакція середовища у водному розчині ZnSo₄? Відповідь аргументуйте.
1.ZnSO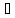 -це розчинна сіль, утворена
сильною кислотою H₂SO₄
та слабкою основою Zn(OH)₂
→ дана сіль
зазнає гідролізу.
-це розчинна сіль, утворена
сильною кислотою H₂SO₄
та слабкою основою Zn(OH)₂
→ дана сіль
зазнає гідролізу.
2.У водному розчині сіль дисоціює на іони:
ZnSO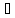 → Zn
→ Zn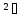 + SO₄²⁻
+ SO₄²⁻
З
водою буде реагувати катіон Zn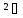 ,
оскільки саме йому
відповідає слабкий електроліт.
,
оскільки саме йому
відповідає слабкий електроліт.
3.Перша стадія гідролізу:
Zn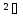 + H₂O
↔ Zn(OH)
+ H⁺
- скорочене іонне рівняння
+ H₂O
↔ Zn(OH)
+ H⁺
- скорочене іонне рівняння
ZnSO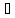 + H₂O
↔ Zn(OH)
+ HSO₄ -
молекулярне рівняння
+ H₂O
↔ Zn(OH)
+ HSO₄ -
молекулярне рівняння
Відповідь: Середовище розчину сульфату цинку кисле, оскільки в результаті гідролізу солі в розчині збільшується кількість іонів Н⁺.
12. Яка реакція середовища у водному розчині (ch₃coo)₂Mg? Відповідь аргументуйте.
1.(СН₃СОО)₂Mg - це розчинна сіль, утворена слабкою кислотою CH₃COOН та сильною основою Mg(OH)₂ → дана сіль зазнає гідролізу.
2.Уводному розчині сіль дисоціює на іони:
(СН₃СОО)₂Mg → 2CH₃COO⁻ + Mg²⁺
З водою буде реагувати аніон CH₃COO⁻, оскільки саме йому відповідає слабкий електроліт.
3.Перша стадія гідролізу:
CH₃COO⁻ + Н₂О ↔ CH₃COOН + ОН⁻ - скорочене іонне рівняння
(СН₃СОО)₂Mg + Н₂О ↔ CH₃COOH + Mg(OH)₂ - молекулярне рівняння
Відповідь: Середовище розчину ацетату магнію лужне, оскільки в результаті гідролізу солі в розчині збільшується кількість іонів ОН⁻.
13. Яка реакція середовища у водному розчині nh₄Cl? Відповідь аргументуйте.
1.NH₄Cl - це розчинна сіль, утворена сильною кислотою HCl та слабкою основою NH₄OH → дана сіль зазнає гідролізу.
2.Уводному розчині сіль дисоціює на іони:
NH₄Cl→NH₄⁺ + Cl⁻
З водою буде реагувати катіон NH₄⁺, оскільки саме йому відповідає слабкий електроліт.
3.Перша стадія гідролізу:
NH₄⁺ + Н₂О ↔ NH₄(ОН) + Н⁺ - скорочене іонне рівняння
NH₄Cl + Н₂О ↔ NH₄(ОН) + HCl – молекулярне рівняння
Відповідь: Середовище розчину хлориду амонію кисле, оскільки в результаті гідролізу солі в розчині збільшується кількість іонів Н⁺.
14. Яка реакція середовища у водному розчині k₂co₃? Відповідь аргументуйте.
|
1. K₂CO₃ - розчинна сіль, утворена слабкою кислотою Н₂CO₃ та сильною основою KOH→ дана сіль зазнає гідролізу. 2. У водному розчині сіль дисоціює на йони: K₂CO₃ → 2К⁺ + CO₃ ²⁻ З водою буде реагувати аніон CO₃ ²⁻, оскільки саме йому віповідає слабкий електроліт. 3. Перша стадія гідролізу: CO₃ ²¯ + Н₂О ↔ НCO₃ ¯ + ОН ¯ - скорочене йонне рівняння K₂CO₃ + Н₂О ↔ КОН + Н₂О + СО₂ - молекулярне рівнянняВідповідь:Середовище розчину калій карбонату лужне, оскільки в результаті гідролізу солі в розчині збільшується кількість іонів ОН¯. |
|
|
