
2 курс / Нормальная физиология / ФЗЛ ЧЕЛОВЕКА
.pdfнужных для жизнедеятельности веществ (органы пищеварения и дыхания) и удаление из организма продуктов обмена (почки, кожа, кишечник). Кроме того, будет изложен материал о системах транспорта веществ в организме (кровь, кровообращение, движение лимфы), а также барьерных функциях и, кроме того, тех процессах обмена веществ и энергии, которые традиционно изучаются в курсе физиологии, т. е. на уровне органов, систем и целостного организма.
Г л а в а 9
ФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
Кровь, лимфа и тканевая жидкость образуют внутреннюю среду организма, омывающую все клетки и ткани тела. Внутренняя среда имеет относительное постоянство состава и физико-химических свойств, что создает приблизительно одинаковые условия существования клеток организма (гомеостаз). Это достигается деятельностью ряда органов, обеспечивающих поступление в кровь необходимых организму веществ и удаление из крови продуктов распада.
Представление о крови как системе создал наш соотечественник Г. Ф. Ланг в 1939 г. В эту систему он включил 4 части: 1) периферическую кровь, циркулирующую по сосудам; 2) органы кроветворения (красный костный мозг, лимфатические узлы и селезенку); 3) органы кроверазрушения; 4) регулирующий нейрогуморальный аппарат.
Система крови представляет собой одну из систем жизнеобеспечения организма
ивыполняет множество функций: ■■.
1.Транспортная функция. Циркулируя по сосудам, кровь осуществляет транспорт ную функцию, которая определяет ряд других.
2.Дыхательная функция. Эта функция заключается в связывании и переносе О2
иСО2.
3.Трофическая (питательная) функция. Кровь-обеспечивает все клетки организма
питательными веществами: глюкозой, аминокислотами, жирами, витаминами, минераль ными веществами, водой.
4.Экскреторная функция. Кровь уносит из тканей «шлаки жизни» — конечные про дукты метаболизма: мочевину, мочевую кислоту и другие вещества, удаляемые из орга низма органами выделения.
5.Терморегуляторная функция. Кровь охлаждает энергоемкие органы и согревает органы, теряющие тепло.
6.Кровь поддерживает стабильность ряда констант гомеостаза — рН, осмотическое давление, изоионию и др.
7.Кровь обеспечивает водно-солевой обмен между кровью и тканями. В артериаль ной части капилляров жидкость и соли поступают в ткани, а в венозной части капил ляров возвращается в кровь.
8.Защитная функция. Кровь выполняет защитную функцию, являясь важнейшим фактором иммунитета, т. е. защиты организма от живых тел и генетически чуждых ве ществ. Это определяется фагоцитарной активностью лейкоцитов (клеточный иммунитет)
иналичием в крови антител, обезвреживающих микробы и их яды (гуморальный иммунитет). Эту задачу выполняет также бактерицидная пропердиновая система.
9.Гуморальная регуляция. Благодаря своей транспортной функции кровь обеспечи вает химическое взаимодействие между всеми частями организма, т.е. гуморальную регу ляцию. Кровь переносит гормоны и другие физиологически активные вещества от кле ток, где они образуются, к другим клеткам.
10.Осуществление креаторных связей. Макромолекулы, переносимые плазмой и форменными элементами крови, осуществляют межклеточную передачу информации, обеспечивающую регуляцию внутриклеточных процессов синтеза белков, сохранение сте пени дифференцированности клеток, восстановление и поддержание структуры тканей.
211
СОСТАВ, КОЛИЧЕСТВО И ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА КРОВИ
СОСТАВ И КОЛИЧЕСТВО КРОВИ
Кровь состоит из жидкой части — плазмы и взвешенных в ней клеток (форменных элементов): эритроцитов (красных кровяных телец), лейкоцитов (белых кровяных телец) и тромбоцитов (кровяных пластинок).
Между плазмой и форменными элементами крови существуют определенные объемные соотношения. Их определяют с помощью гематокрита— специального стеклянного капилляра, разделенного на 100 равных частей. При центрифугировании крови в гематокрите более тяжелые форменные элементы отбрасываются центробежными силами от оси вращения, а ближе к ней располагается плазма. Таким путем установлено, что на долю форменных элементов приходится 40—45 % крови, а на долю плазмы — 55—60%.
Общее количество крови в организме взрослого человека в норме составляет 6—8% массы тела, т.е. примерно 4,5—6 л.
Объемциркулирующей крови относительно постоянен, несмотря на непрерывное всасывание воды из желудка и кишечника. Это объясняется строгим балансом между поступлением и выделением воды из организма. Если в кровь сразу поступает большое количество воды (например, при введении в сосуды кровезамещающей жидкости), часть ее выводится почками немедленно, а большая часть переходит в ткани, откуда постепенно возвращается в кровь и выделяется почками. При недостаточном потреблении жидкости вода из тканей переходит в кровь, а образование мочи уменьшается. Резкое уменьшение массы крови в результате обильного кровотечения, например потеря '/з ее объема, может привести к гибели. В таких случаях необходимо срочное переливание крови или кровезаменяющей жидкости.
ВЯЗКОСТЬ И ОТНОСИТЕЛЬНАЯ ПЛОТНОСТЬ КРОВИ
Если вязкость воды принять за единицу, то вязкость плазмы крови равна 1,7—2,2, а вязкость цельной крови — около 5. Вязкость крови обусловлена наличием белков и особенно эритроцитов, которые при своем движении преодолевают силы внешнего и внутреннего трения. Вязкость увеличивается при сгущении крови, т.е. потере воды (например, при поносах или обильном потении), а также при возрастании количества эритроцитов в крови.
Относительная плотность (удельный вес) цельной крови равен 1,050—1,060, эритро-
цитов — 1,090, плазмы — 1,025—1,034.
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ КРОВИ
Если два раствора разной концентрации разделить полупроницаемой перепонкой, пропускающей только растворитель (например, воду), то вода переходит в более концентрированный раствор. Сила, определяющая движение растворителя через полупроницаемую мембрану, называется осмотическим давлением.
Осмотическое давление крови, лимфы и тканевой жидкости определяет обмен воды между кровью и тканями. Изменение осмотического давления жидкости, окружающей клетки, ведет к нарушениям в них водного обмена. Это видно на примере эритроцитов, которые в гипертоническом растворе NaCl теряют воду и сморщиваются. В гипотоническом растворе NaCl эритроциты, наоборот, набухают, увеличиваются в объеме и могут разрушиться.
Осмотическое давление крови можно определить криоскопически, т.е. измерением температуры замерзания. Она, как известно, тем ниже, чем выше в растворе суммарная концентрация мелких молекул и ионов.
212
У человека температура замерзания крови ниже нуля на 0,56—0,58 °С. При таком понижении температуры замерзания раствора его осмотическое давление равно 7,6 атм. Около 60 % этого давления приходится на долю NaCl. Величина осмотического давления эритроцитов и всех других клеток организма такая же, как окружающей их жидкости.
Осмотическое давление крови млекопитающих и человека довольно постоянное, несмотря на небольшие его колебания вследствие перехода из крови в ткани крупномолекулярных веществ (аминокислот, жиров, углеводов) и поступления из тканей в кровь низкомолекулярных продуктов клеточного метаболизма.
В регуляции осмотического давления участвуют органы выделения, главным образом почки и потовые железы. Благодаря им вода, поступающая в организм, и продукты обмена, образующиеся в организме, выводятся с мочой и потом, не вызывая существенных сдвигов осмотического давления. Осморегулирующая деятельность выделительных органов регулируется сигналами от осморецепторов, т. е. специализированных образований, которые активируются при изменении осмотического давления крови и тканевой жидкости. В отличие от крови осмотическое давление мочи и пота колеблется в довольно широких пределах. Температура замерзания пота на 0,18—0,6 ° ниже нуля, а мочи — на
0,2—2,2°.
РЕАКЦИЯ КРОВИ И ПОДДЕРЖАНИЕ ЕЕ ПОСТОЯНСТВА
Активная реакция крови (рН), обусловленная соотношением в ней водородных (Н+) и гидроксильных (ОН-) ионов, является одним из жестких параметров гомео-
стаза, так как только при определенном РН возможно оптимальное течение обмена веществ.
Кровь имеет слабо щелочную реакцию. рН артериальной крови равен 7,4; рН венозной крови вследствие большого содержания в ней углекислоты составляет 7,35. Внутри клеток рН несколько ниже (7,0—7,2), что зависит от образования в них при метаболизме кислых продуктов. Крайними пределами изменений рН, совместимыми с жизнью, являются величины от 7,0 до 7,8. Смещение рН за эти пределы вызывает тяжелые нарушения и может привести к смерти. У здоровых людей рН крови колеблется в пределах 7,35—7,40. Длительное смещение рН у человека даже на 0,1—0,2 может оказаться гибельным.
В процессе метаболизма в кровь непрерывно поступают углекислота, молочная кислота и другие продукты обмена, изменяющие концентрацию водородных ионов. Однако рН крови сохраняется постоянным, что объясняется буферными свойствами плазмы и эритроцитов, а также деятельностью легких и органов выделения, удаляющих из организма избыток СО2, кислот и щелочей.
Буферные свойства крови обусловлены тем, что в ней содержатся: 1) буферная система гемоглобина, 2) карбонатная буферная система, 3) фосфатная буферная система и 4) буферная система белков плазмы.
Буферная система гемоглобина самая мощная. На ее долю приходится 75 % буферной емкости крови. Эта система состоит из восстановленного гемоглобина (ННв) и его калиевой соли (КНв). Буферные свойства ННв обусловлены тем, что он, будучи более слабой кислотой, чем Н2СО3, отдает ей ион К+, а сам, присоединяя ионы Н+, становится очень слабо диссоциирующей кислотой. В тканях система гемоглобина крови выполняет функции щелочи, предотвращая закисление крови вследствие поступления в нее СО2 и Н+- ионов. В легких гемоглобин крови ведет себя как кислота, предотвращая защелачи-вание крови после выделения из нее углекислоты.
Карбонатная буферная система (Н2СО3+NaНСО3) по своей мощности занимает второе место после системы гемоглобина. Она функционирует следующим образом: NaHCO3 диссоциирует на ионы Na+ и НСО3-. При поступлении в кровь более сильной кислоты, чем угольная, происходит реакция обмена ионами Na+ с образованием слабодиссоциирующей и легкорастворимой Н2СО3. Таким образом предотвращается повышение концентрации Н+-ионов в крови. Увеличение в крови содержания угольной кислоты приводит к тому, что ее ангидрит — углекислый газ — выделяется легкими. В результате
213
этих процессов поступление кислоты в кровь приводит лишь к небольшому временному повышению содержания нейтральной соли без сдвига рН. В случае поступления в кровь щелочи она реагирует с угольной кислотой, образуя бикарбонат NaHCCb и воду. Возникающий при этом дефицит угольной кислоты немедленно компенсируется уменьшением выделения СОг легкими.
Хотя в исследованиях in vitro удельный вес бикарбонатного буфера по сравнению с гемоглобином слабее, в действительности же его роль в организме весьма ощутима. Это обусловлено тем, что связанное с действием этой буферной системы усиленное выведение СОг легкими и выделение NaCl мочой — весьма быстрые проЦессы, почти мгновенно восстанавливающие рН крови.
Фосфатная буферная система образована дигидрофосфатом (ЫаНгРС^) и гидрофосфатом (Na2HPC>4) натрия. Первое соединение слабо диссоциирует и ведет себя как слабая кислота. Второе соединение обладает щелочными свойствами. При введении в
кровь более сильной кислоты она реагирует с ЫаНгРО4, образуя нейтральную соль и увеличивая количество, малодиссоциирующего дигидрофосфата натрия. В случае введения в кровь сильной щелочи она реагирует с дигидрофосфатом натрия, образуя слабо щелочной гидрофосфат натрия. рН крови изменяется при этом незначительно. В обоих случаях избыток дигидрофосфата или гидрофосфата натрия выделяется с мочой.
Белки плазмы играют роль буферной системы благодаря своим амфотерным свойствам. В кислой среде они ведут себя как щелочи, связывая кислоты. В щелочной среде белки реагируют как кислоты, связывающие щелочи.
В поддержание рН крови, помимо легких, участвуют почки, удаляющие из организма избыток как кислот, так и щелочей. При сдвиге рН крови в кислую сторону почки выделяют с мочой увеличенное количество кислой соли NahbPC^. При сдвиге в щелочную сторону почки увеличивают выделение щелочных солей: №гНРСи и №гСОз. В первом случае моча становится резко кислой, во втором — щелочной (рН мочи в норме колеблется от 4,7 до 6,5, а при нарушениях кислотно-щелочного равновесия крови может изменяться в пределах 4,5—8,5).
Выделение небольшого количества, молочной кислоты осуществляется также потовыми железами.
Буферные системы имеются и в тканях, где они сохраняют рН на относительно постоянном уровне. Главными буферами тканей являются клеточные белки и фосфаты. В процессе метаболизма кислых продуктов образуется больше, чем щелочных, поэтому опасность сдвига рН в сторону закисления более велика. В соответствии с этим буферные системы крови и тканей более устойчивы к действию кислот, чем щелочей. Так, для сдвига рН плазмы крови в щелочную сторону требуется прибавить к ней в 40—70 раз больше NaOH, чем к чистой воде. Для сдвига же рН в кислую сторону необходимо добавить к плазме в 300—350 раз больше НС1, чем к воде. Щелочные соли слабых кислот, содержащиеся в крови, образуют так называемый щелочной резерв крови. Величину его определяют по тому количеству миллилитров углекислоты, которое может быть связано 100 мл крови при давлении СОг, равном 40 мм рт.ст., т.е. примерно соответствующем его давлению в альвеолярном воздухе.
Постоянное соотношение между кислотными и щелочными эквивалентами позволяет говорить о кислотно-щелочном равновесии крови.
Несмотря на наличие буферных систем и хорошую защищенность организма от возможных изменений рН, все же иногда при некоторых условиях наблюдаются небольшие сдвиги активной реакции крови. Сдвиг рН в кислую сторону называется ацидозом, сдвиг в щелочную сторону — алкалозом.
Изменения щелочного резерва крови и небольшие колебания ее рН всегда происходят в капиллярах большого и малого кругов кровообращения. Так. поступление СОа в кровь тканевых капилляров закисляет венозную кровь на 0,01—0,05 по сравнению с артериальной кровью. Противоположный сдвиг рН наблюдается в легочных капиллярах вследствие перехода ССЬ в альвеолярный воздух.
214
СОСТАВ ПЛАЗМЫ КРОВИ
Плазма крови содержит 90—92 % воды и 8—10 % сухого вещества, главным образом белков и солей. В плазме находится ряд белков, отличающихся по своим свойствам и функциональному значению: альбумины (около 4,5%), глобулины (2—3%) и
фибриноген (0,2—0,4%).
Общее количество белка в плазме крови человека составляет 7—8 %. Остальная часть плотного остатка плазмы приходится на долю других органических соединений
иминеральных солей.
Вплазме находятся также небелковые азотсодержащие соединения (аминокислоты
ипол и пептиды), всасывающиеся в пищеварительном тракте и используемые клетками для синтеза белков. Наряду с ними в крови находятся продукты распада белков и нуклеиновых кислот (мочевина, креатин, креатинин, мочевая кислота), подлежащие выведению из организма.
Половина общего количества небелкового азота в плазме — так называемого остаточного азота приходится на долю мочевины. При недостаточности функции почек содержание остаточного азота в плазме крови увеличивается.
В плазме находятся также безазотистые органические вещества: глюкоза 4,4—6,7 ммоль/л, или (80—120 мг %), нейтральные жиры и липоиды.
Минеральные вещества плазмы крови составляют около 0,9 %. Они представлены преимущественно катионами Na+, К+, Са2+, и анионами С1-, НСОз-, НРО42-
Содержание органических и неорганических веществ плазмы крови поддерживается на относительно постоянном уровне за счет деятельности различных регулирующих систем организма.
Значение минерального состава плазмы и кровезамещающие растворы
Искусственные растворы, имеющие одинаковое с кровью осмотическое давление, называются изоосмотическими, или изотоническими. Для теплокровных животных и человека изотоническим раствором является 0,9 % раствор NaCl. Такой раствор называют физиологическим. Растворы, имеющие большее осмотическое давление, чем кровь, называются гипертоническими, а меньшее — гипотоническими.
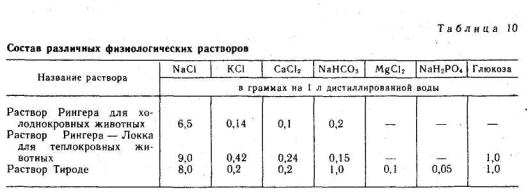
Изотонический раствор NaCl может некоторое время поддерживать жизнедеятельность отдельных органов, например изолированного (вырезанного из организма) сердца лягушки. Однако этот раствор не является полностью физиологическим. Разработаны рецепты растворов, соответствующие своим составом содержанию отдельных солей в плазме. Они являются в большей мере физиологическими, чем изотонический раствор NaCl. Наибольшее распространение получили растворы Рингера, Рингера-Локка и Тироде (табл. 10).
215
Для поддержания деятельности изолированных органов теплокровных животных физиологические растворы насыщают кислородом и добавляют к ним глюкозу. Однако указанные растворы не содержат коллоидов (которыми являются белки плазмы) и быстро выводятся из кровеносного русла, т.е. восполняют объем потерянной крови на очень короткое время. Поэтому в последние годы созданы синтетические коллоидные кровезаменители (реополиглюкин, желатиноль, гемодез, полидез, неокомпенсан и др.), которые вводят человеку после кровопотери и по другим показаниям для нормализации объема крови и артериального давления. Однако идеального кровезаменителя типа «искусственная кровь» пока не создано.
БЕЛКИ ПЛАЗМЫ КРОВИ
Значение белков плазмы крови многообразно: 1) они обусдовливают онкотическое давление, которое определяет обмен воды между кровью и тканями; 2) обладая буферными свойствами, поддерживают рН крови; 3) обеспечивают вязкость плазмы крови, имеющую важное значение в поддержании артериального давления; 4) препятствуют оседанию эритроцитов; 5) участвуют в свертывании крови; 6) являются необходимыми факторами иммунитета; 7) служат переносчиками ряда гормонов, минеральных веществ, липидов, холестерина; 8) представляют собой резерв для построения тканевых белков; 9) осуществляют креаторные связи, т.е. передачу информации, влияющей на генетический аппарат клеток и обеспечивающей процессы роста, развития, дифференцировки и поддержания структуры организма (примерами таких белков являются так называемые «фактор роста нервной ткани», эритропоэтины и т.д.).
Молекулярная масса, сравнительные размеры и форма белковых молекул крови приведены на рис. 111. Как видно из рисунка, размеры молекулы альбумина близки к размерам гемоглобина. Молекула глобулина обладает большими размерами и массой, а Наибольшую молекулярную массу имеет комплекс белка с липидами — липопротеиды. Изменение свойств и структуры липопротеидов играет важную роль в развитии «ржавчины жизни» — атеросклероза. Молекула фибриногена имеет удлиненную форму, что облегчает образование длинных нитей фибрина при свертывании крови.
В плазме крови содержится несколько десятков различных белков, которые составляют 3 основные группы: альбумины, глобулины и фибриноген. Для разделения белков плазмы применяют метод электрофореза, основанный на неодинаковой скорости движения разных белков в электрическом поле. С помощью этого метода глобулины разделены на несколько фракций: α1-, α2-, β-, γ-глобулины. Электрофореграмма белков плазмы приведена на рис. 112.
В последние годы применяют более тонкий метод разделения белков плазмы крови — иммуноэлектрофорез, при котором в электрическом поле передвигаются не нативные белки, а комплексы белковых молекул, связанных со специфическими антителами. Это позволило выделить гораздо большее количество белковых фракций.
Онкотическое давление плазмы крови
Осмотическое давление, создаваемое белками, (т. е. их способностью притягивать воду), называется онкотическим давлением.
Абсолютное количество белков плазмы крови равно 7—8 % и почти в 10 раз превосходит количество кристаллоидов, но создаваемое ими онкотическое давление составляет лишь '/200 осмотического давления плазмы (равного 7,6 атм), т.е. 0,03—0,04 атм (25—30 мм рт. ст.). Это обусловлено тем, что молекулы белков очень велики и число их в плазме во много раз меньше числа молекул кристаллоидов.
В наибольшем количестве содержатся в плазме альбумины. Величина их молекулы меньше чем молекулы глобулинов и фибриногена, а содержание заметно больше, поэтому онкотическое давление плазмы более чем на 80 % определяется альбуминами.
216

Несмотря на свою малую величину, онкотическое давление играет решающую роль в обмене воды между кровью и тканями. Оно влияет на процессы образования тканевой жидкости, лимфы, мочи, всасывания воды в кишечнике. Крупные молекулы белков плазмы, как правило, не проходят через эндотелий капилляров. Оставаясь в кровотоке, они удерживают в крови некоторое количество воды (в соответствии с величиной их онкотического давления).
При длительной перфузии изолированных органов растворами Рингера или РингераЛокка наступает отек тканей. Если заменить физиологический раствор кристаллоидов кровяной сывороткой, то начавшийся отек исчезает. Именно поэтому в состав кровезамещающих растворов необходимо вводить коллоидные вещества. При этом онкотическое давление и вязкость подобных растворов подбирают так, чтобы они были равны этим параметрам крови.
СВЕРТЫВАНИЕ КРОВИ
Жидкое состояние крови и замкнутость (целостность) кровеносного русла являются необходимыми условиями жизнедеятельности. Эти условия создает система свертывания крови (система гемокоагуляции), сохраняющая циркулирующую кровь в жидком состоянии и восстанавливающая целостность путей ее циркуляции посредством образования кровяных тромбов (пробок, сгустков) в поврежденных сосудах.
Всистему гемокоагуляции входит кровь и ткани, которые продуцируют, используют
ивыделяют из организма необходимые для данного процесса вещества, а также нейрогуморальный регулирующий аппарат.
Знание механизмов свертывания крови необходимо для понимания причин ряда заболеваний и возникновения осложнений, связанных с нарушением гемокоагуляции. В настоящее время более 50 % людей умирает от болезней, обусловленных нарушением свертывания крови (инфаркт миокарда, тромбоз сосудов головного мозга, тяжелые кровотечения в акушерской и хирургической клиниках и др.).
Основоположником современной ферментативной теории свертывания крови являет-
ся профессор Дерптского (Юрьевского, а ныне Тартуского) университета А. А. Шмидт (1872). Его теорию поддержал и уточнил П. Моравиц (1905).
За столетие, прошедшее после создания теории Шмидта-Моравица, она была значительно дополнена. Сейчас считают, что свертывание крови проходит 3 фазы: 1) образова-
217
ние протромбиназы, 2) образование тромбина и 3) образование фибрина. Кроме них, выделяют предфазу и послефазу гемокоагуляции. В предфазу осуществляется сосудистотромбоцитарный гемостаз (этим термином называют процессы, обеспечивающие остановку кровотечений), способный прекратить кровотечение из микроциркуляторных сосудов с низким артериальным давлением, поэтому его называют также микроциркуляторным гемостазом. Послефаза включает в себя два параллельно протекающих процесса — ретракцию (сокращение, уплотнение) и фибринолиз (растворение) кровяного сгустка. Таким образом, в процесс гемостаза вовлечены 3 компонента: стенки кровеносных сосудов, форменные элементы крови и плазменная ферментная система свертывания плазмы.
ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
Международный комитет по номенклатуре факторов свертывания крови обозначил плазменные факторы римскими цифрами в порядке их хронологического открытия.
Фактор I—фибриноген — представляет собой самый крупномолекулярный белок плазмы, образуется в печени, его концентрация в крови составляет 200—400 мг %. При свертывании крови фибриноген из состояния золя переходит в гель — фибрин, образующий основу кровяного сгустка. Содержание фибриногена резко возрастает при беременности, в послеоперационном периоде, при всех воспалительных процессах и инфекционных заболеваниях. Во время менструации, а также при болезнях печени его концентрация уменьшается. Кроме участия в гемостазе, фибрин служит структурным материалом для заживления ран.
Фактор II —протромбин — является глюкопротеидом, образуется клетками печени при участии витамина К-
Фактор I I I —тканевый тромбопластин — по своей природе представляет собой фосфолипид и входит в состав мембран всех клеток организма, в том числе эндотелия сосудов. Он необходим для образования тканевой протромбиназы.
Фактор IV— кальций — содержится в крови наполовину в виде ионов и наполовину
ввиде комплексов с белками плазмы. В свертывании участвуют лишь ионы Са2+, которые
необходимы для всех фаз свертывания крови. Кровь доноров предохраняют от свертывания путем связывания ионов Са2+ различными стабилизаторами (например, цитратом натрия).
Факторы V и VI — проакцелерин и акцелерин. Их вместе называют акцелератор-гло- булин (Ас-глобулин). Эти вещества представляют неактивную и активную форму одного и того же фактора, поэтому термин «фактор VI» не применяют. Фактор V образуется
впечени, участвует в 1-й и 2-й фазах гемокоагуляции.
Фактор VI-I — конвертин — синтезируется в печени при участии витамина К, требуется для образования тканевой протромбиназы.
Фактор VIII —антигемофильный глобулин А (АГГ) — необходим для формирования кровяной протромбиназы. Его генетический дефицит служит причиной гемофилии А, протекающей с тяжелыми кровотечениями.
Фактор IX—фактор Кристмаса, или антигемофильный глобулин В — образуется в печени в присутствии витамина К, требуется в I фазе гемокоагуляции. При его генетическом дефиците наблюдается гемофилия В.
Фактор X— фактор Стюарта-П pay эра — назван, как и предыдущий, по фамилиям больных, у которых впервые обнаружен дефицит этого соединения. Синтезируется в печени при участии витамина К, участвует в формировании и входит в состав тканевой и кровяной протромбиназ.
Фактор XI — плазменный предшественник тромбопластина (РТА) — образуется в присутствии витамина К в печени, требуется для образования кровяной протромбиназы, где он активирует фактор IX. Дефицит фактора XI служит причиной гемофилии С.
Фактор XII — фактор Хагемана — активируется при контакте с чужеродной поверхностью (например, местом повреждения сосуда), поэтому его называют также контакт -
218
ным фактором. Фактор XII является инициатором образования кровяной протромбиназы и всего процесса гемокоагуляции. После активации он остается на поверхности поврежденного сосуда, что предупреждает генерализацию свертывания крови. Объектом действия фактора Хагемана является фактор XI, с которым он образует комплекс — продукт контактной активации. Кроме системы гемокоагуляции, фактор XII активизирует калликреинкиновую систему, систему комплемента и фибринолиз. Генетический дефицит этого фактора служит причиной болезни Хагемана.
Фактор XIII —фибринстабилизирующий (фибриназа, фибринолигаза, трансглутаминаза) — содержится в плазме, клетках крови и в тканях. По химической структуре фибриназа является гликопротеидом, синтезируется в печени и при свертывании полностью потребляется. Фактор XIII необходим для образования окончательного или нерастворимого фибрина «I». Действие фибриназы сводится к образованию ковалентных пептидных связей между соседними молекулами фибрин-полимера, после чего фибрин становится механически прочным и устойчивым к фибринолизу. Фактор XIII активируется тромбином и ионами Са2+. При врожденном дефиците фибриназы резко ухудшается заживление бытовых и хирургических ран, что говорит о необходимости этого фактора для регенерации.
ФАКТОРЫ СВЕРТЫВАНИЯ ФОРМЕННЫХ ЭЛЕМЕНТОВ КРОВИ И ТКАНЕЙ
В гемостазе участвуют все клетки крови и особенно тромбоциты.
Тромбоциты — бесцветные двояковыпуклые образования диаметром от 0,5 до 4 мкм, т.е. они в 2—8 раз меньше эритроцитов. В крови здоровых людей содержится 200—400- 109/л тромбоцитов (200 000—400 000 в 1 мкл). Они образуются в костном мозге из мегакариоцитов. Из одной такой клетки формируется 3000—4000 кровяных пластинок. Продолжительность жизни последних составляет 8—12 сут. Имеются суточные колебания количества тромбоцитов: днем их больше, чем ночью. Их число изменяется при эмоциях, физической нагрузке, после еды. При прилипании тромбоцитов к поврежденным сосудам они образуют 2—10 отростков, за счет которых и происходит прикрепление.
Химический состав тромбоцитов очень сложен. Они содержат набор ферментов, адреналин, норадреналин, лизоцим, много АТФ и фермент АТФ-азу, функцию которого выполняет сократительный белок кровяных пластинок тромбостенин.
Впоследние годы втромбоцитахобнаружено много специфических соединений,участвующих в
свертывании крови. Их называют тромбоцитарными (пластиночными) факторами и нумеруют арабскими цифрами.
Одним из наиболее важных тромбоцитарных соединений является фактор 3 — тромбоцитар-
ный тромбопластин, или тромбопластический фактор. Он представляет собой фосфалипид и находится в мембране кровяных пластинок и их гранул. Этот фактор освобождается после разрушения тромбоцитов и используется в I фазе свертывания крови.
Фактор 4 — антигепариновый — связывает гепарин и таким путем ускоряет процесс гемокоагуляции.
Фактор 5 — свертывающий фактор, или фибриноген, определяет адгезию (клейкость) и агрегацию (скучивание) тромбоцитов.
Фактор 6 — тромбостенин — обеспечивает уплотнение и сокращение кровяного сгустка. По своим свойствам он напоминает актомиозин скелетных мышц, состоит из субъединиц А и М, подобных актину и миозину. Будучи АТФ-азой, тромбостенин сокращается за счет энергии расщепляемой им АТФ.
Фактор 10 — сосудосуживающий — представляет собой серотонин, который адсорбируется тромбоцитами из крови. Это соединение суживает поврежденные сосуды и уменьшает кровопотерю.
Фактор 11 — фактор агрегации — по химической природе является АДФ и обеспечивает скучивание тромбоцитов в поврежденном сосуде. Помимо АДФ, эту же задачу выполняет недавно обнаруженный тромбоксан, который является самым мощным стимулятором агрегации. В эндотелии сосудов находится простациклин — самый мощный ингибитор агрегации. Баланс между этими веществами определяет скучивание кровяных пластинок.
219
Кроме участия в гемостазе, тромбоциты осуществляют транспорт креаторных веществ, важных для сохранения структуры сосудистой стенки. Они поглощаются клетками эндотелия, доставляя им находящиеся в тромбоцитах макромолекулы. На эти цели ежедневно расходуется около 15 % циркулирующих в крови тромбоцитов. Без взаимодействия с тромбоцитами эндотелий сосудов подвергается дистрофии и начинает пропускать через себя эритроциты.
В гемостазе участвуют эритроциты. Их форма удобна для прикрепления нитей фибрина, а их очень пористая поверхность катализирует процесс гемокоагуляции. В эритроцитах найдены почти все факторы, которые содержатся в тромбоцитах, за исключением тромбостенина.
Лейкоциты имеют в своем составе тромбопластический и антигепариновый факторы, естественные антикоагулянты (гепарин базофилов), активаторы фибринолиза. Число лейкоцитов по сравнению с эритроцитами невелико, поэтому их роль в гемостазе у здоровых людей незначительная.
Вокруг всех форменных элементов крови имеется «плазматическая атмосфера», из адсорбированных плазменных факторов свертывания, что способствует процессу гемокоагуляции.
Весьма существенную роль в гемостазе играют ткани, особенно стенки сосудов.
Все ткани и органы содержат очень активный тромбопластин (фосфолипиды клеточных мембран), антигепариновый фактор, естественные антикоагулянты, соединения, подобные плазменным факторам Y, YII, X и XIII, вещества, вызывающие адгезию и агрегацию тромбоцитов, активаторы и ингибиторы фибринолиза. При повреждении сосудов и прилежащих тканей все эти вещества контактируют с кровью и активно участвуют в ее свертывании и последующем фибринолизе.
Наибольшей активностью среди факторов свертывания крови, находящихся в тканях, обладает тромбопластин. Он сохраняет свое действие после разведения экстрактов в 5000-500 000 раз. Активаторы фибринолиза прекращают свое влияние после разведения экстрактов тканей в 10—100 раз. Поэтому при проникновении в кровоток тканевой жидкости под влиянием тканевого тромбопластина всегда развивается внутрисосудистое свертывание крови с последующими кровотечениями — тромбогеморрагический синдром (ТГС).
СОСУДИСТО-ТРОМБОЦИТАРНЫЙ ГЕМОСТАЗ
Этот механизм способен самостоятельно прекратить кровотечение из наиболее часто травмируемых микроциркуляторных сосудов с низким артериальным давлением. Он складывается из ряда последовательных процессов:
1.Рефлекторный спазм поврежденных сосудов. Эта реакция обеспечивается сосудо суживающими веществами, освобождающимися из тромбоцитов (серотонин, адрена лин, норадреналин). Спазм приводит лишь к временной остановке или уменьшению кро вотечения.
2.Адгезия тромбоцитов (приклеивание) к месту травмы. Данная реакция связана
сизменением отрицательного электрического заряда сосуда в месте повреждения на положительный. Отрицательно заряженные тромбоциты прилипают к обнажившимся волокнам коллагена базальной мембраны. Адгезия тромбоцитов обычно завершается за 3—10 с.
3.Обратимая агрегация (скучивание) тромбоцитов. Она начинается почти одно-
временно с адгезией., Главным стимулятором этого процесса являются «внешняя» АДФ, выделяющаяся из поврежденного сосуда, и «внутренняя» АДФ, освобождающаяся из тромбоцитов и эритроцитов. Образуется рыхлая тромбоцитарная пробка, которая пропускает через себя плазму крови.
4.Необратимая агрегация тромбоцитов (при которой тромбоцитарная пробка становится непроницаемой для крови). Эта реакция возникает под влиянием тромбина, изме-
няющего структуру тромбоцитов («вязкий метаморфоз» кровяных пластинок). Следы тромбина образуются под влиянием тканевой тромбиназы, которая появляется через 5—10 с после повреждения сосуда. Тромбоциты теряют свою структурность и сливаются в гомогенную массу. Тромбин разрушает мембрану тромбоцитов, и их содержание осво-
220
