
6 курс / Медицинская реабилитация, ЛФК, Спортивная медицина / Клиническая_геронтология_2009_№04_05
.pdf
ПЕРЕДОВАЯ СТАТЬЯ
Infarction (TAMI) I Trial // Circulation. 1988. ¹ 77.
P.1090-1099.
17.Ciaroni S., Delonca I., Righetti A. Early exercise testing after acute myocardial infarction in the elderly: Clinical evaluation and prognostic significance // Amer. Heart J. 1993. ¹ 126. P. 304-311.
18.Deckers J.V., Floretti P., Brower R.W. et al: Ineligibility for pre-discharge exercise testing after myocardial infarction in the elderly: Implications for prognosis // Europ. Heart J. 1984. ¹ 5. P. 97-100.
19.Dellborg M., Held P., Swedberg K. et al. Rupture of the myocardium: Occurrence and risk factors // Brit. Heart J. 1985. ¹ 54. P. 11-16.
20.Duber C., Jungbluth A., Rumpelt H.J., Erbel R., Meyer J., Thoenes W. Morphology of the coronary arteries after combined thrombolysis and percutaneous transluminal coronary angioplasty for acute myocardial infarction // Amer. J. Cardiol. 1986. ¹ 58. P. 698-703.
21.Dublin L.I., Lorka L.I., Spiegelman M. Length of Life A Study of the Life of the Life Table. New York: Ronald Press. 1949.
22.Eckman M.H., Wong J.B., Salem D.N., Pauker S.G. Direct angioplasty for acute myocardial infarction: a review of clinical subsets // Ann. Intern. Med. 1992. ¹ 117. P. 667.
23.Elliott J.M., Maclsaac A.L., Lefkovits J., Horrigan M.C.J., Franco L., Whotlow P.L. New coronary devices in elderly: Comparison with angioplasty // Circulation. 1994. Vol. 90. ¹ 4. P. 1-333.
24.Feinleib M., Gillum R.F. Coronary Heart Disease in the elderly: the magnitude of the problem in the United Slates. In: Coronary Heart Disease in the Elderly. Wenger N.K., Furberg C.D., Pitt E. New York: Elsevier. 1986. P. 29.
25.Figueras J., Cortadellas J., Eoongesrios A. et al. Medical management of selected patients with left ventricular free wall rupture during acute myocardial infarction //
J.Amer. Coll. Cardiol. 1997. ¹ 29. P. 512-518.
26.Fibrinolytic Therapy Trialists (FTT) Collaborative Group: Indications for fibrinolytic therapy in suspected acute myocardial infarction: Results from an international trial of 41,021 patients // Circulation. 1995. ¹ 91.
P.1659-1668.
27.Forman D.E., Berman A.D., McCabe C.H., Bal E. PTCA in the elderly: The «Young-old» versus the «old-old» // J Amer. Geriatric Society. 1992. ¹ 40. P. 19-22.
28.Fries J.F. Aging, mortality, and the compression of mortality // New Engl. J. Med. 1980. ¹ 303. P. 130-136.
29.Goldberg R.J., Gore J.M., Gurwitz J.H. et al. The impact of age on the incidence and prognosis of initial myocardial infarction: The Worcester Heart Attack Study // Amer. Heart J. 1989. ¹ 117.
30.Gottdiener J.S, Shemanski L., Gardin J.M. et al. Echocardiographic predictors of incident congestive heart failure in elderly without prevalent cardiovascular disease: the Cardiovascular Health Study // Circulation. 1996. ¹ 94. P. 1-691.
31.Guralnik J.M., Fitzsimmons S.C. Aging in America: a demographic perspective // Cardiol. Clin. 1986. ¹ 4.
P.175.
32.Grines C.L., Brown K.F., Marco J. et al. A comparison of immediate angioplasty with thrombolytic therapy for acute myocardial infarction. The Primary Angioplasty in Myocardial Infarction Study Group // New Engl. J. Med. 1993. ¹ 328. P. 673-679.
33.Grines C., Brodie Â., Griffin J. et al. Which primary PTCA patients may benefit from new technologies // Circulation. 1995. Vol. 92. P. 1-146.
34.Grines C., Stone G., O'Neill W. PTCA in Unstable ischemic syndromes. The manual of Intervention Cardiology. Ed. M. Freed, C. Grines, R.D. Safian. Birmingham: Physicians Press. MI. 1997. P. 107-152.
35.Granger Ñ.Â., Califf R.M., Topol E.J. Thrombolytic therapy for acute myocardial infarction. A review // Drugs. 1992. Vol. 44. ¹ 3. P. 293-325.
36.Garrahy P.J., Cox D.A., Cavender J.B. et al. Survival following coronary angioplasty in elderly patients: comparison with bypass surgery // Circulation. 1990. ¹ 82.
P.111-618.
37.Hartzler G.O., Rutherford B.D., McConahay D.R. et al. Percutaneous transluminal coronary angioplasty with and without thrombolytic therapy for treatment of acute myocardial infarction // Amer. Heart J. 1983. Vol. 106. ¹ 5. P. 965-973.
38.Holmes D., White H., Pieper K. Effect of age on outcome with primary angioplasty versus thrombolysis // J. Amer. Coll. Cardiol. 1999. ¹ 33. P. 412-419.
39.Holland K.J., O'Neill W.W., Bates E.R. et al. Emergency percutaneous transluminal coronary angioplasty during acute myocardial infarction for patients more than 70 years of age // Amer. J. Cardiol. 1989. ¹ 63.
P.399.
40.ISIS-2 (Second International Study of Infarct Survival) Collaborative Group: Randomized trial of intravenous streptokinase, oral aspirin, both, or neither among 17,187 cases of suspected acute myocardial infarction. ISIS-2 // Lancet. 1988. ¹ 2. P. 349-360.
41.ISIS-3 (Third International Study of Infarct Survival) Collaborative Group: A randomized comparison of streptokinase vs. tissue plasminogen activator vs. anistreplase and of aspirin plus heparin vs. aspirin alone among 41,299 cases of suspected acute myocardial infarction // Lancet. 1992. ¹ 1. P. 53.
42.Kannel W.B., Abbott R.D. Incidence and prognosis of unrecognized myocardial infarction: An update on the Framingham study // New Engl. J. Med. 1984. ¹ 311.
P.1144-1147.
43.Krumholz H.M., Murillo J.E., Chen J. et al. Thrombolytic therapy for eligible elderly patients with acute myocardial infarction // JAMA. 1995. ¹ 273. P. 15091514.
44.Krumholz H.M., Friesinger G.C., Cook E.F. et al. Relationship of age with eligibility for thrombolytic therapy and mortality among patients with suspected acute myocardial infarction // J. Amer. Geriatr. Soc. 1994. ¹ 42.
P.127-131.
45.Krumholz H.M., Pasternak R.C., Weinstein M.C. et al. Cost effectiveness of thrombolytic therapy with streptokinase in elderly patients with suspected acute myocardial infarction // New Engl. J. Med. 1992. ¹ 327.
P.7-13.
46.Kudenchuk P.J., Ho M.T., Weaver W.D. et al. Accuracy of computer-interpreted electrocardiography in selecting patients for thrombolytic therapy: MITI Project Investigators // J. Amer. Coll. Cardiol. 1991. ¹ 17.
P.1486-1491.
47.Kuller L., Borhani N., Furberg C. et al. Prevalence of subclinical atherosclerosis and cardiovascular disease and association with risk factors in the Cardiovascular Health Study // Amer. J. Epidemiol. 1994. ¹ 139.
P.1164-1179.
48.Lee T.C., Laramee L.A., Rutherford B.D. et al. Emergency percutaneous transluminal coronary angioplasty for acute myocardial infarction in patients 70 years of age and older // Amer. J. Cardiol. 1990. ¹ 66. P. 663.
49.Lee K.L., Woodlief L.H., Topol E.J. et al. Predictors of 30-day mortality in the era of reperfusion for acute myocardial infarction: Results from an international trial of 41,021 patients // Circulation. 1995. ¹ 91. P. 6591668.
50.MacDonald J.B. Presentation of acute myocardial infarction in the elderly – a review // Age Aging. 1984. ¹ 13. P. 196.
11

КЛИНИЧЕСКАЯ ГЕРОНТОЛОГИЯ, 4-5, 2009
51.Maggioni A.P., Maseri A., Fresco C. et al. Age-related increase in mortality infarctions treated with thrombolysis // New Engl. J. Med. 1993. ¹ 329. P. 1442-1448.
52.Meyer J., Merx W., Dorr R. et al. Successful treatment of acute myocardial infarction shock by combined percutaneous transluminal coronary recanalization (PTCR) and percutaneous transluminal coronary angioplasty (PTCA) // Amer. Heart J. 1982. Vol. 103. ¹ 1. P. 132-134.
53.Nadelnan J., Fismen W.H., Ooi W.L. et al. Prevalence, incidence and prognosis of recognized and unrecognized myocardial infarction in persons aged 75 years or older: The Bronx Aging Study // Amer. J. Cardiol. 1990. ¹ 66. P. 533-537.
54.O'Neill W.W., de Boer M.J., Gibbons R.J. et al. Lessons from the Pooled Outcome of the PAMI, ZWOLLE and Mayo Clinic Randomized Trials of Primary Angioplasty Versus Thrombolytic Therapy of Acute Myocardial Infarction // J. Invas. Cardiol. 1998. Vol. 10 (Suppl. A). P. 4A-10A.
55.Ottesen M.M., Kober L., Jorgensen S. et al. Determinants of delay between symptoms and hospital admission in 5978 patients with acute myocardial infarction: The TRACE Study Group // Europ. Heart J. 1996. ¹ 17. P. 429-437.
56.Pathy M.S. Clinical presentation of myocardial infection in the elderly // Brit. Heart J. 1967. ¹ 29. P. 190.
57.Ragmin F. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomised multicentre study // Lancet. 1999. ¹ 354. P. 708-15
58. Scharfstein J.S., Abendschein D.R., Eisenberg P.R. et al. Usefulness of fibrinogenolytic and procoagulant markers during thrombolytic therapy in predicting clinical outcomes in acute myocardial infarction. TIMI-5 Investigators. Thrombolysis in Myocardial Infarction // Amer. J. Cardiol. 1996. Vol. 78. ¹ 5. P. 503-510.
59.Simoons M.L., Maggioni A.P., Knatterud G. et al. Individual risk assessment for intracranial hemorrhage during thrombolvtic therapy // Lancet. 1993. ¹ 342.
P.1523-1528.
60.Simoons M.L., Arnold A.E., Betriu A. et al. Thrombolysis with tissue plasminogen activator in acute myocardial infarction: no additional benefit from immediate percutaneous coronary angioplasty // Lancet. 1988. ¹ 1.
P.197-203.
61.Stason W.B., Sanders C.A., Smith H.C. Cardiovascular care of the elderly: economic considerations // J. Amer. Coll. Cardiol. 1987. Suppl. A. 10.
62.Stenestrand U., Wallentin L. Early revascularisation and 1-year survival in 14-day survivors of acute myocardial infarction: a prospective cohort study // Lancet. 2002. ¹ 359. P. 1805-11.
63.Stone G., Grines C., Topol E. Update on PTCA for acute MI. Current Review of Interventional Cardiology. Eds E. Topol, P. Serruys. Philadelhia, PA: Current Medicine. 1995. P. 1-56.
64.Stringer K.A. TIMI grade flow, mortality, and the GUSTO-III trial // Pharmacotherapy. 1998. Vol. 18. ¹ 4. P. 699-705.
65.Sugiura M., Hiraoka K., Ohkawa S. Severity of coronary sclerosis in the aged: A pathological study in 968 consecutive autopsy cases // Jpn. Heart. J. 1976. ¹ 17.
P.471-478.
66.Suman R., Riley M.W. Introducing the oldest old // Milbank Mem. Fund. Q. 1985. ¹ 63. P. 177.
67.Solomon C.G., Lee T.F., Cook E.F. et al. Comparison of clinical presentation of acute myocardial infarction in patients older than 65 years of age to younger patients: The multicenter chest pain study experience // Amer. J. Cardiol. 1989. ¹ 63. P. 776.
68.Solomon C.G., Lee T.F., Cook E.F. et al. Comparison of clinical presentation of acute myocardial infarction in patients older than 65 years of age to younger patients: The multicenter chest pain study experience // Amer. J. Cardiol. 1989. ¹ 63. P.776.
69.Sigurdsson E., Thorgeirsson G., Sigvaldason H. et al: Unrecognized myocardial infarction: Epidemiology, clinical characteristics, and the prognostic role of angina pectoris: The Reykjavik Study // Amer. Intern. Med. 1995. ¹ 122. P. 96-102.
70.SWIFT (Should We Intervene Following Thrombolysis?) Trial Study Group. SWIFT trial of delayed elective intervention v conservative treatment after thrombolysis with anistreplase in acute myocardial infarction // BMJ. 1991 ¹ 302. P. 555-560.
71.The TIMI Research Group. Immediate vs delayed catheterization and angioplasty following thrombolytic therapy for acute myocardial infarction: TIMI II A results // JAMA. 1988. ¹ 260. P. 2849-2858.
72.The TIMI Study Group. Comparison of invasive and conservative strategies after tritment with intravenous tissue plasminogen activator in AMI: results of the thrombolyses in MI (TIMI) phase II trial // New Engl.
J.Med. 1989. ¹ 20. P. 618-627.
73.Terrin M.L., Williams D.O., Kleiman N.S. et al. Twoand three-year results of the Thrombolysis in Myocardial Infarction (TIMI) Phase II clinical trial // Amer. Coll. Cardiol. 1993. ¹ 22. P. 1763-1772.
74.Thompson L., Wood C., Wallagen M. Geriatric acute myocardial infarction: A challenge to recognition, prompt diagnosis, and appropriate care // Crit. Care Nurs. / Clin. North Amer. 1992. ¹ 4. P. 291-299.
75.Tiefenbrunn A.J., Chandra N.C., French W.J. et al. Clinical experience with primary percutaneous transluminal coronary angioplasty compared with alteplase (recombinant tissue-type plasminogen activator) in patients with acute myocardial infarction: A report from the Second National Registry of Myocardial Infarction (NRMI-2) // J. Amer. Coll. Cardiol. 1998. ¹ 31.
P.1240-1245.
76.Topol E.J., Califf R.M., George B.S. et al. A randomized trial of immediate versus delayed elective angioplasty after intravenous tissue plasminogen activator in acute myocardial infarction // New Engl. J. Med. 1987. ¹ 317. P. 581-588.
77.Van Heeckeren D.W., Geha A.S., Ankeney J.L. et al. Changing demographics of coronary bypass patients over the last decade, abstracted // Circulation. 1987. Suppl. IV. ¹ 76. P. 486.
78.Van't Hof A.W., Liem A., Suryapranata H. et al. Angiographic assessment of myocardial reperfusion in patients treated with primary angioplasty for acute myocardial infarction: Myocardial blush grade. Zwolle Myocardial Infarction Study Group // Circulation. 1998. Vol. 97. ¹ 23. P. 2302-2306.
79.Veen G., de Boer M.J., Zijlstra F., Verheugt F.W. Improvement in three-month angiographic outcome suggested after primary angioplasty for acute myocardial infarction (Zwolle trial) compared with successful thrombolysis (APRICOT trial). Antithrombotics in the Prevention of Reocclusion In Coronary Thrombolysis // Amer. J. Cardiol. 1999. Vol. 84. ¹ 7. P. 763-767.
80.White H.D., Barbash G.I., Califf R.M. et al. Age and outcome with contemporary thrombolytic therapy: Results from the GUSTO-I trial // Circulation. 1996. ¹ 94. P. 1826-1833.
81.Williams D.O., Braunwald E., Knatterud G. et al. Oneyear results of the Thrombolysis in Myocardial Infarction investigation (TIMI) Phase II Trial // Circulation. 1992. 85. P. 533-542.
Поступила 20.04.2009
12

ОРИГИНАЛЬНЫЕ СТАТЬИ
ОРИГИНАЛЬНЫЕ СТАТЬИ
ÓÄÊ 617 – 089.844:612.67
ПЛАЗМЕННАЯ ТЕХНОЛОГИЯ В КОМПЛЕКСНОМ ЛЕЧЕНИИ
ХИРУРГИЧЕСКИХ ИНФЕКЦИЙ МЯГКИХ ТКАНЕЙ У ПАЦИЕНТОВ ПОЖИЛОГО ВОЗРАСТА
А.М. Шулутко1, Э.Г. Османов
Московская медицинская академия им. И.М. Сеченова
Обобщен опыт лечения пожилых пациентов с обширными гнойнонекротическими ранами и флегмонозно-некротической формой рожи, разделенных на две группы, которые различались только способом местного лечения. Пациенты контрольной группы пролече- ны по стандартам ОМС. У пациентов основной группы на заклю- чительном этапе традиционной некрэктомии раневую поверхность обрабатывали потоком плазмы. Плазменная технология позволила значительно улучшить результаты комплексного лечения инфекций мягких тканей: ускорила темпы очищения и последующей репарации ран, сократила срок лечения, а также потребность медикаментов и перевязочного материала.
Ключевые слова: плазменные потоки, обширная гнойная рана, флегмонозно-некротическая рожа, пожилой возраст
Key words: laser surgery, necrotic erysipelas, septic wound
Продолжающееся старение населения современной России – один из факторов высокого уровня заболеваемости хирургическими инфекциями мягких тканей. Традиционные лечебные мероприятия у пациентов пожилого возраста не всегда позволяют адекватно справиться с поставленной задачей, особенно при тяжелых нагноительных процессах [9,10,15]. Новейшие тактические концепции (ранняя радикальная некрэктомия), равно как антисептики и антибиотики последних поколений пока также ощутимо не влияют на сложившуюся ситуацию, вы-
1 Шулутко Александр Михайлович, д-р мед. наук, заведующий отделением факультетской хирургии ММА им. И.М. Сеченова. Тел.: 8-499-245-37-35.
нуждая клиницистов прибегать к дополнительным физико-химическим методикам локального воздействия на патологический очаг [3,6,12]. Среди последних заслуженной популярностью пользуется плазменная технология.
Многочисленные исследования, посвященные использованию плазменных потоков в хирургической практике, свидетельствуют о таких их преимуществах, как практически бескровное рассечение и иссечение некротизированных тканей; гемостаз и качественная стерилизация раневой поверхности; создание оптимальных условий для последующей регенерации тканевого субстрата, особенно благодаря биостимулирующему эффекту молекул экзогенного оксида азота воздушно-плазменной струи [1,4,7,13,16].
13

КЛИНИЧЕСКАЯ ГЕРОНТОЛОГИЯ, 4-5, 2009
На сегодняшний день продолжается изучение эффективности данного вида хирургической энергии в разных клинических ситуациях. Представляется интересной оценка возможностей плазменной технологии при лечении лиц преклонного возраста.
МАТЕРИАЛ И МЕТОДЫ
Мы обобщили опыт комплексного лечения 137 пожилых пациентов (85 женщин и 52 мужчины), пролеченных в клинике факультетской хирургии ¹ 2 ММА им. И.М. Сеченова (ГКБ ¹ 61 Москвы) за период 2004–2008 гг. В исследование были включены только лица с тяжелыми формами инфекций мягких тканей, такими, как обширные гнойно-некротические раны и флегмонозно-некро- тическая форма рожи, поскольку при небольших банальных гнойниках, как показывают многолетние наши наблюдения и данные литературы, качественная медицинская помощь пожилым больным не представляет особых затруднений. В зависимости от нозологической формы все наблюдения были распределены в две серии, в каждой из которых формировали основную и контрольную группы (табл. 1).
Клинические группы репрезентативны по тяжести основного заболевания и демографическим показателям. Возраст пациентов 60–82 года, в среднем 68,7 ± 2,6 года. Все они были госпитализированы в экстренном и срочном порядке либо переведены из других отделений клиники и стационаров в связи с развитием основного заболевания либо послеоперационных гнойных осложнений. Самой частой локализацией процесса были нижние конечности (93 наблюдения – 67,9%).
Во всех случаях площадь очага инфекции превышала 50 см2 (70–510 ñì2, в среднем 260 ±
± 10,5 ñì2), тем самым подпадая под общеприня-
|
|
Таблица 1 |
||
Общая характеристика |
|
|||
клинического материала |
|
|||
|
|
|
|
|
|
Группа |
|
||
Заболевание |
|
|
Всего |
|
контроль- |
основ- |
|||
|
|
|||
|
íàÿ* |
íàÿ** |
|
|
|
|
|
|
|
Обширные гнойно-некроти- |
16 |
25 |
41 |
|
ческие раны |
|
|
|
|
Рожа (флегмонозно- |
33 |
63 |
96 |
|
некротическая форма) |
|
|
|
|
Итого |
49 |
88 |
137 |
|
|
|
|
|
|
Примечание. * Общепринятое лечение. ** Применение плазменной технологии.
тое определение «обширная гнойная рана» [5,9]. Согласно классификации D. Ahrenholz (1991), «глубина» мягкотканой деструкции соответствовала II–IV уровням, при этом в большинстве случаев (115 – 83,9%) был II уровень – гнойно-некроти- ческий процесс локализовался в пределах подкожной жировой клетчатки. У всех госпитализированных отмечены отчетливые клинико-лабораторные проявления синдрома системной воспалительной реакции (SIRS). При этом в 107 (78,1%) наблюдениях SIRS был выраженным (3 или 4 установленных признака). 24 (17,5%) пациента поступали с тяжелым сепсисом, органо-системными дисфункциями (l1 балла по шкале SOFA), 3 (2,1%) пациента в возрасте 62, 77 и 80 лет – с картиной септи- ческого шока.
Сопутствующие заболевания у 100% пациентов были однородными в обеих группах, чаще сердеч- но-сосудистые, преимущественно ИБС и гипертони- ческая болезнь (47%), что в целом соответствует неблагоприятной эпидемиологической обстановке на сегодняшний день в России. Далее по частоте – поражение органов желудочно-кишечного тракта (32%) и сахарный диабет (18%). Нередко в ходе обследования диагностировали несколько сомати- ческих болезней, в большинстве случаев требовавших безотлагательной медикаментозной коррекции. Примерно в 36% случаев (всего 50 из 137) число таковых у одного субъекта составляло 3 и более.
Энергичное общее лечение включало инфузион- но-дезинтоксикационную и антибактериальную терапию, десенсибилизирующие средства, ультрафиолетовое облучение крови, полноценное сбалансированное питание, физиотерапию и др. Неотложные мероприятия во всех случаях инфекции, которые осложнились тяжелым сепсисом и септическим шоком, начинали в отделении реанимации и интенсивной терапии. Основой лечебной тактики считаем адекватную хирургическую санацию гнойно-не- кротического очага в срочном порядке и только под общим обезболиванием. Клинические группы различались только способом местного лечения. В контрольной группе (n = 49) пожилые пациенты были пролечены согласно медико-экономическим стандартам ОМС (некрэктомия, в том числе этапная, с помощью обычных стальных инструментов; дальнейшее местное лечение ран с применением растворов антисептиков и поликомпонентных мазей на водорастворимой основе типа «Левомеколь»).
В основной группе (n = 88) на заключительном этапе традиционной некрэктомии раневую поверхность обрабатывали потоком плазмы в режиме диссекции (резки) и бесконтактной термокоагуляции.
14

ОРИГИНАЛЬНЫЕ СТАТЬИ
Источник «высоких» энергий – отечественные плазменные установки последнего поколения: «Скальпель плазменный СП-ЦПТ» (мощность – 2,5 кВт, рабочий газ – аргон) и воздушно-плазменный аппарат «Плазон» (мощность – 0,5 кВт, рабочий газ – атмосферный воздух). В послеоперационном периоде проводили сочетанную (метахронную) плазменную обработку потоком аргоновой и воздушной плазмы только в режиме стимуляции. Очередность воздействия различными по источнику потоками плазмы принципиального значения не имела. Термическое поражение мягких тканей при этом было полностью исключено, поскольку температура потоков, подаваемых на рану, не превышала 40°C. Продолжительность обработки зависела от площади патологического очага, составляя в среднем 15 с на одну зону площадью в 1 см2 при аргоноплазменной стимуляции и до 10 с на зону в 2 см2 в ходе NO-терапии. По завершении процедур раны рыхло тампонировали с мазью «Левомеколь».
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Сравнительный анализ результатов показал, что высокотемпературная плазменная струя в режиме резки и коагуляции хорошо дополняет традиционную некрэктомию, обеспечивая ускоренное очищение очага от гнойно-некротичес- ких масс, стерилизацию раны и гемостаз за счет коагуляции сосудов диаметром до 1 мм. Развитие грануляций и начало краевой эпителизации в основной группе на фоне дистанционного плазменного воздействия (режим терапии) происходило на 5–7 сут раньше, чем в контрольной (табл. 2).
Динамика макроскопических изменений подтверждалась данными цитологического и гистологического исследования. В мазках–отпечатках наблюдали существенное уменьшение содержания лейкоцитов при более быстром снижении дистрофически измененных и распадающихся нейтрофилов. Морфологически уже к 8–9-м суткам отмечалось постепенное усиление макрофагальной реакции и пролиферации фибробластов, новообразование капилляров, рост полноценной грануляционной ткани (12–16-е сутки). Все это обусловлено одномоментным воздействием нескольких физико-химических факторов (экзогенный оксид азота, ультрафиолетовое излуче- ние, озон, физиотерапевтическое действие ионизированных потоков) на тканевой кровоток по всей зоне очага инфекции.
Вследствие выраженной сорбционной способности обугленного слоя тканей после комбинированной некрэктомии с использованием «высоких» энергий существенно сокращалась раневая экссудация и быстрее купировалось перифокальное воспаление (табл. 2). Разумеется, указанные положительные сдвиги не могли не отразиться на динамике ряда важных клинических показателей (табл. 3).
Таблица 2
Показатели раневого процесса при различных методах лечения
|
Группа |
|
||
Показатели |
|
|
p |
|
контрольная |
основная |
|||
|
||||
|
|
|||
|
(n = 49) |
(n = 88) |
|
|
|
|
|
|
|
Очищение раны, сут |
9,9 ± 0,8 |
4,9 ± 0,4 |
<0,05 |
|
Появление грануля- |
10,8 ± 1,0 |
5,2 ± 0,5 |
<0,05 |
|
öèé, ñóò |
|
|
|
|
50% – гранулирова- |
15,0 ± 1,7 |
8,9 ± 1,4 |
<0,05 |
|
íèå ðàíû, ñóò |
|
|
|
|
100% – гранулирова- |
19,1 ± 0,8 |
12,0 ± 1,1 |
<0,05 |
|
íèå ðàíû, ñóò |
|
|
|
|
Начало краевой эпите- |
14,3 ± 2,0 |
7,9 ± 1,5 |
<0,05 |
|
лизации, сут |
|
|
|
|
Скорость заживления |
2,9 ± 0,4 |
3,8 ± 0,5 |
<0,05 |
|
по тесту Л.Н. Поповой |
|
|
|
|
(1942) ê 14-ì ñóò |
|
|
|
|
êàì,% |
|
|
|
|
Купирование перифо- |
22,1 ± 2,8 |
16,3 ± 1,4 |
<0,05 |
|
кального воспаления, |
|
|
|
|
ñóò |
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 3 |
||
Клинические данные при различных методах |
|||||
|
местного лечения |
|
|
||
|
|
|
|
|
|
|
|
Группа |
|
||
Параметры |
|
|
p |
||
контрольная |
основная |
||||
|
|
|
|||
|
|
n = 49 |
n = 88 |
|
|
|
|
|
|
||
Интраоперационная |
310 ± 30 |
235 ± 10 |
<0,01 |
||
кровопотеря, мл |
|
|
|
||
Число этапных некрэк- |
4,0 |
2,6 |
<0,05 |
||
томий, среднее |
|
|
|
||
Продолжительность опе- |
14,6 ± 4,4 |
18,9 ± |
>0,05 |
||
рации, мин |
|
|
3,0 |
|
|
Срок купирования лихо- |
9,0 ± 0,7 |
5,2 ± 0,5 |
<0,05 |
||
радки, сут |
|
|
|
|
|
Срок купирования боле- |
12,8 ± 0,4 |
8,2 ± 0,4 |
<0,05 |
||
вого синдрома, сут |
|
|
|
||
|
стационар- |
35,8 |
24,4 |
<0,05 |
|
Ñðîê ëå÷å- |
íûé ýòàï |
|
|
|
|
íèÿ, ñóò |
амбулатор- |
18,5 |
11,6 |
<0,05 |
|
|
íûé ýòàï |
|
|
|
|
|
|
|
|
|
|
15

КЛИНИЧЕСКАЯ ГЕРОНТОЛОГИЯ, 4-5, 2009
Изучение динамики раневого процесса при гнойно-некротических осложнениях рожи показало, что для общепринятого лечения характерно медленное очищение ран – в среднем на 12,6 сут. Наступление репаративной фазы было несколько запоздалым, а процессы грануляции и эпителизации протекали вяло вследствие более выраженных, чем при других клинических вариантах этой инфекции, микроциркуляторных расстройств в патологическом очаге, о чем сообщают и другие авторы [2,8,11,14]. Тем не менее по основным параметрам раневого процесса основная группа опережала контрольную в 1,5–2,2 раза (p < 0,05).
При исследовании транскутанного напряжения кислорода в перифокальной зоне к 14-м суткам на фоне регулярной сочетанной плазменной обработки (аргоноплазменная стимуляция + NO-терапия) отмечен его подъем в 7–8,5 раза по сравнению с исходным, в контрольной группе – в 5,6 раза (p < 0,05). Нормализация стандартных лабораторных показателей (лейкоцитарный индекс интоксикации, уровень лейкоцитов, мочевины, креатинина в крови и др.) также происходила раньше, чем при общепринятом лечении. Это объяснимо ускоренным течением всех фаз раневого процесса, следовательно, ускоренной ликвидацией гной- но-некротического очага как источника массивных белковых потерь.
Микробиологические исследования в динамике доказали высокую эффективность санации гнойной раны с помощью плазменной технологии, бактериальный титр раневого отделяемого с первых суток послеоперационного периода не превышал общепринятый критический (<105 микробных тел на 1 г ткани очага). Плотная пленка термокоагуляционного некроза после высокоэнергетической диссекции не позволяла гноеродной микрофлоре проникать с поверхности обширной раны в глубокие слои мягких тканей. К тому же все раны после некрэктомии дополнительно санировались потоком плазмы в режиме стимуляции. Стабильно безопасный уровень микробной обсемененности при общепринятом лечении ран достигался лишь к 8–9-м суткам (2,9•104 ± 10 микробных тел на 1 г ткани, p < 0,05).
К очевидным преимуществам плазменной технологии, наряду с многопрофильным лечебным воздействием на гнойный очаг, следует отнести широкие возможности комбинированной терапии (в том числе принципиально иными средствами местного лечения), хорошую переносимость процедур, отсутствие непосредственного физического контакта и необходимости в каком-либо лабораторном контроле. В отличие от других физико-химических методик, не требуется привлечения дополнительных устройств и приспособлений; отсутствует потребность в особых (трудоемких) способах стерилизации рабочей части и средствах защиты пациента и медицинского персонала. Поскольку генерация физической плазмы происходит внутри плазматрона, то никакого электромагнитного воздействия на тело пациента не оказывается. Это особенно важно для больных с кардиальной патологией с имплантированным водителем ритма сердца.
Благодаря применению плазменной технологии удалось снизить общую летальность примерно в 2,6 раза: 2,3% в основной группе (2 пациента) и 6,1% в контрольной (3 пациента). Средний возраст погибших составил 76,4 года (70–80 лет), площадь гнойно-некротического очага во всех наблюдениях превышала 300 см2. Исходное состоянии этих пациентов расценивали как крайне тяжелое (SIRS4, полиорганная недостаточность l4 баллов по шкале SOFA). В их числе двое из трех, поступавших с клини- ческой картиной септического шока. Из сопутствующих заболеваний решающее значение имели ИБС (2 наблюдения), сахарный диабет (3 наблюдения), цирроз печени (1). Во всех подобных ситуациях тяжелое общее состояние, запредельная эндогенная интоксикация, нарушения в различных звеньях системного гомеостаза (на фоне декомпенсации соматических заболеваний) предопределяли безуспешность лечебных мероприятий локальной направленности, в том числе инновационных методик. В 1 (2%) наблюдении контрольной группы, несмотря на энергичные комплексные мероприятия, мы были вынуждены выполнить ампутацию бедра в связи с прогрессированием гнойно-некротичес- кого процесса.
16

ОРИГИНАЛЬНЫЕ СТАТЬИ
Благодаря использованию плазменной энергии в различных режимах в основной группе подготовка гранулирующих ран к восстановительным вмешательствам сокращалась на 5–7 дней по сравнению с контрольной группой (p < 0,05), составив в среднем 17,8 ± 1,5 сут. (16–20 сут). Традиционное местное лечение (растворы антисептиков, мазевые повязки) сравнительно медленно стимулировало раневой процесс, что, в свою очередь, удлиняло срок до выполнения аутодермопластики и других пособий: к 21– 26-м суткам от начала лечения (в среднем 23,4 ± 2,1 сут).
ВЫВОДЫ
Плазменная технология значительно улучшает результаты комплексного лечения тяжелых хирургических инфекций мягких тканей у пациентов пожилого возраста. Ее применение в различных режимах позволяет существенно ускорить темпы очищения и последующей репарации обширных постнекрэктомических ран, уменьшить степень микробной контаминации. Сокращение общего срока лечения, а также потребность в меньшем количестве медикаментов и перевязочных материалов в ходе внедрения инновационной методики в клиническую практику в конечном итоге должно иметь ощутимое экономическое значение.
ЛИТЕРАТУРА
1.Брюсов П.Г., Кудрявцев Б.П. Плазменная хирургия. М., 1995.
2.Гейниц А.В., Дербенев В.А., Толстых М.П., Воронов К.Е. Комплексное лечение рожи с использовани-
ем физических и физико-химических методов. М.: Научный мир, 2006.
3.Давыденко А.В. Обоснование тактики хирургического лечения глубоких флегмон бедра. Автореф. дис. ...
канд. мед. наук. Ростов-на-Дону, 2004.
4.Жиляев Е.Г., Хрупкин В.И., Марохонович Л.А., Кудрявцев Б.П. Перспективы применения воздушноплазменных потоков в медицине. // Военно-медицин- ский журнал. 1998. ¹ 6. С. 46-49.
5.Кузин М.И., Костюченок Б.М. Раны и раневая инфекция. М., 1990.
6.Липатов К.В., Сопромадзе М.А., Емельянов А.Ю., Канорский И.Д. Использование физических методов в лечении гнойных ран // Хирургия. 2001. ¹ 10. С. 56-61.
7.Нигматзянов С.С. Клинико-экспериментальное обоснование применения плазменных технологий в гнойной хирургии. Автореф. дис. ... канд. мед. наук. Уфа, 2004.
8.Степанкина Е.Л. Хирургическая тактика и изменение состояния системы гомеостаза у больных с осложненными формами рожи. Автореф... дис. канд. мед. наук. Саратов, 2004.
9.Федоров В.Д., Светухин А.М. Избранный курс лекций по гнойной хирургии. М.: Миклош. 2007.
10.Шляпников С.А. Хирургические инфекции мягких тканей - старая проблема в новом свете // Инфекции в хирургии. 2003. Том 1. ¹ 1. С. 4-21.
11.Anaya D., McMahon K., Nathens A., Sullivan S., Foy H., Bulger E. Predictors of mortality and limb loss in necrotizing soft tissue infections // Arch. Surg. 2005. Vol. 140. ¹ 2. P. 151-157.
12.Chapnick E., Abter E. Necrotizing soft-tissue infections // Infect. Dis. Clin. North. Amer. 1996. Vol. 10. ¹ 4. P. 835-855.
13.Glover J., Bendick P., Link W. The plasma scalpel: a new thermal knife // Laser surgery. 1998. Vol. 3. ¹ 1. P. 101-106.
14.Lazzarini L., Conti E., Tositti G., de Lalla F. Erysipelas and cellulites: clinical and microbiological spectrum in an Italian tertiary care hospital // J. Infect. 2005. Vol. 51. ¹ 5. P. 383-389.
15.Malangoni M. Necrotizing soft tissue infections: Are we making any progress? // Surg. Infect. 2001. Vol. 2. ¹ 2. P. 145-150.
16.Witte M., Barbul A. Role of nitric oxide in wound repair // Amer. J. Surg. 2002. Vol. 183. ¹ 2. P. 406412.
Поступила 20.04.2009
17

КЛИНИЧЕСКАЯ ГЕРОНТОЛОГИЯ, 4-5, 2009
ÓÄÊ 617-089≈616.089:612.67
ОСТРЫЙ ПАНКРЕАТИТ У ПАЦИЕНТОВ СТАРШЕЙ ВОЗРАСТНОЙ ГРУППЫ
С.Ф. Багненко, В.Р. Гольцов1, И.А. Реутская, С.С. Бреус, Д.А. Палей, Д.А. Дымников, Е.В. Батиг
ГУ НИИ скорой помощи им. И.И. Джанелидзе, Санкт-Петербург
Проблема острого панкреатита с каждым годом становится все более актуальной во всех возрастных группах. Деструктивные формы острого панкреатита составляют примерно 14%, а летальность при них достигает 17–25% в среднем и 40–70% у пациентов старше 70 лет. Наиболее частой причиной острого панкреатита у лиц пожилого возраста являются ишемия на фоне атеросклероза и билиарная гипертензия, сопровождающая желчнокаменную болезнь. Клиническая картина, диагностика и лечебная тактика у них имеет свои особенности, поскольку тяжесть состояния и прогноз в большой степени определяет исходный преморбидный фон и степень декомпенсации других органов и систем. Для диагностики тяжести заболевания, общего состояния у лиц пожилого возраста возможно использовать традиционные методы инструментальных, лабораторных, прогностических исследований. Оценочные прогностические шкалы обладают довольно высокой информативностью (APACHE II – 92%, SAPS – 68%, SOFA – 47%). Наибольшее число осложнений острого панкреатита регистрируется именно у пожилых пациентов. Непосредственной причиной смерти в каждой фазе острого деструктивного панкреатита является полиорганная недостаточность, чаще всего развиваются дисфункция и недостаточность сердечно-сосудистой (80%), дыхательной (70%), почечной (65%) систем.
Ключевые слова: острый панкреатит, фазы заболевания, клинические данные, осложнения, летальность
Key words: acute pancreatitis, stage of disease, clinical evidence, complications, lethality
В настоящее время острый панкреатит выходит на первое место в структуре острых хирургических заболеваний [1]. Заболеваемость острым панкреатитом охватывает все возрастные
1 Гольцов Валерий Ремирович, д-р мед. наук. Руководитель панкреатологической клиники НИИ скорой помощи им. И.И. Джанелидзе, тел.: (812) 709- 60-92, e-mail: govare@yandex.ru.
категории населения. Отмечен его рост у пациентов старшей возрастной группы [6], что отражает общую тенденцию к старению населения, в частности, в Санкт-Петербурге. Отмечается рост общей заболеваемости острым панкреатитом за 2007–2008 гг. по сравнению с 2004 г. на 37–40%, причем число пациентов старшей возрастной группы возросло на 70–98%. При этом ежегодно процент пациентов старше 70 лет сре-
18

ОРИГИНАЛЬНЫЕ СТАТЬИ
ди всех больных данным заболеванием остается примерно одинаковым и составляет в среднем 14,8% [6]. Деструктивные формы в структуре общей заболеваемости острым панкреатитом составляют от 10 до 19%, в среднем 14% [7], у больных старше 70 лет – 12,05%. Результаты лечения этих больных, несмотря на широкие возможности современного здравоохранения, остаются неутешительными. Летальность пациентов старшей возрастной группы неизменно высока, достигает при некоторых его формах 42% [9], у лиц моложе 70 лет – 17–25%.
МАТЕРИАЛ И МЕТОДЫ
Проведен анализ 112 случаев заболевания острым панкреатитом у лиц старше 70 лет, находившихся на лечении в клинике панкреатологии в период с 2004 по 2008 гг., 50 мужчин и 62 женщины. Этиология заболевания выглядит следующим образом (рис. 1).
У пациентов старше 70 лет ведущим является билиарный и ишемический острый панкреатит. Билиарный панкреатит возникает на фоне желчнокаменной болезни, сопровождающейся желчной гипертензией. Как правило этот панкреатит возникает у пациентов после погрешности в диете. В результате реализуются два взаимоотяжеляющих патогенетических компонента заболевания, такие, как панкреатическая гиперсекреция и протоковая гипертензия – пусковые механизмы острого панкреатита [3].
Ишемический панкреатит развивается на фоне гипертонической болезни, выраженного атеросклероза брюшного отдела аорты и чревного ствола, аневризмы брюшного отдела аорты, вызывающих так называемый ишемический абдоминальный синдром. Ишемия органов живота, в которую вовлекается и поджелудочная железа, приводит к некрозу ацинарной ткани и панкреатиту [3]. При наличии у пациента как билиарного, так и сосудистого компонента можно говорить о билиарно-ишемической этиологии заболевания, на долю которой у пациентов старшей возрастной группы приходится около 8% всех наблюдений.
11,6% |
4,5% 0,9% |
41,9% |
|
|
|
Билиарный |
|||
|
|
|
|||||||
|
|
|
|
||||||
|
|
|
|
Ишемический |
|||||
|
|
|
|
|
|
|
|
|
Алиментарный |
|
|
|
|
|
|
|
|
|
|
15,2% |
|
|
|
|
|
|
|
|
Алкогольный |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Послеоперационный |
|
|
|
|
|
|
|
|
и травматический |
||
|
|
|
|
|
|
||||
25,9% |
|
|
|
|
|
Токсический |
|||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Рис. 1. Этиология острого панкреатита.
В исследовании использовалась классификация острого панкреатита, разработанная в панкреоцентре НИИ СП им. И.И. Джанелидзе и принятая Ассоциацией хирургов Санкт-Петербурга в 2004 г. [2]. Данная классификация основана на тесной связи тяжести заболевания (легкая, средняя, тяжелая) с его морфологическими проявлениями (отеч- ная форма; мелко-, крупноочаговый, субтотальный панкреонекроз) и учитывает фазовое течение острого деструктивного панкреатита (ферментативная, реактивная фазы, фаза асептической или септической секвестрации).
Для верификации острого панкреатита использовались клинико-лабораторные, инструментальные (УЗИ, КТ, ЭКГ, ФГДС и др.), интраоперационные диагностические исследования по общепринятым методикам.
Степень тяжести заболевания и состояния определялись по многопараметрическим диагностическим системам: оригинальной (А.Д. Толстой, 1997), RANSON, АРАСНЕ-II, SAPS, SOFA.
Анализ данных производился с помощью пакета прикладных программ Statistica for Windows 5,0.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Особенности клинической картины отеч- ной формы острого панкреатита у пациентов старшей возрастной группы. Эти пациенты далеко не всегда предъявляют жалобы на характерную боль в животе. У 34% больных боль локализуется в правом подреберье, 22% жалуются на боль в области лопатки, в плече, за грудиной, в области сердца. У 15% пациентов возникает одышка. Более чем у 50% отмечается многократная рвота, не приносящая облегчения, иногда с примесью желчи. Температура тела повышается до субфебрильной. Кожные покровы чаще бледные, отмечается сухость слизистых оболочек. Характерна тахикардия, однако у больных с ишемической болезнью сердца (ИБС) возможна и брадикардия, и другие нарушения ритма. Часто наблюдается цианоз носогубного треугольника и одышка вследствие дыхательной или сердечной недостаточности. При аускультации легких определяются жесткое дыхание, рассеянные мелкопузырчатые застойные хрипы в нижних отделах легких. АД чаще повышено: пациенты зачастую страдают гипертонической болезнью. Могут усиливаться проявления цереброваскулярной болезни. Больных беспокоит задержка стула и газы.
19
КЛИНИЧЕСКАЯ ГЕРОНТОЛОГИЯ, 4-5, 2009
% |
|
|
|
|
0,7 |
|
|
|
|
0,6 |
|
|
|
|
0,5 |
|
|
|
|
0,4 |
|
|
|
|
0,3 |
|
|
62% |
64% |
|
|
|
||
0,2 |
31% |
40% |
38% |
|
|
|
|
||
0,1 |
|
|
|
|
|
|
12% |
|
|
0 |
|
|
|
|
|
|
|
|
 Повышение гематокрита
Повышение гематокрита
 Лейкоцитоз
Лейкоцитоз
 Палочкоядерный сдвиг
Палочкоядерный сдвиг
 Лимфопения
Лимфопения
 Гиперамилаземия
Гиперамилаземия  Гипергликемия
Гипергликемия
Рис. 2. Данные лабораторного исследования.
% |
|
|
|
|
80 |
|
|
|
Эндотоксиновый |
|
|
|
70% |
|
70 |
|
|
øîê |
|
|
|
|
||
60 |
|
60% |
|
ÎÑÑÍ |
|
|
|
Острый инфаркт |
|
|
|
|
|
|
50 |
|
|
|
миокарда |
|
|
|
|
Инсульт |
40 |
|
|
|
ÎÄÍ |
30 |
|
|
|
ÎÏÍ |
|
|
|
ÎÊÍ |
|
|
|
|
|
|
20 |
|
|
14% |
ОПечН |
10 |
6% |
8% 7% |
10% |
|
|
3% |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
Рис. 3. Осложнения острого панкреатита. ОССН – острая сердечно-сосудистая недостаточность. ОДН – острая дыхательная недостаточность. ОПН – острая почечная недостаточность. ОКН – острая кишечная непроходимость. ОпечН – острая печеноч- ная недостаточность.
При осмотре наблюдается вздутие живота, боль при пальпации в эпигастральной области.
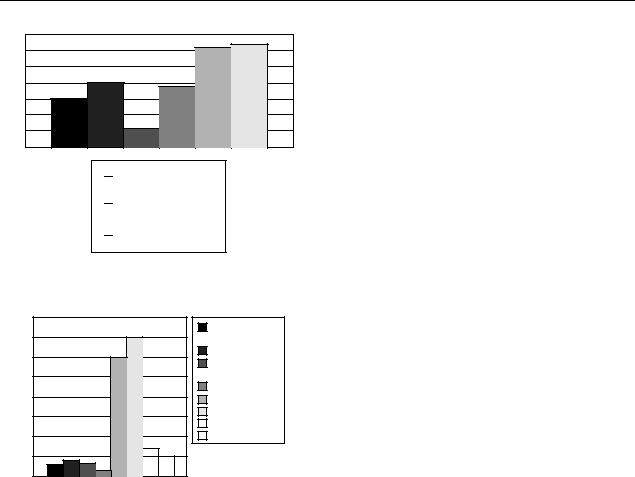
При лабораторной диагностике часты (помимо гиперамилаземии) гипергликемия, признаки гемоконцентрации, лейкоцитоз со сдвигом влево, лимфопения (рис. 2).
При УЗИ брюшной полости определяется увеличенная поджелудочная железа гипоэхогенной плотности, с неоднородной структурой, за- частую признаки острого панкреатита сочетаются с явлениями ее хронического воспаления, кроме того, частой находкой является желчнокаменная болезнь.
При отечной форме заболевания у пациентов старше 70 лет клинические проявления купируются за 5–7 дней при обязательном применении базисного [2] медикаментозного лечения, адаптированного к данному возрасту. Однако паци-
енты могут находиться в стационаре и более длительное время из-за декомпенсации сопутствующих хронических заболеваний. При выписке больным следует рекомендовать продолжение лечения в амбулаторных условиях.
Клиническая картина и диагностика острого деструктивного панкреатита у пациентов старшей возрастной группы. Тяжесть состояния пациентов определяется степенью не только интоксикации, но и декомпенсации хронических заболеваний. Показатели пульса, АД, частоты дыхания, суточное количество мочи у этих пациентов вариабельны и сугубо индивидуальны. Даже при морфологически среднетяжелой форме острого деструктивного панкреатита общее состояние пациентов расценивается как тяжелое и требует немедленной коррекции [1].
Наиболее часты осложнения представлены на рис. 3.
Ферментативная фаза [2] острого деструктивного панкреатита у пациентов старше 70 лет сопровождается высокой летальностью, а при развитии эндотоксинового шока в ранние сроки заболевания достигает практически 100%. 50% всех пациентов старшей возрастной группы при остром деструктивном панкреатите погибают, причем 50% летального исхода приходится на ферментативную фазу болезни [5].
Прогнозировать тяжесть острого деструктивного панкреатита в первые 3 сут от начала можно, основываясь на целом ряде прогностических систем. Наиболее приемлемыми в условиях оте- чественного здравоохранения мы считаем системы RANSON и оригинальную схему.
Для оценки тяжести общего состояния возможно использовать неспецифические шкалы APACHE II, SAPS, SOFA.
Информативность шкал RANSON и оригинальной шкалы представлена в таблице.
Информативность этих шкал не отличается от таковой у пациентов более молодого возраста. Прогностическая ценность систем оценки
|
Информативность шкал, % |
|
Сутки от начала |
|
|
|
|
|
болезни |
RANSON |
оригинальная |
|
шкала |
|
|
|
|
|
|
|
Первые |
25 |
48 |
Вторые |
82 |
87 |
|
|
|
20
