Vit D+ Vit K
.docКальциферолы. Д.
Они же циклогенсанолэтиленгидриндановые витамины.
В конце XIII в. было установлено, что рахит у детей излечивается приемом в пищу жира печени рыб, а в начале XIX в. был обнаружен лечебный эффект солнечного света. Позднее было обнаружено, что рахит развивается при нарушении обмена кальция и фосфора.
В 20-х годах 20 века выделены провитамины D (стерины), содержащиеся в подкожной клетчатке.
В 1930-1932 гг. Виндоуз выделил продукт облучения стерина из дрожжей – назвал его эргокальциферол (D2). Эргокальциферол усиливает абсорбцию кальция в кишечнике и усиливает его доставку в кости и эмаль зубов.
Витамин D1 – смесь эргокальциферола с токсическими продуктами. Витамины группы D имеют стероидную структуру и отличаются заместителями в положении 17.
 Холестан
– основа всех провитаминов D
(в чистом виде в природе не встречается).
Холестан
– основа всех провитаминов D
(в чистом виде в природе не встречается).
 Секохолестан
(секостерин) - основа структуры витаминов
группы D.
Секохолестан
(секостерин) - основа структуры витаминов
группы D.
Промышленное производство основано на использовании природных стеринов, которые представляют собой своеобразные провитамины кальциферолов. Провитаминные стерины подвергают фотоизомеризации.
Витамины группы D
|
Формула |
Название |
|
|
Ergocalciferolum (D2) 24-Метил-9,10-секохолеста-5,7,10(19),22-тетраен-3-бета-ол
|
|
|
По МФ: (5Z,7E,22E)-9,10-Секоэргоста-5,7,10,(19),22-тетраен-3-бета-ол. Провитамин
|
|
|
Провитамин эргокальциферола (эргостерин) 5,7,22-двойные связи
|
|
|
Holecalciferolum (D3) 9,10-Секохолеста-5,7,10,(19), -триен-3-бета-ол |
|
|
Провитамин холекальциферола Содержится в подкожной клетчатке |
|
|
22-Дигидроэргокальциферол (D4)
|
|
|
Ситокальциферол (24-Этилхолекальциферол (D5)) Выделен из масла пшеницы |
|
|
Стигмакальциферол (D6) Выделен из масла бобовых |
|
|
24-Альфа-метилхолекальциферол (D7) Получен синтетически |
Получение:
Фотолиз, облучение УФ светом при определенной длине волны. Источник – мицелий после получения пенициллина. Эти отходы содержат до 0,5% эргостерина.


Побочные продукты: токсистерин, супрастерин.
Описание: бесцветные или слегка желтоватые кристаллы (D2 – призматические или иглы, D3 –иглы) или кристаллический порошок без запаха. Не устойчив к действию света и кислорода воздуха.
Растворимость: ПНР в воде, ЛР в спирте, хлороформе, эфире, ацетоне, УР в жирных маслах.
Подлинность:
1. Температура плавления 113-1180С (D2); 84-850C (D3); 106-1080C (D4).
2. Удельное вращение - +83,50 (D2); +83-890 (D3); +89,30 (D4).
3. УФ-спектр (в спирте 1 максимум при 265 нм)
4. ИК-спектр
5. ТСХ
6. Реакция Либермана-Бурхарда по МФ (со смесью уксусного ангидрида и концентрированной серной кислоты) – переход окраски от красно-фиолетовой через синюю к темно-зеленой.
5. Отличие D2 и D3:
Д+спирт + к. H2SO4 -> D2-красное, D3-желтое.
6. С хлороформным раствором хлорида сурьмы (III) – оранжевая окраска, переходящая в розовую (без химизма).
Solutio Ergocalciferoli oleosa 0,125%
Состав: Д2 кристаллический 1,25
Масло соевое (подсолнечное) до 1 литра.
Описание: прозрачная маслянистая жидкость светло-желтого до темно-желтого цвета без прогорклого запаха.
Подлинность:
1. Навеску растворяют в хлороформе и добавляют раствор хлорида сурьмы III в хлороформе, содержащий 2% раствор ацетилхлорида (стабилизатор окраски) – появляется оранжево-розовое окрашивание. Продукт имеет максимум поглощения при длине волны 500 нм.
Очень чувствительная реакция. Люмистерин дает красное окрашивание, Холестерин –желтое.
2. ТСХ на пластинах с Al2O3 в сравнении с СОВС. Система хлороформ + ДМФА. 1 пятно основного вещества, дополнительно допускается 1 пятно примеси. Проявитель SbCl3 + CH3-COCl
Чистота: ТСХ
Количественное определение:
Фотоколориметрия
Берут точную навеску масляного раствора, подвергают щелочному гидролизу на водяной бане с обратным холодильником в присутствии гидрохинона (антиоксиданта). Разбавляют водой, неомыляемую фракцию извлекают эфиром. Эфир отгоняют в токе азота, чтобы не окислился сам D2. Остаток растворяют в хлороформе и проводят реакцию с SbCl3 + CH3-COCl. Затем измеряют оптическую плотность при 500 нм. Параллельно проводят реакцию с хлороформным раствором стандартного образца D2.

1 г эргокальциферола соответствует 40 млн. МЕ.
1 мл р-ра около 50000 МЕ
500 МЕ – профилактическая доза; 10000 15000 – лечебная.
Хранение: Список Б., в герметично закрытой емкости при температуре не выше 10 градусов.
Применение: профилактика заболеваний кож и слизистых ,рахит, туберкулез.
Производные нафтохинона. К.
Биологическая роль – повышает способность крови к коагуляции, антигеморрагическое действие. Суточная доза – 1,5-2 мг. Лечебная доза 10-15 мг/сут.
Производные 2-метил-1,4-нафтохинона:

Филлохиноны (К1) – R-это длинная цепь из 20 атомов изопреноидная.
Менахиноны (К2) – R состоит из различного числа частично насыщенных изопреноидных звеньев.

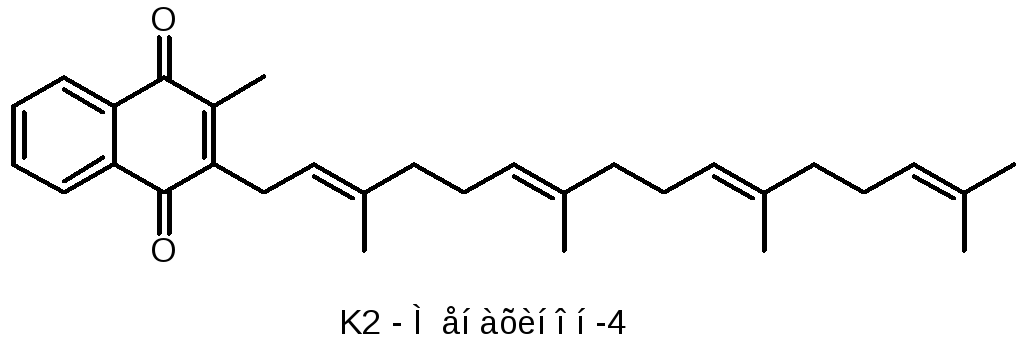
Витамины К2 (менахиноны) являются продуктами жизнедеятельности микроорганизмов, вырабатываются м/о в кишечнике человека.
Описание: К1 – желтая вязкая маслянистая жидкость с tплавления 20°С. К2 – желтые кристаллические вещества.
Для анализа используют ФМА и ФХМА:
Подлинность: УФ-СФМ, растворитель 2,2,4-триметилпентан, 4 максимума.
Чистота: ТСХ, рефрактометрия, E1%1см
Количественное определение:
1. УФ-СФМ в 2,2,4-триметилпентане.
Зависимость структура-активность:
Способность увеличивать свертываемость крови обусловлена ядром метилнафтахинона, при удалении метильной группы активность исчезает. Фитольный радикал в положении С3: при увеличении числа атомов углерода – увеличивается активность (до С20), при дальнейшем увеличении, уменьшается активность. Если в положении 3 убрать фитол, то активность увеличивается в 3 раза, но при этом увеличивается и токсичность.
Витамин К3: 2-метил-нафтахинон-1,4.

Описание: Вещество желтого цвета (в медицине не применяется, т.к. токсичен).
Витамины К способны к обратному окислению-восстановлению:

Получается витамин К4 (производное нафтагидрохинона).

K5 (2-метил-1-окси-4-аминонафталин) – активность как у К1.

К6 (2-метил-1,4-диаминонафталин)
Викасол – Vicasolum (Vikasolum)

2,3-дигидро-2-метил-1,4-нафтохинон-2-сульфонат натрия тригидрат.
Получение:
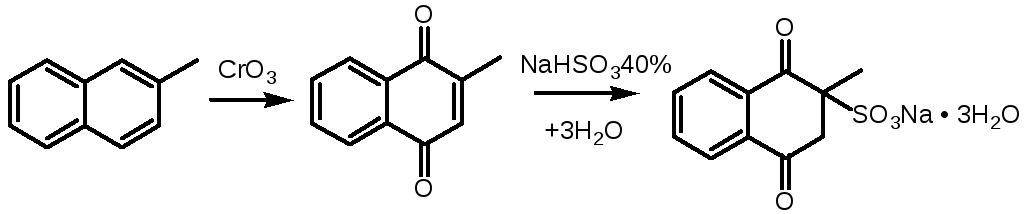
Описание: белый или белый с желтоватым оттенком кристаллический порошок без запаха.
Растворимость: легко растворим в воде, умеренно растворим в спирте 95%, ОМР в эфире.
Подлинность:
1. Щелочной гидролиз: готовится водный раствор ЛП, добавляют NaOH, через некоторое время выпадает осадок 2-метил-1,4-нафтохинона. Осадок извлекают хлороформом, фильтруют, хлороформ удаляют в вакууме, остаток растворяют в спирте, спирт удаляют досуха, определяют температуру плавления (104-107°С).

Реакцию можно использовать для количественного определения викасола методом гравиметрии.
2. На натрий – пламя.
3. + к. H2SO4 – отщепляется сульфогруппа в виде SO2 (запах). Потом (Не по ГФ) можно доказать SO2 с йодаткрахмальной бумагой:
5SO2 + 2KIO3 -> I2 + K2SO4 + 4SO3
Чистота:
1). Прозрачность и цветность.
2). Гидросульфит натрия. Допустимая примесь (до 2%).
Определяют йодометрически: навеску растворяют в воде, добавляют 0,1М H2SO4, точный избыток 0,1М I2:
H2O + NaHSO3 + I2 ->(H2SO4) NaHSO4 + 2HI
Выдерживают некоторое время, непрореагировавший йод титруют тиосульфатом.

3). 2-Метил-1,4-нафтогидрохинон-3-сульфонат. Недопустимая примесь. К раствору препарата в воде добавляют о-фенантролин. Не должна появиться муть.
Количественное определение:
1. Прямая цериметрия. Точную навеску растворяют в воде, добавляют 5М NaOH (гидролиз до минадиона). Минадион извлекают хлороформом, фильтруют, удаляют хлороформ под вакуумом. Сухой остаток растворяют в ледяной уксусной кислоте и р. HCl, добавляют 3,0 Zn пыли порциями, выдерживают 30 минут в темном месте, перемешивают (идет восстановление до витамина К4). Отфильтровывают избыток Zn пыли, к фильтрату добавляют индикатор о-фенантролин, титруют Ce(SO4)2 до зеленой окраски.



f=1/2
КТТ:

Не ГФ: гравиметрия осадка минадиона; полярография (основана на обратимом окислении-восстановлении).
Формы выпуска: порошок; таблетки по 0, 015 г; 1 % раствор в ампулах по 1 мл.
Хранение: список Б. В хорошо укупоренной таре, предохраняющей от действия света.
Применение: состояния сопровождающиеся гипопротромбинемией и кровоточивостью. При капиллярных кровотечениях.
Антивитамин К:
Препятствует образованию протромбина и влияет на другие факторы свертываемости крови. Антикоагулянты непрямого действия. Применяется при тромбозах, тромбоэмболиях, тромбофлебите. Лекарственные препараты отличаются по скорости наступления эффекта. Действуют через 12-18 часов после введения и прекращают действовать через 2-7 дней после отмены. Существует три подгруппы:
1. Подгруппа дикумарина: дикумарин исключен из списка ЛС из-за высокой токсичности. Используют:
 Neodicumarinum.
Neodicumarinum.
Этиловый эфир ди-(4-окси-кумаринил)-уксусной кислоты.
Белый мелкокристаллический порошок. ОМР в воде, список А.
2. Подгруппа производных 3-этил-4-гидроксикумарина.
|
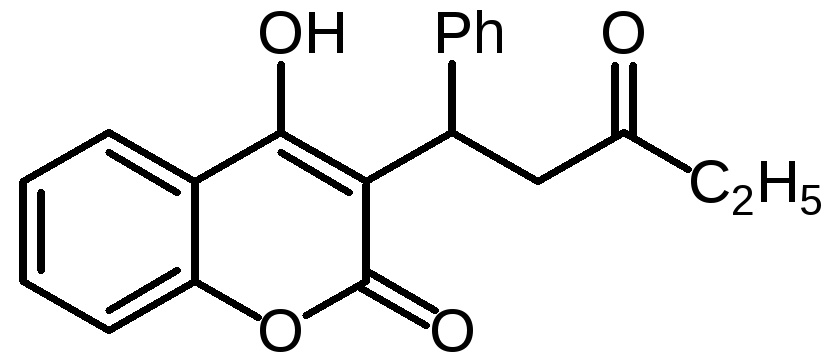
Phepromarolum. 3-(2-фенил-бета-проионилэтил) -4-гидроксикумарин. |
Nitropharinum. 3-(альфа-п- нитрофенил-бета-пропионилэтил) -4-гидроксикумарин.
|
|
Syncumar. 3-(альфа-фенил- бета-ацетил)-4-гидроксикумарин. Список А. |
|
3. Подгруппа производных 1,3-индандиона.
|
Phenylinum. 2-фенил-индандион-1,3. |
Omephinum. 2-фенил-2-гидроксиметил-индандион-1,3. Список А. |