- •Министерство здравоохранения российской федерации
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот и сульфохлоридов
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •8. Сульфирование хлорсульфоновой кислотой
- •9. Другие методы получения сульфокислот
- •10. Получение хлорангидридов сульфоновых кислот
- •Основные методы получения ароматических сульфохлоридов
- •Сульфохлорирование ароматических углеводородов
- •Сульфохлорирование аренов хлорсульфоновой кислотой в среде инертного органического растворителя
- •Сульфохлорирование алканов
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью азотной и уксусной кислот
- •7. Нитрование смесью концентрированной азотной кислоты или ее солей с уксусным ангидридом
- •8. Нитрование разбавленной азотной кислотой
- •Глава 3. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором
- •2. Окисление растворов бромида натрия гипохлоритом натрия:
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •Синтез геминальных полигалогеналканов из карбонильных соединений и карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •6. Некоторые реакцииполучения нитрозо- и диазосоединений
- •Глава 5. Замещение галогена и сульфогруппы на другие функциональные группы
- •1. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизме реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы
- •Замена атома галогена на меркапто- и алкил(арил)тиогруппы
- •Замена атома галогена на аминогруппы
- •Замена атома галогена на цианогруппу
- •Замена атома галогена на группу -so3Na
- •2. Нуклеофильное замещение сульфогруппы
- •Реакции щелочного плавления
- •Примеры нуклеофильной замены сульфогруппы в промышленности
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
- •Глава 8. Методы восстановления
- •1. Химические методы восстановления
- •Восстановление металлами и солями металлов
- •Восстановление натрием
- •Восстановление оловом и хлоридом олова (II) в кислой среде
- •Восстановление цинком
- •Восстановление железом
- •Восстановление алкоголятами алюминия (метод Меервейна-Понндорфа-Верлея)
- •Восстановление гидридами металлов
- •Восстановление по Кижнеру-Вольфу
- •Восстановление соединениями серы
- •Восстановление сульфидами щелочных металлов
- •Восстановление нитрогруппы серой в щелочной среде
- •Восстановление сернистой кислотой и ее солями
- •Восстановление дитионитом натрия
- •Каталитическое восстановление водородом
- •Восстановление на никелевых катализаторах
- •Восстановление на платиновых и палладиевых катализаторах
- •3. Электролитическое восстановление
- •Глава 9. Методы окисления
- •1. Синтез алкенов методами каталитического и окислительного дегидрирования
- •2. Синтез альдегидов с использованием методов окисления и дегидрирования
- •3. Окислительные методы получения кетонов
- •4. Окислительные методы получения карбоновых кислот
- •5. Окисление непредельных углеводородов
- •6. Окисление ароматического цикла
10. Получение хлорангидридов сульфоновых кислот
Введение группы –SO2Clв молекулу органического соединенияиспользуетсякак для получения сульфохлоридовAr(R)SO2Cl, так и сульфокислот последующим гидролизом сульфохлоридов. Последний способ является одним из основных при получении алкансульфокислот.
Сульфохлориды являются важными промежуточными продуктами в синтезе сульфаниламидных препаратов. Они используются для получения амидов, анилидов, эфиров сульфокислот и др. соединений.
Основные методы получения ароматических сульфохлоридов
Аренсульфохлориды в основном получают:
1. Сульфохлорированием аренов избытком хлорсульфоновой кислоты (основной промышленный метод):
![]()
2. Действием хлоридов фосфора, тионилхлорида или HSO3Clна сульфокислоты и их соли:
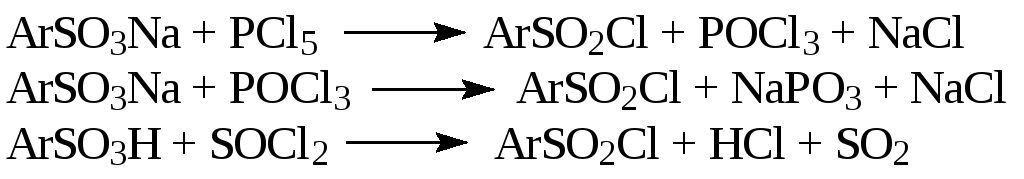
3. Окислением хлором сульфиновых кислот, сульфонов, тиофенолов, их производных, дисульфидов. Этот метод имеет практическое значение, но применяется реже:
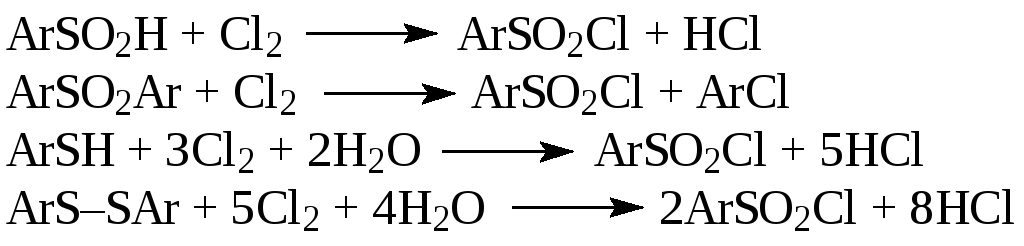
4. Взаимодействием аренов с сульфурилхлоридом в присутствии хлорида алюминия (в качестве побочных продуктов образуются сульфоны):
![]()
Другие способы получения ароматических сульфохлоридов имеют меньшее значение.
Сульфохлорирование ароматических углеводородов
Замена атома водорода в молекуле ароматического соединения на группу –SO2Clс помощью хлорсульфоновой кислотыявляется сложным процессом. Считают, что сначала образуются соответствующие сульфокислоты, которые затем превращаются в сульфохлориды.
![]()
В качестве побочных продуктовпри сульфохлорировании образуются сульфоны и аренсульфокислоты:
![]()
![]()
Для увеличения выхода целевого продукта и уменьшения избытка хлорсульфоновой кислоты предлагаютдобавлять к сульфомассе хлорид натрия,который частично связывает серную кислоту, образующуюся в ходе реакции, что в некоторых производствах привело к увеличению выхода сульфохлорида и уменьшению количества сульфокислот:
![]()
Другие способы связывания серной кислоты и замены хлорсульфоновой кислоты практического применения не нашли.
В большинстве случаев реакцию ведут при 40—50 °С и 5—6 кратном избытке хлорсульфоновой кислоты.
Процесс сульфохлорирования можно вести какнепрерывным, так ипериодическимспособом. Периодический метод применяется значительно чаще.
Выделение сульфохлоридов, как правило, осуществляютразбавлением сульфомассы при выливании ее на лед или воду, охлаждаемую льдом или рассолом. Сульфохлориды не растворяются или плохо растворяются в холодной воде ивыпадают в осадок. Процесс выделения следует проводить при низкой температуре и возможно более быстро, т.к. перегрев может привести к гидролизу сульфохлорида:
![]()
Технологический режим выделения сульфохлорида из сульфомассы может бытьнепрерывным в аппарате колонного типа с мешалкой. Через штуцеры, находящиеся в нижней части аппарата, непрерывно подаются сульфомасса и холодная вода (рис. 3). Скорость смешения регулируется таким образом, чтобы температура суспензии не превышала 20—25 °С, и сульфохлорид выделялся в виде гранул.

Рис. 3. Аппарат для непрерывного выделения сульфохлоридов
Это ускоряет фильтрацию и промывку осадка в 3—4 раза и приводит к увеличению выхода сульфохлорида на 5 % за счет уменьшения потерь при гидролизе. Кроме того, гранулированный продукт более стабилен при хранении, так как имеет меньшую влажность и лучше отмыт от кислоты.
Выделяющийся в процессе реакции хлороводород улавливаютводой в поглотительной системе. Для более полнойутилизацииотходов производства процесс разложения сульфомассы можно вестив две стадии:
1. Разложение избытка хлорсульфоновой кислоты до серной кислоты. Эту операцию можно проводить непосредственно в сульфураторе после охлаждения сульфомассы. Хлороводород полностью улавливают с получением соляной кислоты.
2. Разбавление полученного раствора сульфохлорида в серной кислоте и выделение сульфохлорида.
Этот способ позволяет почти полностью утилизировать хлористый водород. Выход сульфохлорида при этом не снижается.
Сульфохлорирование фенилуретилана и ацетанилидаимеет наибольшее промышленное значение (синтезсульфаниламидных и др. препаратов):
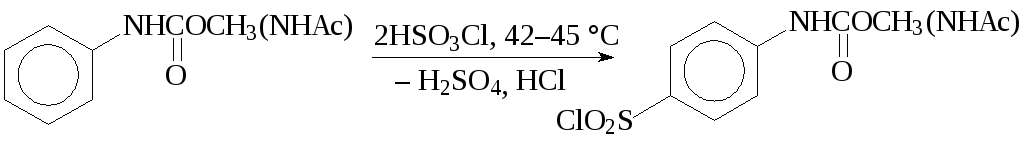
Реакцию проводят при температуре 42—45 °С и избытке хлорсульфоновой кислоты в 5,3—5,5 раза. Выход сульфохлорида составляет 82—83 %.
о- и п-Толуолсульфохлоридыиспользуются в производствах сахарина и лекарственного препарата этамид.