
№3 ЗЕРТХАНАЛЫ_ Ж_МЫС БУЛАНУ ТЕПЕ –ТЕ_ДІГІ
.doc
№4 ЗЕРТХАНАЛЫҚ ЖҰМЫС
БУЛАНУ ТЕПЕ –ТЕҢДІГІ
|
4.1 Жұмыстың мақсаты Зерттелетін сұйықтың бу қысымын әр түрлі температурада өлшеу арқылы булану энтальпиясын анықтау. 4.2 Жалпы мәліметтер Химиялық әрекеттесуі жоқ гетерогендік жүйелерде бөлшектердің тек қана бір фазадан екінші фазаға өту процестерінің тепе-теңдігін фазааралық тепе-теңдік немесе фазалық өзгерістер деп атайды. Таза заттың агрегаттық бір күйден екінші күйге айналуы, мысалы, балқу, булану, айдау (возгонка) және қатты денелердің бір модификациядан екіншісіне өту процестері қызықты мәліметтер береді. |
|
Бүл процестерде әрбір қысымға белгілі бір температура сәйкес келеді. Осы температурада екі фаза термодинамикалық тепе-теңдік күйінде болады. Таза заттардың фазалық өзгеріс температурасы (мысалы Тбалқу, Тқайн.) тәжірибенің жағдайларына емес, тек қана қысымға тәуелді болады. Фазалық өзгеріс температурасының қысымға тәуелділігі Клаузиус–Клапейрон теңдеуімен сипатталады.
![]() ,
(4.1)
,
(4.1)
мұндағы Нфаз – фазалық өзгеріс жылуы, Дж/моль;
V – фазалардың мольдік көлемдерінің айырымы;
Т - температура.
Булануы немесе қайнауы кезінде сұйықтың мольдік көлемін бу көлемі-мен салыстырғанда ескермеуге болады және буды идеал газ деп алып келесіні қабылдау керек:
V = Vбу - Vсұй. = Vбу, ал Vбу = RT/P. (4.2)
(4.2) теңдеуді (4.1) теңдеуге қойып, булану процесіне былай жазуға болады:
![]() .
(4.3)
.
(4.3)
(4.3) теңдеуді интегралдау (4.4) теңдеуге келтіреді:
![]() .
(4.4)
.
(4.4)
(4.4) теңдеуід түзу сызықтың теңдеуі болып келеді. Егер ордината өсіне lnP, ал абсцисса өсіне 1/Т – мәндерін салсақ, түзу сызық шығатынын көруге болады (4.1 сурет). Алынған түзу сызықтың абсцисса өсімен беретін бұрышының тангенсі бойынша фазалық өзгеріс жылуын анықтауға болады (берілген жағдайда булану жылуын Нбул.).
Нбул. = Rtg. (4.5)
|
4.1 - сурет |
Булану жылуын графиктік әдіспен ғана емес, сонымен қатар (4.3)-теңдеуден де есептеп шығаруға болады. Ол үшін (4.3) теңдеуді Р1 және Р2 сәйкес келетін Т1 мен Т2 аралығында интегралдасақ, онда (4.6) жуықтық теңдеуді алуға болады:
|
Осыдан булану жылуын есептеуге болады және бірнеше мәндерінен оның орташа мәнін анықтайды.
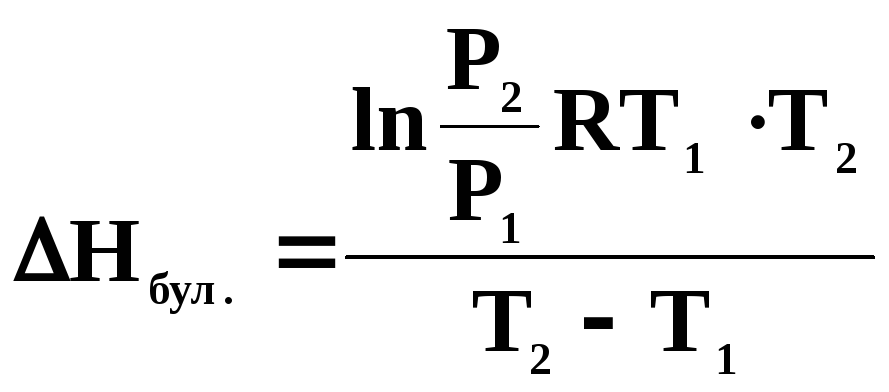 .
(4.7)
.
(4.7)
4.3 Құралдар, ыдыстар, реактивтер
-
Сандық температура өлшегіші, 4-2.
-
Температура көрсеткіш, Pt100.
-
Температура көрсеткішнің қорғағыш қаптамасы
-
Қол барометрі/ манометрі.
-
Қысым бергіш.
-
Калориметр.
-
Түбі дөңгелек колба, 100 мл, 3-мойынды.
-
1- тік жолды кран
-
3 - жолды кран.
-
Қауіпсіз ыдыс қысымы манометрімен.
-
Ағын су насосы.
-
шыны таяқша, l=300 мм, d=8 мм
-
шыны түтікше.
-
Силикондық түтікшелер.
-
Өлшегіш цилиндр, 50 мл
-
Оңай ұшатын сұйық.
-
Мұз, су, натрий хлориді.
4.4 Жұмысты жүргізу тәртібі
Тәжірибелік қондырғы 4.2 суретте көрсетілген.
Температуралардың әр мәні кезіндегі сұйық бетіндегі тұрақталған сұйықтың бу фазасының меншікті қысымы будың қысымы деп аталады. Егер бу фазасын шығару арқылы сыртқы қысымды төмендетсек сұйық фазасының булануы арқылы тепе-теңдік орнына келеді.

4.2 сурет
3-мойынды колбаның бір мойыны қорғағыш қаптамасына салынған температура көрсеткіші кранмен бекітілген және жоғарғы мойыны өткізгіш арқылы сандық манометрге қосылған. 3-ші мойыны колбаның қауіпсіз ыдысына, одан әрі 3-жолды кран арқылы ағын су насосына қосылған.
Жылудың берілуін жақсарту үшін колбаның мойнындағы қорғағыш қаптамасына бірнеше тамшы оңай ұшатын сұйық тамызамыз, сонан соң оған температура көрсеткішін саламыз. Екінші температура көрсеткішін калориметрге саламыз. Екі көрсеткіште температураның сандық өлшегішіне қосылады.
Қондырғыны ток көзіне қосамыз. Температура өлшегішін артқы панеліндегі кнопканы басып қосамыз. Колбадағы да және калориметрдегі де температура температураның сандық өлшегішінде Цельсий градусін көрсетеді. Барометрдегі «on» кнопкасын басу арқылы оны іске қосамыз. Онда жүйедегі қысымның мәні (гПа) пайда болады.
Калориметрге мұз, мұздай су және ас тұзы (оқытушының айтуы бойынша) қоспасын саламыз, сонан соң қоспаның температурасын температура өлшегіші арқылы бақылаймыз.
50 мл оңай ұшатын сұйықты дөңгелек колбаға құйып, салқын қоспаға батырмай қоя тұрамыз. 3-жолды кранды манометрі бар қауіпсіз ыдыста «қызыл белгі-төменде» қалпына келтіріп, ағын су насосына қосып оңай ұшатын сұйық қайнағанша колбадан ауаны айдаймыз. Оңай ұшатын сұйық қайнағаннан кейін тура (прямой) кранды жауып, дөңгелек колбаны салқын қоспаға батырамыз. Қалай колбадағы температура калориметрдегі температурамен теңескен кезде, яғни, олар қосылған температура өлшегішінде температура бірдей мәнді көрсеткен кезде тура (прямой) кранды ашып, колбадағы қалдық ауаны жібереміз. Қысым тұрақты мәнге жеткен кезде сол кранды жабамыз және 3-жолды кранды абайлап ашып, ауаны қауіпсіз ыдысқа жібереміз («қызыл белгі» - сол жақта).
Насосты жауып, дөңгелек колбадағы қысымды манометрдің көмегімен анықтаймыз. 10 минут ішінде 10 гПа-ға дейін көтерілу тиіс (басқаша айтқанда, қосылыстардың ауа жібермейтінін (герметичность) тексереміз).
Дөңгелек колбаның температурасын, салқын қоспаға шыны түтікше көмегімен жылы су қосып (қоспаны жақсылап шыны таяқшамен араластырады) 2-3°C сайын көтеріп отырады. Температураның әр көтерілісінде буланудың қайтадан тепе-теңдікке келуін тосады (калориметрдің және колбаның температураларының мәндері өте жақын болулары тиіс), сонан соң оңай ұшатын сұйықтың колбадағы температурасын және оған сәйкес қысымын жазып алу керек.
Осылай тәжірибенің температурасы бөлме температурасына жеткенше жалғастыру керек. Содан кейін кранды абайлап ашып, ауаны колбаға жібереміз.
Тәжірибе нәтижелерін 4.1 кестесіне жазыңыздар.
4.1 кесте
|
№ тәжірибе |
t0C |
T, K |
Манометр көрсеткіші P, гПа |
lnP |
1/T |
Hбул. |
|
|
|
|
|
|
|
|
Алынған нәтижелердің негізінде:
-
зерттеліп отырған сұйықтың бу қысымының Р температураға Т тәуелділік графигін тұрғызыңыздар;
-
lnP-ң 1/Т-ға тәуелділік графигін тұрғызыңыздар;
-
lnP-ң 1/Т-ға тәуелділік графигінен 4.1 суретінде көрсетілгендей тангенс бұрышы бойынша булану жылуының Hбул. мәнін анықтаңыздар;
-
булану жылуын бірнеше температура аралығы үшін Клаузиус-Клапейронның (4.7) жуықтық теңдеуін қолдана отырып есептеңіздер және осы мәндердің орта мәнін график жолымен алынған мәнмен салыстырыңыздар.
4.5 Есеп беру мазмұны
-
Жұмыстың атауы мен мақсаты.
-
Қондырғының тізімдемесі.
-
Жұмыстың орындалу әдістемесі .
-
Тәжірибелік мәндер кестесі, графиктер, тапсырма бойынша есептер.
-
Қорытынды.
4.6 Тексеру сұрақтары
-
Қаныққан бу қысымын өлшеу әдістің принципі мен схемасы.
-
Булану және балқу процестері үшін Клаузиус-Клапейрон теңдеуін қорыту және оны талдау.
-
Сұйықтардың булану процесіне арналған Клаузиус-Клапейронның жуықтық теңдеуі. Булану жылуын Клаузиус-Клапейронның теңдеуі бойынша аналитикалық және графиктік жолмен есептеу.
Құрастырушылар: Осадчая Э.Ф.
Журсумбаева М.Б.
Бектурганова Н.
№13 бұйрықпен 18.06.10ж.
Химия кафедрасының мәжілісінде бекітілген


