
- •Введение
- •Глава 1. Технология производства многослойных печатных плат (мпп) как источник образования сточных вод
- •1.1. Процессы химического меднения в производстве мпп
- •1.2. Гальваническое меднение
- •Глава 2. Реагентный метод очистки
- •2.1. Реагентная очистка сточных вод от ионов тяжелых металлов
- •Глава 3. Аппараты очистки сточных вод в реагентном методе
- •3.1. Отстойники
- •Процесс отстаивания сточной воды
- •Горизонтальные отстойники
- •Вертикальные отстойники
- •Радиальные отстойники
- •Осветлители
- •Тонкослойные отстойники
- •3.2. Усреднители
- •3.3. Решетки
- •3.4. Шламоуплотнитель
- •3.5. Фильтр-прессы
- •3.6. Двухслойные фильтры
- •Глава 4. Расчет и чертеж реактора-отстойника для очистки сточных вод.
- •Литература
1.1. Процессы химического меднения в производстве мпп
Электрохимический способ получения печатных плат осуществляется посредством следующих основных операций: резки заготовок, сверления отверстий, подлежащих металлизации; подготовки поверхности; химического меднения; усиления меди гальваническим меднением; нанесения защитного рельефа на пробельные места гальванического меднения; гальванического покрытия сплавом олово—свинец; удаления защитного рельефа; травления меди с пробельных мест.
Процесс химического восстановления меди имеет каталитическую природу, т.е. осаждение металла начинается только на активной поверхности катализатора и продолжается автокаталитически уже на меди. Операция, в результате которой на диэлектрике создаются каталитические частицы, называется активированной.
В практике химического меднения полимерных материалов активирование осуществляют последовательной обработкой деталей вначале в растворе хлористого олова (SnCl2·H2O 20 — 25 г/л, NaCl 40 — 60 мл/л), а затем после промывки в воде детали погружают в раствор хлористого палладия, содержащий 0,5 — 1,0 г/л PlCl2 и 12 — 18 мл/л HCl плотностью 1190 кг/м3 и снова промывают. Двухзарядные ионы олова, адсорбирующиеся на поверхности диэлектрика, восстанавливают ионы палладия на диэлектрике до металла по реакции:
Sn2+ + Pd2+ —— ” Sn4+ + Pd
Для осуществления процесса химического меднения рекомендуется много разнообразных растворов. Состоят они из соли двухвалентной меди (чаще всего сернокислой), комплексообразователя, восстановителя-формалина, стабилизирующих и ускоряющих добавок, гидроокиси натрия, регулирующей кислотность раствора.
В зависимости от комплексообразователя различают виннокислые, трилоновые (этилендиаминтетрауксуснокислые) и другие растворы. Наибольшие практическое применение получили первые из них. Они содержат виннокислый калий-натрий (называемый сегнетовой солью, или солью Рошеля), который образует с медью довольно прочный комплексный анион [CuC4H4O6(OH)2]2-. Значительное распространение получили трило-новые растворы, содержащие в качестве комплексообразователя трилон Б.
В качестве стабилизаторов процесса применяют различные тиосоединения (чаще всего тиосульфат натрия, тиомочевину, сульфид свинца, цистин, диэтилдитиокарбамат натрия, роданин, 2-меркаптобензтиазол), а также цианиды, роданиды, полисульфиды, фенантролины и их производные, соединения селена, ртути, различные высокомолекулярные вещества, некоторые окислители, в том числе кислород, и др.
Реакция восстановления меди в процессе химического меднения может быть выражена следующим уравнением:
2Н2СО
+ Cu2+
+
4OH¯
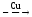 Cu
+ H2
+ 2HCOO¯
+ 2H2O.
(1)
Cu
+ H2
+ 2HCOO¯
+ 2H2O.
(1)
Она протекает при комнатной температуре и в щелочной среде при pH>10,5. Одновременно с реакцией (1) происходит побочная реакция Канниццаро, вследствие которой формальдегид окисляется в формиат-ион и метиловый спирт:
2Н2СО
+ OH¯
 HCOO¯
+ СH3OН.
(2)
HCOO¯
+ СH3OН.
(2)
Возможна также реакция восстановления Cu2+ до Cu+ с образованием закиси:
2
Cu2+
+
5OH¯
+ Н2СО
 Cu2O
+ HCOO¯
+ 3H2O.
(3)
Cu2O
+ HCOO¯
+ 3H2O.
(3)
В результате протекания приведенных реакций в растворе меднения уменьшается содержание Cu2+, формальдегида OH¯, накапливаются Na2SО4, CH3OH и HCOОNa (сернокислый натрий, метиловый спирт и формиат натрия – муравьино-кислый натрий).
На скорость осаждения меди, стабильность раствора и физические свойства покрытия (плотность, цвет, блеск и т.п.) влияют природа комплексообразователя и его концентрация в растворе. В большинстве случаев, чем прочнее образующееся комплексное соединение меди и больше концентрация комплексообразователя в растворе, тем меньше скорость восстановления Cu2+ и выше стабильность раствора. Повышение концентрации формальдегида в виннокислых растворах мало влияет на скорость меднения.
С повышением температуры растворов скорость восстановления меди и меднения возрастает с одновременным снижением их стабильности.
По опыту ряда предприятий достаточно хорошей стабильностью обладает раствор следующего состава:
Сернокислая медь 10—15 г/л; винограднокислый калий-натрий 60—70 г/л;
едкий натр 20—25 г/л; кальцинированная сода 20 г/л; хлористый никель 4 г/л; формальдегид (37 %-ный), 10—15 мл/л; диэтилдитиокарбомат, 50 мг/л;
pН 12,8 [2].
