- •Раздел 1. Понятие о биотехнологии
- •Нанобиотехнология -соединение биотехнологии и нанотехнологий - радикально меняет стратегию создания новых препаратов. Например, создание биосенсоров для индикации биологически активных веществ.
- •Ферментативный катализ и основы кинетики ферментативных реакций
- •Носители для иммобилизации ферментов
Носители для иммобилизации ферментов
По Дж. Порату (1974), идеальные материалы, используемые для иммобилизации ферментов, должны обладать следующими основными свойствами: нерастворимостью; высокой химической и биологической стойкостью; значительной гидрофильностью; достаточной проницаемостью как для ферментов, так и для коферментов, субстратов и продуктов реакции; способностью носителя легко активироваться (переходить в реакционноспособную форму).
В зависимости от природы носители делятся на органические и неорганические материалы.
Органические полимерные носители. Иммобилизация многих ферментов осуществляется на полимерных носителях органической природы. Существующие органические полимерные носители можно разделить на два класса: природные и синтетические полимерные носители. В свою очередь, каждый из классов органических полимерных носителей подразделяется на группы в зависимости от их строения.
Среди природных полимеров выделяют белковые, полисахаридные и липидные носители, а среди синтетических — полиметиленовые, полиамидные и полиэфирные.
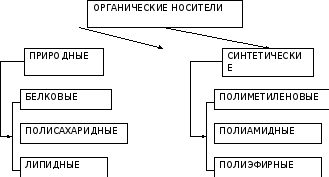
Рис. 4.
К преимуществам природных носителей следует отнести их доступность, полифункциональность и гидрофильность, а к недостаткам - биодеградируемость и достаточно высокую стоимость.
Из полисахаридов для иммобилизации наиболее часто используют целлюлозу, декстран, агарозу и их производные.
Из природных аминосахаридов в качестве носителей для иммобилизации применяют хитин, который в значительных количествах накапливается в виде отходов в процессе промышленной переработки крабов и креветок. Хитин химически стоек и имеет хорошо выраженную пористую структуру.
Синтетические полимерные носители. Благодаря разнообразию и доступности материалы этой группы широко используются как носители для иммобилизации. К ним относятся полимеры на основе стирола, акриловой кислоты, поливинилового спирта; полиамидные и полиуретановые полимеры.
Носители неорганической природы. В качестве носителей наиболее часто применяют материалы из стекла, глины, керамики, графитовой сажи, силикагеля, а также силохромы, оксиды металлов. Их можно подвергать химической модификации, для чего носители покрывают пленкой оксидов алюминия, титана, гафния, циркония или обрабатывают органическими полимерами. Основное преимущество неорганических носителей - легкость регенерации. Подобно синтетическим полимерам, неорганическим носителям можно придать любую форму и получать их с любой степенью пористости.
Методы иммобилизации ферментов
Существуют два принципиально различных метода иммобилизации ферментов: без возникновения ковалентных связей между ферментом и носителем (физические методы иммобилизации) и с образованием ковалентной связи между ними (химические методы иммобилизации).
Физические методы иммобилизации ферментов:
Адсорбция ферментов на нерастворимых носителях.
Иммобилизация ферментов путем включения в гель.
Иммобилизация ферментов в полупроницаемые структуры.
Химические методы иммобилизации ферментов.
Иммобилизация ферментов на носителях, обладающих гидроксогруппами.
Иммобилизация ферментов на носителях, обладающих аминогруппами.
Иммобилизация на носителях, обладающих активированными производными карбоксильной группы.
Иммобилизация на носителях, обладающих сульфгидрильными группами.
Источники ферментов
Ферменты присущи всем живым организмам, но для их выделения используют те природные объекты, в которых содержание энзимов составляет не менее 1%. Для промышленного получения ферментов используют проросшее зерно различных злаков и бобовых, латекс и сок зеленой массы ряда растений, а также отдельные ткани и органы животных. Практически неограниченный источник ферментов – микроорганизмы (бактерии, грибы, дрожжи), содержание которых можно повысить в десятки и сотни раз методами мутагенеза, селекции и индукции биосинтеза.
Как известно, ферменты животного происхождения преимущественно выделяют из органов, в которых протекают интенсивные биохимические процессы.Из слизистой желудка свиней и крупного рогатого скота получают препарат пепсина. Из поджелудочной железы свиней получают смеси трипсина, хемотрипсина, липаз и амилаз. Из желудка телят выделяют сычужный фермент, широко используемый в сыроделии. Для нужд медицины и биохимии ферментные препараты выделяют из мышц, в том числе из сердца, печени, селезенки, почек, тонкого кишечника. Некоторые широко известные ферменты животного происхождения получают в виде различных препаратов (табл. 20).
Таблица 20 Некоторые ферменты животного происхождения
|
Фермент |
Источник |
|
Лактатдегидрогеназа |
Крупный рогатый скот, сердце |
|
Каталаза |
Крупный рогатый скот, свинья, печень |
|
Сычужный фермент |
Крупный рогатый скот, сычуг |
|
Щелочная фосфатаза |
Крупный рогатый скот, кишечник |
|
Гиалуронидаза |
Крупный рогатый скот, семенник |
|
Фумараза и трансаминаза |
Свинья, сердце |
|
Трипсин, химотрисин, карбоксилпептидаза, эластаза |
Свинья, поджелудочная железа |
|
Пепсин |
Свинья, желудок |
|
Аминоацилаза |
Свинья, почки |
|
Люцифераза |
Светляки, мышечная ткань |
|
Ацетилхолинэстераза |
Электрический угорь, мышечная ткань |
Из ферментов растительного происхождения наиболее широко в народном хозяйстве используют амилазы и папаин. Условно ферментным препаратом можно назвать и ячменный солод, в котором содержится до 1% амилаз.
Растительная протеаза – папаин – содержится в плодах дынного дерева. Только в США ежегодно расходуют около 100 т папаина для обработки (тендеризации, т.е. размягчения) мяса. Папаин, а также протеазы фицин и бромелин, контактируя с мясом в течение 2 ч при комнатной температуре, расщепляют белки соединительной ткани - коллаген и эластин.
Таблица 21
Некоторые ферменты растительного происхождения
|
Фермент
|
Источник
|
|
Амилазы
|
Ячмень
|
|
Протеазы Папаин Фицин Бромелин
|
Дынное дерево Фиговое дерево Ананас
|
|
Кислая фосфатаза
|
Картофель
|
|
Пероксидаза
|
Хрен
|
|
Уреаза
|
Канавалия мечевидная
|
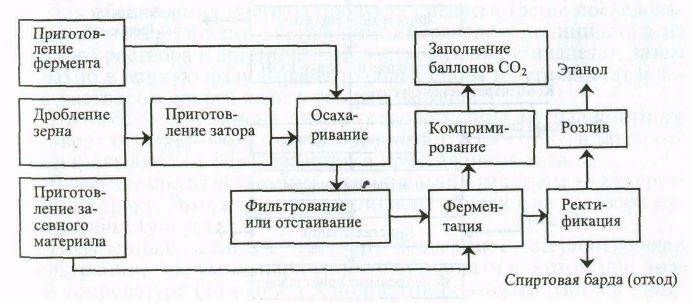
Получение спирта