
- •1.Введение
- •2.Описание технологической схемы установки
- •3.Расчет и выбор основного оборудования
- •3.1. Расчет подогревателя исходного раствора
- •3.1.1. Задание на расчет подогревателя исходного раствора
- •3.1.2 Уточненный выбор конструкции теплообменника и его размеров
- •3.2 Расчет двухкорпусной выпарной установки
- •3.2.1 Задание на расчет двухкорпусной прямоточной выпарной установки
- •3.2.2 Расчет поверхности теплообмена
- •3.2.3 Размеры сепарационного пространства
- •3.2.4 Тепловая изоляция аппарата
- •3.2.5 Диаметры штуцеров и трубопроводов для материальных потоков
- •3.2.6 Механический расчет элементов аппарата
- •3.3 Блок создания и поддержания вакуума
- •3.3.1 Расчет барометрического конденсатора смешения
- •3.3.2 Расчет и выбор вакуум-насоса
- •4. Расчет и выбор вспомогательного оборудования
- •4.1 Перекачивающие насосы
- •4.2 Конденсатоотводчики
- •4.2.1 Конденсатоотводчик для подогревателя исходной смеси
- •4.2.2 Конденсатоотводчик для первого корпуса
- •4.2.3 Конденсатоотводчик для второго корпуса
- •4.3 Емкости
- •4.3.1 Емкость для исходного раствора
- •4.3.2 Емкость для упаренного раствора
- •5. Список литературы
3.2.2 Расчет поверхности теплообмена
1. Общее количество выпаренной воды


Предварительное распределение W по корпусам выполним с учетом отбираемого экстра-пара E1:




Проверка:

2. Концентрация раствора в I корпусе находится из формулы (3.22)


Температурную депрессию в
I корпусе находим как стандартную по
 :
:
 .
Более удобно находить
.
Более удобно находить
 по графику (рис.3.1) построенному по
табличным данным [7, с. 187].
по графику (рис.3.1) построенному по
табличным данным [7, с. 187].

Рис. 3.1 Зависимость стандартной температурной депрессии от концентрации водного раствора NH4NO3.
Расчет температуры кипения t2 и температурной депрессии δ2 для II корпуса.
При концентрации
 температура кипения раствора при
атмосферном давлении (рис. 3.1) равна
температура кипения раствора при
атмосферном давлении (рис. 3.1) равна
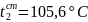 (следовательно,
стандартная депрессия
(следовательно,
стандартная депрессия
 ).
).
Депрессия при малом давлении P2 (во II корпусе) меньше стандартной и может быть рассчитана по правилу Бабó:

Давление насыщенных паров воды при
температуре кипения раствора
составляет
 [6, приложение 2]. При стандартных условиях
[6, приложение 2]. При стандартных условиях
 ,
так что константа Бабó равна:
,
так что константа Бабó равна:

Тогда из (3.25) давление насыщенных паров воды при температуре кипения раствора будет равна:

Где

По этому давлению в таблицах для
насыщенного водяного пара [6, приложение
2] находим температуру кипения раствора
во II корпусе
 Поскольку температура вторичного пара
во II корпусе определяется по заданному
Поскольку температура вторичного пара
во II корпусе определяется по заданному
 Па и равна
Па и равна
 то температурная депрессия, найденная
по правилу Бабó равна:
то температурная депрессия, найденная
по правилу Бабó равна:


Поправку Стабникова при расчете
температурной депрессий
 для концентрированного раствора NH4NO3
рекомендуется учитывать [1].
для концентрированного раствора NH4NO3
рекомендуется учитывать [1].
Согласно этому методу, температурная депрессия δ при любом рабочем давлении может быть вычислена по формуле:

где
 – температурная
депрессия, определяемая по правилу
Бабо;
– температурная
депрессия, определяемая по правилу
Бабо;
 – поправка
к температурной депрессии;
– поправка
к температурной депрессии;
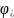 –
корректирующий
множитель, зависящий от рабочих
температуры и давления.
–
корректирующий
множитель, зависящий от рабочих
температуры и давления.
Знак
и величина поправки
 зависят
как от величины и знака
зависят
как от величины и знака
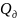 – дифференциальной
теплоты растворения, так и от величины
и знака корректирующего множителя
– дифференциальной
теплоты растворения, так и от величины
и знака корректирующего множителя
 Значения
дифференциальных теплот дегидратации
Значения
дифференциальных теплот дегидратации
 [6,
Приложение 3],
значения
[6,
Приложение 3],
значения
 [6,
Приложение 4].
[6,
Приложение 4].

Таким образом, в этом расчете для раствора NH4NO3 рабочая температура кипения раствора во втором корпусе:


Гидравлическую депрессию при переходе вторичного пара из первого корпуса во второй принимаем в интервале от 1 до 2:

3. Суммарная полезная разность температур и её предварительное распределение
Суммарная полезная разность температур:

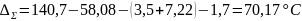
Здесь Т1=140,7°С найдена по давлению греющего пара в I корпусе Pгр.1=0,38МПа [6, приложение 2].
Предварительно распределяем найденное значение Δ∑ на Δ1 и Δ2 в пропорции: Δ1: Δ2 = 1: 1,5. Так как Δ1+Δ2 = 70,17 °С, то находим Δ1=28,07 °С и Δ2= 42,1 °С.
4. Определение параметров ведения процесса в корпусах
Зная Δ1 и Δ2, заполняем таблицу предварительного варианта I приближения с использованием формул:








По найденным температурам греющего и вторичного паров находим недостающие давления, а также энтальпии этих паров [6, приложение 2], заполняем таблицу 3.1
Таблица 3.2 Сводная таблица расчетных значений
№ п/п |
Название |
Символ |
Размерность |
1 приближение |
|||||
Предварительное |
Окончательное |
||||||||
1 корп. |
2 корп. |
1 корп. |
2 корп. |
||||||
1 |
Температура греющего пара |
T |
°С |
140,66 |
107,40 |
140,66 |
99,47 |
||
2 |
Полезная разность температур |
Δ |
°С |
28,07 |
42,10 |
35,99 |
34,06 |
||
3 |
Температура кипящего раствора |
t |
°С |
112,60 |
65,30 |
104,67 |
65,41 |
||
4 |
Температурная депрессия |
δ |
°С |
3,50 |
7,22 |
3,50 |
7,22 |
||
5 |
Температура вторичных паров |
θ |
°С |
109,10 |
58,08 |
101,17 |
58,08 |
||
6 |
Гидравлическая депрессия |
δг |
°С |
1,70 |
1,70 |
||||
7 |
Давление греющего пара |
Pгр |
бар |
3,80 |
1,35 |
3,80 |
1,03 |
||
8 |
Давление в сепараторе |
P |
бар |
1,43 |
0,19 |
1,05 |
0,19 |
||
9 |
Энтальпия |
Гр. Пара |
h |
кДж/кг |
2736 |
2687 |
2736 |
2677 |
|
Втор. Пара |
i |
кДж/кг |
2692 |
2604 |
2678 |
2604 |
|||
10 |
Концентрация раствора |
a |
% масс. |
26,44 |
39,00 |
25,80 |
39,00 |
||
11 |
Количество выпаренного растворителя |
W |
кг/с |
0,63 |
0,51 |
0,59 |
0,55 |
||
5. Расчёт потоков W1 и W2 выпаренной воды в корпусах
Тепловой баланс для II корпуса [1]:

Из формулы (3.33) получаем выражение для расчета W1:

Теплоемкость с0 для α0=19% водного раствора NH4NO3 находим [6, приложение 1] при температуре t1 = 112,6 °C: с0 = 3,62 .


Теплоемкости воды при температуре t2 = 65,3: св = 4,18 .
Теплоемкость конденсата при температуре T2 = 107,4: cК2 = 4,23 [6, Приложение 2].
Итак, W1=0,58 кг/с, и, следовательно,
из (3.23):

6. Определение тепловых нагрузок в корпусах
В I корпусе находим [1]:


Во II корпусе [10]:


Расчет комплексов А1 и А2
Для расчета этих величин необходимо задаться высотой труб в греющей камере выпарного аппарата в пределах от 2 до 6 м. Ориентировочное значение коэффициента теплопередачи в первом корпусе выбираем на уровне 1000÷2000 , а именно: Kop=2000 , тогда соответствующая поверхность
теплообмена будет равняться по (3.1):

В каталоге имеется вертикальный аппарат с естественной циркуляцией и вынесенной греющей камерой:
F = 25 м2; высота труб Н = 4 м; диаметр труб 38 × 2 мм [7, с. 183]. Материал – сталь 09Г2С [8, с. 298, Лащинский], теплопроводность λст = 17,2 .
Для вертикальных труб значение комплекса А (3.7):
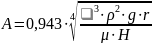
Предварительно находим физические характеристики (таблица 3.2) [6, приложение 2].
Таблица 3.3 Значения физических характеристик для расчета комплексов А
Параметр, ед. изм. |
Температура |
|
T1= 140,7°C |
T2 =107,4°C |
|
Теплопроводность конденсата λ [Вт/м*К] |
0,685 |
0,685 |
Плотность конденсата ρ [кг/м3] |
925 |
953 |
Вязкость конденсата μ [Па*с] |
201*106 |
266*106 |
Теплота парообразования r [кДж/кг] |
2143 |
2237 |


Расчет величин B01 и B02
Эти величины рассчитываются по формулам:


Для I корпуса (3.38):
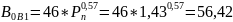
Для II корпуса (3.38):

Здесь Р1 и Р2 – рабочие давления в корпусах, бар.
Относительные
коэффициенты теплоотдачи в корпусах I
и II для водных растворов неорганических
веществ находим по формуле:
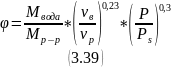
Для I корпуса молярная масса раствора М1 (при концентрации a1=0,26 кг/кг) рассчитывается с помощью формулы:
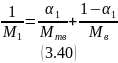
Где Mтв и Mв – молярные массы вещества и воды
Для соли NH4NO3 значение Мтв = 80 кг/кмоль, а для воды Мв = 18 кг/кмоль.
Для I корпуса M1 (3.40):


Для II корпуса M2 (3.40):


Кинематическая вязкость воды νв
при температуре ее кипения под атмосферным
давлением равна νв = 0,294 10-6
м2/c.
10-6
м2/c.
Кинематические вязкости растворов ν1 и ν2 находим при их температурах кипения под атмосферным давлением в зависимости от концентрации (рис. 3.2) [6, приложение 2]:

Рис. 3.2 Зависимость вязкости ν, м2/с (·106) кипящего под атмосферным давлением раствора NH4NO3 от концентрации
ν1 = 0,345*10-6 м2/с – вязкость раствора соли с концентрацией α1. [2]
ν2 = 0,377*10-6 м2/с – вязкость раствора соли с концентрацией α2. [2]
Отношение P/Ps в корпусах согласно правилу Бабó зависит лишь от концентрации раствора. Константа Бабó для раствора во II корпусе найдена ранее в пункте 2 расчета (3.25): (P/Ps)2 = 0,798
В
I корпусе при концентрации
 температура
кипения при атмосферном давлении равна
103,14°C. Соответствующее этой температуре
давление насыщенного водяного пара Ps
=
1,14
бар = 1,14
атм, и константа Бабó в I корпусе равна
(3.25): (P/Ps)1
=1/1,14 = 0,88 [6,
приложение 1;2].
температура
кипения при атмосферном давлении равна
103,14°C. Соответствующее этой температуре
давление насыщенного водяного пара Ps
=
1,14
бар = 1,14
атм, и константа Бабó в I корпусе равна
(3.25): (P/Ps)1
=1/1,14 = 0,88 [6,
приложение 1;2].


Тогда комплексы В0n (3.37):


7. Расчёт поверхности теплообмена в корпусах и соответствующее ей распределение Δ∑ по корпусам, т.е. значения Δ1 и Δ2.
Находим F [1] для 2-х корпусной установки:



 72,39
72,39
Находим F методом последовательной итерации, приняв F = 30 м2 (таблица 3.4).
Таблица 3.4 Нахождение поверхности теплообмена F методом итерации
F |
F1/3 |
1575,7/F1/3 |
F0,7 |
72,39* F0,7 |
F' |
30 |
3,1072 |
507,1108 |
10,8139 |
782,8681 |
22,5690 |
22,5690 |
2,8259 |
557,5776 |
8,8605 |
641,4509 |
21,2728 |
21,2728 |
2,7708 |
568,6800 |
8,5011 |
615,4345 |
21,0603 |
Итак, F= 21,06 м2
С этой поверхностью теплообмена в корпусах находим разности температур в каждом корпусе; соответствующие тепловым нагрузкам Q1 и Q2 и условиям теплообмена:



Проверка правильности расчетов:

Полученная сумма точно совпадает с суммарной полезной разностью температур Δ∑.
8. Определение параметров ведения процесса по найденным Δ1 и Δ2
Аналогично пункту 4 заполняем таблицу окончательного варианта I приближения с использованием формул (3.29 – 3.32):




По найденным температурам греющего и вторичного паров так же находим недостающие давления, а также энтальпии этих паров, заполняем таблицу 3.1 [6, приложение 2].
9. Уточнение величин W1 и W2 и тепловых нагрузок в корпусах
Из баланса II корпуса (см. пункт 5) уточняем величины W1 и W2.
Из (3.34):

Теплоемкость с0 для α0=19% водного раствора NH4NO3 находим [6, приложение 1] при температуре t1 = 104,67 °C: с0 = 3,62 .


Теплоемкости воды при температуре t2 = 65,3: св = 4,18 .
Теплоемкость конденсата при температуре T2 = 107,4: cК2 = 4,23 [6, Приложение 2].
Итак, W1 = 0,59 кг/с, и, следовательно, из (3.23):
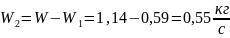
Пересчитаем значение концентрации раствора α1 для окончательного значения W1 (3.24):

Тепловые нагрузки:
В I корпусе (3.35):


Во II корпусе (3.36):


10. Проверка правильности расчета
Находим расхождения в значениях Qi по предварительному и окончательному вариантам I приближения:

Для I корпуса (3.43):

Для II корпуса (3.43):

Найденная поверхность теплообмена каждого корпуса F=21,06 м2 является окончательной.
Подбираем ближайший больший выпарной аппарат с высотой труб Н = 4 м и толщиной стенок труб δст = 2 мм (т.к. эти значения были приняты в расчетах). Выбранный ранее (см. пункт 4) выпарной аппарат с вынесенной греющей камерой (F =25 м2; высота труб Н = 4 м; диаметр труб 38 × 2 мм) подходит.
Согласно справочным данным [14, с. 22] данный теплообменник имеет номинальную поверхность теплообмена F = 25 м2 и действительную F = 21 м2. Проверим запас прочности по действительной поверхности теплообмена.
Запас теплообмена совпадает с рекомендуемыми значениями:


Расход греющего пара в I корпусе находим по формуле [1]:


где rгр.1 – скрытая теплота парообразования при T1=140,66 °C [6, приложение 2].
