
Охрана вод часть 1
.pdf
81
где rст - относительный радиус стенки конической части гидроциклона
rст =1−0,5(1−d сл )tg α2 .
11. Диаметр граничного зерна определяют по формуле в м
δ = |
3 С |
|
|
ρ |
ж |
d |
сл |
V 2 |
||||||
|
|
|
|
|
|
|
|
|
r сл , |
|||||
|
8 |
|
R n |
|
(ρтв − ρж ) |
|
Vτ2сл |
|
||||||
|
|
|
eδ |
|
|
|
|
|
|
|
|
|
|
|
где Reδ - критерий Рейнольдса по частице |
|
|
|
|
|
|||||||||
|
|
|
R |
|
|
= |
Vrсл δ |
, |
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
eδ |
|
|
ν |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
где ν - коэффициент кинематической вязкости;
ρтв и ρж – плотность твердой и жидкой фаз;
С и n – постоянные величины, зависящие от области сопротивления:
если Reδ ≤1, |
то C=24; |
n=1 |
1 < Reδ ≤ 50 , |
C=23,4; |
n=0,723 |
50 < Reδ ≤ 700 , |
C=7,8; |
n=0,425 |
700≤Reδ ≤ 2 106, |
C=0,48; |
n=0 |
Reδ > 2 106 , |
C=0,18; |
n=0 |
Диаметр граничного числа вычисляют методом последовательных приближений. В качестве первого приближения задаётся требуемый диа-
метр граничного зерна δтр.
12. При несоответствии полученного диаметра граничного зерна заданному изменяется диаметр гидроциклона D согласно равенству
δ1 δ |
= |
D1 D , |
|
2 |
2 |
и расчет повторяется.
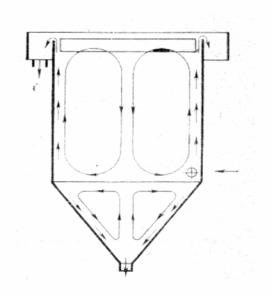
В открытых гидроциклонах (рис. 5.7) тангенциальный впуск жидкости вызывает вращательное движение всего потока. При этом взвешенные
82
частицы концентрируются в пристенной зоне и по образующей конического днища перемещаются к шламовому патрубку, а осветленная вода движется вверх к водосливу.
Открытые гидроциклоны отличаются большой производительностью, простотой конструкции, занимают малую площадь и не требуют затрат электроэнергии. Такие аппараты находят применение на станциях очистки бытовых сточных вод в качестве песколовок, для очистки производственных сточных вод в качестве сооружений грубой очистки.
Рис. 5.7. Открытый гидроциклон с периферийным водосливом
6. ФИЗИКО-ХИМИЧЕСКАЯ ОЧИСТКА СТОЧНЫХ ВОД
Физико-химические методы играют значительную роль при очистке сточных вод. Они применяются как самостоятельно, так и в сочетании с механическими, химическими и биохимическими методами. В последние
83
годы область применения физико-химических методов очистки расширяется, и доля их среди других методов возрастает.
К физико-химическим методам очистки относятся коагуляция, флотация, сорбция, флокуляция, экстракция, ионный обмен, гиперфильтрация, кристаллизация и др.
6.1. КОАГУЛЯЦИЯ
Коагуляция - это слипание частиц при их столкновении в процессе теплового движения, перемешивания или направленного перемещения во внешнем силовом поле. В результате коагуляции образуются агрегаты - более крупные (вторичные) частицы, состоящие из скопления мелких (первичных). Первичные частицы в таких агрегатах соединены силами межмолекулярного взаимодействия непосредственно или через прослойку окружающей (дисперсионной) среды. Коагуляция сопровождается прогрессирующим укрупнением частиц и уменьшением их общего числа в объёме дисперсионной среды.
Эффективность очистки сточных вод коагуляцией определяется устойчивостью дисперсной системы, которая зависит от свойств, характеризующих данную систему в целом, а также от свойств дисперсионной среды и дисперсной фазы. Поскольку сточные воды содержат разнородные частицы, отличающиеся химической природой, знаком или величиной поверхностного заряда, то в этих случаях наблюдается гетерокоагуляция. Теория гетерокоагуляции частиц в растворах электролитов была создана Б.В. Дерягиным на базе общего подхода к теории ДЛФО (теория Дерягина- Ландау-Фербея-Овербека), т.е. учета баланса сил молекулярного притяжения и электрических сил отталкивания. Коагуляцию можно вызвать, вводя в сточную воду электролиты, флокулянты и коллоиды - частицы, которые
84
имеют знак электрического заряда, противоположный знаку заряда частиц загрязнений.
Мицеллы гидролизованных коагулянтов коагулируют спонтанно во всём объёме дисперсной системы с образованием агрегатов преимущественно за счет межмолекулярных сил Ван-дер-Ваальса. Взаимодействие мицелл протекает в области быстрой коагуляции, когда все частицы, находящиеся в броуновском движении, при сближении слипаются.
Скорость быстрой коагуляции, по Смолуховскому, является функцией концентрации частиц (Сч), интенсивности броуновского движения, характеризуемого коэффициентом диффузии D, радиусом притяжения частицы R или расстояния l, на которое должны приблизиться центры частиц для того, чтобы произошло слипание.
− |
dC4 |
= KC2 , |
(25) |
dτ ч
где К - константа, характеризующая вероятность сближения частиц; τ - время.
Интегрируя выражение (25) с граничным условием Сч=Счо при τ=0 и введя время половинной коагуляции θ, получим
С = |
|
|
|
Счо |
, |
(26) |
||
1 |
|
|||||||
ч |
|
+τθ |
|
|||||
где Счо - начальная численная концентрация частиц. |
|
|||||||
Учитывая, что |
|
|
|
|
|
|
|
|
К = 4πDl , |
|
|||||||
получим из формулы (25) |
|
|
|
|
|
|
|
|
− |
dCч |
|
= 4πDlCч2 . |
(27) |
||||
|
||||||||
|
|
dτ |
|
|
|
|||

85
По формулам (26) и (27) определим расстояние l
l |
r |
= 3η |
2 |
C |
K'Tθ , |
(28) |
|
|
чo |
|
|
где r - радиус частиц;
η - динамическая вязкость дисперсионной среды; K' - константа Больцмана;
T - температура.
Силы притяжения начинают действовать, когда частицы приблизятся на очень малое расстояние и столкнутся. В этом случае энергия молекулярного притяжения мицелл больше теплового, а следовательно, броуновского движения. Из формулы (28) следует, что чем больше размер частицы, тем на большем расстоянии может происходить коагуляция.
Подставив в выражение (27)
D = 6RTπηr ,
получим
− dCч = 2 RTlCч2 . dτ 3 ηr
Т.е. скорость быстрой коагуляции находится в прямой зависимости от температуры, расстояния и концентрации частиц и в обратной зависимости от динамической вязкости и радиуса частиц. Принято различать гравитационную и градиентную коагуляции. Гравитационная коагуляция осуществляется в результате инерционных явлений осаждения захватом и подтягиванием частиц. Инерционные силы действуют при прямом столкновении относительно крупных (более 100 нм) полидисперсных частиц. Мелкие частицы чаще осаждаются захватом и подтягиванием по искривлённым траекториям. Градиентная коагуляция характеризуется интенсивным перемешиванием жидкости с целью обеспечения наиболее благопри-
86
ятных условий для гидролиза коагулянтов, максимальной скорости образования достаточно крупных быстрооседающих хлопьев. Скорость градиентной коагуляции частиц определяется по формуле
ddrCч = Kгγ 3Gω3Cч2 ,
где Kг - коэффициент, зависящий от режима движения среды (Kг=4/3 - для ламинарного и Kг=12 - для турбулентного потока);
ω - отношение сферы действия межмолекулярных сил к размеру частиц; G - средний градиент скорости с-1, определяемый по формуле
G =  ηWAτ ,
ηWAτ ,
здесь А - работа, затрачиваемая на перемешивание, Дж; W - перемешиваемый объём, м3;
τ - время перемешивания, с;
η - динамическая вязкость воды, Па с.
Градиентная коагуляция происходит в поли- и монодисперсных системах при наличии частиц размером более 200 ÷ 300 нм.
Образовавшиеся в результате гидролиза коагулянтов мицеллы и более крупные шарообразные агрегаты золя (r=10 ÷ 100 нм) сорбируются на поверхности частиц очищаемой жидкости. При этом происходит нейтрализация заряда частиц, в результате чего они покрываются плотным слоем гидрооксида коагулянта. Т.о. проявляется опалесценция (скрытая фаза коагуляции). Затем наступает период построения цепочных структур и образования большого количества мельчайших хлопьев, которые агрегируют в более крупные и, достигнув определённых размеров, под действием сил тяжести оседают. В действительности эти процессы перекрывают друг друга, а не следуют один за другим.

87
Процесс коагуляции может быть ускорен при добавлении к коагулянтам флокулянтов - высокомолекулярных веществ. Механизм действия этих веществ в настоящее время мало изучен. Согласно теории Ла Мера, при флокуляции сначала происходит первичная адсорбция и каждая микромолекула прикрепляется несколькими сегментами к одной коллоидной частице. Адсорбированные молекулы занимают часть поверхности (F) частиц (активных центров, на которых возможна адсорбция), а остальная поверхность (1-F) остаётся свободной. Затем в процессе вторичной адсорбции свободные сегменты адсорбированных молекул закрепляются на поверхности других частиц, связывая их полимерными мостиками. С учетом электрического заряда коллоидных частиц и макроионов, а также природы адсорбционных сил, скорость флокуляции может быть выражена уравнением
ddCτч = −KфRфϕфF(1− F )Сч2 ,
где Кф - коэффициент, характеризующий условия сближения частиц;
Rф - сфера действия аттракционных сил (расстояние между центрами частиц, при которых происходит флокуляция);
ϕф - коэффициент, учитывающий суммарные действия возникающие между частицами и молекулами Ван-дер-Вальсовых и Кулоновских сил; F(1-F) - фактор, определяющий вероятность того, что свободная поверхность одной частицы расположится около макромолекул, адсорбированных на поверхности другой частицы (формально этот фактор указывает на то, что не все возможные столкновения между частицами эффективны и приводят к флокуляции).
88
6.1.1.Коагулянты и вещества, способствующие коагуляции
Внастоящее время наиболее распространенными коагулянтами являются сернокислый алюминий, алюмокалиевые квасцы, алюминат натрия, сернокислое и хлорное железо. В мировой практике также используют высокоосновный 5/6-гидрооксохлорид алюминия и хлорид алюминия. Сфера применения коагулянта определяется составом сточной воды, его свойствами, стоимостью, способностью удалять те или иные группы загрязнений, а также требованиями, предъявляемыми к устройствам для приготовления и дозирования растворов реагентов.
Сернистый алюминий во многих случаях по эффективности удаления загрязнений превосходит соли железа. Он более эффективен, чем алюминат натрия. Существенным недостатком этого коагулянта является то, что эффективность его действий ограничивается узкой областью значений рН и температуры воды.
Для коагуляции сточных вод широко используют известь. По эффективности коагулирующего действия она уступает солям алюминия и железа, но достаточно эффективно снижает содержание фосфатов. Осадки, образующиеся при коагуляции сточных вод известью, легче обезвоживаются, чем осадки, полученные при использовании солей железа или алюминия. Недостатками применения извести являются её значительный расход, необходимость последующей рекарбонизации воды и возможность зарастания загрузки фильтров карбонатом калия.
Перспективным коагулянтом является высокоосновный 5/6- гидрооксохлорид алюминия Al2(OH)5Cl, обладающий высоким содержанием водорастворимого алюминия; при его полном гидролизе на один атом алюминия выделяется в 6 раз меньше ионов гидроксония, чем при гидролизе Al2(SO4)3, поэтому щелочность исходной воды снижается меньше и коагулянт работает в более широком диапазоне рН. Он незначительно по-
89
вышает солесодержание очищаемой воды. Расход этого коагулянта на 15 ÷ 30% ниже, чем сернокислого алюминия, скорость образования хлопьев больше, чем у Al2(SO4)3, и он даёт незначительное количество остаточного алюминия в обработанной воде.
В практике очистки сточных вод довольно часто используют смешанный коагулянт, представляющий собой смесь сернокислого алюминия и хлорного железа. В этом случае достигаются лучшие результаты, чем при раздельном использовании солей алюминия и железа. При этом наблюдается расширение зоны оптимальных значений рН, которое можно объяснить большим разнообразием продуктов гидролиза со своими индивидуальными свойствами, а ускоренное осаждение хлопьев - изменением структуры коагулянта за счет более плотной упаковки частиц.
Для ускорения процесса коагуляции и повышения эффективности этого процесса применяют высокомолекулярные вещества, называемые флокулянтами. В настоящее время известно более 2000 флокулянтов. Все флокулянты по их природе делят на природные и синтетические. В большинстве случаев эти вещества принадлежат к классу линейных полимеров. Для удобства рассмотрения синтетические флокулянты подразделяют на неионные, анионные и катионные соединения.
Наиболее распространенным и эффективным анионным флокулянтом является полиакриламид (ПАА), который представляет собой сополимер акриламида с акрилатом аммония, натрия или кальция с содержанием акрилатов до 10%. У нас в стране применяют два вида ПАА:
1) известковый ПАА - сополимер акриамида и акрилата кальция
([−СН2 |
−CH −СОNH2 ][CH2 |
−CH −COOCaOOC −CH −CH2 ] ); |
|
I |
Ι |
2) аммиачный ПАА - сополимер акриламида и акрилата аммония
([−CH2 −CH −CONH2 ][−CH2 −CHCOONH4 ]).
Ι
90
За рубежом выпускается широкий ассортимент ПАА в порошкообразном, гранулированном и гелеобразном виде под коммерческими названиями: Сепаран; Суперфлок 16, 20 и 84; Пулифлок А-22; Магнофлок 990, 985, 971 и 860; Могул СО-983; Кей-Флок; Полифлок и т.д. Эти вещества отличаются молекулярной массой, степенью гидролиза (которая колеблется от 5 до 41%) и содержанием основного вещества в продукте.
Наиболее простым по строению катионным флокулянтом является полиэтиленимин (ПЭИ). Он состоит из звеньев двух типов:
−CH 2 − CH 2 − NH −
−CH 2 −CH 2 − N −СН2 −СH 2 NН2
Этот коагулянт получают полимеризацией этиленимина в присутствии инициаторов - эпихлоргидрина, дихлоргидриглицирина и т.д. Техни-
ческий ПЭИ представляет собой водный раствор, содержащий 20÷50% полимера. Внешне он выглядит как густая вязкая жидкость. Основными недостатками полиэтиленимина являются:
•высокая коррозионная активность (разрушает сталь, резину, эпоксидные смолы);
•умеренная токсичность.
Так как мономер этиленимин является канцерогенным соединением и возможно его наличие в готовом продукте, производство данного полиэлектролита в промышленных масштабах у нас в стране запрещено.
Кроме органических флокулянтов в практике очистки сточных вод используют неорганические полимеры. Примером таких полиэлектролитов может служить активная кремнекислота (АК). Она является высокомолекулярным неорганическим полимером анионного типа. Это вещество не относится к стандартным продуктам с определёнными свойствами. Её получают на очистных станциях непосредственно перед использованием пу-
