
- •1 Точка 1 семестр Методы объемного анализа.
- •Зависимость эквивалента вещества от реакции.
- •Понятие об эквиваленте. Объемные методы анализа. Методы расчета в объемном методе анализа.
- •Понятие об эквиваленте. Объемные методы анализа. Эквивалент простых и сложных веществ.
- •2 Точка 1 семестр Молекулярность и порядок реакций
- •Зависимость скорости реакции от концентраций реагирующих веществ.
- •Зависимость скорости реакции от температуры.
- •Гомогенный, гетерогенный и микрогетерогенный катализ.
- •Химическая термодинамика Первое начало термодинамики. Закон Гесса.
- •Химическая термодинамика. Основные термодинамические понятия.
- •Химическая термодинамика Второй закон термодинамики. Свободная энергия.
- •Принцип Ле-Шателье.
- •Костанта равновесия.
- •Химическая связь.
- •Современное представление о строении атома.
- •2 Точка 2 семестр
- •Комплексные соединения.
- •3 Точка 1 семестр Учения о растворах Теория электролитической диссоциации. Сильные и слабые электролиты.
- •Учение о растворах Коллигативные свойства растворов.
- •Учения о растворах Коллоидная химия
- •Учения о растворах. Буферные системы
- •Учения о растворах Ионное произведение воды и водородный показатель.
- •Учения о растворах Гидролиз солей.
- •Учения о растворах Способы выражения концентрации растворов.
- •3 Точка 2 семестр
Учения о растворах. Буферные системы
1. Задание {{ 376 }} ТЗ № 376
Ацетатная буферная система состоит из
- H2CO3 и NaHCO3
+CH3COOH и CH3COONa
- Na2HPO4 и NaH2PO4
- NH4OH и NH4Cl
2. Задание {{ 377 }} ТЗ № 377
Бикарбонатная буферная система состоит из
+ H2CO3 и KHCO3
- CH3COOH и CH3COONa
- NaH2PO4 и Na2HPO4
- NH4OH и NH4Cl
3. Задание {{ 378 }} ТЗ № 378
Фосфатная буферная система состоит из
- H2CO3 и KHCO3
- CH3COOH и CH3COONa
+ NaH2PO4 и Na2HPO4
- NH4OH и NH4Cl
4. Задание {{ 379 }} ТЗ № 379
Аммиачная буферная система состоит из
- H2CO3 и KHCO3
- CH3COOH и CH3COONa
- NaH2PO4 и Na2HPO4
+ NH4OH и NH4Cl
5. Задание {{ 380 }} ТЗ № 380
pH буферного раствора состоящего из слабой кислоты и ее соли образованной сильным основанием можно рассчитать по формулам
+
pH = pK + lg
![]()
-
pH = 14-pK - lg
![]()
+pH
= pK - lg
![]()
-
pH = pK - lg
![]()
6. Задание {{ 381 }} ТЗ № 381
pH буферного раствора состоящего из слабого основания и ее соли образованной сильной кислотой можно рассчитать по формуле
-
pH = pK + lg
![]()
-
pH = pK - lg
![]()
+
pH = 14-pK - lg
![]()
-
pH = 14-pK + lg
![]()
7. Задание {{ 382 }} ТЗ № 382
Соотношение между концентрациями соли и слабой кислоты в буферной системе с pH=1,35 и pKk=2,35
- 1:1
- 1:2
- 1:5
+ 1:10
8. Задание {{ 383 }} ТЗ № 383
pH
буферного раствора, содержащего 3,6 мл
0,2 н NH4Cl
и 3,6 мл 0,2 н NH4OH,
если KNH![]() OH=10-5
OH=10-5
- 2
- 4
- 5
+ 9
9. Задание {{ 384 }} ТЗ № 384
pH ацетатной буферной системы равен 5. Константа диссоциации уксусной кислоты в такой системе, если соотношение между компонентами близко к 1 равна
- 10-3
+ 10-5
- 10-9
- 10-14
10. Задание {{ 385 }} ТЗ № 385
Отметьте
правильный ответ . pH
ацетатной буферной смеси, состоящей
из 100 мл 0,2 н CH3COOH
и 200 мл 0,1 н CH3COONa,
если KCH![]() COOH
= 10-6
COOH
= 10-6
- 4
+ 6
- 8
- 10
11. Задание {{ 386 }} ТЗ № 386
Соотношение между концентрациями слабой кислоты и ее соли в буферной системе имеющей pH=11, а pKk=9
- 1:1
- 1:5
- 1:10
+ 1:100
12. Задание {{ 387 }} ТЗ № 387
pH
буферной системы CH3COOH+CH3COONa,
содержащей по 0,25 моль/л каждого из
веществ, если KCH![]() COOH=10-5
COOH=10-5
- 2
- 3
- 4
+ 5
13. Задание {{ 388 }} ТЗ № 388
pH
буферного раствора, содержащего 3,6 мл
0,2 н NH4Cl
и 2,4 мл 0,3 н NH4OH,
если KNH![]() OH=10-5
OH=10-5
- 3
- 5
+ 9
- 14
14. Задание {{ 389 }} ТЗ № 389
pH
буферного системы состоящей из СH3COOH
и CH3COONa,
если соотношение между компонентами
равно 1, а KСH![]() COOH=10-6
равен
COOH=10-6
равен
- 3
- 5
+ 6
- 8
15. Задание {{ 390 }} ТЗ № 390
pH
буферного раствора, содержащего 5 мл
0,1 н NH4Cl
и 5 мл 0,1 н NH4OH,
если KNH![]() OH=10-6
OH=10-6
- 5
- 6
- 7
+ 8
16. Задание {{ 391 }} ТЗ № 391
Приготовим
раствор, содержащий уксусную кислоту
и ацетат натрия в равных молярных
концентрациях. pH
такого раствора, если KСH![]() COOH=10-5
равен
COOH=10-5
равен
- 2
- 4
+ 5
- 9
17. Задание {{ 392 }} ТЗ № 392
Буферную емкость можно рассчитать по формуле
-
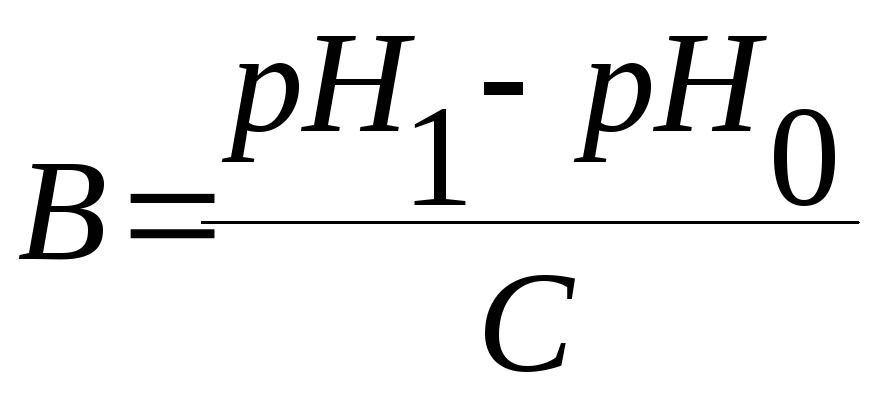
+

-
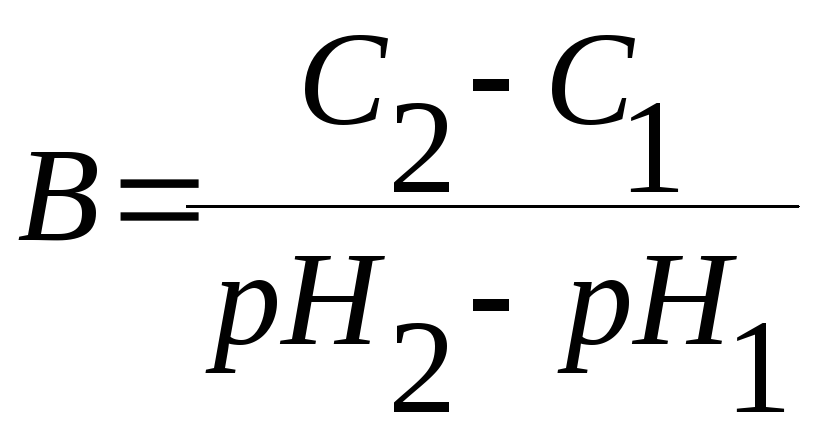
18. Задание {{ 393 }} ТЗ № 393
В состав крови входит буферных систем
- 1
- 2
- 3
+ 4
19. Задание {{ 394 }} ТЗ № 394
Самая мощная буферная система крови
- бикарбонатная
- фосфотная
+ гемоглобиновая
- белковая
