- •Физические свойства бензола.
- •Способы получения бензола
- •Химические свойства бензола.
- •Реакции электрофильного замещения в бензоле
- •Влияние заместителей на скорость и направление реакций электрофильного и нуклеофильного замещения в бензольном ряду
- •Электроноакцепторные заместители
- •Нуклеофильное замещение атомов галогенов в бензольном ядре
- •Реакции активированного нуклеофильного замещения с аммиаком и аминами
- •Электронодонорные заместители
- •Пространственное влияние на направление химической реакции
- •Согласованное и несогласованное влияние заместителей
- •Особая группа заместителей
- •Наиболее важные производные ароматических углеводородов
- •Способы получения фенола и его аналогов
- •Электронное и пространственное строение фенола.
- •Химические свойства фенолов
- •Ароматические амины
- •Алкилирование натрового производного ацетанилида галогенпроизводными алканов:
- •Гидролиз n-алкильного производного ацетанилида
- •Содержание
Алкилирование натрового производного ацетанилида галогенпроизводными алканов:
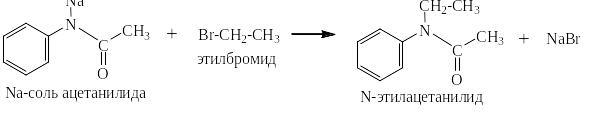
Гидролиз n-алкильного производного ацетанилида
При кипячении N-алкилацетанилида в течение одного часа в 2 – 5 % растворе серной или другой сильной кислоты образуются моноалкильное производное ароматического амина и карбоновая кислота:
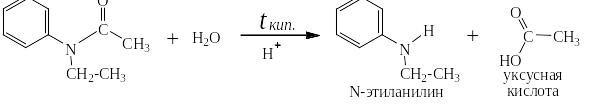
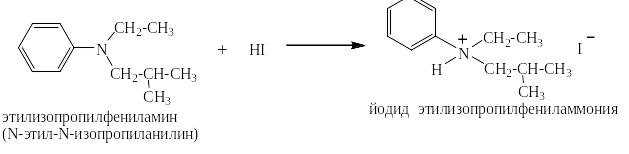
При необходимости моноалкильное производное можно ещё раз проалкилировать другим галоидным алкилом, например:

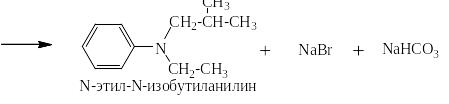
И первичные ароматические амины, и вторичные и третичные, полученные из них, быстро при температуре близкой к 0оС реагируют с нитритом натрия в присутствии кислот как реагентов.
Первичные ароматические амины реагируют с нитритом натрия и соляной кислотой с образованием относительно стойкой при температурах от 0 до 5оС соли диазония. Эта реакция впервые опубликована в 1858 году в немецком химическом журнале Петером Гриссом и носит его имя:
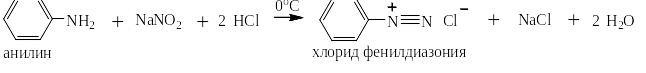
В реакцию Грисса вступают многочисленные гомологи анилина, содержащие алкильные заместители в о-,м- и п-положении к аминогруппе:
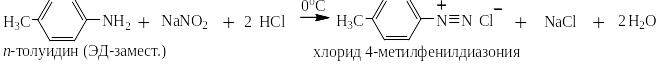
Так же в неё вступают производные анилина, содержащие электроноацепторные, электронодонорные заместители и заместители особой группы, например:
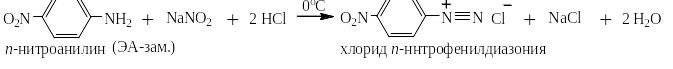
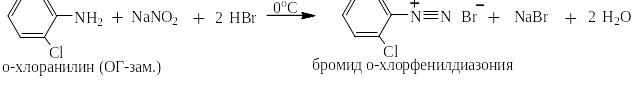
На производстве соли диазония сразу же используют для проведения следующих стадий синтеза, но в лаборатории их часто выделяют по реакции обмена с насыщенным раствором тетрафторобората натрия:
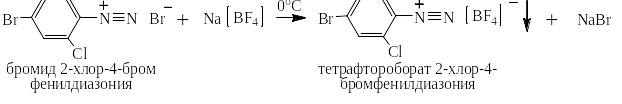
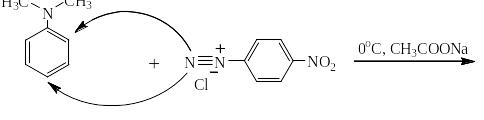
Соли диазония чаще всего используют для получения многочисленных азокрасителей по реакции азосочетания с фенолами (нафтолами) и ароматическими третичными аминами, например:
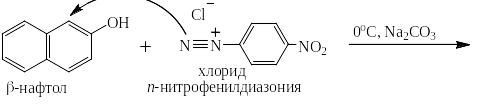
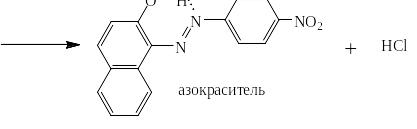
Получившийся азокраситель является рН-индикатором: в кислой среде за счёт образования водородной связи он имеет плоскую структуру, в которой электронодонорное влияние гидроксильной группы ослаблено – эта форма окрашена в жёлтый цвет. В щелочной от гидроксильной группы отрывается протон, возникает «фенолят-ион», являющийся сильнейшим ЭД-заместителем, и окраска меняется на красно-оранжевую:
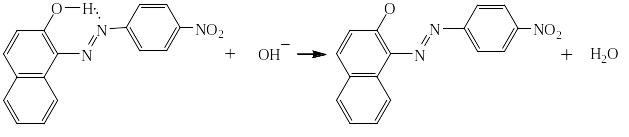
Роль соды в ходе реакции азосочетания – связывание образующейся соляной ( или другой сильной ) кислоты в кислую соль – гидрокарбонат натрия:
![]()
Смесь карбоната и гидрокарбоната натрия является буферным раствором, создающим слабо-щелочную среду.
С третичными ароматическими аминами азосочетание должно проходить в слабо кислой среде, что обеспечивается добавкой солей, гидролизующихся по аниону, например, ацетата натрия. В сильно кислой среде амин даёт соль аммония, катион которой с катионом диазония естественно не реагирует.
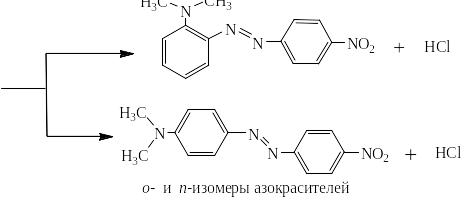
Ацетат натрия мгновенно реагирует с образующейся соляной кислотой. В результате образуется буферный раствор, состоящий из слабой уксусной кислоты и избыточного ацетата натрия. Он обеспечивает слабокислую среду:
![]()
Вторичные ароматические амины реагируют с нитритом натрия и соляной кислотой с образованием N-нитрозаминов. Например, N-метиланилин даёт N-нитрозо-N-метиланилин – жёлтое масло с крайне неприятным запахом, отвердевающее при 13ОС:
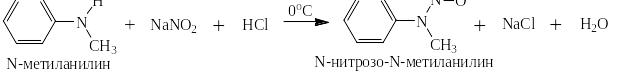
Ароматические N-нитрозоамины как и алифатические – канцерогены. Так же вызывают рак печени, так же применяются в экспериментальной онкологии.
Ароматические N-нитрозоамины под действием сухих хлоро- или бромоводородов или под действием концентрированной серной кислоты претерпевают перегруппировку впервые опубликованную в 1886 году в немецком химическом журнале О.Фишером и Е.Хеппом. В указанных условиях нитрозогруппа селективно переносится в п-положение:

Полученый в результате перегруппировки 4-нитрозо-N-метиланилин обладает совершенно иными физическими свойствами и биологической активностью. Это зелёное твёрдое вещество с температурой плавления 113ОС. В растворах в органических растворителях флюоресцирует. Канцерогеном не является, правда, вызывает дерматиты.
Третичные ароматические амины реагируют с нитритом натрия и соляной кислотой, давая С-нитрозосоединения. Нитрозогруппа селективно направляется в п-положение:
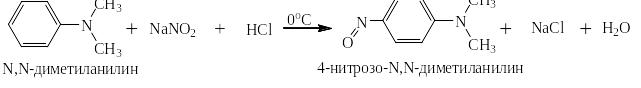
С-нитрозосоединения легко восстанавливаются водородом на никеле Ренея. При этом получаются несимметричные диалкилдиамины, например:
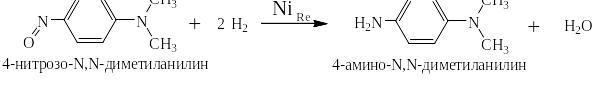
На стр.30 и 31 данного пособия было высказано предположение о лёгкости протекания в ароматических аминах реакций электрофильного замещения в орто- и пара-положения бензольного ядра. Действительно анилин легко бромируется сразу во все эти положения:
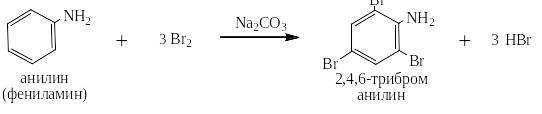
N,N-диалкиланилины сульфируются, нитруются и вступают в реакцию азосочетания в орто- и пара-положения:
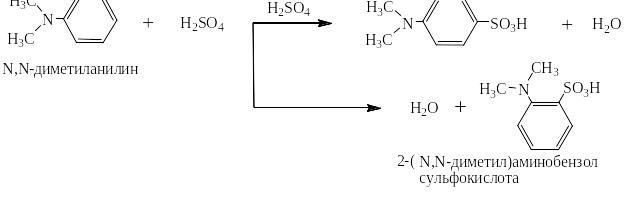
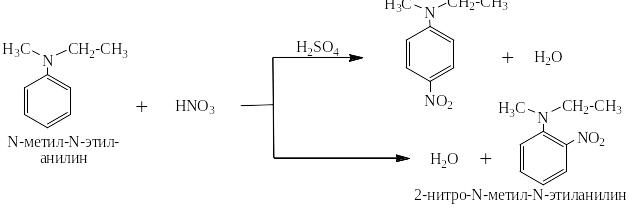
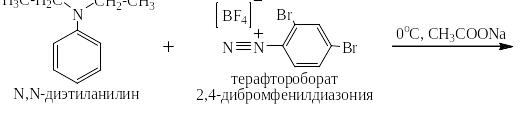
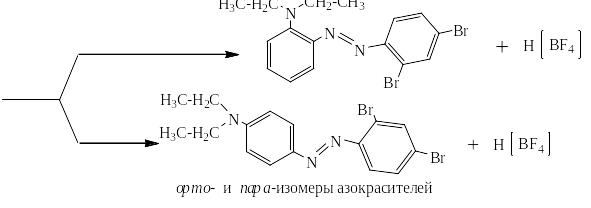
Ацетатом натрия сильная комплексная кислота переводится в слабую – уксусную:
![]()
Первичные ароматические, а так же вторичные и третичные жирноароматические амины являются основаниями, так как на атоме азота у них имеется неподелённая пара электронов, которая может быть акцептирована свободной орбиталью протона из воды или кислот с возникновением новой четвёртой ковалентной связи. Впрочем основность этих аминов как минимум в 100000 раз меньше основности аммиака и,тем более, алифатических аминов. Тем не менее, ароматические амины с разбавленными водными растворами сильных кислот дают соли:
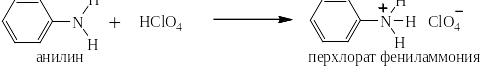
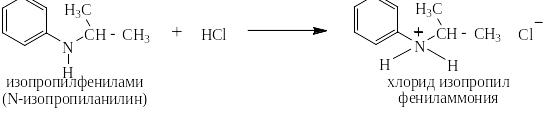
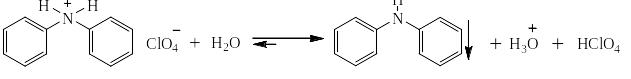
Вторичные ароматические амины так же способны образовывать соли под действием концентрированных сильных кислот, но при разбавлении водой эти соли гидролизуются, давая слабое основание, то есть исходный амин:
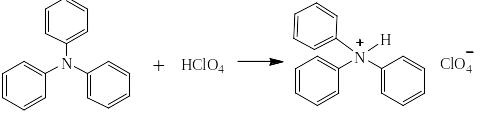
Третичные ароматические амины, как очень слабые основания, не дают солей ни с концентрированной соляной, ни с серной кислотами. Правда, трифениламин всё же даёт с хлорной кислотой перхлорат:
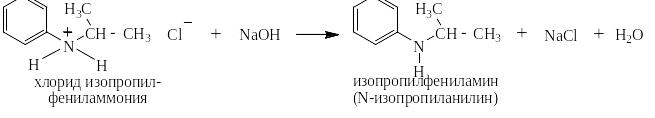
Соли ароматических и жирно-ароматических аминов можно легко перевести обратно в амины действием щелочей:

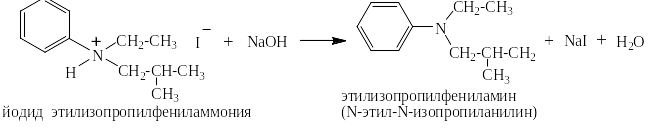
Кислотно-основные превращения карбоновых кислот ароматического ряда
Бензойная кислота имеет pKa = 4,18. То есть она кислота примерно в 2,5 раза более слабая, чем муравьиная, и примерно в 4 раза более сильная, чем уксусная. Она охотно реагирует со щелочами:

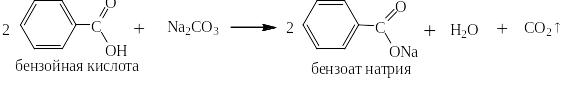
С солями более слабых кислот:

а так же нестойких кислот:
В инертных по отношению к щелочным и щелочноземельным металлам растворителях – бензоле, толуоле или смеси ксилолов, бензойная кислота, растворимость которой в бензоле почти в 36 раз больше, чем в воде, и равна при 20ОС 11 г на 100 г бензола, легко реагирует не только с этими металлами, но и с цинком и оловом. Аналогично ведут себя и другие карбоновые кислоты ароматического ряда:
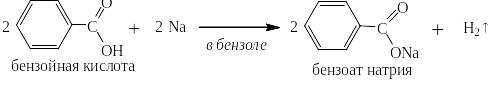
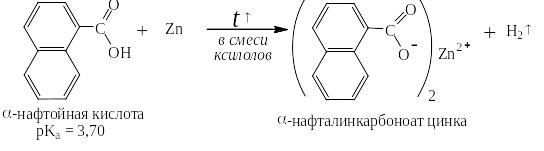
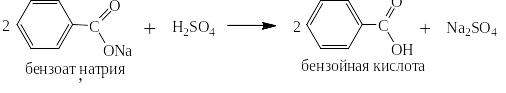
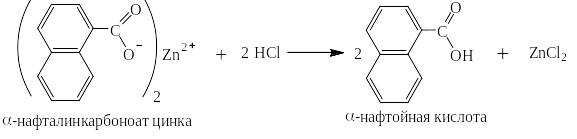
Действием более сильных кислот соли ароматических карбоновых кислот могут быть обратно переведены в эти кислоты:
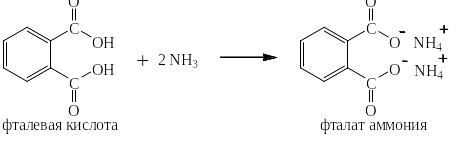
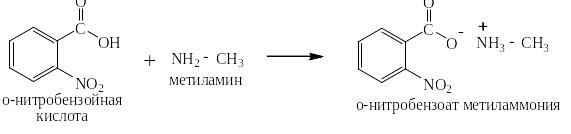
С аммиаком и аминами ароматические карбоновые кислоты так же дают соли:
Действием горячих щелочей аммонийные соли ароматических карбоновых кислот могут быть переведены в металлические соли с выделением аммиака или летучих аминов:
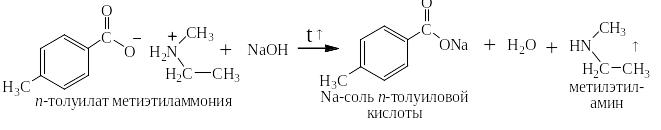
Действием более сильных кислот аммонийные соли ароматических карбоновых кислот могут быть обратно переведены в эти кислоты:
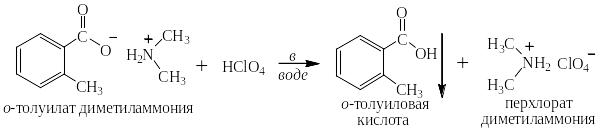
Кислотно-основные превращения сульфокислот ароматического ряда
Бензолсульфокислота имеет pKa = 0,70. То есть она кислота средней силы; примерно в 32 раза менее сильная, чем хромовая по первой ступени, равная по силе трихлоруксусной кислоте и примерно в 30 раз более сильная, чем ортофосфорная кислота по первой ступени диссоциации. Бензолсульфокислота нейтрализуется щелочами:

Реагирует так же с амфотерными гидроксидами и нерастворимыми в воде основаниями:
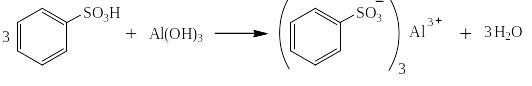
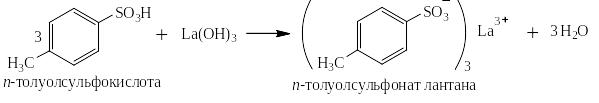
Водные растворы сульфокислот ароматического ряда охотно реагируют с основными и амфотерными оксидами:
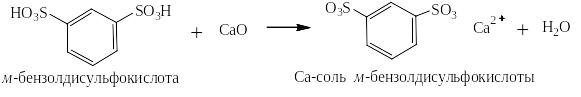

Как кислоты средней силы ароматические сульфокислоты вытесняют слабые кислоты из их солей:
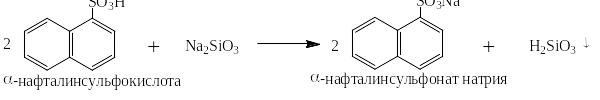
Очень охотно они реагируют с аммиаком и аминами всех типов:

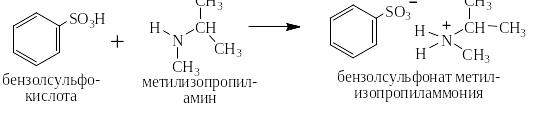
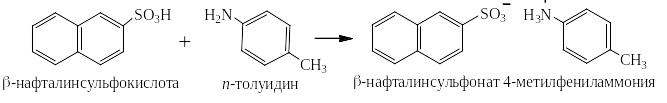
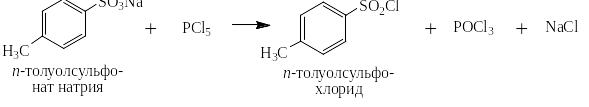
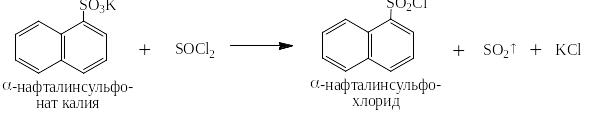
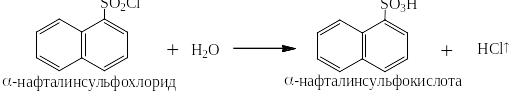
Соли хорошо растворимых в воде и близких к сильным ароматических сульфокислот перевести в одну стадию обратно в кислоты невозможно, но можно сначала перевести их в сульфохлориды действием либо пентахлорида фосфора, либо хлористого тионила (оксидадихлорида серы IV), а затем путём гидролиза сульфохлоридов в кислоты:
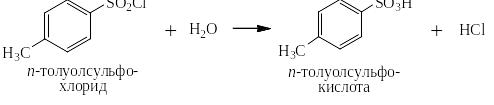
Медико-биологическое значение ароматических соединений
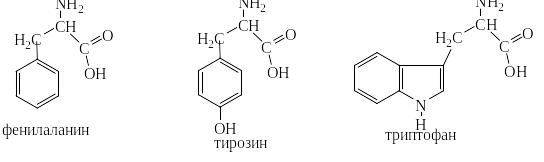
Ароматические соединения имеют колоссальное медико-биологическое значение. Без таких производных бензола и фенола как аминокислоты – фенилаланин, тирозин и триптофан невозможен синтез белков.
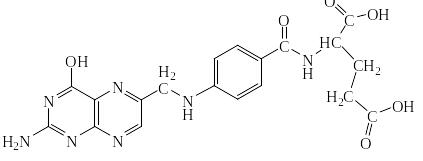
Фрагменты бензольных колец входят в состав формул ряда витаминов: рибофлавина (В2) и его производных, фолиевой кислоты (ВС), цианокобаламина (В12),рутина, венорутона (Р4), кверцетина, ацетата токоферола (Е), витамина К. В качестве примера приведём формулу фолиевой кислоты, в которой содержится остаток алкиламида п-аминобензойной кислоты:
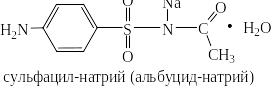
В очень многих лекарственных средствах содержатся остатки бензола. Так, например, во всех сульфаниламидных препаратах имеется фрагмент 4-аминобензолсульфокислоты:
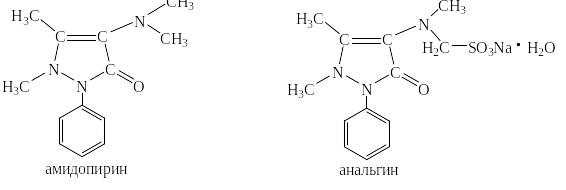
В болеутоляющих препаратах таких как амидопирин и анальгин так же есть бензольные остатки:
Противоглистный препарат – нафтамон и сосудосуживающий препарат – нафтизин, применяемый, например, при насморке содержат остатки нафталина:
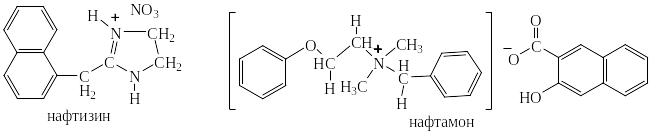
Среди почти 6000 лекарственных средств, представленных в справочнике М.Д. Машковского, примерно каждое пятое содержит остатки ароматических углеводородов.
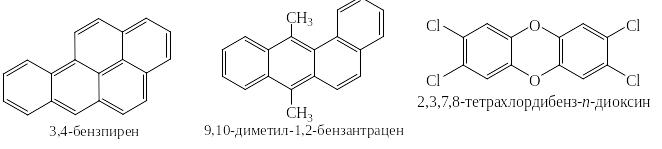
Наряду с полезными производными ароматических углеводородов имеется и множество вредных. Например, канцерогенами являются β-нафтиламин вызывающий рак мочевого пузыря, N-нитрзамины вызывающие рак печени, полициклические углеводороды, которые в зависимости от способа попадания в организм могут вызывать рак желудка, лёгких или мошонки (рак лондонских мальчиков-трубочистов). Так основным канцерогенным веществом дёгтя является 3,4-бензпирен, а одним из самых сильных канцерогенов этого класса, часто применяемым в экспериментальной онкологии, считается 9,10-диметил-1,2-бензантрацен.
Хорошо известны также диоксины – опасные ксенобиотики и кумулятивные яды. Среди них один из наиболее токсичных 2,3,7,8-тетрахлордибензо-п-диоксин. Однако токсичны так же и диоксины с другим количеством и расположением атомов хлора в бензольных ядрах. Диоксины обладают мощным мутагенным, иммунодепрессантным, тератогенным и эмбриотоксическим действием.
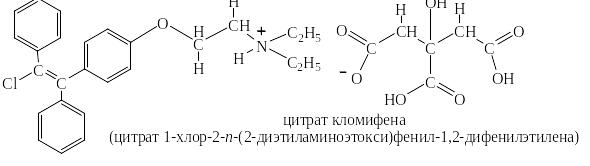
К сожалению и многие лекарственные препараты обладают тератогенным действием. Ниже приведены примеры таких препаратов, приводящих к уродствам плода в случае их применения на некоторых сроках беременности. Так медикамент – кломифен, назначаемый при бесплодии, маточных кровотечениях и аменорее, является безусловно вредным для плода, если беременность наступила.
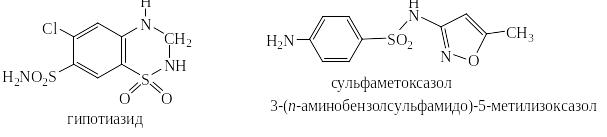
Гипотиазид (дихлотиазид) – ценное средство для лечения гипертонической болезни, сопровождающейся недостаточностью кровообращения, очень вреден для плода в первые месяцы беременности.
Сульфометоксазол – составная часть фармацевтического препарата бисептол эффективного в отношении многих бактерий. Есть чёткие доказательства его тератогенности.