
- •Физические свойства бензола.
- •Способы получения бензола
- •Химические свойства бензола.
- •Реакции электрофильного замещения в бензоле
- •Влияние заместителей на скорость и направление реакций электрофильного и нуклеофильного замещения в бензольном ряду
- •Электроноакцепторные заместители
- •Нуклеофильное замещение атомов галогенов в бензольном ядре
- •Реакции активированного нуклеофильного замещения с аммиаком и аминами
- •Электронодонорные заместители
- •Пространственное влияние на направление химической реакции
- •Согласованное и несогласованное влияние заместителей
- •Особая группа заместителей
- •Наиболее важные производные ароматических углеводородов
- •Способы получения фенола и его аналогов
- •Электронное и пространственное строение фенола.
- •Химические свойства фенолов
- •Ароматические амины
- •Алкилирование натрового производного ацетанилида галогенпроизводными алканов:
- •Гидролиз n-алкильного производного ацетанилида
- •Содержание
Нуклеофильное замещение атомов галогенов в бензольном ядре
В этих реакциях атакующей частицей является анион или нейтральная молекула, содержащая в своей структуре атом с неподелённой парой электронов. Примером реакции с анионом может быть получение фенола из хлорбензола:
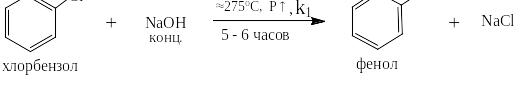
Механизм её следующий: щёлочь в водном растворе диссоциирует на ионы:
![]()
Отрицательно
заряженный гидроксид-ион атакует атом
углерода, связанный ковалентной полярной
связью с атомом хлора. При этом обратимо
возникает отрицательно заряженный
σ-комплекс, который затем необратимо
распадается на фенол и хлорид-ион:
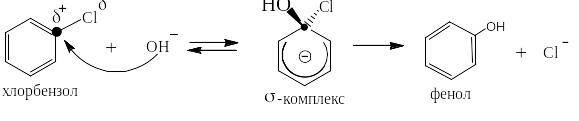
Существование σ-комплексов строго доказано. Американским учёным Джексону и Мезенгеймеру, удалось сохранять представленный ниже комплекс при - 80ОС более года.

Наличие в о- или п- положении к атому галогена ЭА-заместителей, как было сказано выше, сильно ускоряет реакции нуклеофильного замещения. Это можно легко объяснить тем, что на атоме углерода, связанном с атомом галогена образуется дополнительный частичный положительный заряд за счёт переноса электронной плотности на ЭА-заместитель. Например, реакция п-нитрохлорбензола с водным раствором щёлочи проходит менее, чем за час:
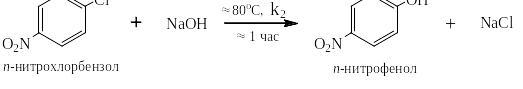
Проведя расчёт с помощью формулы Вант-Гоффа, оценим разницу в константах скоростей реакции нуклеофильного замещения для хлорбензола и его п-нитропроизводного.
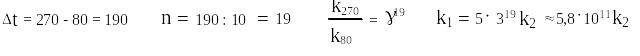
То есть константа скорости нуклеофильного замещения хлора в хлорбензоле в 580 миллиардов раз ниже, чем для хлорбензола с ЭА-заместителем в п- положении.
Реакцию хлорбензола с аммиаком не удаётся провести ни при каких условиях:
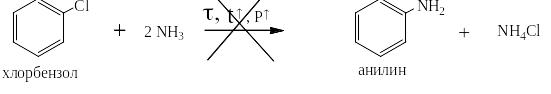
Введение нитрогруппы в п- или о- положение к атому хлора приводит к возможности течения реакции с аммиаком в реально достижимых условиях:

Накопление ЭА-заместителей в о- и п-положении к атому галогена приводит к ещё большему ускорению реакции, например:
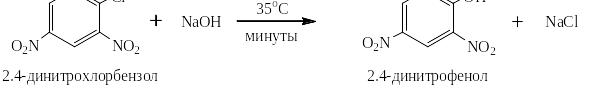
Добавление третьей нитрогруппы во второе о-положение позволяет вместо щёлочи провести реакцию с водой в мягких условиях:
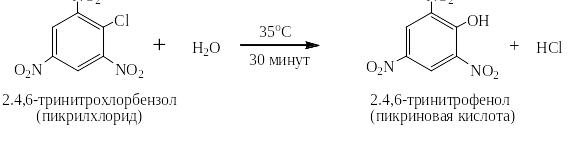
Реакции ативированного нуклеофильного замещения с алкоголятами
Если растворить натрий или калий в избытке какого-либо абсолютного спирта, то получится спиртовый раствор соответствующего алкоголята:
![]()
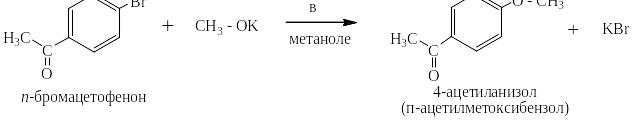
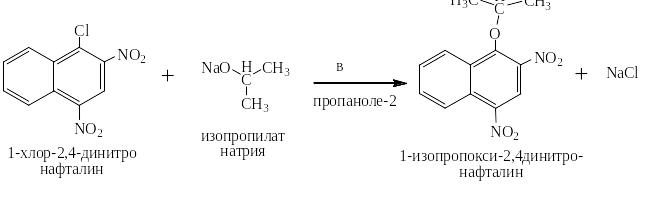
Если в полученный раствор добавить ароматическое галогенпроизводное с ЭА-заместителем в п- или о- положении (или и в том, и в другом сразу), то в тех же самых условиях с заметно большей скоростью пойдёт реакция замещения галогена на алкоксигруппу, например:
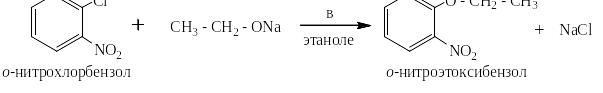
Реакции активированного нуклеофильного замещения с аммиаком и аминами
На стр. 27 было показано, что наличие в п-положении к к атому галогена ЭА-заместителя приводит к возможности протекания реакции с аммиаком в реально достижимых условиях. Накопление ЭА-заместителей в о- и п-положении к атому галогена приводит к ещё большему ускорению реакции, например:

Небольшое давление (порядка 6 атм) необходимо для того, чтобы удержать аммиак в реакционной массе.
Аналогично аммиаку, но быстрее в силу их большей основности, реагируют первичные амины:

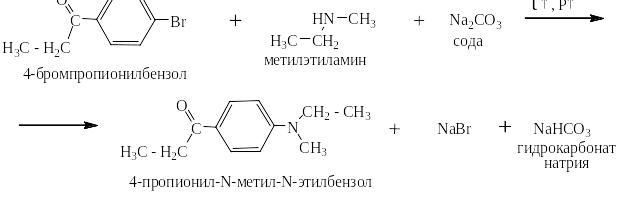
Наиболее активно при прочих равных условиях реагируют самые основные вторичные алифатические амины:
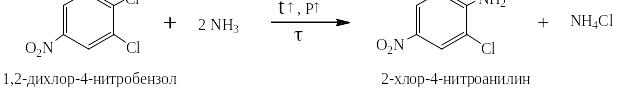
Если в молекуле имеется два атома галогена: один в о- или п-положении к ЭА-заместителю, а другой в м-положении, то замещается на гидроксил, алкоксил или аминогруппу только первый, например:
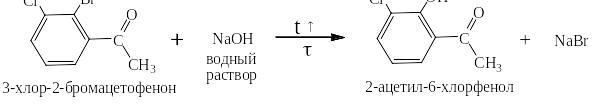
Если ЭА-заместителей в молекуле имеется два, то каждый из них активирует замещение атомов галогенов в о- и п-положении по отношению к себе:
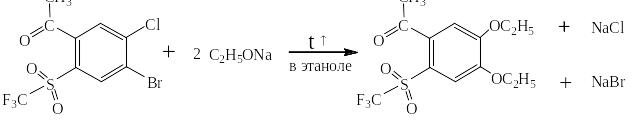
В представленном примере ацетильный заместитель способствует замещению брома на этоксигруппу, а заместитель Ягупольского (трифторметилсульфонил) замещению хлора.
